海水制氢技术发展现状与展望*
万晶晶 张 军 王友转 张丽佳 董 星
(广东省科技图书馆(广东省科学院信息研究所),广州 510070)
全球能源格局正在经历由依赖传统化石能源向追求清洁高效能源的深刻转变,各国都在大力发展清洁能源,减少传统化石能源的使用,积极寻找替代能源。氢作为一种理想的二次能源载体,其燃烧最终产物只有水,表观上是一种绝对清洁的燃料,可用于储能、发电、各种交通工具用燃料、家用燃料等[1,2]。
在氢能利用方面,制氢是第一个关键的技术环节。目前全世界每年约产氢0.7亿吨,主要作为工业原料用于化学工业、合成氨和石油加工工业。其来源主要是化石燃料制氢(煤炭、天然气)、工业副产氢(乙烷、丙烷脱氢、重整、氯碱、焦炉煤气等)、甲醇重整制氢和电解水制氢,这些都是较为成熟的技术[3]。此外还包括生物及生物质制氢、太阳能光解水制氢、热化学分解水制氢等试验性方法。国际可再生能源机构(International Renewable Energy Agency,IRENA)数据显示[4],目前超过95%的氢气从化石燃料中制取,制氢过程中会排放大量二氧化碳,因此对现有制氢工艺进行改进或者开发全新的绿氢工艺以减少碳排放是氢气规模化应用的关键所在。
水资源是地球上最大的“氢矿”,是制取氢气的理想来源。根据美国能源部和日本经济产业省的预测,未来水制氢成本可能与化石燃料成本持平[5]。过去,无论是已商业化的电解水制氢技术,还是大部分水制氢试验性研究,都是以淡水为原料。考虑到淡水的稀缺,若全球需氢量剧增,以丰富的海水资源制备氢气将是一种有前景的技术。
目前,国内外海水制氢研究并不多见,在Web of Science和Incopat数据库中检索发现,主要论文与专利文献约1000余篇,大多数是有关海水光/电解制氢的催化机理、催化剂的设计与开发、制氢装置与成本效率等方面的研究成果。本文结合全球海水制氢产业的开发进展情况,进一步梳理总结了当前海水制氢的研发与商业化进展,旨在为我国氢能领域的研发布局和产业发展提供参考依据。
1 海水制氢的技术路线
海水占地球全部水量的96.5%,与淡水不同,其成分非常复杂,涉及的化学物质及元素有92种。海水的盐度大约为35‰,其中钠(Na+)、镁(Mg2+)、钙(Ca2+)、钾(K+)、氯(Cl-)、硫酸离子占海水总含盐量的99%以上[6]。海水中所含有的大量离子、微生物和颗粒等,会导致制取氢气时产生副反应竞争、催化剂失活、隔膜堵塞等问题。为此,以海水为原料制氢形成了海水直接制氢和间接制氢两种不同的技术路线。
海水直接制氢的路线主要通过电解水制氢或光解水制氢方式制取,全球主要研究机构有中国科学院、法国国家科学研究中心、日本东北工业大学、北京化工大学、印度科学工业研究理事会、美国休斯敦大学等;海水间接制氢则是将海水先淡化形成高纯度淡水再制氢,即海水淡化技术与电解、光解、热解等水解制氢技术的结合。
2 海水直接制氢的研究现状
2.1 海水电解制氢
海水电解反应包括阴极析氢反应(Hydrogen Evolution Reaction,HER)和阳极析氧反应(Oxygen Evolution Reaction,OER)两个半反应[7]。理论上同时驱动OER和HER的最小电压为1.23 V,但是,在实际电解过程中需要额外的电位去激活和克服原始反应能垒,即过电位(η)。因此,尽可能地降低水电解的过电位、降低能耗是发展电解制氢的关键,而加入催化剂可以降低过电位,提高反应速率。
在海水电解制氢过程中,对于HER,天然海水中存在各种溶解的阳离子(Na+、Mg2+、Ca+等)、细菌/微生物和小颗粒等杂质。这些杂质可能会随海水电解过程的进行而产生Mg(OH)2、Ca(OH)2沉淀物覆盖催化剂活性位点,从而使催化剂中毒失去活性。对于阳极来说,OER是一个复杂的四电子转移反应,反应动力学缓慢,需要更高的过电位。而海水中的高浓度氯离子带来的析氯反应(Chlorine Evolution Reactions,ClER)和次氯酸盐的形成都是二电子反应,与OER反应相比,反应动力学较快,因此会干扰OER并与之竞争,进而降低转化效率。因此,开发具有高活性、高选择性的海水电解催化剂,对于避免海水中离子及杂质的影响至关重要[1]。在国内外海水电解制氢方面,目前研究主要围绕HER催化剂、OER催化剂、双功能催化剂以及电解系统等开展。
2.1.1 HER催化剂
铂系金属被认为是HER基准电催化剂,在酸性、碱性和中性条件下均表现出最好的性能。但是,在海水电解过程中,其HER性能与在淡水电解质中的表现相差甚远。另外,贵金属的稀缺和高成本极大地阻碍了其大规模应用。因此,在实际应用中,在保持高活性的同时减少铂的使用至关重要[8]。Yang Fengning等[9]通过两步法制备Pt/Ni-Mo析氢催化剂,在113 mV的过电势下模拟海水和工业条件,可在碱性溶液下稳定运行超过140小时,盐水(1MKOH+0.5MNaCl)中达到2000 mA·cm-2的电流密度,是迄今为止的最佳性能,并能够实现700 cm2大面积制备。
除贵金属催化剂以外,探索廉价、高效和稳定的电催化材料是海水电解制氢的重要方向。过渡金属的催化活性被认为仅次于Pt族金属,而且价格便宜,其中Ni被认为是最有前途的催化剂之一。一些研究人员制备了基于Ni的合金催化剂Ti/NiM(M=Co、Cu、Au、Pt),在 HER中表现出显著的活性,但新型镍基催化剂还存在稳定性不足的问题,这是其应用的潜在障碍[10]。
此外,非贵金属HER催化剂还包括过渡金属氧化物和氢氧化物、过渡金属氮化物(TMNs)、过渡金属磷化物(TMPs)、过渡金属硫族化物、过渡金属碳化物、过渡金属杂化物等[7]。TMPs因含量丰富、活性高和稳定性良好被用于海水HER。Lv Qingliang等[11]报道了一种多孔的 PF-NiCoP/NF析氢催化剂,在天然海水中具有高活性和持久性,且在287 mV过电势下可达到10 mA·cm-2的电流密度,优于商业化的Pt/C(20 wt%),其研究认为三维形貌、空穴结构和导电基板提高了比表面积、电子转移和活性位点,从而有利于H2释放。
2.1.2 OER催化剂
长久以来,高析氧活性的电催化剂通常是IrO2和RuO2等贵金属氧化物催化剂,然而这两种元素的稀有性决定了发展储量丰富的过渡族OER高活性催化剂的必要性。由于OER复杂的四电子转移过程呈现反应动力学缓慢的特征,为应对ClER与OER竞争这一挑战,针对OER的选择性海水电解提出了三种主要策略,即碱性设计原理、具有OER选择性位点催化剂和Cl-阻挡层[8,12]。碱性设计原理主要基于热力学和动力学考虑,可以最大化OER和ClER之间的热力学电势差,从而保证对OER的高选择性。过渡金属氧化物和氢氧化物因引入氧空位,在碱性水中具有效活性位点,从而对OER具有良好的电催化性。此外,通过掺杂 Mo、Co、Fe、Ni、Mn或增加活性位点,可以提高 OER的选择性[13]。Yun Kuang等[14]将硫化镍(NiSx)生长在泡沫镍上,又在硫化镍外电沉积一层NiFe-LDH层状双金属氢氧化物,形成多层电极结构。其中泡沫镍起到导体的作用,NiFe-LDH为催化剂,中间硫化镍会演变成负电荷层,由于静电相斥而排斥海水中的氯离子,从而保护了阳极。正因为这种多层设计,阳极可以在工业电解电流密度(0.4~1A·cm-2)下运行1000小时以上。但是,该研究尚存在诸多待研究的工程细节,实现规模化、工业化需要进行放大实验。
2.1.3 双功能催化剂
设计具有较高活性和持久性的HER和OER双功能电解催化剂仍具有挑战。尽管碱性介质中存在不同类型的双功能水电解催化剂,如可对电子结构和形貌进行必要改变的金属硫族化合物、氮化物、氧化物和磷化物,但其中可在海水中直接电解的还很少[13,15]。2020年,Wu Libo等[16]通过“原位生长-离子交换-磷化”三步合成方法制备了双金属异质磷化物Ni2P-Fe2P,是一种具备了OER和HER双功能的催化剂,实现了对海水的高效稳定全分解产氢,在2.004V电压下全解水系统可达到500 mA·cm-2的电流密度,并且能稳定运行38小时以上。
2.1.4 电解系统
从应用角度来看,除了开发稳定高效的催化剂外,还必须设计合适的高性能、低成本海水电解槽。目前,碱性水电解槽(Alkaline Water Electrolysers,AWE)和质子交换膜水电解槽(Proton Exchange Membrane Water Electrolyser,PEMWE)两种低温(<100℃)电解槽在商业市场较为成熟;另外还有低温的阴离子交换膜水电解槽(Anion Exchange Membrane Water Electrolyser,AEMWE)和高温水电解槽(High-Temperature Water Electrolysers,HTWE)两种新兴技术,其中高温电解包括质子导电陶瓷电解(150~400℃)和固体氧化物电解(800~1000℃)。这些电解槽直接用来电解海水时,海水复杂的天然成分会对电解产生影响。其中主要问题是离子交换膜的物理或化学堵塞和金属组件的腐蚀,例如海水中的Na+、Mg2+和 Ca2+离子会降低 HTWE和 PEMWE质子交换膜的性能;Cl-、Br-、SO2-4等阴离子又会对AEMWE、AWE和HTWE的膜性能产生不利影响。因此,开发稳定的隔膜是海水直接电解面临的重要挑战。研究认为采用超滤、微滤对天然海水进行简单过滤,可以很大程度上解决固体杂质、沉淀物和微生物造成的物理堵塞[8,12]。Liu Zhao等[17]基于固体氧化物电解技术尝试了在高温下进行海水电解制氢,在未使用贵金属催化剂的条件下,以200 mA·cm-2的电流密度进行了420 h的长期恒流电解,产氢速率为183 mL/min。在不回收高温废气的前提下,其能量转化效率可高达72.47%。且该方法由于先将海水加热蒸发,海水中的绝大部分杂质不与电解槽接触,因而难以对电解槽造成破坏,因此具有良好的应用前景。
目前,海水电解制氢是直接利用海水制备氢气最为成熟的技术,尽管已取得良好进展,但依然面临着一些关键性挑战,例如:设计高活性、廉价且稳定持久的非贵金属HER/OER催化剂;各种离子、细菌/微生物和小颗粒等杂质带来的海水电解槽结垢、膜污染和腐蚀等问题。为解决以上问题,未来通过纳米工程、表界面工程、掺杂、包覆、理论计算辅助探究活性位点来开发高性能HER/OER催化剂,采取选择性渗透、覆盖钝化层、净化、海水蒸气等方式来避免海水离子和杂质对电解反应的干扰,以及开展海水电解制氢的放大试验将进一步促进海水电解制氢技术的发展[1,8,18]。
2.2 海水光解制氢
1972年,Fujishima A等发现TiO2单晶电极在光照下能分解水产生氢气,之后,太阳能直接转换为化学能成为可能。光解制氢是在光的作用下,直接将光能转化为化学能,其本质是半导体材料(Semiconductor,SC)的光电效应,当入射光的能量不小于半导体的禁带宽度(Eg)时,价带(Valence Band,VB)电子跃迁到导带(Conduction Band,CB),产生光生电子和空穴。电子和空穴迁移到材料表面,与水发生氧化还原反应,产生氧气和氢气[19]。
研究光催化剂制氢主要有光催化和光电催化(Photoelectrocatalytic,PEC)两种方式(图1)。光催化分解水是将光催化剂粉末直接分散在水溶液中,在光照射下产生氢气和氧气,其优点是催化剂能与水充分接触且装置简单,缺点是生成的氢气和氧气难以分离,且光激发的电子空穴容易复合。PEC则是将光催化剂制成电极浸入水溶液中,与对电极通过导线相连,在光照和偏压作用下,在两电极分别产生氢气和氧气,其优点是氢气和氧气易分离,且在偏压作用下降低了电子空穴复合概率,缺点是光照面积小且需要提供额外能量[20]。
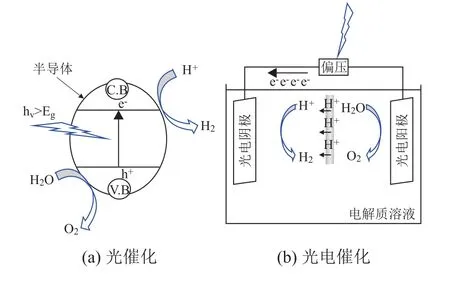
图1 光催化和光电催化水分解示意图[21]Fig.1 Representation of Photochemical and PEC Water Splitting Reactions[21]
光催化剂的Eg要大于水的理论分解电压,一般应在2 eV以上,最佳值取决于对太阳光的利用,研究认为具有2.53 eV的Eg较合适。美国能源部将太阳光照射发生的光催化分解水制氢效率(Solar-To-Hydrogen efficiency,STH)达到 10%作为商业化标志[18]。其中,STH=产生氢气的能量/入射太阳光的能量×100%。要实现10%的STH,光催化剂的光吸收范围要在600 nm以上,且表观量子产率(Apparent Quantum Yield,AQY)需要达到 60%以上[22]。
由于海水的成分复杂和缺乏高效的催化剂,光解制氢还停留在机理探索和早期试验阶段,直接利用海水光解制氢的研究并不多,研究主要围绕催化剂、助催化剂、牺牲剂、光源、海水的影响等开展。在PEC中,光电极设计和偏压设定是关键因素。
2.2.1 光催化剂
TiO2由于具有适宜的能带结构、化学性质稳定、无毒和成本低等优点,成为最常见的光催化剂。在光电催化制氢体系中,TiO2系材料主要用作催化剂工作电极。但是至今TiO2的光制氢性能仍然很低,主要源于其较大的禁带宽度(Eg=3.0~3.2e V),只能吸收占全部太阳光的5%左右的紫外光;且TiO2自身光生电子-空穴对易复合。为解决这些问题,采取的主要手段有掺杂、表面修饰、缺陷工程和构建异质结等[23,24]。Cao Shuang等[25,26]研究了一种使用多孔结构纳米TiO2作为光催化剂和Pt作为助催化剂的光催化系统,在紫外线和自然光照射下,光催化海水分解的氢气产生率分别为 7200μmol·g-1·h-1和3600μmol·g-1·h-1,是报道的不使用牺牲剂的TiO2催化系统的最高记录。其他无机半导体光催化剂还有 d10阳离子(如 Ga3+、Ge4+、In3+、Sb5+、Sn4+)或 d0过渡金属阳离子(如 Mo6+、Nb5+、Ta5+、Ti4+、W6+、Zr4+)的氧化物、(氧)硫化物、(氧)氮化物等[18]。
在聚合物半导体方面,g-C3N4因类似石墨的层状结构,具有优异的热稳定性、化学稳定性,较窄的禁带宽度(Eg=2.7eV),可调的能带结构,以及能够对可见光响应等诸多优点,成为光催化和光电催化制氢的研究热点,但其应用受到电子-空穴高复合率的限制。Zhang GG[27]等将聚合物氮化碳(Polymeric Carbon Nitride,PCN)在 NaCl/KCl低共熔盐中进行简单的后煅烧处理合成了一种三嗪-庚嗪的共聚物,所构筑的内部三嗪-庚嗪供体-受体(D-A)异质结构显著加速了界面电荷转移,从而共同提高海水中光催化活性,在420 nm条件下,AQY达到突破性的60%。
2.2.2 助催化剂与牺牲剂
除光催化剂以外,助催化剂和牺牲剂也是光催化体系中的关键部分。由于单纯光催化剂体系在产氢过程中的活性仍相对较低,在催化剂表面负载助催化剂可以有效捕获光生电子或空穴,从而降低光生载流子的复合。同时,助催化剂有时还可以降低反应活化能或产氢过电势[28],因此寻找高效的助催化剂也是研究方向之一。海水光解制氢中采用的助催化剂有贵金属助催化剂(Pt[25]、Au[29])、过渡金属氧化物或硫化物(如CuO[30]、Rh2-yCryO[31]3、NiS[32]、NiO[33])、过渡金属磷化物(CoP[34])等。
牺牲剂的作用是消耗光生空穴或电子,从而阻止光生电子与空穴复合,加速产氢速率。Xu Wenming等[35]采用低成本碱金属卤化物(NaI、KI、RbI、CsI、CsBr和 CsCl)对氮化碳(CN)进行改性,制备得到具有大量负电荷的催化剂MX-CN,同时采用三乙醇胺(TEOA)作为牺牲剂,在420 nm光照下,在海水中的表观量子效率(Apparent Quantum Efficiency,AQE)达到72%,是目前报道的最高水平,为设计海水中光催化剂与牺牲剂之间的电子转移提供了新研究方向。
2.2.3 光源
太阳光谱中,紫外光(200~400 nm)能量约占5%;可见光(400~760 nm)能量约占45%;红外光(760~2500 nm)约占50%。遗憾的是,太阳光谱中红外光激发的半导体材料不能用于光解水[22]。目前海水光催化和PEC系统中采用的光源有自然光源(太阳光)和人工光源(可见光、紫外光、AM1.5G模拟太阳光)。光源的发射强度越大,提供的光子就越多,产生的光生电子和空穴也越多,从而提升催化效率。但是过高的光强不利于光生电子-空穴对的迁移,也增加了能源消耗[36]。目前,研究人员倾向于使用太阳光或可见光作为光源,这也是实现太阳能直接转化为化学能的最终目标[26]。
2.2.4 光电极
在PEC海水分解中,通常用金属Pt作阴极,n型半导体作光电阳极。常用的光催化剂TiO2、g-C3N4作为光电阳极的报道较多。Li Yuangang等[37]制备 TiO2@ g-C3N4纳米阵列作为光电阳极,并用Co-Pi进行表面修饰,铂丝作为阴极,在1.23 V条件下光电流密度可维持在1.6 mA·cm-2,证明Co-Pi的表层修饰进一步促进了载流子的迁移和电荷有效分离。其他金属氧化物材料(例如 CO3O4、BiVO4、Fe2O3和 WO3)也被用作PEC的光电阳极。相对光电阳极而言,光电阴极研究还较少,且存在价格昂贵、光腐蚀严重、毒性高等问题,因此急需开发出廉价、稳定、高效的新型光阴极材料来解决上述难题。理论上,用p型半导体作为光电阴极材料,与n型半导体光电阳极组合形成PEC,可提高制氢效率,因此探索合适的阴极材料,也是提高PEC效率的新研究方向。在这方面,MM Ayyub等[10]报道了 Cu2OCuO-NixPy作为光电阴极、BiVO4-MDH作为光电阳极的海水光电催化体系。
2.2.5 偏压
偏压可以有效促进光生电子和空穴对的分离。在海水光电催化体系中,张冀宁等[36]报道在TiO2系材料作为光电极时,不同研究采用的偏压存在差异,一般在0.5~3.0 V不等;其他材料作为光电极时,偏压在0.5~1.23 V不等。偏压的选取需要结合反应体系选择合适的范围。在一定范围内,增大偏压可以降低光生电子和空穴对的复合速率,且提升光生电流密度。但过高的偏压会造成能源浪费,因此应充分考虑产氢速率,从而选用最优偏压条件。
2.2.6 海水的影响
光催化纯水的机理已经比较成熟,海水中离子的作用机理还在探索阶段,需进一步开展研究。到目前为止,不同系统还没有通用机制,主要围绕Na+和 Cl-对海水光催化的影响进行研究。在Cl-的影响方面,部分研究认为Cl-影响了反应物在光催化剂表面的吸附,从而降低了光催化的活性。也有研究认为海水中的无机盐可以充当牺牲剂,从而使海水制氢效率高于纯水。总体来说,大都认为海水中无机盐可以改变光催化剂表面的物理和化学性质,从而影响最终的制氢效率[26]。
因可同时解决能源和环境问题,海水光解制氢极具前景。但不管是光催化还是光电催化,制氢过程都要依赖太阳光,其光吸收效率仍然偏低,且空穴电子复合快,光解制氢的转化效率仍然受限,目前还处于实验室早期研究阶段。在光催化制氢中,由于不需要膜和额外能量,如果光催化剂对太阳能的利用率能进一步提高,未来有望达到美国DOE的商业化目标。开发含量丰富、禁带宽度低的光催化剂以及低成本、可持续的助催化剂将是潜在解决方案。在光电催化体系中,其光电流密度还限制在10 mA·cm-2数量级,比最先进的电解制氢系统低50~200倍,但依然是提高海水光催化活性的有效途径。未来PEC活性有待进一步提高,随着研究的深入,将具更大发展空间[10,18,38]。
3 海水间接制氢的产业开发进展
海水间接制氢本质上是淡水制氢,淡水电解制氢已商业化,而光解水制氢还处于早期研究阶段,仍然极具挑战。目前海水制氢的国内外示范项目中,实质也是海水淡化后电解制氢技术,再利用海上风能和太阳能将水分解成氢气和氧气。从产能来看,国内外可再生能源制氢项目仍是小规模试点,且大多处于在建或拟建阶段。
3.1 国外示范项目
2019年,国外多个可再生能源海上制氢项目开始启动(表1)。德国Tractebel Overdick在2019年提出一种海上风电制氢平台,包括风力涡轮机、电解装置、变压器和脱盐装置。该平台适用于容量为100~800 MW的风力涡轮机。先通过脱盐装置将海水淡化成高纯度水,再利用海上风能发电将水电解为氢和氧。当风力涡轮机容量为400 MW时,产氢量达80000 m3/h。电解后的氢气存储起来,用作能源载体或工业原料[39];英国Logan Energy的Seafuel项目针对岛屿等偏远地区用电成本高、对陆地基础设施依赖程度强等问题,通过可再生能源(包括太阳能、风能或海洋能)电解海水生产的氢气为岛屿交通提供动力。电解产生的氢气储存在氢燃料站台,作为燃料电池车的储备能源,所述燃料电池车续航里程达500~600 km[40];荷兰海王星能源公司2019年参与建立了全球首个海上绿氢试点项目PosHYdon,旨在通过荷兰北海的Q13a平台整合北海中的三种能源系统:海上风能、海上天然气和海上氢气。由海上风力涡轮机产生的电力为Q13a平台上的制氢装置提供动力,将海水转化为软化水,然后通过电解装置电解为氢气和氧气。氧气直接排放到空气中,氢气由天然气大型管道公司NOGAT和Noordgastransport,与天然气一起运输给工业、交通部门和荷兰家庭用户,项目已于2021年7月开始生产氢气,采用了1.25 MW的PEM电解槽,每天最多可产生500公斤的绿色氢气[41]。
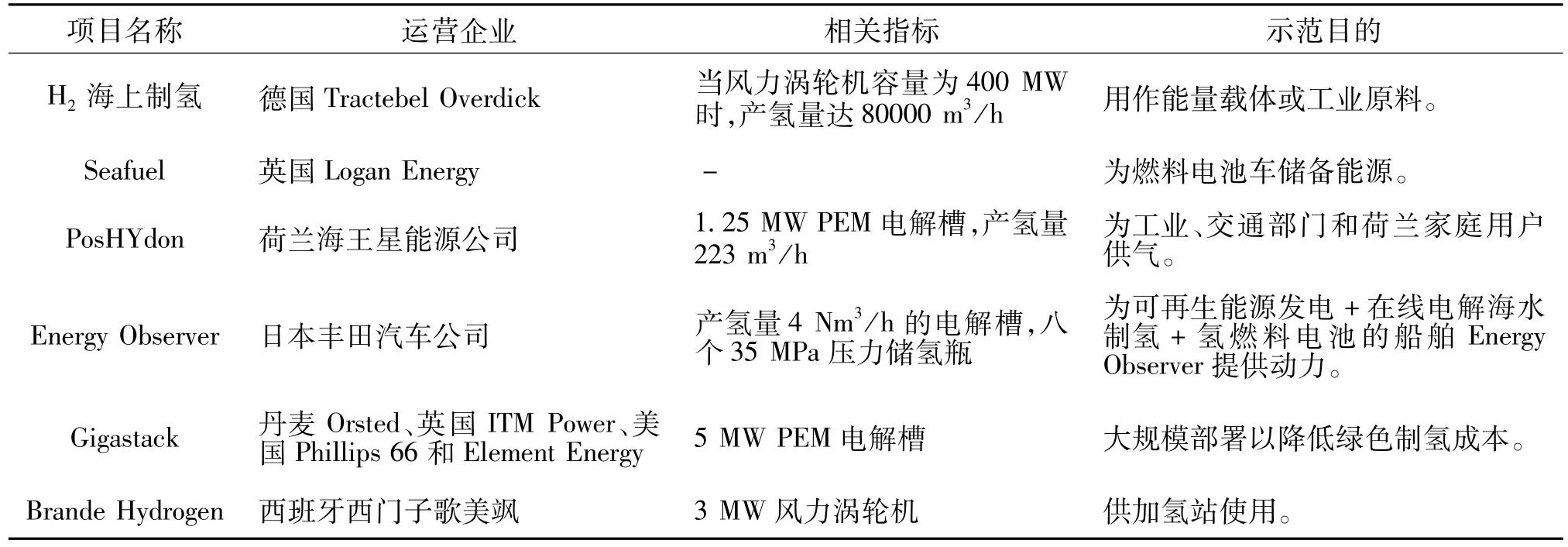
表1 国外海水间接制氢主要示范项目Tab.1 Demonstration Projects of Hydrogen Production from Desalinated Seawater Abroad
2020年,丰田汽车公司为利用可再生能源发电+在线电解海水制氢+氢燃料电池的船舶Energy Observer提供燃料电池系统,该船在2020年行驶了1万海里。其动力系统结构包括采用多级反渗透法的脱盐系统、产氢量4 Nm3/h的电解槽、压缩机、八个35 MPa压力储氢瓶、丰田燃料电池技术系统、总面积141 m2的光伏板、风力发电系统Oceanwings wings和锂电池。该船主要提供三种动力模式:1)正常航行中,由太阳能或风能直接为推进提供动力;2)发电量暂时下降期间,锂电池组将接管,为推进提供动力;3)长时间停船期,燃料电池将接管,消耗氢气发电和储电[42]。海上风电+制氢Gigastack项目2020年初获得英国政府750万英镑的财政补贴,计划于2022年建成投产,由世界最大的海上风电开发商Orsted运营,与 ITM Power、Phillips66和 Element Energy一起,旨在通过在千兆瓦规模的工厂制造“可堆叠”的5 MW PEM电解槽,实现首款工业规模的100 MW电解槽,并大规模部署到海上风电场,以大幅降低绿色制氢成本[43];2020年12月,西门子歌美飒在丹麦启动了全球首个以“孤岛模式”运行的风电制氢试点项目Brande Hydrogen,于2021年1月开始运行。该项目将容量为3 MW的风力涡轮机连接到碱性电解槽上,制备出的氢气由油轮运输到岸上,供加氢站使用,单台3 MW的风力涡轮机可为50~70台出租车提供足额氢能燃料[44]。
3.2 国内示范项目
国内海水间接制氢示范项目的启动相对较晚,大多利用海上风能电解水制氢。2020年6月,全国首个海上风电场项目在青岛启动,该项目将开展海上风电+波浪发电、海上风电+制氢储氢、海上风电+海水淡化、海上风电+海洋化工、海上风电+海洋科学研究等多样化融合试验与示范应用。拟于2021年开建,总建设容量为2000 MW,达产后可年产风电60亿度,实现年产值 30亿元[45]。
2020年9月,福建漳州市政府与三峡集团、明阳集团签署投资合作协议,两大集团将联合建设漳州深远海海上风电产业园项目,并配套规模化开发深远海海上风电资源,其中包含海上风电制氢等产业项目[46]。
2021年3月,广东省2021年重点建设项目计划“海上漂浮式风电+海洋牧场+海水制氢”项目获批。该项目总投资530亿元,分两期建设。一期建设“海上风电+海洋牧场(部分)+海上漂浮式风电”,风电装机容量1000 MW;二期建设“海上漂浮式风电+海洋牧场+海水制氢”,风电装机容量 2000 MW[47]。
4 海水制氢的发展展望
海水制氢的未来发展取决于以下主要因素:
首先是对氢产量的需求。目前,氢能正在世界范围内掀起第二次热潮,美国、德国、日本等发达国家已将氢能上升为国家能源战略,我国也提出加速发展“绿氢”制、储、用等氢能产业链技术装备,促进氢能燃料电池技术链、氢燃料电池汽车产业链发展。但需要注意的是,到目前为止,全世界氢的生产几乎都是作为工业原料而不是作为能源载体使用,后者用量可以忽略不计。只有当氢能源的广泛应用带来电解水制氢规模的高度膨胀,以海水为原料的工业化制氢才有可能迎来发展机遇。一般主要国家氢能战略中实现重大发展的时间点大都在2050年左右,国际能源署预测到2050年全球氢年需求量约近3亿吨,到2070年达到5.2亿吨[48];中国氢能联盟预测我国到2050年接近6000万吨[2]。中期来看,未来20年内,以氢燃料为动力的重载运输是氢能唯一有望取得实质性渗透的行业领域,且仍面临与电动汽车的直接竞争,且需求量较有限。
其次是电力来源的成本和可行性。目前超过95%的氢气采用化石燃料生产,蒸汽-甲烷重整是最常见的氢气生产方式,石油和煤炭气化方式也被广泛使用。这些方式的主要问题是能耗巨大且CO2排放强度高。在应对全球气候变化、包括我国在内的排放大国纷纷承诺加快实现碳中和的背景下,利用可再生能源电力电解水制氢理论上不但是氢能源的主要生产方式,也有可能取代传统的化石燃料制氢。这一前景的实现有赖于可再生能源,特别是陆上风电、海上风电以及太阳能发电的规模扩大和全生命周期成本产生显著竞争力。根据国际能源署分析,随着制氢规模的扩大,可再生能源发电成本到2030年可下降30%[3]。美国能源部DOE分析,采用可再生能源和电网并行供电时,PEM电解槽制氢成本在2.5~6.8美元/千克之间,已接近DOE 2美元/千克的目标[49]。因此,在需求充分的情况下,未来可再生电力将有条件为海水制氢提供充足的电力来源保障。
最后是技术可行性。根据上述海水制氢技术发展分析可以看到,目前的海水直接制氢技术尚停留在技术研发与验证阶段,全球范围内的研发强度尚不活跃。在电解制氢方面,海水会带来Cl析出、结垢、膜污染和腐蚀等问题,针对海水直接电解还缺乏准确的技术经济评估,尽管海水的使用可能会大大降低水的成本,但如果电解槽稳定性欠缺,其运行成本可能增加6倍以上,而且研究估计传统的铂族金属(Platinum Group Metal,PGM)电极寿命会缩短至少一个数量级。而制备稳定、高效的电解催化剂和电解槽依然面临着很大挑战。在光解制氢方面,因光吸收效率低、空穴电子复合快和表面反应动力学有限等问题,STH仍然低于10%的商业化转换目标,实现产业化应用依旧是一个巨大挑战[18,50]。海水淡化制氢近年来国外已有较大规模的示范项目开始布局,理论上没有太大技术障碍,但仍需通过示范解决复杂生产流程中存在的问题,如工艺衔接、储存、输运等。

