我院儿外科全肠外营养医嘱合理性与不合理的原因分析
顾洁莹
(南通市妇幼保健院 临床药学部,江苏 南通 226000)
0 引言
儿童患危重症的情况较多见,在病情的影响下患儿无法正常地进食,加之疾病对能量的消耗,多存在营养不良的困扰,而营养不良又会降低患儿抵抗力,增加其发生并发症的风险,是此类患儿入院后必须解决的问题。全肠外营养(TPN)即将机体活动所必要的葡萄糖、脂肪乳、氨基酸、电解质、维生素、微量元素等营养物质经静脉人工输注到患者体内的一种支持疗法[1]。合理的TPN治疗使外科收治的无法正常进食患儿得以维持与正常儿童一致水平的能量与营养,帮助其顺利度过病情危重阶段,同时也能够对一些并发症起到积极的预防作用,加速伤口在术后的恢复,增强患儿免疫力,增加患儿存活率[2]。基于在外科临床给予合理TPN医嘱的目的,本研究选取了部分住院TPN治疗患儿进行如下分析。
1 资料和方法
1.1 一般资料
通过医院信息系统(HIS)抽取本院2020年1月-2020年12月儿外科接受TPN治疗的47例患儿,共631条全肠外营养医嘱进行统计分析。
1.2 方法
参照药品说明书、《临床肠外营养支持治疗(2011~2012)》和《中国儿科肠内肠外营养支持临床应用指南》等,对TPN医嘱的适应证、热氮比、糖脂比、电解质浓度、葡萄糖终浓度、氨基酸终浓度、糖速、渗透压等使用情况进行统计分析。
1.3 统计学方法
采用SPSS 22.0版本统计学软件分析,计数资料采用χ2检验,以(%)表示,P<0.05表示差异有统计学意义。
2 结果
2.1 研究资料详情
此次分析对象包括男25例,女25例,将重复医嘱排除后剩余全肠外营养医嘱共有631条;≤3岁、4~10岁、11~15岁等各年龄段分别有43例、2例、2例;体质量1.15~59.00kg,平均(7.13±1.21)kg。
2.2 疾病种类及TPN使用时间
47例患儿原发病分布如:肠梗阻10例(21.28%)、肛门闭锁8例(17.02%)、肠系膜扭转7例(14.89%)、巨结肠4例(8.51%)、腹腔囊肿4例(8.51%)、十二指肠狭窄和闭锁4例(8.51%)、肠套叠3例(6.38%)、幽门狭窄3例(6.38%)、腹股沟斜疝2例(4.26%)、阑尾炎2例(4.26%)。患儿使用TPN时间为3~20d。
2.3 TPN组成成分
我院儿外科TPN成分主要包括:①葡萄糖类:50%葡萄糖注射液、10%葡萄糖注射液;②脂肪乳类:中/长链脂肪乳注射液(C6~C24);③氨基酸类:小儿复方氨基酸注射液(19AA-Ⅰ)、复方氨基酸注射液(18AA);④电解质类:注射用氯化钾、10%氯化钠注射液、葡萄糖酸钙注射液、硫酸镁注射液;⑤维生素类:注射用水溶性维生素;⑥微量元素类:多种微量元素注射液(Ⅱ)、甘油磷酸钠注射液等药品。
2.4 TPN医嘱热氮比
631条医嘱中,热氮比不合理医嘱共41条,占总医嘱数的6.49%,其中<100有5条,>200有36条,见表1。
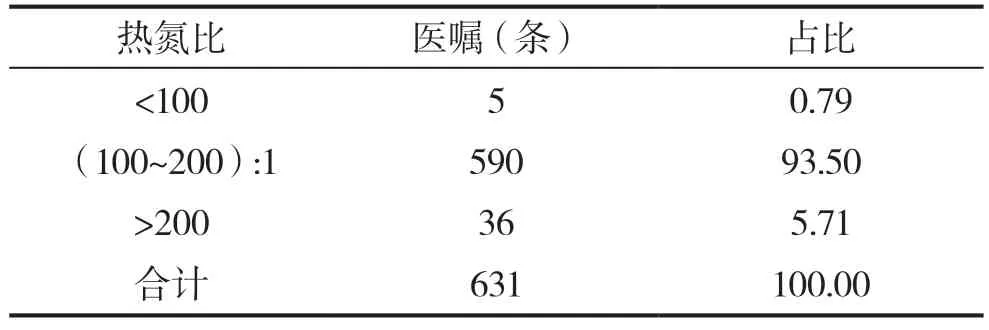
表1 TPN中热氮比情况(n,%)
2.5 TPN医嘱糖脂比
631条医嘱中,糖脂比不合理医嘱共46条,占总医嘱数的7.29%,其中<1:1有22条,>3:1有24条,见表2。
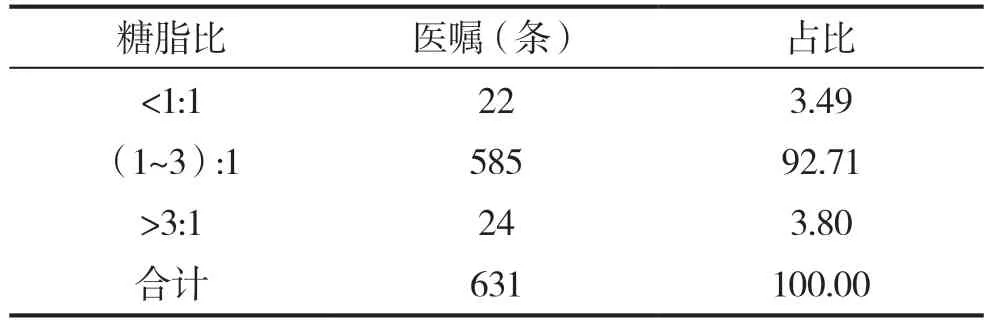
表2 TPN中糖脂比情况(n,%)
2.6 TPN医嘱电解质浓度、糖速、渗透压等情况
631条医嘱中,电解质浓度、葡萄糖终浓度、氨基酸终浓度、糖速、渗透压等情况见表3。
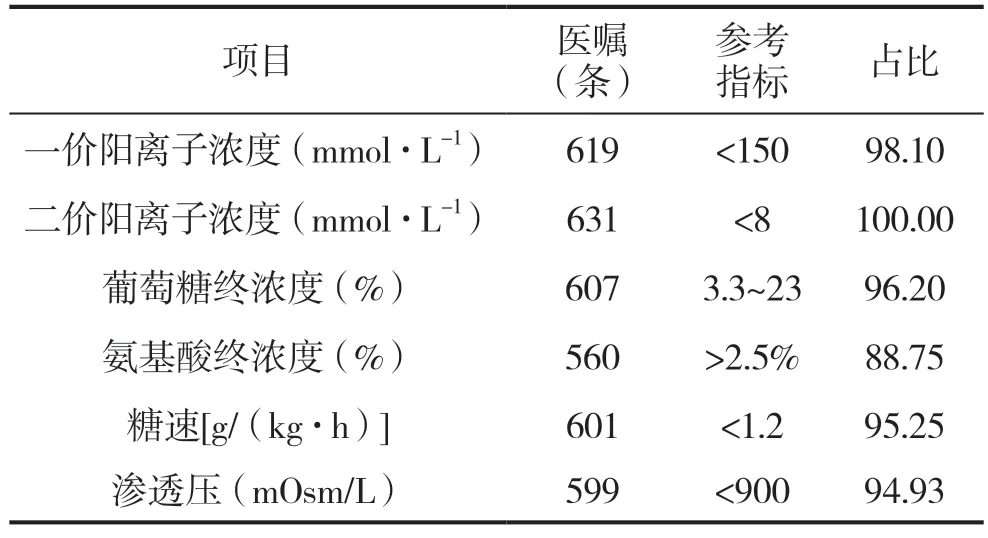
表3 TPN中各组分浓度、糖速、渗透压情况(n,%)
3 讨论
3.1 适应证
欧洲肠内肠外营养学会(ESPEN)、美国肠外营养学会(ASPEN)均认为最好在患儿入院24h内完成对其机体营养风险的筛查工作,以便能够及时发现营养不良、营养风险的存在,并及早实施必要的干预措施[3]。通过对各种疾病住院患儿开展营养风险筛查工作,分析结果发现,营养风险较高的几种原发病以肠梗阻、肠粘连、肠套叠以及其他肝胆系统疾病最为常见[4]。此次所选患儿共47例,经过对其围手术相关记录、原发病情等的分析发现,均属于无法正常进食或者说其肠内营养无法满足机体日常消耗能量或蛋白质的患儿,因此应用TPN治疗适应证基本合理。
3.2 TPN成分
我院TPN成分主要包括:葡萄糖类、氨基酸类、脂肪乳类、维生素类、电解质类及微量元素类等药品。我院儿外科使用中/长链脂肪乳注射液,因为比长链脂肪乳更加容易吸收。欧洲肠外营养指南推荐新生儿应补充小儿必需氨基酸,我国儿科肠内肠外营养指南推荐≤3岁婴幼儿可选用小儿专用氨基酸,对于>3岁儿童,欧洲肠外营养指南尚未说明,我国指南推荐>3岁儿童和青少年可选用成人配方[5]。故临床药师建议≤3岁婴幼儿选择19AA-Ⅰ。生长和发育需要维生素[6]。在维生素的遴选上,单一选择水溶性维生素,建议可以使用儿童专用维生素或者注射用脂溶性维生素(Ⅱ)/水溶性维生素。我院在TPN药物的遴选上是基本合理的。
3.3 热氮比
热氮比若合理,则可以对机体内蛋白质的分解产生一定抑制作用,有助于蛋白质的合成,让机体处于正氮平衡状态[7]。热氮比过低,则会促进氨基酸向能量的转化,导致浪费。热氮比过高,则机体内多余的非蛋白热量则会向脂肪转化,进而诱发肝脏浸润以及高血糖等问题。表1显示,分别有5条医嘱<100和36条医嘱>200,提出对氨基酸量、总热量等进行调整有助于合理控制热氮比。
3.4 糖脂比
脂肪与糖为TPN处方最主要的能源物质,若糖脂占比不合理,则可能进一步刺激代谢并发症。通常碳水化合物功能占非氮热量50%~70%,脂肪乳剂供能30%~50%,糖脂供能比应为(1~3):1[8]。糖脂比过高,可能会使应急高血糖受刺激进一步加重,促使机体糖代谢处于紊乱状态;糖脂比过低,则会进一步增加机体内糖异生与糖分解,有引发酮中毒与高脂血症等问题的风险。表2显示,分别有22条医嘱糖脂比<1:1,24条医嘱糖脂比>3:1。建议根据患儿病情调整葡萄糖和脂肪乳的用量。
3.5 TPN各组分浓度
氨基酸分子呈电中性,可起到一定缓冲效果,于TPN中可以作用于保护脂肪乳酸。在氨基酸浓度过低时,其缓冲肠外营养液的效果较差,可能引起不稳定的脂肪乳,造成“破乳”现象。表3显示,有71条医嘱氨基酸浓度<2.5%,占比达到11.25%,这一点需要临床医生在审核中予以足够的重视。
阳离子价位越高对脂肪乳稳定性影响越大[9]。表3显示,有4条医嘱存在一价阳离子超标。一价阳离子超标,尤其是钾离子超标,恐影响到患儿的安危[10]。
3.6 渗透压
美国胃肠外营养学会(A.S.P.E.N.)建议将外周溶液的渗透压限制在900mOsm/L,以最大限度降低浸润引起静脉炎的风险[11]。降低肠外营养液的渗透压可减少其对外周血管的刺激,降低静脉炎发生率[12-13]。外周静脉耐受的最高渗透压是900mOsm/L,但>600mOsm/L时,静脉炎发生率明显增加。给药次数越多,输注时间越长,静脉炎风险较高。94.92%的医嘱渗透压<900mOsm/L,47例患儿中有2例患儿渗透压比较高的患儿发生静脉炎不良反应,主要表现为Ⅰ度静脉炎:主诉疼痛,查体局部发红或肿胀,静脉无条索状改变,未触及硬结。临床药师对医护以及患儿家属进行培训、宣教,尽可能降低渗透压,可以有效降低静脉炎的发生率。
综上所述,我院2020年儿外科TPN医嘱基本合理,但仍存在不合理的情况。分析如下:①我院较少对全院临床医师进行统一的全肠外营养相关培训,导致临床医师对糖脂比、热氮比、氨基酸终浓度等营养学术语比较陌生,缺少软件辅助医师,医师无法快速计算各组分浓度;②临床营养支持团队发展不成熟[14];③无前置审方系统等信息化手段。临床药师应该充实营养知识体系[15],开展全肠外营养专项医嘱点评工作,适当进行科普与宣教或者举办儿童营养相关讲座,为临床护师与临床医生提供更多实用性强的专业建议,有需要还可以在科室考核中将相关评估结果作为一项重要指标,以便最大程度地避免不合理用药现象,为儿童用药安全、用药疗效给予保障。

