化学实验方案的设计与评价知识梳理
王晓波

化学实验方案的设计与评价是高考试题的热点、难点和创新点,更是高三复习备考的侧重点和成绩拔尖的突破口。每一年的复习备考中全国各地的一线备考师生,无不在此驻足,精打细磨、反复推敲和锤炼相关知识,甚至刷题练习、凝练规律和做题模板。本文从以下几点进行归纳总结,供师生借鉴和参考。
1.实验方案设计的注意问题
(1)药品和仪器是部分给出还是多余。若药品和仪器只部分给出,则应做必要的补充,若多余,则应进行筛选和淘汰。
(2)条件有无特殊要求。如采用最简单或最合理的实验步骤等要求对考虑反应原理、选择药品和装置、确定操作步骤等都做了限定,应高度重视。
(3)实验过程中的隐蔽性操作。如某些必要的干燥、除杂、冷凝等,这些都是实验中必不可少的,往往被忽略。
(4)药品的描述。有些题目要求指出药品的名称,如有些药品的准确描述为硫酸铜粉末、澄清石灰水、酸性高锰酸钾溶液、浓硫酸、饱和碳酸氢钠溶液等,其中的“粉末”“澄清”“酸性”“浓”“饱和”等词不可省略。此外也应注意某些仪器的规格。
(5)其他注意事项。①冷凝回流的问题;②冷却问题;③防止倒吸问题;④具有特殊作用的实验改进装置。如为使分液漏斗中的液体能顺利流出,用橡皮管连接成连通装置;为防止气体从长颈漏斗中逸出,可在发生装置中的漏斗末端套一支小试管等。
2.实验设计题答题策略
(1)细审题:明确实验目的和原理。实验原理是解答实验题的核心,是实验设计的依据和起点。实验原理可从题干给定的化学情境(或题目所给的实验目的)并结合元素及其化合物等有关知识获取。在此基础上,遵循可靠性、简洁性、安全性的原则,确定符合实验目的、要求的方案。
(2)想过程:弄清实验操作的先后顺序。根据实验原理所确定的实验方案,确定实验操作的步骤,把握各步实验操作的要点,弄清实验操作的先后顺序。
(3)看准图:分析各项实验装置的作用。有许多综合实验题图文结合,思考容量大。在分析解答过程中,要认真细致地分析图中所示的各项裝置,并结合实验目的和原理,确定它们在该实验中的作用。
(4)细分析:得出正确的实验结论。实验现象(或数据)是化学原理的外在表现。在分析实验现象(或数据)的过程中,要善于找出影响实验成败的关键以及产生误差的原因,或从有关数据中归纳出定量公式,绘制变化曲线等。
3.化学实验评价的五大视角
(1)可行性视角。
只有合理且切实可行的实验方案才有意义。可行性是方案的第一要素,评价方案时应注意从实验原理和操作两个方面分析:
①理论上要科学合理;
②操作上要简单可行。
(2)经济效益视角。
评价一种实验方案,不仅要从科学性上判断是否可行,还要从经济效益上考虑是否切合实际。
(3)绿色化视角。
①分析实验药品是否有毒,是否会造成环境污染;
②仪器药品是否价格低廉、易得;
③反应是否充分,原子经济性是否较强。
(4)安全性视角。
①避免炸裂:受热不均匀、液体倒吸、气流不畅、易燃气体中混有助燃气体等。
②防污染:有毒尾气未经处理、剩余药品随意丢弃,实验产生的废液肆意倾倒等。
③防失火:点燃或熄灭酒精灯的方法不正确,易燃试剂与明火接触等。
④防吸水:极易水解、吸水性强(潮解)的物质未密封保存或与潮湿空气接触,大量吸水导致液体溢出或反应变质等。
(5)规范性视角。
①仪器的安装与拆卸;
②试剂添加的顺序与用量;
③加热的方式方法和时机;
④仪器的查漏,气密性检验;
⑤温度计的规范使用,水银球的位置;
⑥实验数据的读取;
⑦冷却、冷凝的方法等。
4.实验数据统计与整理的一般方法
(1)数据的表格化。
①根据实验原理确定应记录的项目:所测的物理量。
②注意数据的有效数字、单位及必要的注解。
③设计好的表格要便于数据的查找、比较,便于数据的计算和进一步处理,便于反映数据间的关系。
(2)数据的图像化。
图像化是用直线图或曲线图对化学实验结果进行处理的一种简明化形式,适用于一个量的变化引起另一个量的变化的情况。图像化的最大特点是直观、明了。
5.实验数据筛选与处理策略
对实验数据筛选的一般方法和思路为“五看”:一看数据是否符合测量仪器的精确度,如用托盘天平测得的质量的精确度为0.1g,若精确度值超过了这个范围,说明所得数据无效;二看数据是否在误差允许范围内,若所得的数据明显超出误差允许范围,要舍去;三看反应是否完全,是否少量或者过量的反应物作用下所得的数据,只有完全反应时所得的数据才能应用;四看所得数据的测量环境是否一致,特别是气体体积,只有在温度、压强一致的情况下才能进行比较、运算;五看数据测量过程是否规范、合理,错误和违反测量规则的数据要舍去。
6.实验数据综合分析策略
解决这类试题的关键是如何用好、选好数据。一般方法是比较数据,转变物质,分析利弊,确定实验数据处理方案。
例题 Na2O2是常用的强氧化剂,CO和H2是常用的还原剂。某学习小组以“探究过氧化钠能否氧化CO、H2”为目标开展下列研究:
【提出假设】假设1:过氧化钠只氧化CO。
假设2:过氧化钠只氧化H2。
假设3:____。
【查阅资料】赤热的焦炭能与水蒸气反应生成CO和H2,同时CO与水蒸气在高温下反应生成少量的CO2。
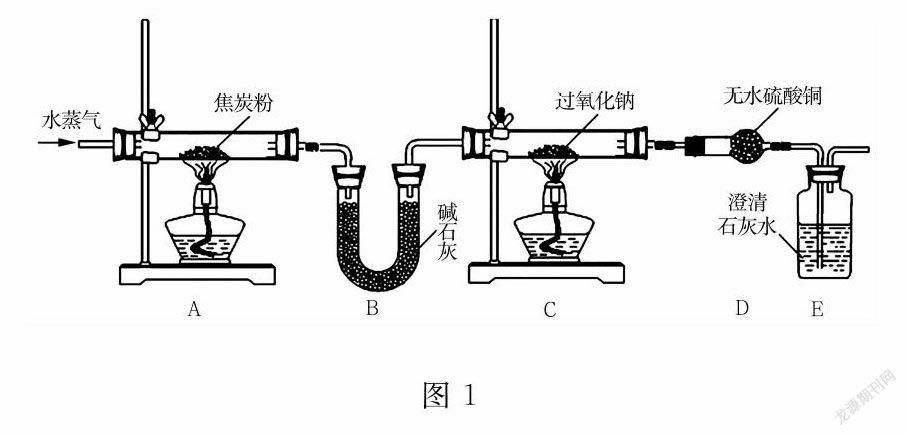
【设计实验】学习小组的同学根据实验目标设计如图1所示实验(假设装置中药品都充足)。
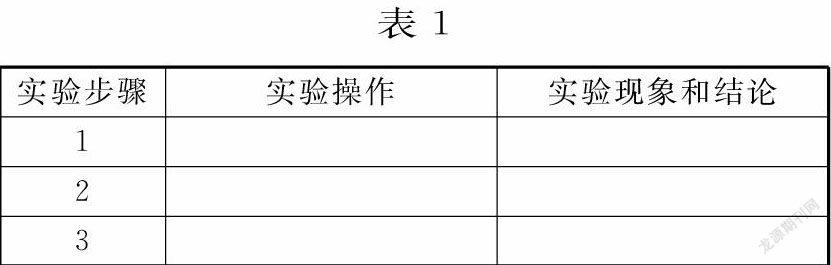
主要实验步骤:
①连接装置并检查装置气密性;
②点燃A处酒精灯,缓慢通入水蒸气,待装置内空气排尽后,点燃C处酒精灯;
③浅黄色的过氧化钠熔融完全变白色时,熄灭C处酒精灯;
④继续通入水蒸气至C处玻璃管冷却,停止通水蒸气并熄灭A处酒精灯。
实验过程中,无水硫酸铜没有变蓝色,澄清石灰水没有变浑浊。
【问题探究】(1)上述方案有不足之处,请你提出修改建议:____。B装置的作用是____。
(2)确认步骤②“装置内空气排尽”的操作是____。

