脱氢表雄酮对卵巢低反应患者妊娠结局及卵泡液的影响
李新宁 林秀峰 郑湘琼 杜静 李洁亮 程立子
随着生育政策的改变以及女性生育年龄的推迟,卵巢低反应(poor ovarian response,POR)的发生率有上升的趋势,具体表现为窦卵泡计数少,对外源性促性腺激素反应低下,促性腺激素用量大,排卵少,和(或)卵子质量差,最终导致所获胚胎质量差、临床妊娠率低及妊娠丢失率高等。在诊治过程中,为改善此类患者的妊娠结局,临床医生一直在探寻着可行的方法,其中在控制性超促排卵过程中予以添加辅助治疗为最受关注的方向,自2000年Casson等[1]首次报道脱氢表雄酮(dehydroepiandrosterone,DHEA)可改善卵巢低反应患者妊娠结局以来,后续的研究关于DHEA能否改善POR患者的妊娠结局提供了有争议的结论,且目前关于DHEA添加后卵泡微环境的变化尚未明确,因此,本研究目的在于探讨DHEA对接受体外受精-胚胎移植(in vitro fertilization and embryo transfer,IVF-ET)的博洛尼亚标准下的POR人群的卵巢反应性及临床结局的影响,以及通过分析卵泡液成分探讨DHEA对于卵泡微环境的影响。
1 资料与方法
1.1 一般资料
选取2018年10月—2019年8月于中山市博爱医院生殖中心(笔者所在医院)接受治疗的POR患者85例。根据制定的博洛尼亚(Bologna)标准[2],POR人群需满足以下至少两个条件:(1)具有卵巢储备功能降低的高危因素,如高龄(≥40岁)或任何其他POR危险因素;(2)先前的POR史;(3)双侧卵巢基础窦卵泡数(antral follicle count,AFC)<7个或抗苗勒管激素(anti-mullerian hormone,AMH)<1.1 ng/mL等卵巢储备功能异常指标。或连续两个大剂量卵巢刺激方案周期仍出现POR的患者。排除标准:(1)存在不适宜妊娠的禁忌证的内外科合并症;(2)有化疗、盆腔放射史及卵巢手术史;(3)有黏膜下肌瘤、宫腔粘连、子宫畸形等子宫异常因素;(4)男方存在严重的精液异常:如少精甚者无精;(5)夫妻双方至少一方存在染色体异常。研究经医院伦理委员会批准。将符合标准且同意试验的POR患者,随机分为用药组(n=41)和对照组(n=44),两组患者年龄、BMI、基础激素水平、窦卵泡数差异无统计学意义(P>0.05),说明两组患者卵巢储备具有可比性,详见表1。

表1 两组患者一般情况比较(x- ±s)
1.2 治疗方法及检测指标
两组行促排前均于月经第3天晨起空腹检测血清性激素基础水平:包括卵泡刺激素(follicle stimulating hormone,FSH)、雌二醇(estradiol,E2)、黄体生成激素(luteinizing hormone,LH)水平以及AMH水平,并行经阴道B超计数AFC。用药组予DHEA(GNC,美国)25 mg/次,每天3次,12周。对照组直接进入周期。两组均使用拮抗剂方案,重组促卵泡素(果那芬,瑞士默克雪兰诺)进行促排卵,第5天开始加用拮抗剂(西曲瑞克,瑞士默克雪兰诺)0.25 mg/d。定期性阴道超声监测卵泡生长并根据患者情况调整促性腺激素用量。扳机时机为双侧卵巢内直径>18 mm的卵泡不少于2个时,扳机药物为人绒毛膜促性腺激素250μg(艾泽,瑞士默克雪兰诺)。扳机后36 h左右取卵。根据精液情况,采用体外受精(in vitro fertilization,IVF)或卵胞浆内单精子显微注射技术(intracytoplasmic sperm injection,ICSI)即受精。取卵后3 d行胚胎移植,移植后予黄体支持。对于有多个胚胎且首次移植不成功者,采用玻璃化冷冻进行解冻周期移植直至妊娠或胚胎用尽,计算累计活产率 。新鲜周期(取卵周期内移植未经冷冻的胚胎)临床妊娠率指临床妊娠次数/移植周期数×100%。
1.3 样本收集及检测
1.3.1 卵泡液收集 选择取卵日穿刺的第1个直径>16 mm的卵泡,为去除卵泡液中有形成份,将拾卵后的卵泡液置于离心机中,离心机转速为3 000 r/min,离心时间为10 min,将离心后的上清液密封保存于-80℃冰箱中。
1.3.2 检测 卵泡液中的AMH、DHEA-s、IGF-1采用酶联免疫吸附试验(enzyme-linked immunosorbent assays,ELISA)进行检测。生长分化因子-9(growth differentiation factor-9,GDF-9)的蛋白含量采用Western blotting方法测定。
1.3.3 妊娠判断标准 进行常规IVF或ICSI授精(根据男方精液情况决定),是否进行新鲜周期移植取决于患者有无存在影响移植的因素如存在子宫内膜不均、孕酮过高等。若新鲜周期移植,于取卵后第3天移植1~2个第3天(D3)胚胎,于取卵后5 d移植囊胚1枚,并予黄体支持。若为解冻周期移植,则等待移植的影响因素消除后择期行冻融胚胎移植(frozen embryo transfer,FET)。移植后14 d,检测血β-HCG>25 U/L诊断为生化妊娠。超声见妊娠囊、卵黄囊为临床妊娠。累计活产率=获得活产的患者数/1次COS患者数×100%。
1.4 统计学处理
所有数据均采用SPSS 20.0统计软件处理。计量资料表示为 (x-±s),采用t检验,若不符合正态分布,表示为 [M(P25,P75)],检验方法为Mann-Whitney U检验;计数资料表示为(n,%),采用χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 对照组与用药组患者促排卵情况及临床结局比较
用药组促性腺激素总量少于对照组[(2 498.13±747.13)U vs . (2 322.08±792.72)U],用药组平均获卵数、卵裂数、平均可利用胚胎数均较对照组多,但差异无统计学意义(P>0.05)。同时HCG日血清FSH、E2、子宫内膜厚度等差异无统计学意义(P>0.05)。新鲜周期移植用药组20例(临床妊娠5例,妊娠率25.00%),对照组15例(临床妊娠5例,妊娠率33.33%),组间差异采用卡方检验,P>0.05,其余因HCG日孕酮升高行全胚冷冻。累计活产率用药组高于对照(29.55% vs.34.15%),但差异无统计学意义(P>0.05)。详见表2和表3。
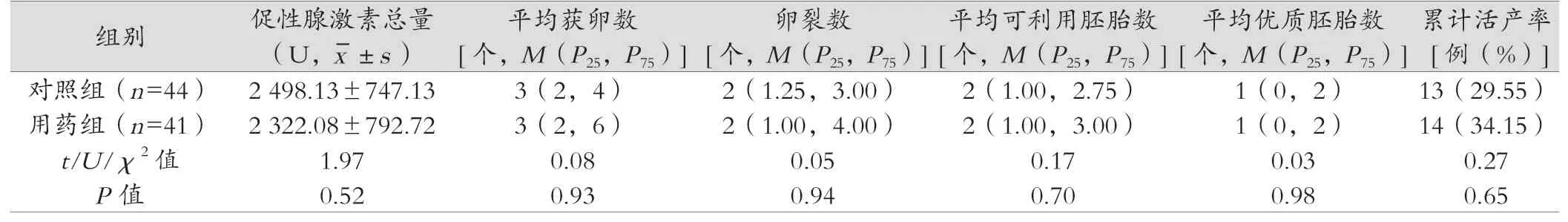
表2 卵巢反应性及妊娠结局的比较

表3 HCG日内膜厚度及激素水平比较
2.2 卵泡液指标比较
两组患者卵泡液AMH、DHEA-s、IGF-1、GDF-9测定差异无统计学意义(P>0.05)。如表4。

表4 卵泡液指标
3 讨论
随着受教育水平提高、社会压力的增加,生育年龄呈现逐渐延后趋势,特别是随着“三孩”政策落地,面临生育难题的高龄女性越来越多,其中卵巢低反应是导致这些女性接受辅助生殖技术治疗临床结局不理想的主要原因。成功分娩一个健康活婴是辅助生殖技术的终极目标,而获取的卵子数量以及质量对妊娠结局有直接影响。获卵数量是POR患者妊娠结局的决定性因素,如何改善低储备患者的卵巢反应性长久以来都是研究的热点。在研究中,笔者观察了POR患者IVF周期前使用DHEA预处理与否,对IVF周期结局以及对卵泡液中AMH、IGF1以及GDF9的表达影响。笔者观察到与对照组相比,DHEA组有更高的获卵数以及受精数,但差异无统计学意义(P>0.05),同时两组间妊娠结局差异无统计学意义(P>0.05)。
普遍认为DHEA是通过转化为雄激素发挥作用的,雄激素是调控卵子发育的重要因素[2-3],补充雄激素可改善POR患者临床结局[4-5],DHEA是雄激素合成的前体,仅有较弱的激动雄激素受体作用且可在卵泡转化为目标激素发挥作用。因此,DHEA是理想的雄激素替代药物。2000年Casson等[1]首次发现DHEA能提高卵巢反应性。但随后的研究就DHEA能否改善卵巢反应存在争议[6-7]。一Meta分析指出,DHEA对提高获卵无益[8-9],但可改善卵子质量来提高妊娠率[10],可能与DHEA 可以改善线粒体功能有关[11]。而另一研究[12]认为不能改善卵母细胞质量。在一项Cochrane系统评价中发现去除偏倚因素后DHEA的作用不再具有显著性[13]。另一研究和本研究一致[14],未能观察到DHEA改善POR的临床结局。
伏静等[15]研究中DHEA处理后卵泡液DHEA-s增高。在另一研究[16]中,卵泡内DHEA-s虽升高,但其代谢产物并无增加。DHEA转化为雄激素需要不同酶的参与,本研究中DHEA-s水平无增加,可能是其卵泡内与激素代谢相关的酶存在缺陷所致。
关于卵子的发生发育机制尚未明确,目前认为卵泡的生长及成熟受多种内分泌及旁分泌信号调控,特别是卵泡微环境中的AMH、IGF-1以及GDF-9等。AMH仅由颗粒细胞分泌,DHEA处理12周后,观察到与先前的试验一致的结果,即DHEA不能提高POR患者的AMH水平[17-18],笔者认为这是由于POR患者卵巢储备处于严重耗尽的极端,而卵巢储备自出生那一刻已经被决定,DHEA并不能使其储备增加[19]。GDF-9协同骨形态发生蛋白-15参与卵泡发育和成熟[20-22]。即使在卵巢反应有所改善的研究中,GDF-9表达也无明显增加[23]。因此,DHEA不通过GDF-9影响卵子发育。IGF-1对保持卵泡正常功能有重要作用[24]。IGF-1可提高原始卵泡对FSH的敏感性来增加卵泡反应性[25]。然而,本研究没有发现两组之间卵泡IGF-1水平有任何差异。因此DHEA考虑不能增加IGF-1的表达而影响卵子发育。
文章亮点在于:(1)在以往研究的基础上通过收集卵泡液样本分析DHEA疗效。(2)本研究以前瞻性方式进行,以确保研究组与对照组的一致性和可比性。研究的局限性:(1)本研究为随机对照研究,无法获得分到DHEA组患者治疗前的卵泡液样本,但两组患者的一般情况及卵巢储备情况差异无统计学意义(P>0.05),具有可比性。(2)由于POR因生育时间有限而不愿意接受安慰剂治疗,因此这不是安慰剂对照试验。
本研究中,POR女性通过12周DHEA处理后,卵巢反应性、妊娠结局上并无明显改善。同时,卵泡液中AMH、IGF-1、GDF-9含量也无显著增加。鉴于目前对于DHEA能否使POR女性获益仍存在争议,尽管本试验存在一定的局限性,但也能为将来研究DHEA对于POR女性的作用机制提供参考。对于DHEA的疗效以及作用机制仍需大样本、多中心的随机对照研究以及基础研究来进一步阐明。

