化学发光免疫分析法筛查隐匿性乙型肝炎病毒的应用价值
余照斌 葛晶晶 张广清

[摘要]目的研究化學发光免疫分析法(CIA)在隐匿性乙型肝炎病毒(HBV)筛查中的价值。方法选取2019年5—12月于清远市妇幼保健院进行 HBV 筛查的患者60例,所有患者均采用 CIA 进行 HBV 五项检测进行初筛,将初筛中乙型肝炎表面抗原(HBsAg)(-)、乙肝核心抗体(HBcAb)(+)样本进行复筛,并采用实时荧光定量聚合酶链式反应(FQ-PCR)法检测各样本中 HBV DNA 病毒载量,统计 CIA 检测情况以及 HBsAg(-)、HBcAb(+)样本复筛及 HBV DNA 检测情况。结果60例 HBV 样本 CIA 结果检出 HBsAg(+)15例,阳性率为25.00%, HBsAg(-)、HBcAb(+)样本39例。以 HBV DNA 检测结果作为金标准, ELISA 检测灵敏度为46.67%,特异度为66.67%; CIA 检测灵敏度为86.67%,特异度为91.67%;与 ELISA 比较, CIA 检查灵敏度、特异度更高(χ2=5.400、4.547,P=0.020、0.033)。结论 CIA 检测 HBsAg 具有较高的灵敏度,但当样本存在 HBsAg(-)、HBcAb(+)的情况下,需进行复筛和 FQ-PCR HBV DNA 检测,以免造成漏诊的情况。
[关键词]隐匿性乙型肝炎病毒;化学发光免疫分析法;酶联免疫吸附试验;病毒载量;灵敏度
[中图分类号] R512.6+2 [文献标识码] A [文章编号]2095-0616(2022)07-0146-04
Application value of chemiluminescence immunoassay in screening occult hepatitis B virus
YU Zhaobin GE Jingjing ZHANG Guangqing
Maternal and Child Health Hospital of Qingyuan City, Guangdong, Qingyuan 511500, China
[Abstract] Objective To study the value of chemiluminescence immunoassay (CIA) in screening occult hepatitis B virus (HBV). Methods A total of 60 patients who underwent HBV screening at Maternal and Child Health Hospital of Qingyuan City from May to December 2019 were selected as study subjects. All patients were initially screened for the five HBV markers by CIA, and samples of hepatitis B surface antigen (HBsAg)(-) and hepatitis B core antibody (HBcAb)(+) undergoing the initial screening were re-screened. The real- time fluorescence quantitative polymerase chain reaction (FQ-PCR) was used to detect the viral load of HBV DNA in each sample, and the CIA results and the re-screening and HBV DNA detection results of HBsAg (-) and HBcAb (+) samples were counted. Results In the CIA results of 60 HBV samples, 15 cases of HBsAg (+) samples were detected, with a positive rate of 25.00%, and 39 cases of HBsAg (-) and HBcAb (+) samples were detected. Using HBV DNA detection results as the gold standard, the sensitivity was 46.67% and the specificity was 66.67% for the detection by enzyme-linked immunosorbent assay (ELISA), and the sensitivity was 86.67% and the specificity was 91.67% for the detection by CIA. Compared with ELISA, CIA has higher sensitivity and specificity(χ2=5.400,4.547;P=0.020,0.033). Conclusion CIA has a high sensitivity for detecting HBsAg, but when HBsAg (-) and HBcAb (+) are present in the sample, re-screening and HBV DNA detection by FQ-PCR are needed to avoid missed diagnosis.
[Key words] Occult hepatitis B virus; Chemiluminescence immunoassay; Enzyme-linked immunosorbent assay; Viral load; Sensitivity
乙型肝炎病毒(hepatitis B virus, HBV)可以经血液、母婴以及生殖细胞等方式进行传播,是引起乙型肝炎的重要病原体[1]。乙肝表面抗原(HBsAg)是检测 HBV 感染最常用的指标,酶联免疫吸附试验(ELISA)是其主要的检测方法,具有成本低、操作简单等优势,但该方法灵敏度偏低,干扰因素较多,因此临床应用存在一定的局限性。临床上,将 HBsAg(-)但 HBV DNA(+)的现象称为隐匿性 HBV,由于此种现象的患者也存在传播的可能性,可对机体造成严重的危害,因此仅以 HBsAg(+)作为筛查标准可能导致漏诊[2]。化学发光免疫分析法(CIA)是目前检测 HBV 感染的常用方法,其具有灵敏度高的优势,且属于全自动操作[3-4]。本研究通过分析 CIA 在隐匿性 HBV 筛查中的价值,现报道如下。
1资料与方法
1.1 一般资料
选取2019年5—12月于清远市妇幼保健院进行 HBV 筛查的患者60例,年龄18~69岁,平均(38.88±4.79)岁,男43例,女17例。本研究相关操作符合伦理,经医院医学伦理委员会批准,参与研究者均知情且签署同意书。纳入标准:①年龄不小于18岁;②既往无肝肿瘤放化疗和手术史患者;③对体格检查、血液采样以及本研究其他相关操作知情同意。排除标准:①其他类型(丙型、丁型)肝炎病毒患者;②合并人类免疫缺陷病毒感染患者;③存在免疫功能缺陷障碍患者。HBV 感染诊断标准[5]:由乙型肝炎病毒持续感染引发,可以分为乙型肝炎病毒 e 抗原(HBeAg)(+)慢性乙型肝炎和HBeAg(-)慢性乙型肝炎;HBeAg(+)慢性乙型肝炎: HBV DNA 定量水平>2×107 IU/ml,血清HBsAg>1×104 IU/ml,丙氨酸氨基转移酶(ALT)持续或反复异常或肝组织学检查有明显炎症坏死和/或纤维化(≥ G2/S2);HBeAg(-)慢性乙型肝炎:血清 HBsAg(+)、HBeAg持续(-),多同时伴有抗-HBe(+), HBV DNA 定量水平≥2×103 IU/ml, ALT 持续或反复异常,或肝组织学有明显炎症坏死和/或纤维化(≥ G2/S2)。隐匿性 HBV 感染诊断标准:血清 HBsAg(-)、HBcAb(+),且血清和/或肝组织中 HBV DNA(+)。
1.2 方法
所有患者均采集靜脉血2管,每管各5 ml,并分装在带分离胶真空采血管中送检,以3000 rpm 的速率离心8 min 获取血清。1管采用化学发光免疫分析法(CIA)配套试剂盒由郑州安图生物工程股份有限公司提供,进行 HBV 五项检测,分别为 HBsAg、乙型肝炎病毒表面抗体(HBsAb)、HBeAg、乙型肝炎病毒 e 抗体(HBeAb)、乙型肝炎病毒核心抗体(HBcAb)。初筛出39例 HBsAg(-)、HBcAb(+)样本,判定标准:信号值比临界信号值(S/Co)≥1为有反应性(+), S/Co<1为无反应性(-)。针对上述 HBsAg(-)、HBcAb(+)样本进行复筛,分别采用 ELISA(试剂盒购自上海荣盛生物技术有限公司)、CIA 进行检测。换用另1管血清进行是实时荧光定量聚合酶链式反应(FQ-PCR)法 HBV DNA病毒载量检测,操作按照试剂盒说明进行,试剂盒购自湖南圣湘生物科技有限公司。以 HBV DNA 病毒载量>20 IU/ml 记为(+)。
1.3 观察指标
所有患者均采用 CIA 进行 HBV 五项检测进行初筛,将初筛中 HBsAg(-)、HBcAb(+)样本进行ELISA、CIA 复筛,并采用 FQ-PCR 法检测各样本中 HBV DNA 病毒载量,统计 CIA 检测情况、HBsAg (-)、HBcAb(+)样本 ELISA、CIA 复筛及 HBV DNA 检测情况,并以 HBV DNA 检测结果作为金标准,计算 ELISA、CIA 对隐匿性 HBV 感染的诊断价值。
1.4 统计学方法
采用 SPSS 22.0统计学软件进行数据处理,计量资料用均数±标准差( x ± s)表示,采用 t 检验,计数资料用[n (%)]表示,采用χ2检验, P <0.05为差异有统计学意义。
2结果
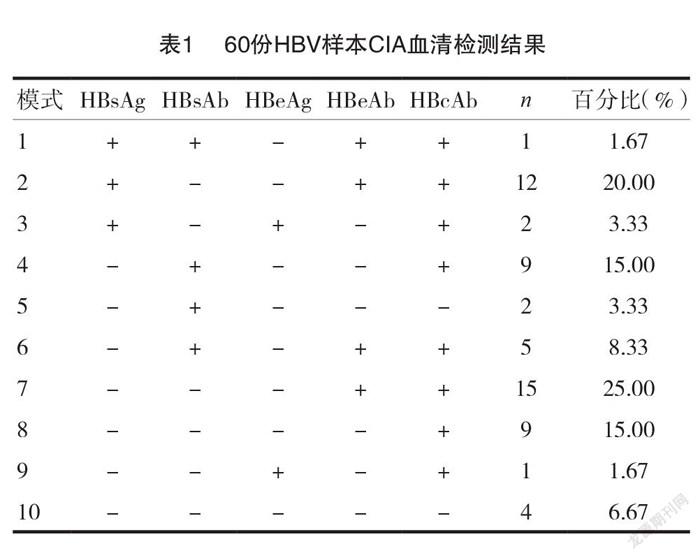
2.1 60份HBV样本CIA检测结果
以 HBsAg(+)和(-)为界,将60份 HBV 样本 CIA 结果分为10种模式,检出 HBsAg(+)15例,阳性率为25.00%。见表1。
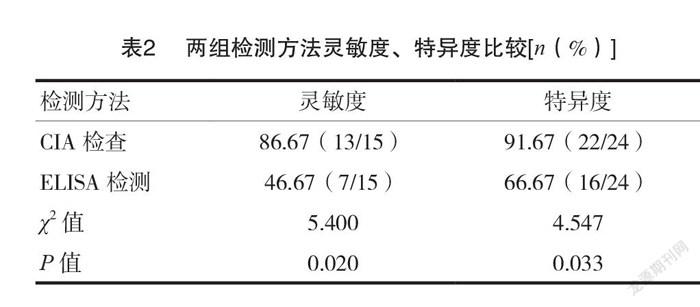
2.2 HBsAg(-)、HBcAb(+)样本复筛及HBV DNA检测结果
将 HBsAg(-)、HBcAb(+)样本39例分别进行 CIA 和 ELISA 复筛,ELISA 筛查出HBcAb强(+)样本7例,阳性率为17.95%; CIA 筛查出HBcAb强(+)样本13例,阳性率为33.33%; HBV DNA 检测结果显示病毒载量>20 IU/ml 样本15例, HBV DNA 阳性率为38.46%,以 HBV DNA 检测结果作为金标准, ELISA 检测灵敏度为46.67%,特异度为66.67%; CIA 检测灵敏度为86.67%,特异度为91.67%;与 ELISA 比较, CIA 检查灵敏度、特异度明显提升(χ2=5.400、4.547, P=0.020、0.033)。见表2。
HBV DNA 检测结果阳性样本分为5种模式,与模式2、3比较,模式4、5 HBV DNA 阳性率有所升高。见表3。
3讨论
HBV 感染是一个全球性的健康问题,HBsAg (+)是目前大多数国家筛查该感染的唯一标准,但在20世纪70年代,相关研究发现, HBsAg(-)也有可能引发 HBV 感染,即引出了隐匿性 HBV 感染的概念[6]。ELISA 是 HBV 感染经典的检测方法,但该方法需要重复多次的加样和洗板操作,容易掺杂较多的人为操作因素,从而对结果造成一定的影响,导致漏诊[7-8]。且 ELISA 检测的灵敏度也较差,加之隐匿性 HBV 感染患者可能存在基因突变的现象[9-10],因此寻找一种对结果影响小、灵敏度更高的方法以降低漏诊或者隐匿性 HBV 的情况出现很有必要。
CIA 是一种全自动化操作的 HBV 感染检测方法,其可以避免因人为操作而对结果产生的误差,从而相较于 ELISA 具有更高的准确度。同时,CIA 是检测抗原和抗体免疫结合反应的一种 HBV 检测方法,其可以对微量的抗原和抗体进行免疫标记和定量检测,从而可以极大地提高检测的灵敏度[11-12]。本研究中,在对样本进行了 CIA 检测之后,同时对 HBsAg(-)、HBcAb(+)样本做了进一步的筛查,以检验是否存在漏诊隐匿性 HBV 的情况。HBcAb是 HBV 感染患者体内比较稳定的抗体,HBcAb(+)的出现说明患者可能处在乙肝的慢性感染期或者恢复期,此时 HBV 病毒复制水平也较低,导致 HBsAg 浓度也较低,可能未达到试剂可测水平,从而产生病毒隐匿性,出现漏诊的情况。本研究结果显示,CIA 检测阳性率为25.00%,高于普通水平,分析原因可能与样本选择的差异以及样本量较小存在关联。而复筛及 HBV DNA 检测结果显示,HBsAb(+)HBeAg(+)HBcAb(+)模式 HBV DNA 阳性率最高,且整体阳性率也偏高,说明 CIA 检测存在漏诊的现象。刘晓红等[10]采用 HBV DNA 检测复筛 CIA 检测发现的 HBsAg(-)、HBcAb(+)样本也显示,在该类样本中存在隐匿性 HBV 感染的可能,且发生风险随HBcAb反应性 S/Co 值升高而升高,与本研究结果相似。有研究[13]显示,隐匿性 HBV 的出现,一个重要的原因可能是存在基因的突变,而HBsAb(+)HBeAg(+)HBcAb(+)模式的最高阳性率也表明,HBeAg(+)按照常规应该是有 HBsAg,但这种模式中 HBsAg 却为(-),说明其不存在或者水平极低,这也表明隐匿性 HBV 患者可能存在基因的突变,与李韦杰等[14-15]的研究结果相似。对复筛中 ELISA、CIA 检测结果进行分析显示,与 ELISA 比较,CIA 检测灵敏度、特异度明显提升,说明 CIA 检测可以提升对隐匿性 HBV 感染的诊断价值。
综上所述,CIA 对 HBV 感染的检测灵敏度较高,但还是存在隐匿性 HBV 的可能性,对于检测中 HBsAg(-)、HBcAb(+)的患者需做进一步的核酸检测,以降低漏诊情况的发生。本研究选取病例数较少,可能会对结果造成一定的影响,在后续研究中,需扩大病例数进行更加具有代表性的研究;同时,虽然进行了初筛和复筛,但仍然存在漏诊的病例,在后续研究中,需进行联合检测方法的研究或者寻找新的生物标志物来进一步提高隐匿性 HBV 感染检测诊断率。
[参考文献]
[1] Fukano K,WatashiK.From the Establishment of HepatitisB Virus Cell Culture Systems to Drug Discovery[J].YakugakuZasshi,2019,139(1):81-87.
[2] Mak LY,Wong DK,Pollicino T,et al.Occult hepatitisB infection and hepatocellular carcinoma: Epidemiology, virology, hepatocarcinogenesis and clinical significance[J]. J Hepatol,2020,73(4):952-964.
[3]庞栋,姜莹,张翙,等.电化学发光免疫分析法联合核酸检测在酶联免疫吸附法双试剂 HBsAg+/-献血者归队筛查中的应用[J].广西医学,2018,40(19):2346-2348.
[4] Luo L,Zhou X,Pan Y,et al.A simple and sensitiveflow injection chemiluminescence immunoassay for chloramphenicol based on gold nanoparticle-loaded enzyme[J].Luminescence,2020,35(6):877-884.
[5]中华医学会感染病学分会,中华医学会肝病学分会.慢性乙型肝炎防治指南(2019年版)[J].中华肝脏病杂志,2019,27(12):938-961.
[6] Tang Y,Liu X,Lu X,et al.Occult Hepatitis BVirus Infection in Maintenance Hemodialysis Patients: Prevalence and Mutations in "a" Determinant[J].Int J Med Sci,2020,17(15):2299-2305.
[7] Ye X, Li T, Li R, et al.Molecular characteristics ofHBV infection among blood donors tested HBsAg reactive in a single ELISA test in southern China[J].BMC Infect Dis,2021,21(1):83.
[8] Adeleke AS,Fasola FA,FowotadeA.ComparativeAnalys is of Rapid T es t and Enzym e L inked Immunosorbent Assay for Screening of Blood Donors for Hepatitis B Surface Antigen Seropositivity[J].West Afr J Med,2021,38(1):19-23.
[9]李奇,张凯,思兰兰,等.隱匿性 HBV 感染患者HBVS 基因突变特点及突变病毒株致瘤性研究[J].传染病信息,2019,32(3):208-214.
[10]刘晓红,单颖,孙朝庆,等.HBsAg 阴性伴HBcAb阳性+患者血清 HBV-DNA 含量检测对隐匿性乙型肝炎病毒感染的检出价值[J].陕西医学杂志,2021,50(3):362-365.
[11]邓中凤,陈萍,邹杨.隐匿性乙型肝炎病毒感染血液透析患者的分子特性及转归[J].肾脏病与透析肾移植杂志,2020,29(4):328-332.
[12]崔晓蕾.血站 HBV 筛查 ELISA 阴性 NAT 阳性标本的确认结果分析[J].中国输血杂志,2019,23(3):251-254.
[13]何成山,马晨芸,陆志成.化学发光免疫分析法检测HBcAb阳性、HBsAg 阴性血清中隐匿性乙型肝炎病毒感染的分析[J].标记免疫分析与临床,2019,26(1):130-133,172.
[14]李韦杰,徐东平,韩佳琪,等.乙型肝炎自然进程中血清 HBV RNA 的动态变化及其与肝组织 HBV cccDNA的关系[J].标记免疫分析与临床,2019,26(9):1445-1451.
[15]周怡,史恩溢,曹谊,等.HBsAg 阴性献血者隐匿性 HBV感染的血清学特征及其与病毒载量的关系[J].临床输血与检验,2017,19(6):570-573.
(收稿日期:2021-07-23)

