基于体外药效研究复方夏枯草颗粒的制备工艺*
黄艳萍,郭殊玮,刘 微,廖万忠,蒋伟哲,付书婕
(广西医科大学药学院,南宁 530021)
复方夏枯草颗粒的处方来源于广西壮要方医院,由夏枯草、连翘、槐花、甘草四味药组成,具有清肝明目、软坚散结、活血消瘿之功效,多年的临床应用显示该方剂对各类亚急性、慢性甲状腺炎、淋巴结节、乳腺增生、痔疮肿痛等具有良好疗效。为方便患者服用,促进中药方剂的临床应用,拟将原方汤剂开发为复方颗粒剂,在早期研究对人甲状腺癌B-CPAP细胞抑制作用的基础上,进一步优化提取工艺,并依照颗粒剂的制剂工艺要求进行成型工艺研究,以期为该传统方剂进一步的药效及作用机制研究提供质量稳定的颗粒剂。
1 仪器与材料
1.1 仪器
酶标仪(美国Biotek Synergy H1);超净工作台(ESCO OptiMair);CO2培养箱(美国Thermo);倒置荧光显微镜(Leica DMi8);Agilent 1260 Infinity液相色谱仪和G1314F紫外检测器;十万分之一分析天平(Mettler-Toledo XS205DU);超声波清洗仪(上海冠特SG3300HPT)。
1.2 药材、细胞与试剂
夏枯草(批号:200401)、连翘(批号:190901)、槐花(批号:200501)、甘草(批号:200301)均购于广西蓝正药业;迷迭香酸对照品(批号:111871-202007,含量以98.1%计);连翘苷对照品(批号:110821-201816,含量以95.1%计)均购自中国食品药品检定研究院;甲状腺癌B-CPAP细胞购自中国科学院上海细胞库;RPMI-1640培养基(Gibco);胎牛血清(Gemini,批号:A15H74K);CCK-8试剂盒(尚宝生物,批号:202104);PBS、胰蛋白酶、青链霉素混合液均为Solarbio。
2 方法与结果
2.1 复方夏枯草颗粒处方提取物对甲状腺乳头状癌细胞B-CPAP的抑制作用
2.1.1供试品溶液的配制 称取处方比例药材,分别用0%、20%、35%、50%、65%、80%乙醇回流提取2次,每次加12倍量溶媒回流1 h;合并两次提取液,65℃减压浓缩至一定稠度后,转移放入烘箱,60℃干燥至干膏。刮取干膏,充分研磨成粉后密封储存备用。每个浓度的乙醇提取重复3次。
精密称取各干膏粉约0.2 g,加入10 mL PBS,超声30 min使充分溶解,过滤,吸取5 mL转移到10 mL容量瓶内,PBS定容,混匀。细胞给药前用0.22μm微孔滤膜过滤除菌后,用完全培养基稀释至1 mg/mL。
2.1.2细胞抑制率检测 取处于对数生长期且生长状态良好的B-CPAP细胞[1-2],调整细胞浓度为6×104个/mL(通过细胞个数优选实验得出的最适细胞浓度),以100μL孔接种于96孔板中(为避免边缘效应,最外一圈不接种细胞,每孔加100μL PBS),置于37℃恒温、5%CO2饱和湿度培养箱中培养24 h,待细胞贴壁后加药;每组设6个副孔,吸弃旧培养基,每孔加100μL已配制好的含药培养基(1 mg/mL),培养箱中培养24 h、48 h后取出,倒置显微镜下观察后,吸弃含药培养基,每孔加入含10%CCK-8的无血清培养基100μL,继续在培养箱中孵育2 h后于酶标仪490 nm波长下检测OD值。按下列公式计算抑制率:细胞生长抑制率=(对照组OD平均值-实验组OD平均值)/(对照组OD平均值-空白组OD平均值)×100%。通过抑制率大小来确定最佳醇提浓度,见表1、图1。
由表1和图1可知,不同浓度的处方醇提物分别处理B-CPAP细胞24 h和48 h后,35%和50%醇提物对细胞的抑制作用最强,作用24 h时,抑制率分别为85.9%、86.05%;作用48 h时,抑制率分别为93.98%、93.32%。两个时间点的抑制率比较,差异无统计学意义(P>0.05),可认为在作用时间为24 h、48 h时,35%和50%醇提物对B-CPAP细胞的抑制作用相同。

图1 不同浓度乙醇提取物对甲状腺癌细胞B-CPAP增殖的影响

表1 不同乙醇浓度提取物对人甲状腺癌细胞增殖的抑制率 n=6
2.2 复方夏枯草颗粒处方提取物中指标性成分的含量测定
2.2.1色谱条件 色谱柱:Inertsil ODS-3柱(250 mm×4.6 mm,5μm),流动相:乙腈(A)-0.1%甲酸(B),梯度洗脱(0~25 min,20%A→35%A;25~35 min,35%A→20%A;35~40 min,20%A)[3-4],流速1.0 mL/min,检测波长:278 nm,柱温:30℃,进样量:5μL。
2.2.2溶液制备(1)混合对照品溶液制备:精密称定迷迭香酸和连翘苷适量,分别置于两个10 mL容量瓶中,用甲醇稀释成含迷迭香酸1.28 mg/mL含连翘苷1.60 mg/mL的单标储备液。再分别精密吸取上述两种单标储备液各5 mL于10 mL量瓶中,甲醇定容至刻度,摇匀,制成含迷迭香酸0.64 mg/mL、含连翘苷0.80 mg/mL的混合对照品溶液。(2)供试品溶液制备:精密称定各提取物粉末约1 g,置具塞锥形瓶中,精密加入25 mL的50%甲醇,称定重量,超声(250 W,40 kHz)30 min,放冷,再称重,50%甲醇补足减失重量,摇匀,滤过,取续滤液,过0.22μm滤膜,即得。(3)阴性样品溶液制备:精密称取缺夏枯草和连翘的阴性样品1 g,制备方法同供试品溶液。
2.2.3系统适用性试验 按照“2.2.1项”下的色谱条件进样测定混合对照品溶液、供试品溶液、阴性样品溶液,色谱图见图2。结果显示:迷迭香酸和连翘苷的保留时间分别约为16.5 min和19.1 min,阴性样品无干扰,迷迭香酸和连翘苷与相邻杂质峰分离良好,理论塔板数按连翘苷峰计不低于3 000,按迷迭香酸峰计不低于6 000,均符合规定。
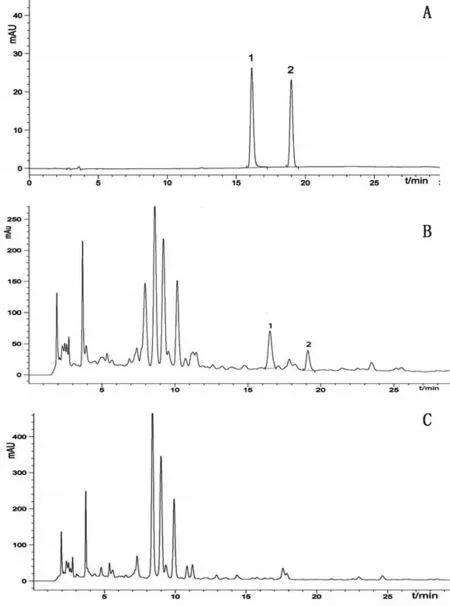
图2 对照品和提取物供试品HPLC图
2.2.4线性关系考察 分别精密吸取“2.2.2项”下的混合对照品溶液适量,加甲醇稀释成迷迭香酸(0.04 mg/mL、0.08 mg/mL、0.16 mg/mL、0.24 mg/mL、0.32 mg/mL、0.64 mg/mL)和连翘苷(0.05 mg/mL、0.10 mg/mL、0.20 mg/mL、0.30 mg/mL、0.40 mg/mL、0.80 mg/mL)的系列标准溶液,按照“2.2.1项”下的色谱条件进样测定。以对照品峰面积(Y)为纵坐标,对照品浓度(X,mg/mL)为横坐标,绘制标准曲线,结果见表2。结果表明,迷迭香酸在0.04~0.64 mg/mL,连翘苷在0.05~0.80 mg/mL范围内与峰面积呈良好的线性关系。

表2 回归方程与线性范围
2.2.5不同乙醇浓度提取物中指标性成分的含量测定 按照“2.2.2项”下方法将“2.1.1项”下不同浓度乙醇提取的干膏粉制成供试品溶液,每组平行制备3份,以迷迭香酸和连翘苷转移率为指标,为最佳乙醇提取浓度的选择提供参考,见表3。
由表3可知,50%醇提物中的迷迭香酸转移率最高,其次是35%醇提物;连翘苷在高浓度醇提物中的转移率更高,在35%和50%醇提物中的转移率较低,但也达到了80%以上,这与对B-CPAP细胞的抑制率趋势并不一致,说明在对甲状腺癌B-CPAP细胞的抑制作用中,连翘苷并不是处方中最重要的有效成分,其可能与其它成分共同发挥抑癌作用。
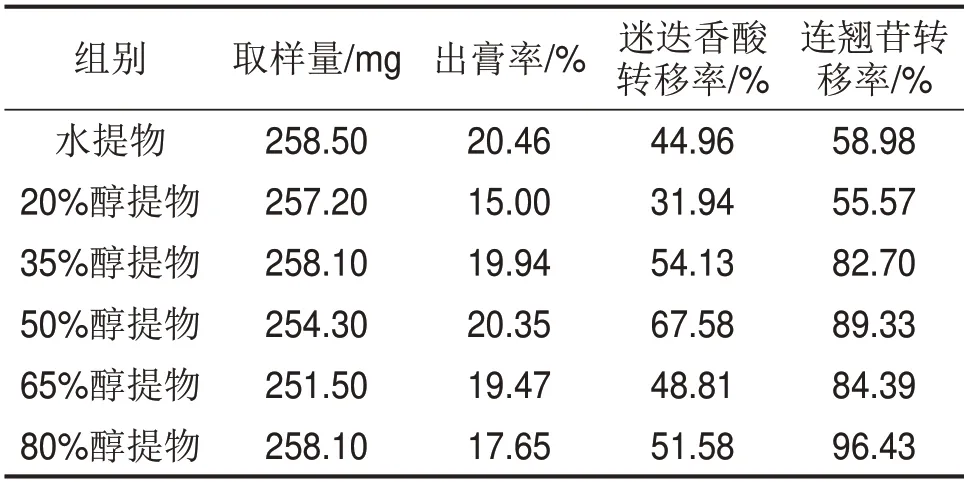
表3 不同乙醇浓度提取物中迷迭香酸和连翘苷的转移率
2.3 最佳乙醇提取浓度确定
由细胞实验可知,35%和50%醇提物对B-CPAP细胞的抑制作用最强,且二者差异无统计学意义。通过指标性成分的含量测定发现,迷迭香酸在50%和35%醇提物中的转移率较高,而连翘苷的转移率与对B-CPAP细胞的抑制率没有显著一致性。主要基于对细胞的抑制作用选择,以及尽量减少提取溶剂中乙醇的含量,综合考虑,选取35%乙醇作为复方夏枯草颗粒处方的最佳提取溶剂。
2.4 不同给药浓度的35%醇提物对人甲状腺癌BCPAP细胞增殖的抑制作用
精密称取35%醇提物粉末20 mg,加入2 mL PBS,超声溶解,过0.45μm微孔滤膜,备用;细胞给药前用0.22μm微孔滤膜过滤除菌后,用完全培养基稀释至1 mg/mL的母液,其它给药浓度用此母液做梯度稀释,补充溶剂为用PBS和完全培养基按1∶9稀释的溶液。
由表4可知,随着药物浓度增大、作用时间延长,抑制作用越大,说明35%醇提物对人甲状腺癌B-CPAP细胞有时间和浓度依赖性,表现出明显的量—效和时—效关系,24 h、48 h的IC50分别为0.69 mg/mL、0.56 mg/mL。
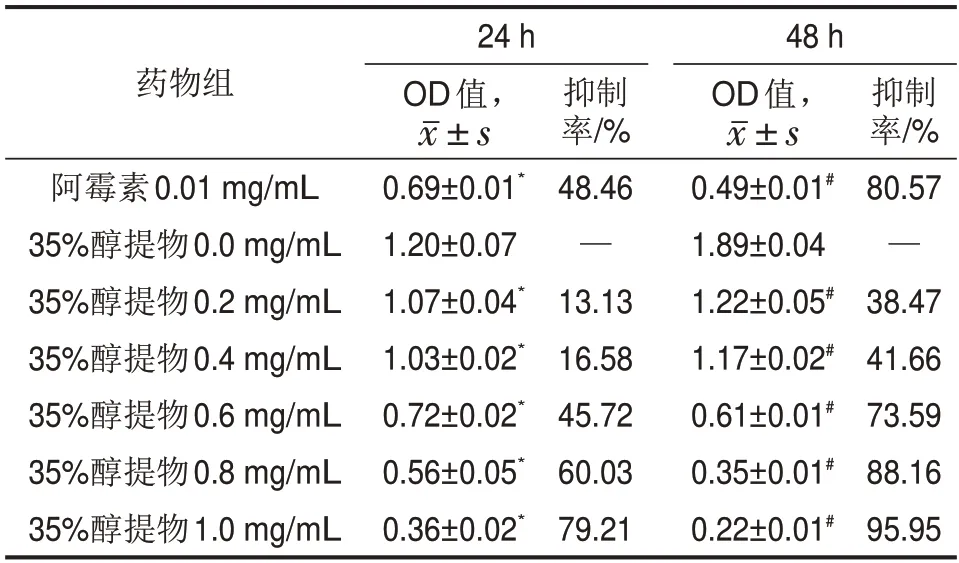
表4 不同浓度35%醇提物对人甲状腺癌B-CPAP细胞不同作用时间的OD值及抑制率 n=6
2.5 提取工艺研究
2.5.1浸泡条件考察 浸泡使药材充分湿润、膨胀,使其有效成分易于溶出,并可避免蛋白质凝固及淀粉糊化。通过测定药材吸水率,确定加水量及浸泡时间。吸水率=(药材湿重-药材干重)/药材干重×100%。如图3所示,0~30 min药材吸水率增加最快,30 min时为168.2%,30 min后吸水趋势减缓,60 min时为205.1%,即吸水量为药材的2.05倍。为节约时间,增加效率,选择浸泡30 min,加水量浸过药材2 cm左右为宜,约为12倍量水。

图3 药材吸水率与浸泡时间关系
2.5.2提取工艺研究以35%乙醇为提取溶剂,采用L9(34)正交表进行正交试验,考察液料比、提取时间、提取次数3个因素。按处方比例称取药材,按正交设计表进行提取,每组做3个平行试验,各项指标计算平均值[5-6]。通过细胞实验发现,迷迭香酸转移率和对细胞的增殖抑制趋势较为一致,所以以迷迭香酸含量和综合评分(综合评分=迷香酸含量×0.4+连翘苷含量×0.4+干膏率×0.2)为分析指标,选择最佳提取条件,见表5、表6。
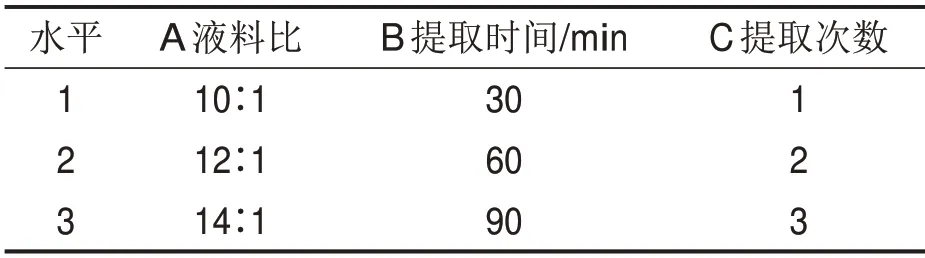
表5 正交试验因素水平
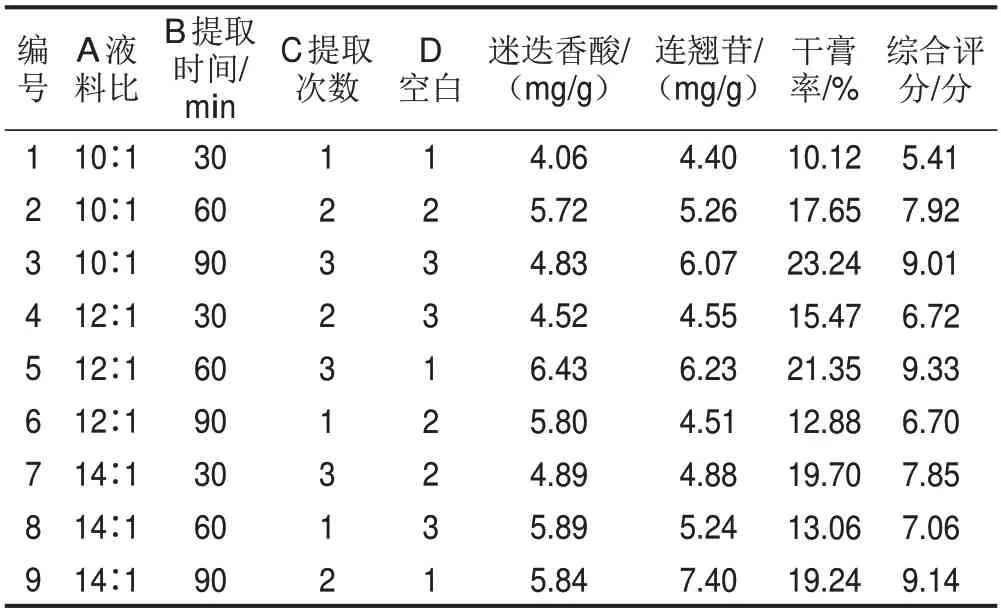
表6 正交试验表及实验结果
极差可以反映各因素对指标的影响程度,由表7对各因素3个水平均值的极差分析可知,迷迭香酸组中,3个因素的影响程度为B>A>C,其中B因素中水平2的均值(B2)最高,A因素中A2最高;综合评分组中,3个因素的影响程度为C>B>A,C因素中C3最高,各因素优选两个指标中的极差较大者,则最佳提取条件为A2B2C3,即加入12倍量35%乙醇,提取3次,每次60 min。
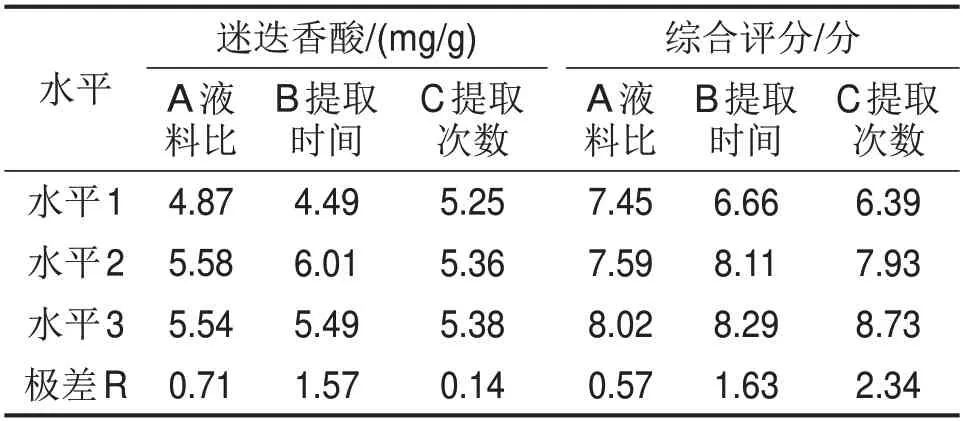
表7 迷迭香酸含量和综合评分的极差分析
2.6 最佳提取工艺验证
为了验证结果的准确性,保证工艺的稳定可行,称取处方量药材按照选定的最佳工艺重复3次试验。根据3次重复试验结果,表明该工艺稳定可行,见表8。

表8 工艺验证结果
2.7 成型工艺研究
本方的处方量药材约为35 g,提取率约为20%,则每次干膏粉服用量为7 g,一般口服颗粒剂剂量为10~15 g/包,则辅料加入量控制在3~8 g(药辅比1∶0.4~1∶1.1)为宜。
采用湿法制粒,制剂工艺步骤:中药提取物(干膏粉)+适当辅料→制软材→制颗粒→干燥→整粒。通过考察颗粒成型率、流动性、吸湿性、溶化性等指标对辅料进行筛选。
2.7.1干膏粉的制备 按处方比例称取药材,根据优选的最佳提取工艺进行提取、浓缩、干燥,烘干成干膏后粉碎备用(易吸湿,干燥柜内储存)。
2.7.2辅料的选择 预实验选择润湿剂(乙醇)的浓度分别为60%、70%、80%、90%,发现由于干膏粉含糖量较高,且易吸湿,黏性强,在用60%、70%、80%乙醇时,若用量少则较松散,加大用量则明显变黏,制粒时易堵塞筛孔;90%乙醇制得的软材较合适制粒,故本实验选择乙醇浓度为90%。
取“2.7.1项”下干膏粉约20 g,分别与糊精、可溶性淀粉两种常用辅料按照不同配比混匀,以90%乙醇作润湿剂制备软材,软材的软硬度标准为“手握成团,轻压即散”,筛选结果见表9。
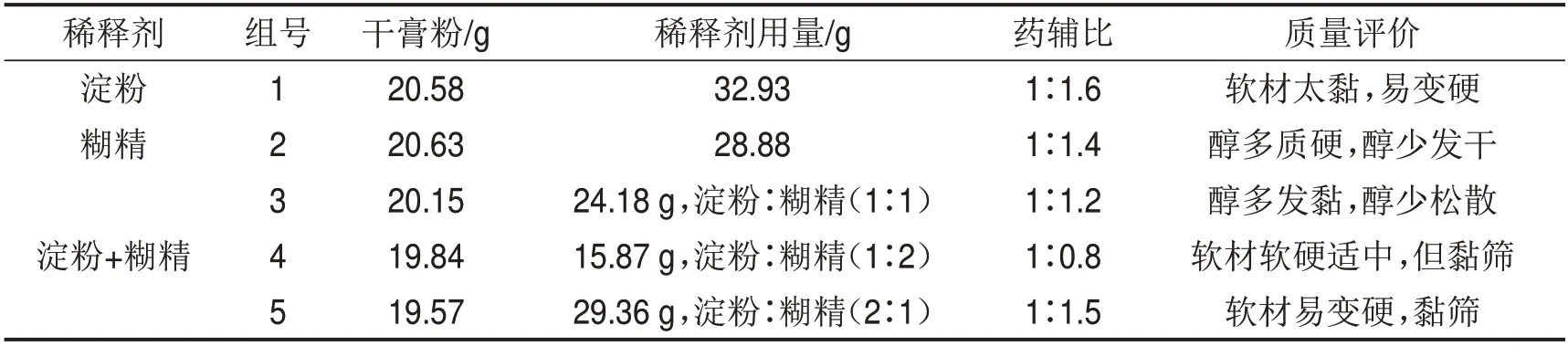
表9 辅料种类及配比筛选结果
2.7.3成型工艺考察评价指标 为优选复方夏枯草颗粒的最佳辅料及其配比,实验在各组软材质量的基础上,优选第2、3、4号组软材制粒,以成型率、流动性、吸湿性、溶化性为指标,考察最佳成型工艺,结果见表10。

表10 成型工艺指标评价表
根据制得的软材情况并结合表11的颗粒剂考察指标可知,单用糊精、复合辅料淀粉∶糊精(1∶1)和(1∶2)时制得的软材较易制备颗粒,通过比较3组颗粒的成型率、流动性、吸湿性和溶化性,发现4号组的成型率及流动性最好,3号组的吸湿性最大,各组都能在5 min内全部溶化,且4号组所用的辅料量最少,药辅比(1∶0.8)在1∶0.4~1∶1.1的合理范围内,综合考虑最佳辅料选择淀粉∶糊精(1∶2),乙醇浓度为90%。
2.8 放大验证试验
按照最佳提取工艺和成型工艺,制备3批复方夏枯草颗粒,按处方比例称取各味药材共约1 200 g,浸泡、提取、浓缩、干燥、粉碎后得浸膏粉,与适量辅料淀粉∶糊精(1∶2)混匀,喷以90%乙醇制软材,湿法制粒,过16目筛整粒,60°C干燥至恒重。
由表11可知,3批药材的平均出膏率为21.24%,制得的平均颗粒剂量为532.81 g,损失较小,颗粒收率较高,可进一步进行中试生产。
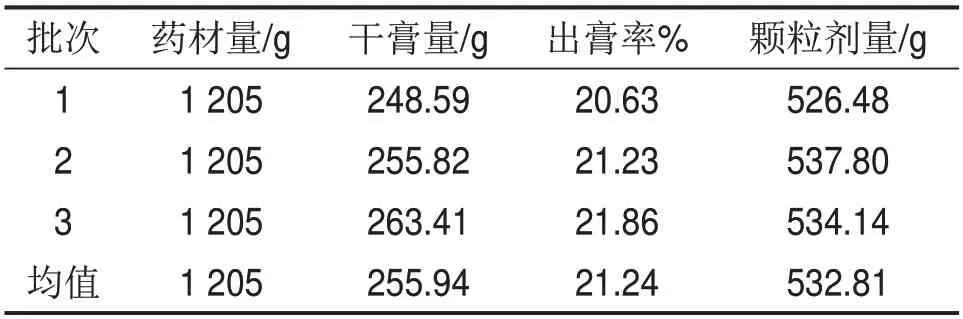
表11 3批颗粒剂的制备
3 讨论
本实验基于体外药效研究,发现35%和50%醇提物对人甲状腺癌B-CPAP细胞的抑制作用最强;并通过HPLC法测定处方不同乙醇浓度提取物中指标性成分的含量,发现50%和35%醇提物中迷迭香酸的转移率较高,而连翘苷的转移率与细胞抑制率趋势无显著关系,综合分析,确定最佳提取溶媒为35%乙醇。传统煎煮法为水提,不利于有效成分最大限度的溶出,本实验基于对甲状腺癌细胞的抑制作用,筛选出活性最强的提取物,以优化处方的提取工艺,增强处方的治疗作用。
处方中的君药夏枯草散结消肿、疏肝解郁,其主要成分迷迭香酸可抑制多种人源肿瘤细胞增殖和诱导肿瘤细胞凋亡[7],与本实验前部分的研究结果相契合,提取物中迷迭香酸的含量越高,对细胞的抑制作用越强。连翘具升浮宣散之力,清热解毒,软坚散结,其专属性成分连翘苷、连翘酯苷具有显著的生物学活性,各成分之间发挥协同作用而用于不同疾病的治疗[8]。本实验发现,处方中连翘苷的含量与其对细胞的增殖抑制没有明显的浓度依赖性,连翘苷是否是处方中抗甲状腺癌的活性成分,还有待继续研究。
本实验采用多指标综合评价的方法,将体外活性研究与指标性成分的含量测定综合考察,优化中药提取工艺以提高药物疗效,有利于筛选出中药复杂成分中的重要活性成分。将原方汤剂改进为方便携带服用的颗粒剂,在保证原有功效的基础上,优化提取工艺,确定最佳提取条件为加入12倍量35%乙醇,回流提取3次,每次60 min,煎煮前浸泡30 min;最佳成型工艺为辅料淀粉和糊精(1∶2),药辅比约1∶0.8,90%乙醇为润湿剂,所制得的颗粒符合颗粒剂的各项检查标准。

