双功能零维碳基纳米材料碳量子点的设计合成及应用*
傅 政,常帅兵,贾丰春
(河南工学院 材料科学与工程学院,河南 新乡453003)
碳量子点作为一类新生零维碳基纳米材料,由于具有光学性能好、可协调的表面功能性、极好的水溶性及良好的生物相容性,备受研究者关注。但原始制得的碳量子点荧光显色单一,不利于细胞多色成像;缺乏对目标的特殊选择性,许多应用受到限制。
铜离子作为人体第三丰富的微量元素,在许多生理过程中发挥着重要作用。铜离子含量失衡往往会导致许多疾病的发生[1,2],因此,对Cu2+进行高选择性、灵敏性检测,对人类健康和环境保护十分重要。
本文采用4-BTSC对合成的原始碳量子点表面结构进行修饰,成功设计并合成了具有细胞多色成像及铜离子高效检测的双功能碳量子点。
1 材料与方法
1.1 药品及仪器
药品:异硫氰酸丁酯(99%)购自源叶生物技术有限公司(上海);EDC(1-乙基-3-(3-二甲基氨基丙基)碳二亚胺盐酸盐))和NHS(N-羟基琥珀酰亚胺)购自安耐吉化学有限公司(上海);乙二胺四乙酸二钠、水合肼(85%)、无水乙醇及常见金属阳离子由国药化学试剂有限公司(上海)提供。水为自制超纯水,缓冲体系采用PBS缓冲体系(0.01 M,pH=7.4)。
仪器:Cary Eclipse荧光光谱仪(美国);高分辨透射电子显微镜(JEOL,日本);傅里叶变换红外光谱仪(FT-IR)(PerkinElmer, 美国);紫外-可见光谱仪(UV-vis)(TU-1810,中国); Leica激光共聚焦荧光显微镜(TCSSP5,德国)。
1.2 制备4-BTSC
合成[3]:将15 mmol异硫氰酸丁酯溶解于10 mL无水乙醇中,冰浴下,将2.3 mL水合肼逐滴加入。然后,保持温度为10℃,反应1 h。减压下蒸发溶剂,得到粗4-BTSC。再利用CH2Cl2-石油醚重结晶,得到纯品4-BTSC。
1.3 制备BTSC-CDs
50 mL高压反应釜内加入30 mL 含0.1 g mL-1乙二胺四乙酸二钠盐的超纯水溶液。然后,将其放入加热器中加热至180 ℃,反应10 h。冷却离心,上清液过膜,滤液干燥,得到CDs。
取20 mL 超纯水加入0.2 g CDs,再分别加入10 mL 20 mM EDC和5 mL 20 mM NHS,37 ℃、磁力搅拌器下反应0.5 h。随后,加入5 mL 5.0 g L-14-BTSC反应3 h,反应后的产物即为BTSC-CDs。将BTSC-CDs用纤维膜透析,干燥,即得到固体BTSC-CDs。
1.4 荧光检测
1.5 mL离心管中分别加入200 μL 0.01 g L-1BTSC-CDs和适量的Cu2+,PBS定容至1.0 mL。再在室温下反应5 min后,在360 nm的激发波长(λex)下记录荧光光谱。
1.5 BTSC-CDs的细胞毒性
采用MTT法评估BTSC-CDs的细胞毒性。方法:将HeLa接种在微量滴定板中,保持细胞浓度为5×104/孔。然后,加进DMEM培养基,37 °C 、5% CO2环境下培养24 h。接着,再加入BTSC-CDs溶液,继续培养24 h后,将20 μL 5 g L-13-(4,5二甲基噻唑-2基)-2、5-溴化二苯基四唑(MTT)滴入每孔,进一步培养4 h。PBS清洗,加入150 μL 二甲基亚砜(DMSO),室温下震荡5 min,570 nm处测吸光度,则细胞的存活率为:
Cell viability(%)=(ODt/ODc)×100%
ODt和ODc分别为加入BTSC-CDs培养后实验组和对照组的吸光度值。
1.6 细胞成像
采用HeLa和KYSE410细胞研究细胞成像。
对照组:37℃,HeLa和KYSE410细胞在培养基里培养24 h,然后 PBS缓冲溶液洗3次,细胞成像。
测定组:培养好的HeLa和KYSE410细胞里加入浓度为0.1 g L-1BTSC-CDs溶液,37 ℃孵育8 h,同样洗3次,观察荧光图像。然后,将30μM Cu2+加入吸收了BTSC-CDs的HeLa和KYSE410细胞里再孵育4 h,洗涤后在激光共聚焦荧光显微镜下分析样品。
2 结果与讨论
2.1 BTSC-CDs表征
碳量子点表面的活性基团,对目标物的检测影响非常大。为了证实碳量子点的表面结构被4-BTSC成功修饰,对其进行了高分辨透射电镜、FT-IR、XPS、UV-vis表征。
用高分辨透射电镜表征发现,修饰后的碳量子点在水里外貌近似球形,且呈单分散性(图1),表明其在水里溶解性极好。其粒径主要分布在1.8~4.2 nm范围内,平均粒径2.9 nm。
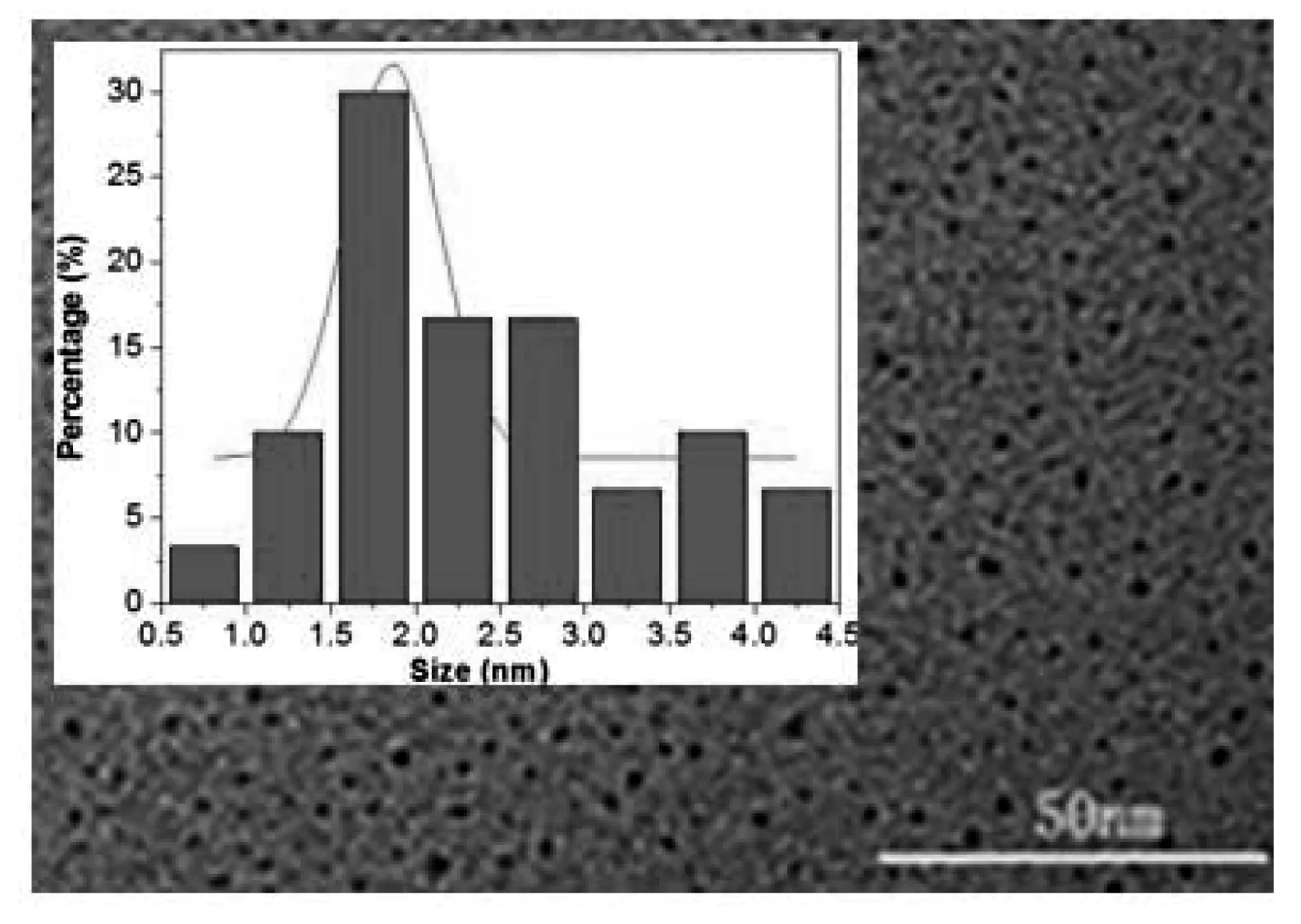
图1 BTSC-CDs的高分辨透射电镜图谱(插图:粒径分布图)
用红外表征,结果显示(图2(b))原始CDs N-H/O-H和C=O的伸缩振动峰分别分布在3426 cm-1和1622 cm-1处,而-COOH中O-H的伸缩振动峰和O-H变形峰则分别处在3055 cm-1和1324 cm-1,表明CDs表面富含-NH2、-COOH和-OH,水溶性极好。与CDs相比,BTSC-CDs红外光谱中(图2(c)),CDs在3426 cm-1和1622 cm-1处的峰值仍存在,但3055 cm-1处的峰值消失,表明CDs的-COOH转变为其他基团。BTSC-CDs在1298 cm-1处(υ-NHC=O)出现的新吸收峰,证实了这一结果,表明CDs表面的-COOH和BTSC的-NH2发生了酰胺反应。而来自4-BTSC(图2(a))3309 cm-1(υ-N-H)处的峰值,在BTSC-CDs红外图上只有微小的位置变动,移至3426 cm-1;其1493 cm-1、1230 cm-1、813 cm-1处的C=S弯曲振动和拉伸振动,C-S拉伸振动峰,在BTSC-CDs光谱中仍存在,证明BTSC成功对CDs表面结构进行了修饰。
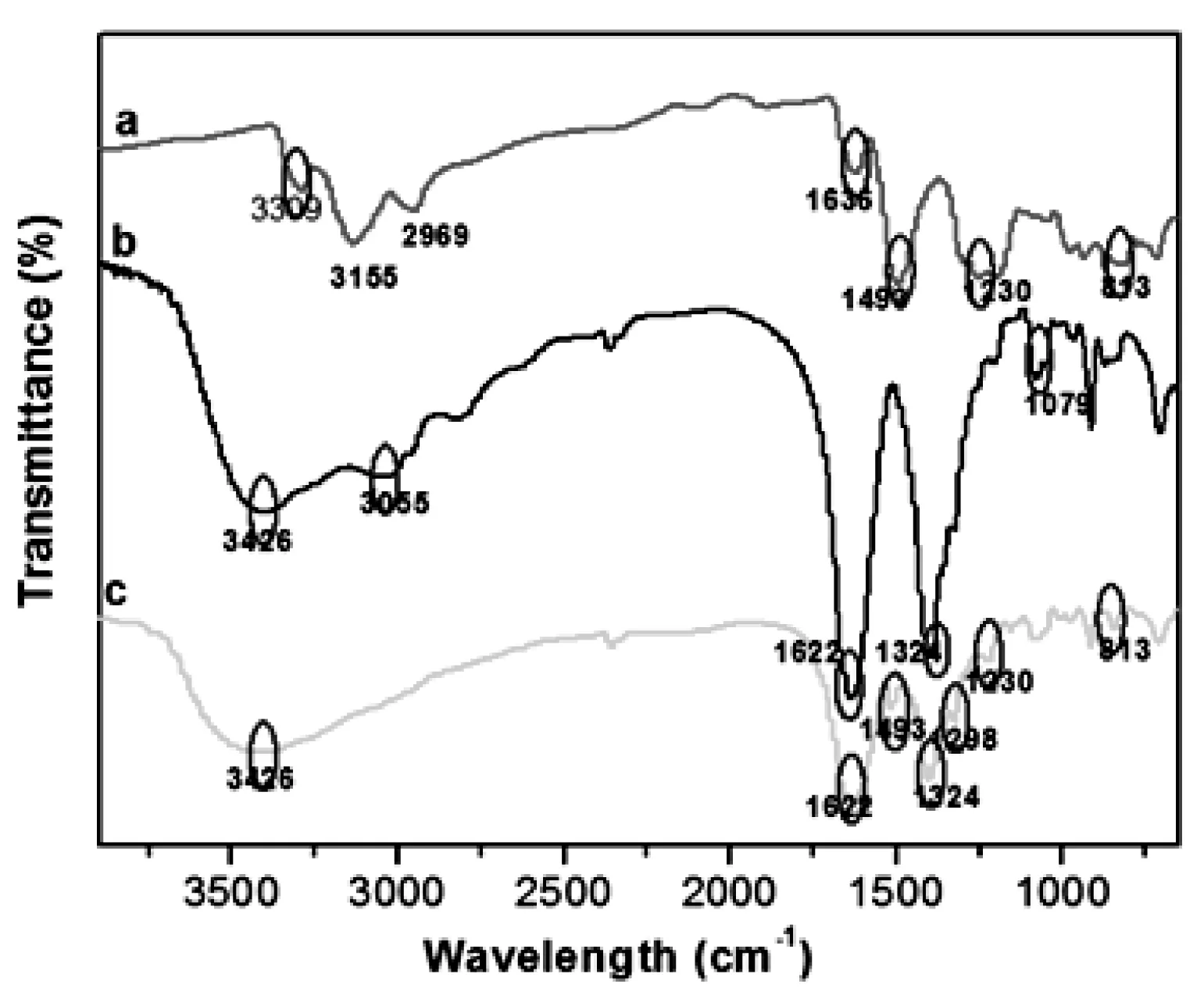
(a)BTSC;(b)CDs;(c)BTSC-CDs图2 红外光谱图
BTSC-CDs的XPS全谱图显示(图3),在157.1 eV 、223.0 eV 、285.5 eV、399.9 eV和531.7 eV处分别出现了五个峰值,它们分别归属于S2p、S2s、C1s、N1s和O1s。且元素在BTSC-CDs材料中的含量分别为2.3%(S)、14.7%(N)、20.2%(O)、62.8%(C),表明4-BTSC成功修饰在CDs上。
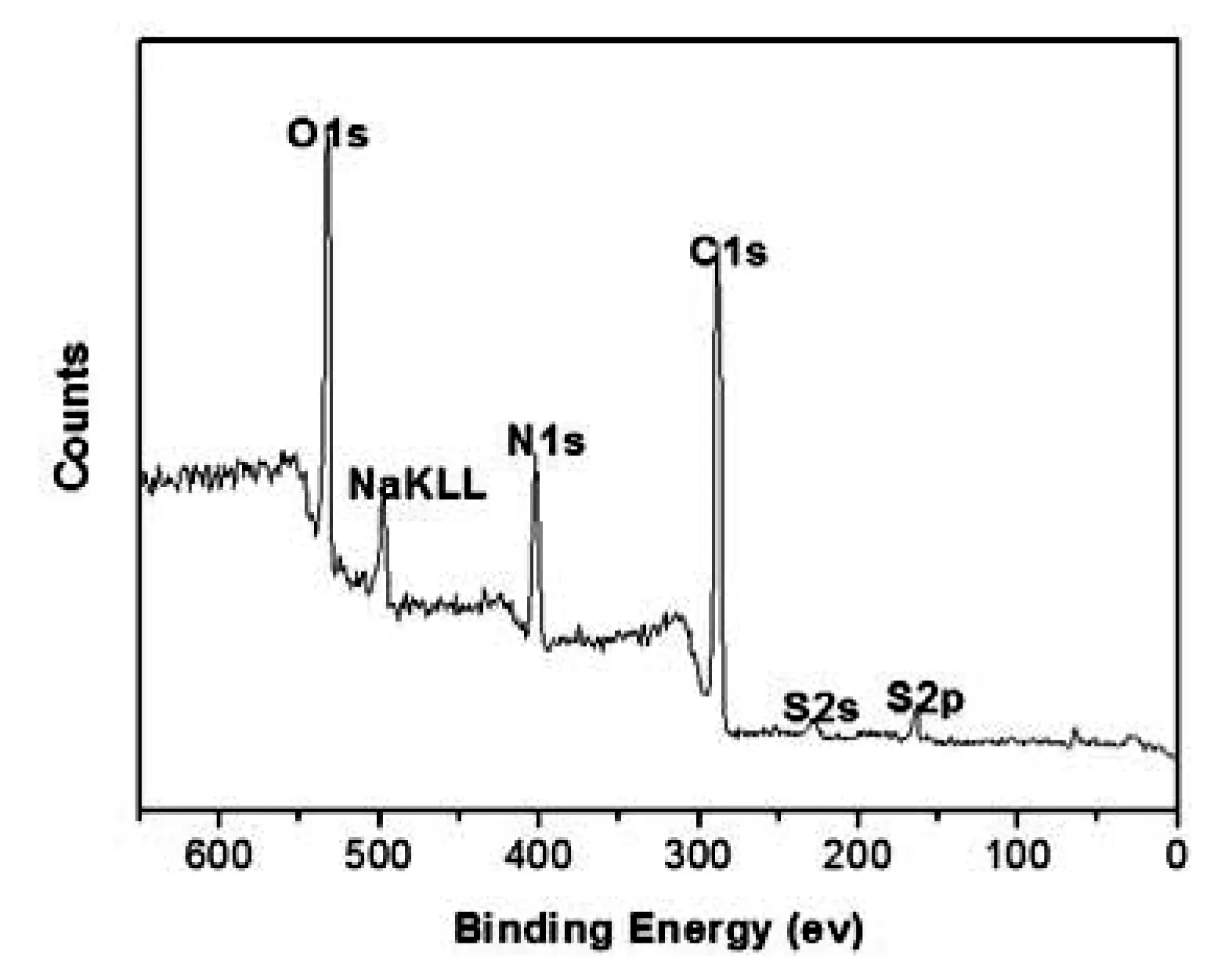
图3 BTSC-CDs的XPS全谱图
BTSC-CDs的UV-vis结果如图4,图谱里除了具有原始CDs的吸收峰外,在238 nm处又有了新的吸收峰,证实有新物质生成,说明BTSC和原始CDs成功键合在一起,实现了CDs的表面结构修饰。
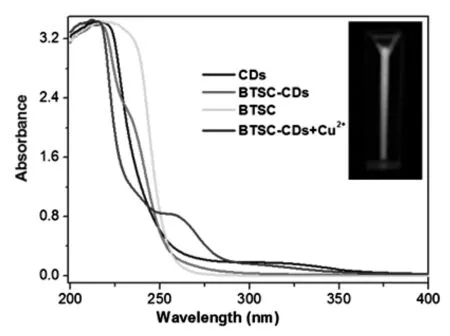
图4 紫外-可见光谱图
2.2 材料的光学性质
BTSC-CDs荧光谱图显示(图5),当λex在320~450 nm内,荧光发射具有波长依赖性。当λex从320 nm增加到450 nm时,最大发射峰(λem)从415 nm移动到510 nm,随着λex的增加λem红移比较明显,这可能是由于4-BTSC修饰到CDs表面导致其表面具有不同的发射位点引起的[4]。BTSC-CDs的最佳λex为360 nm,λem为450 nm。
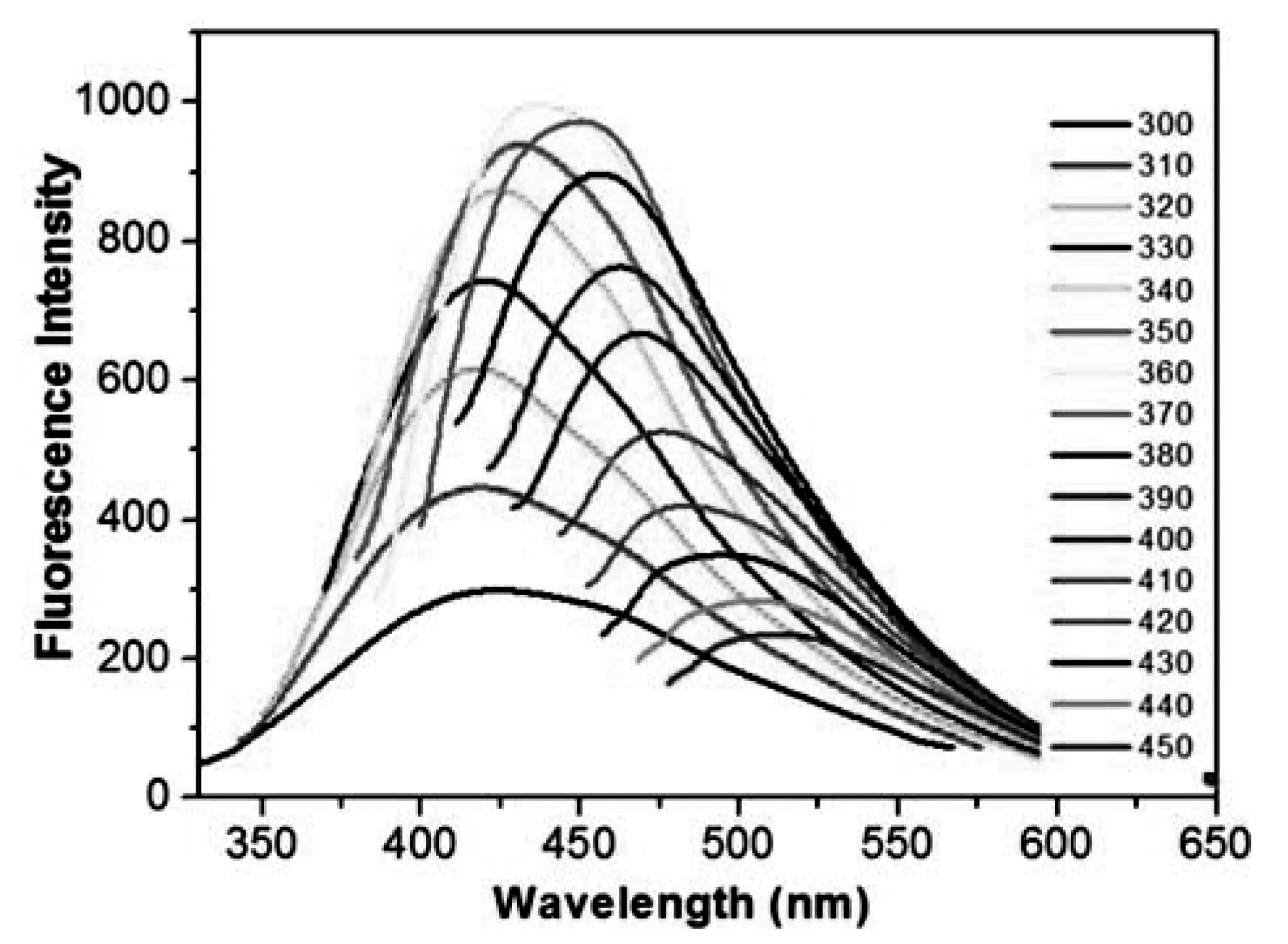
图5 BTSC-CDs的发射光谱
此外,对BTSC-CDs发光性能的影响因素酸碱度、缓冲体系和离子强度(根据氯化钠的浓度)进行了研究。发现当pH值由3增加到10时(图6(a)),BTSC-CDs的荧光强度变化不大。缓冲液对发光性能的影响如图6(b),BTSC-CDs处于PBS体系时,荧光相对较强。而在不同离子强度的溶液里,即使离子强度高达1.0 M时,BTSC-CDs的荧光强度变化也很小(图6(c))。以上结果均表明材料具有稳定的光学性能。
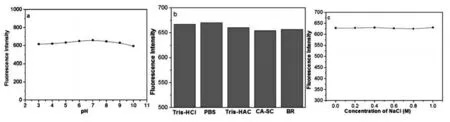
(a)酸碱度; (b)缓冲溶液; (c)离子强度图6 BTSC-CDs发光性能的影响因素
2.3 检测条件选择
为了获取最佳检测条件,分析了BTSC-CDs(0.01 g L-1)的用量、pH值、反应时间的影响(图7)。结果(图7(a))发现,刚加入100μL BTSC-CDs时,荧光强度变化较小;增加材料加入量,荧光响应增大。但是,当加入量由200μL增加到600μL时,荧光响应几乎不变,说明材料与Cu2+已完全反应。当材料加入量大于800μL时,荧光响应稍有升高,这可能是由于材料聚集自猝灭引起的。本文检测选BTSC-CDs的用量为200 μL。
pH值对检测的影响如图7(b)。当pH值由3增加到10时,荧光响应变化较小,但pH值过高时金属Cu2+易水解,及考虑后面的细胞实验,检测选择最佳pH值为7.4。
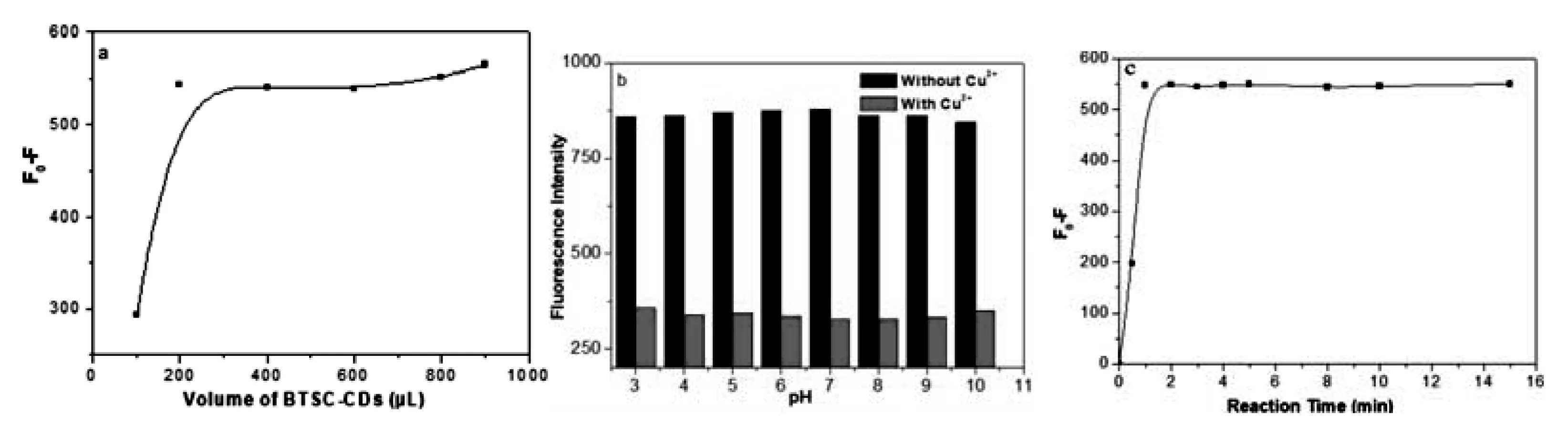
(a)BTSC-CDs用量 (b)pH (c)反应时间图7 Cu2+检测的影响因素
反应时间对检测的影响(图7(c))也表明,该材料对Cu2+响应速度很快,反应1 min和15 min响应变化不大,检测选择反应时间为5min。
2.4 检测的选择性与灵敏性
选择性。分别加入相同浓度(30.0 μM)的不同金属离子于BTSC-CDs溶液里,结果如图8(a),Cu2+可使材料的荧光明显猝灭,猝灭率达63.3%; Ag+、Hg2+、Fe3+对材料的荧光猝灭率分别为14.3%、11.7%和10.6%;而其他金属离子的荧光猝灭率均小于5.0%,该材料用于Cu2+检测具有高度选择性。将上述金属离子加入含有同浓度Cu2+的BTSC-CDs溶液里,共存离子对Cu2+的检测影响较小(图8(b))。说明材料可对Cu2+选择性检测。
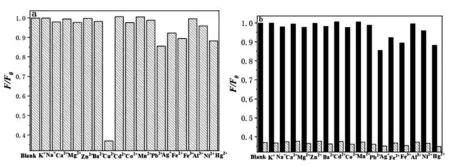
(a)加入常见金属离子材料荧光的变化;(b)干扰离子对Cu2+检测的影响(黑色框:未加入Cu2+;斜线框:Cu2+存在;实验条件相同)图8 Cu2+检测的选择性
Cu2+的检测机理。Cu2+具有空轨道,N原子有孤对电子,可与Cu2+强配位,且C=S键中的S、C=O键中的O也是Cu2+的有效配位点[5]。而BTSC-CDs结构中富含这些原子,均增强了BTSC-CDs和Cu2+的配位能力,它们之间发生配位反应可能导致BTSC-CDs荧光猝灭。而这一推测也通过Stern-Volmer方程得以证实。方程如下:
F0/F=1+Kqτ0[Q]=1+Ksv[Q]
F0和F分别为在BTSC-CDs中加入和未加入Cu2+时的荧光强度;[Q]是Cu2+的浓度;Kq为猝灭速率常数;τ0为未加入Cu2+时材料的荧光寿命;KSV为Stern-Volmer猝灭常数。
通过检测F0/F与加入[Cu2+]间的关系,可得到其Stern-Volmer方程为F0/F=0.9988+0.7190[Q]。其KSV常数为7.19×105L·mol-1。而BTSC-CDs的τ0为1.42×108s,Kq计算为5.06×1013L mol-1s-1(Kq=Ksv:τ0),明显高于各种类型猝灭剂的最大动态Kq值(2.0×1010L mol-1s-1)[6],表明检测Cu2+是基于静态的猝灭,是 BTSC-CDs和Cu2+之间形成了基态配合物引起[7]。此外,检测体系的UV-vis光谱也进一步证实了该推测(图4),在BTSC-CDs溶液中加入Cu2+后,光谱上显示在261 nm处出现了新的吸收峰,证明有新物质的产生,即BTSC-CDs和Cu2+之间发生了反应。
在材料溶液里加入不同浓度Cu2+,研究Cu2+检测的灵敏性,结果见图9(a),BTSC-CDs的荧光随着[Cu2+]的加大而逐渐减弱。当[Cu2+]在0~0.10 μΜ和4~50 μΜ(图9(b)和(c))范围内时,得到其线性方程分别为F0/F=1.0011+0.6568 [Cu2+](R2=0.9956)及F0/F=1.0987+0.0693 [Cu2+](R2=0.9985)。对空白样品进行平行检测,其检测限为5.05 nM,远低于美国规定的饮用水中Cu2+的最大允许浓度(20μM)[8],也大大低于或相当于其他检测Cu2+方法的检测限[9-14]。
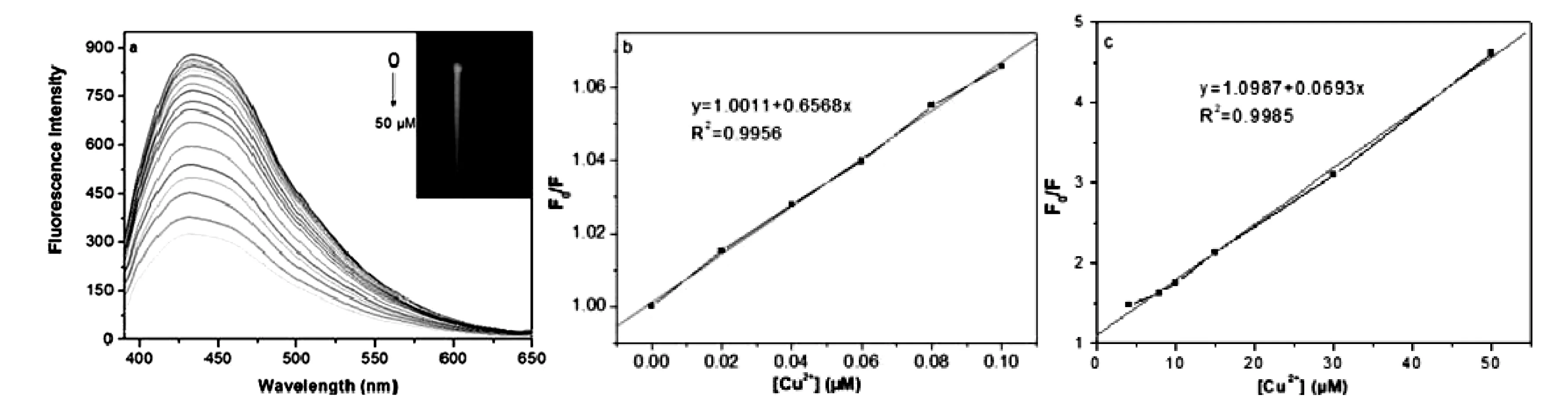
(a)BTSC-CDs的荧光随[Cu2+]的变化;(b)[Cu2+]=0~0.1 μM时,F0/F与[Cu2+]的关系;(c)[Cu2+]=4~50μM时,F0/F和[Cu2+]的关系图9 Cu2+检测的线性关系
2.5 细胞成像
为了对细胞成像,研究了BTSC-CDs的细胞毒性。研究结果显示(图10),采用浓度为0.1~0.5 g L-1BTSC-CDs 培养HeLa细胞24小时后,细胞存活率为91.8%。而增加浓度为1.0 g L-1、1.5 g L-1和2.0 g L-1时,细胞存活率仍分别达到87.5%、87.2%和86.7%,表明BTSC-CDs毒性低,细胞相容性好。
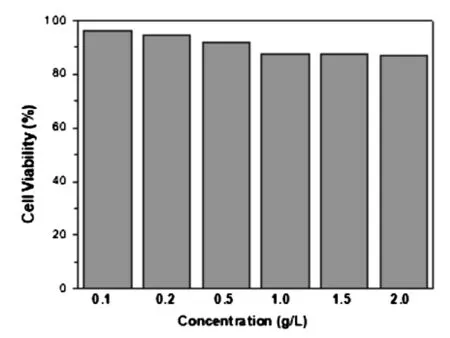
图10 BTSC-CDs细胞毒性实验
将BTSC-CDs加到HeLa、KYSE410细胞里孵育后,显微镜下发现,当λex分别为405 nm和488 nm时,细胞分别发出了蓝色(图11(d)、(h))和绿色荧光(图11(c)、(g))。说明BTSC-CDs进入HeLa、KYSE410细胞后,使二者分别发射出荧光。而对照组细胞则没有荧光信号发出(图11(b)、(f))。说明BTSC-CDs可用于细胞多色成像。
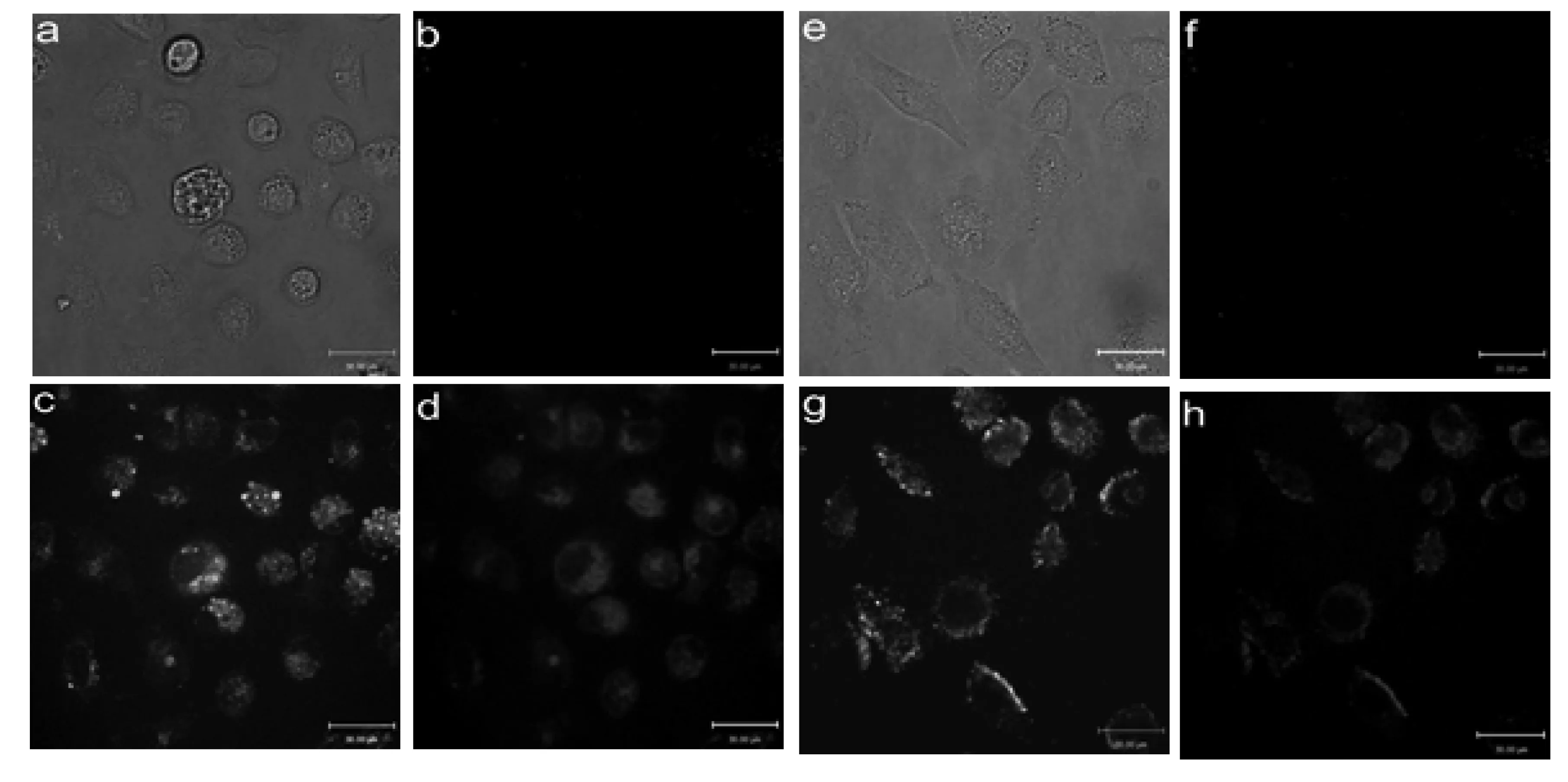
(a~d)KYSE410细胞;(e~h)HeLa细胞;((b、f)对照组;(a、e)明场;(d、h)λex=405 nm;(c、g)λex=488 nm)图11 细胞成像
3 结论
本文采用4-BTSC对零维碳基纳米材料CDs表面进行结构修饰,成功设计并合成了具有双功能的CDs。该材料不仅可用来简单、快速、双浓度范围及高效检测Cu2+,更重要的是它水溶性极好、毒性低、细胞相容性好,还可用于细胞多色成像。该研究对今后生物医学成像剂的开发及构建新型功能纳米材料具有指导意义。

