pH值演变对果蔬垃圾厌氧发酵效能的影响研究
石 川, 刘 越, 罗 娟, 吴厚凯, 王凯军*, 周岳溪,2.3,*
(1.清华大学 环境学院,环境模拟与污染控制国家重点实验室, 北京 100084; 2. 中国环境科学研究院环境污染控制工程技术研究中心, 北京 100084; 3.中国环境科学研究院环境标准与风险评估国家重点实验室, 北京 100084)
2021年,我国颁布的《“十四五”循环经济发展规划》强调了我国资源利用效率大幅提升的目标,明确了资源循环利用产业的未来发展趋势。同时,我国为应对气候变化、环境污染、能源资源紧缺等问题,做出了“二氧化碳排放力争2030 年前达到峰值,努力争取2060 年前实现碳中和”的目标承诺。在规划和政策推动下,高效处理生物质废弃物,资源化利用其富含的生物质能源资源,实现其可再生利用成为新的研究热点。中国每年约有1亿t的果蔬垃圾产生[1],但只有不到20%的果蔬废弃物能够得到适宜的处理处置。一方面,由于高含水量和易降解性的特性,果蔬垃圾不当处理易造成严重的环境问题,如恶臭和对土壤、水和空气的污染[2]。另一方面,通过厌氧发酵技术将果蔬垃圾进行处理,可实现天然气、电能等能量转化利用。据报道,95.6万t的生活垃圾经厌氧发酵技术处理后可转化为300×106Nm3甲烷,相当于北京市天然气消耗量的3.35%[3]。因此,在“十四五”生态环境保护重要时期,果蔬垃圾厌氧发酵性能的研究与提升具有重大意义。
厌氧发酵是一种绿色环保,符合可持续发展的废弃物处理技术。厌氧发酵过程包含有机物水解、酸化和产甲烷等3个阶段,最终实现有机物的降解、转化和循环利用。除产物甲烷外,厌氧发酵的发酵液富含酸化产物及营养物质,可用于农业生产。据研究,底物中65.8%的碳源存留在发酵液中[4],剩余碳源转化为甲烷或流失,可见以沼气为目标产物,资源利用率较低。比较而言,厌氧发酵所产的脂肪酸(Yolatile Fatty Acids)具有更高的能量密度,运储安全方便,具有更高的经济价值和更大的市场需求[5]。在此基础上,更多研究关注于厌氧发酵所产脂肪酸类产物的产能等生产应用。
为避免厌氧条件下甲烷的大量生成,采用pH值调控的手段可抑制甲烷生成并引导产生多种脂肪酸类产物[6]。pH值参数的变化决定体系内微生物群落的生态位,影响细胞内外酶活,进而调节不同酸化产物的代谢途径[7]。因此,为获得不同酸化产物的产量和产率,pH值调控是一种重要手段。Wang[8]等发现在pH值为8.0和10.0的条件下,酸化产物总量明显高于pH值 3.0和7.0的酸化产物产量。Chen[9]等发现以污泥为底物时,碱性条件pH 值10.0能够提高酸化产物产量达到最高值。另外,不同底物在不同pH值条件下,产物组分也表现出不同的形式。任南琪[10]等在以糖类废水为底物的高有机负荷环境中,大量且连续获得乙酸和乙醇混合产物,发现并提出乙醇型发酵类型。吴远远[11]等在果蔬垃圾厌氧发酵pH值调控4.0的条件下,首次发现大量乳酸的生成,产量可达10 g·L-1。经研究,pH值向碱性方向调控,是有助于乙酸和丁酸等产物生成的。pH值从4.0~4.5调节到4.4~4.9是有利于乙醇型发酵向丁酸型转变[12]。李永峰[13]等投加碳酸氢钠控制进水pH值在6.75~7.15范围内。20天后,系统处于混合型发酵类型,酸化产物组分为乙醇9.9%、乙酸23.9%、丙酸51.8%和丁酸14.4%。目前,针对果蔬垃圾厌氧发酵的pH值调控策略和发酵性能的研究还不完善,仍有研究空间去提升和导向酸化产物的生成。本研究通过比较果蔬垃圾不同pH值调控条件下的性能和细胞状态,分析酸、碱性果蔬垃圾厌氧发酵的优势,为果蔬垃圾厌氧发酵产物目标性转化和资源化利用提供依据。
1 材料与方法
1.1 试验材料
试验接种污泥为厌氧絮状污泥取自北京市高碑店污水处理厂厌氧池,取回后放置于35℃ 环境保存。接种污泥初始性质经检测如下:总固体(TS)为22.11±1.50 g·L-1;总挥发性固体(VS)为11.93±0.68 g·L-1;总化学需氧量(TCOD)为28325±18.6 g·L-1;溶解性化学需氧量(SCOD)为4381.75±0.1 g·L-1;pH值为 6.4±0.1。试验中采用人工模拟配制的果蔬垃圾作为基质。模拟的果蔬垃圾组成包括苹果、西瓜、菠菜、生菜和土豆(购买于北京市海淀区清华大学清河农贸市场),其中苹果、西瓜、菠菜、生菜和土豆按照3∶6∶4∶3∶3的质量比例破碎混匀。模拟果蔬垃圾采用垃圾处理器(In-Sink-Erator company, Model 55,410W,USA)进行破碎处理[14],具体操作将切块后的果蔬置于粉碎机中,粉碎20 min,破碎混匀后的固液混合物,置于-20℃的冰箱冷冻保存。为了方便使用,用密封袋分装,每次进料前,于-4℃条件下化冻后使用。该模拟果蔬垃圾底物性质检测如下:总固体(TS)为10.58 %±0.5 %,总挥发性固体(VS)为9.81 %±0.4%,总化学需氧量(TCOD)为36575±64 g·L-1; 溶解性化学需氧量(SCOD)为33873.4±18.9 g·L-1, pH值为4.4±0.2。
1.2 试验设计
本试验考察pH值稳定演变对厌氧发酵体系的效能影响,试验设计如下:以接种泥和果蔬垃圾混合后有机负荷为6 gVS·L-1·d-1,水力停留时间为4 d,反应温度35℃为设置条件,将400 mL 接种泥和150 mL 模拟果蔬垃圾底物进行混合,置于反应器中反应,使用氮气(80 mL·min-1)曝气10 min以保证整体厌氧环境。通过pH值控制器连续稳定改变反应体系pH值,其中酸性演变反应器R1从pH值 7.0±0.1(标记为R1-7)降至 pH 值2.0±0.1(标记为R1-2),碱性演变反应器R2从pH值 8.0±0.1(标记为R2-8)升至 pH 值12.0±0.1(标记为R2-12),试验共连续运行95 d。同时设置空白对照组进行对比。反应器取样采用半连续方式运行,每天进出料,每隔2日检测出料性质。具体实验操作参数详见表1。

表1 实验操作参数
1.3 实验装置
采用CSTR 厌氧消化反应器及pH值控制器联合进行实验(见图1)。反应器有效体积为800 mL(总体积为1 L)。反应器的反应温度通过恒温室加热器维持在35℃±2 ℃。此外,反应器通过磁力搅拌的方式,将发酵原料和微生物充分混合。磁力搅拌器的搅拌速度设为200 rpm,确保反应器内反应体系充分混合。为防止反应器漏气,反应器各出口进行了密封,并连接集气袋以收集产气。在实验过程中,pH值控制器(Clear, pH500)控制各反应器的pH值参数处在设定值±0.1范围内。调节反应器pH值的酸性物质为盐酸溶液(2M)和碱性溶液氢氧化钠溶液(2M)。

图1 pH值控制CSTR反应器装置图
1.4 检测方法

本研究中的水解率、酸化率和VFA转化率见公式(1)~(3)。其中,酸化率计算公式中的总VFA为各个代谢物质转化为COD后的浓度之和。
水解率=SCOD/TCOD×100%
(1)
酸化率=总VFA(以COD计)/TCOD×100%
(2)
VFA转化率=总VFA(以COD计)/SCOD×100%
(3)
2 结果与分析
2.1 果蔬垃圾自然厌氧发酵性能
果蔬垃圾在无pH值调控自然发酵情况下,其pH值和酸化产物变化如图2。由图2可知,果蔬垃圾自然厌氧发酵过程中pH值为酸性,波动范围在3.0~5.0。发酵第1天~第6天,pH值主要稳定在4.5左右。从第7天~第47天,pH值开始呈现下降趋势,平均维持在3.8。第47天开始,pH值出现波动,pH值后期维持在3.6。随着pH值变化,果蔬垃圾自然厌氧产酸发酵过程中丙酮酸、乙酸、乳酸和乙醇等产物的产量有明显变化。反应前15 d产物变化趋势无明显变化,可看作是厌氧发酵驯化稳定期。此稳定期乙酸产量占比最大,平均产量可达4416.26±111.46 mg·L-1。其次,丙酮酸产量平均可达3787.91±106.27 mg·L-1。从第16天开始,乳酸产量明显上升成为特征产物,最高可达14885.09±61.28 mg·L-1。从第47天开始,乙醇产量明显提高,相比前期乙醇产量至少提高了99.89%,最高产量可达6389.52±2.64 mg·L-1。丙酮酸为碳水类化合物代谢的中间产物,糖类物质酵解为丙酮酸后,再根据不同代谢途径生成乙醇、乳酸、乙酸和丁酸等酸化产物[16]。丙酮酸产量可以标志糖酵解进入到厌氧代谢酸化途径的程度。果蔬垃圾自然厌氧发酵条件下,丙酮酸产量无明显波动,产量维持在2298.34±131.17 mg·L-1,乳酸平均产量为8412.92±159.46 mg·L-1,乙酸平均产量为2557.89±83.39 mg·L-1。
pH值在厌氧发酵中是影响产物组分的关键参数[17]。酸性条件下,乳酸和乙醇是果蔬垃圾厌氧发酵的主要产物。关联分析图2中pH值和产物组分的关系,可得到pH 值3.8~4.5范围内,乳酸的产量明显高于乙醇,呈现乳酸型发酵。当pH值继续酸化低于3.8,乙醇产量明显提高,呈现乳酸-乙醇共发酵类型。因此,果蔬垃圾自然厌氧发酵pH 值呈酸性且会持续下降,产物组分会由乳酸为主转化为乙醇和乳酸共同发酵。丙酮酸的产量变化也与酸化产物的总量变化具有一致性。

图2 果蔬垃圾自然厌氧发酵pH值及性能变化
2.2 pH值演变条件下酸化产物组分
通过pH 值控制器,将酸性反应器中pH值由7.0 稳定调节至2.0,碱性反应器中pH 值由8.0 稳定调节至12.0,具体酸化发酵产物如图3。由图可知,在酸性3.0~5.0条件下,主要产物为乙醇和乳酸。其中,pH值为4.0时,乳酸产量最大,高达18291.46±97.84 mg·L-1。当pH值降至3.0时,发酵产物以乙醇为主,其产量可达4197.71±7.73 mg·L-1。在pH 值6.0~10.0条件下,果蔬垃圾厌氧发酵产物主要由乙酸、丙酸和丁酸组成。在pH值由5.0向 6.0演变时,乳酸产量下降,乙酸和丁酸产量明显提升,平均分别可达6459.90±2.88 mg·L-1和1866.81±111.22 mg·L-1。随着pH值升至10.0,乙酸产量升到最高,平均产量为10283.94±111.15 mg·L-1。其他产物如丙酸产量为1128.33±97.06 mg·L-1,丁酸产量为770.06±105.34 mg·L-1。当pH值保持在11.0和12.0的碱性条件下,酸化产物产量降低,主要产物为乙酸,产量仅为3938.89±134.70 mg·L-1。同时,丙酮酸产量在pH值为2.0、11.0和12.0 条件下也呈现下降趋势,标志强碱和强酸环境中糖类物质向丙酮酸转化速率降低,进而导致丙酮酸向其他酸化产物的代谢受到抑制。厌氧反应体系中pH值下降,细胞生长以及代谢化合物的生长受到抑制[18]。在pH值稳定调控的厌氧发酵体系中,产物产量相对稳定。总体上,在pH 值3.0~5.0 范围,主要酸化产物如乳酸和乙酸平均产量分别为9198.54±148.11 mg·L-1和3908.53±436.50 mg·L-1,均高于果蔬垃圾自然厌氧发酵的产量。相比其他文献报道[19],本实验中乳酸产量较低。以厨余垃圾为底物进行厌氧发酵更有助于乳酸产量的提高,可达到52400 mg·L-1。厨余垃圾中含有大量的淀粉、葡萄糖等物质,且大部分产乳酸菌的有机碳来源于此[20]。因此,有较多的研究发现厨余垃圾更适合乳酸的生成。另外,与其他文献相比,本实验中乙醇产量合理。以果蔬垃圾为底物的厌氧发酵中,乙醇产量处于3500~16500 mg·L-1范围,主要变化取决于pH值和有机负荷[17]。一些研究表明,丁酸主要是蛋白质类物质的酸化代谢产物[21],在以厨余垃圾为底物的厌氧发酵中产量较大。

图3 果蔬垃圾厌氧发酵pH值演变下酸化效能变化
不同发酵体系可呈现不同发酵类型,获得不同的特征产物。根据定义[22],乙醇代谢产物在发酵组分中比例大于30%,且乙醇和乙酸共占比大于50%,则为乙醇型发酵;乙酸浓度为主,其他产物(如丙酸、丁酸等)浓度差异不大,则为混合酸型发酵;丁酸占比大于30%,且丁酸和乙酸共占比大于50%,则为丁酸型发酵。另外,乳酸型发酵虽未有明确定义,但已有多篇文献证明乳酸型发酵在酸性发酵条件下呈现[11, 20]。在不同pH 值调控条件下,发酵体系呈现不同的发酵类型如图4:在pH值 2.0、4.0、5.0、10.0和11.0厌氧体系中分别呈现为乙醇型、乳酸型、混合型、乙酸型和丁酸型发酵。整体而言,酸性条件下厌氧发酵产物主要由乙醇、乳酸和乙酸组成;碱性条件下,优势产物为乙酸、丙酸和丁酸。不同pH值条件下,优势产物主要由微生物组分和代谢途径中所需辅因子(如能量ATP、氧化还原力NADH/NAD+和酶活)决定。发酵类型的演变与pH值稳定演变具有相关性[23],pH值可作为实现不同发酵类型的操控因子。不同pH值条件下微生物群落会进行演变,但不利pH值因子不会导致某一物种完全消失。除了微生物群落变化,胞外pH值也影响胞内参与代谢途径的辅因子的抑制与激活[24]。这些辅因子是调控糖酵解代谢途径的主要操控因子,可抑制和激活不同代谢中间产物的生成[25]。另外,pH值、优势菌群和产物之间存在的关系,也是产酸发酵细菌种群生理生态学的一种呈现。许多文献通过人为控制pH值参数得到了不同的产物组分,检测出已形成了不同的优势种群。本质上,形成不同的优势种群与呈现不同发酵类型是微生物代谢的因果。任南琪[26]等发现乙醇型发酵的优势种群主要为拟杆菌属等专性厌氧菌,丁酸型发酵的优势种群主要为梭状芽孢杆菌。不同pH值条件下,微生物的生存耐性和代谢活动有差异,导致了不同微生物发酵代谢末端产物的转化率不同,进而形成了不同发酵类型。在pH值演变的过程中,不同的优势菌群接替占据主导位置,其主要代谢产物反映为不同发酵类型。代谢末端不同产率本质原因在于离子物质(如H+、OH-等)影响了微生物细胞膜运输性能及细胞内酸碱敏感成分稳定性(如DNA、ATP等)。且基于微生物的不同生理结构和耐受能力,微生物代谢能力呈现差异。因此,随着pH值的变化,微生物群落中不同种群的竞争演替,形成了不同生态位,形成了优势种群,出现了发酵产物差异。本文中pH 值2.0、4.0、5.0、10.0和11.0的厌氧体系所形成的不同发酵类型,也是体现了相应优势种群在该适宜pH值条件下生存和代谢能力较有竞争优势。
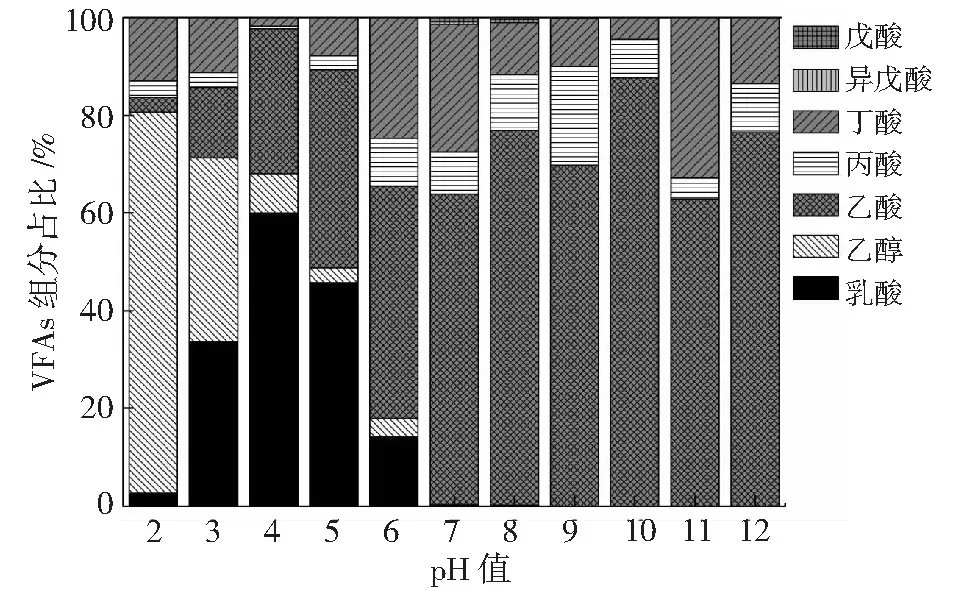
图4 不同pH值演变下厌氧体系的VFAs组分影响
2.3 pH值演变条件下厌氧水解酸化速率
在厌氧发酵过程中,水解率和酸化率标志发酵过程中糖类物质水解和酸类产物转化的程度。据文献报道,水解率是厌氧发酵过程中的主要限速步骤[27]。在不同pH值条件下,水解率、酸化率和VFA转化率如图5。酸性条件下,水解率较低处于35.89%~47.08%,酸化率处于35.21%~42.29%。中性偏碱性条件下,水解率和酸化率明显提升。在pH值为9.0时,水解率最高为84.94%,酸化率最高为75.18%。VFA转化率可体现VFA产物占溶解性COD的比例。酸性条件下,溶解性有机物质主要成分为VFA,比例高达99.20%。碱性条件下,溶解性有机物质中VFA比例可占到31.27%~97.10%。碱性条件可促进蛋白质类物质水解,经碱处理的污泥中蛋白质含量明显高于未处理组[28]。污泥碱性发酵体系中水解程度普遍高于酸性,主要原因是碱性条件溶解了细胞膜导致胞内物质流出,且水解微生物的活性更高,水解酶活更高,能够更高效地水解有机物。

图5 不同pH值演变下厌氧体系水解率、酸化率和VFAs转化率的变化
2.4 pH值演变条件下氮磷营养释放
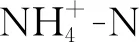

图6 不同pH值演变下厌氧体系氮磷元素释放情况
2.5 pH值演变对细胞能量浓度及VFAs产量影响
不同pH值调控条件下厌氧发酵过程中VFAs总浓度和能量变化如图7所示。酸性条件下,细胞裂解后的ATP 含量都较低,平均发光强度为85.4±5.65 RLU。当厌氧发酵体系调控在碱性条件下,ATP的含量逐渐提高。在弱碱性条件,ATP含量水平可达 196.33±4.83 RLU。然而,在pH值为12.0时,ATP含量显著提高,可能是碱性条件下细胞破裂,造成细胞裂解液中单位ATP含量较高。据文献报道,通过添加外源抑制剂,降低光滑球拟酵母 CCTCC M202019中的胞内ATP含量43%,可促进葡萄糖消耗速度360%,提高丙酮酸生成速度17%。胞内能量ATP含量降低能够提高糖酵解速率,主要原因是提高了磷酸果酸激酶和丙酮酸激酶的活性[31]。如图7中,能量浓度和VFAs总浓度呈负相关性。当能量浓度处在68~200 RLU范围时,酸化产物的总量可实现11471.71~20902.24 mg·L-1。然而,能量浓度再次提高至200 RLU以上,酸化产物总量显著减低。当能量浓度达1003.5 RLU时,总VFAs产量仅为6811.76 mg·L-1。在pH值 6.0和9.0时,总VFAs产量最高,分别是20235.67mg·L-1和20902.24 mg·L-1。
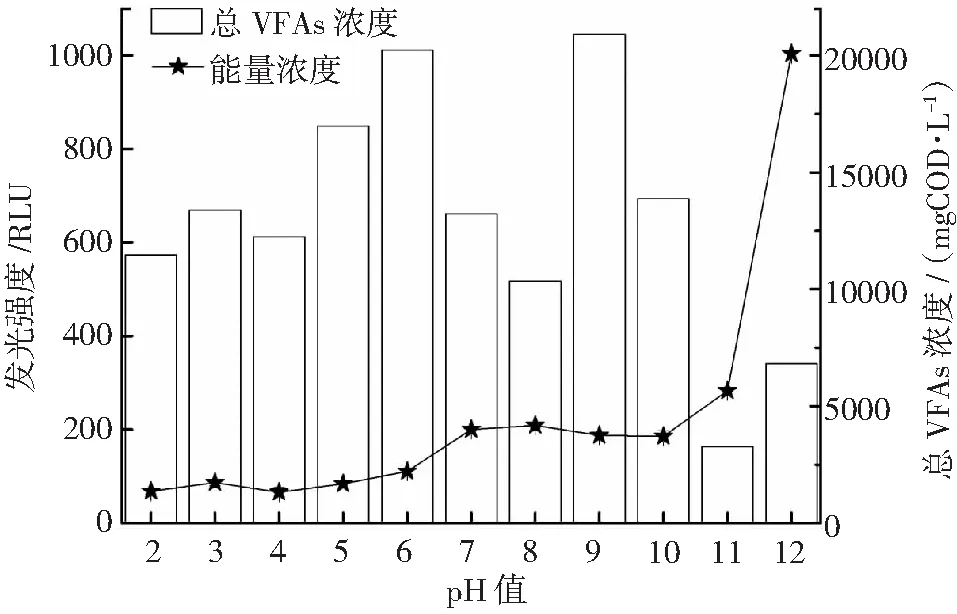
图7 不同pH值演变下厌氧体系的能量与VFAs产物浓度
3 结论
(1)果蔬垃圾自然厌氧发酵过程中,由于酸化产物不断生成,pH值会不断下降。果蔬垃圾自然厌氧发酵体系中主要产物由乳酸转化为乙醇。丙酮酸产量变化趋势与酸化产物产量变化一致。
(2)果蔬垃圾厌氧发酵中pH值调控可稳定发酵类型和产物产量。当pH值稳定在2.0、4.0、10.0和11.0时,发酵体系形成乙醇型、乳酸型、乙酸型和丁酸型发酵。其中,各发酵类型中特征产物产量分别为乙醇4106.31±260.13 mg·L-1, 乳酸11619.99±169.08 mg·L-1,乙酸10284.16±111.15 mg·L-1和丁酸 1017.55±124.30 mg·L-1。
(3)不同pH值调控的果蔬垃圾厌氧发酵体系中,碱性条件下的水解速率和酸化速率高于酸性条件。然而,酸性条件下,溶解性有机物主要为酸化产物。厌氧体系中氨氮释放量高于磷酸盐的释放,pH 值2.0条件下,氨氮和磷酸盐含量最高。强碱条件下,能量浓度较高,总VFAs产量较低,而在pH 值6.0和9.0的条件下,酸化产物的总产量较理想。

