探究阿昔洛韦联合纳洛酮治疗小儿病毒性脑炎的临床疗效及安全性分析
史彦香,郭春霞,楚汉雨
(1.莒县人民医院小儿内科;2.莒县人民医院内科,山东日照 276500)
病毒性脑炎为儿科常见感染性疾病,主要特征为意识状态异常、发热、癫痫,具有起病急、病程进展快、病死率高等特点,需积极治疗,减轻对患儿身心健康的影响[1]。临床针对小儿感染性疾病,较常应用阿昔洛韦治疗,该药物是一类核苷酸类抗病毒药,可通过抑制病毒的DNA合成而起到抗病毒的作用,能显著减轻患儿痛苦;此外,纳洛酮在小儿感染性疾病的治疗中亦应用广泛,该药物为阿片受体拮抗剂,对减轻患儿头痛、改善患儿意识障碍症状有积极作用[2]。基于此,本次研究选取124例小儿病毒性脑炎患儿,将阿昔洛韦、纳洛酮联合用于该类患儿的治疗中,观察是否能增强疗效,现报道如下。
1 资料与方法
1.1 一般资料 选取莒县人民医院2019年4月至2021年5月收治的124例小儿病毒性脑炎患儿,按照随机数字表法分为对照组、观察组,各62例。对照组:男患儿35例,女患儿27例,年龄3~11岁,平均年龄(7.32±1.32)岁,病程1~4 d,平均病程(2.53±0.32)d;观察组:男患儿34例,女患儿28例,年龄2~12岁,平均年龄(7.30±1.33)岁,病程1~5 d,平均病程(3.01±0.98)d。两组患儿基本资料比较,差异无统计学意义(P>0.05)。本研究经莒县人民医院医学伦理委员会批准,患儿父母或法定监护人均对本研究知情,并签署知情同意书。纳入标准:通过临床辅助检查均确诊为病毒性脑炎[3]。排除标准:①精神疾病者;②凝血功能异常者;③对本研究所用药物有过敏史者。
1.2 治疗方法 两组患儿均给予镇静、降低颅内压、解痉、抗感染、维持电解质平衡等基础治疗,对照组在此基础上给予患儿阿昔洛韦(辅仁药业集团有限公司,国药准字H20068119,规格:10 mL∶0.25 g),静脉滴注,用0.9%生理盐水或5%葡萄糖注射液稀释至100 mL,使药物浓度<7 g/L,按照每次10 mg/kg标准给予患儿静脉滴注,1次/12 h,持续治疗1周。
观察组患儿于对照组基础上联合纳洛酮(北京华素制药股份有限公司,国药准字H10900021,规格:1 mL∶0.4 mg),采取浓度为5% 100 mL葡萄糖注射液稀释后,按照每次0.02 mg/kg标准静脉滴注,1次/8 h,持续治疗1周。
1.3 观察指标 ①观察两组患儿的临床疗效。显效:发热、肌肉酸痛、惊厥等症状消失,脑电图等影像检查无异常;有效:症状缓解,脑电图检查显示好转;无效:症状及体征未见改善,甚至加重。总有效率=[(显效+有效)例数/总例数]×100%。②观察两组患儿血清神经元特异性烯醇化酶(NSE)、中枢神经特异蛋白(S-100β)水平。治疗前后采集患儿晨起空腹血液3 mL,采用离心机(武汉医捷迅安商贸有限公司,湘长械备20140072号,型号:TDZ5-WS)离心,半径为6 cm,离心速率1 500 r/min,离心时间10 min,获取上层血清。应用酶标仪(美国BioRad公司,型号:Med550),采取酶联免疫吸附法检测NSE、S-100β。③观察两组患儿炎症因子水平。治疗前后采集患儿晨起空腹血液3 mL,采用离心机离心,半径6 cm,离心速率2 500 r/min,离心时间10 min获取上层血清,用全自动生化分析仪(武汉宏康世纪科技发展有限公司,粵械注准20162400884,型号:SL800)及配套试剂,采取双抗体夹心酶联免疫吸附法,检测白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α),采取散射比浊法检测C反应蛋白(CRP)。④观察两组患儿不良反应发生情况,包括皮肤瘙痒、胃肠道反应、血压升高、心率加快,计算不良反应发生率。
1.4 统计学分析 以统计学软件SPSS 22.0处理数据,临床疗效、不良反应发生率等计数资料采取[例(%)]表示,χ2检验,血清NSE、S-100β水平、炎症因子水平等计量资料以()表示,用t检验,P<0.05代表组间差异有统计学意义。
2 结果
2.1 两组患儿临床疗效比较 观察组、对照组治疗有效率分别为90.32%、74.19%,观察组治疗有效率高于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组患儿临床疗效比较[例(%)]
2.2 两组患儿血清NSE、S-100β水平比较 治疗前,两组患儿血清NSE、S-100β水平组间比较差异无统计学意义(P>0.05);治疗后,两组患儿上述各项血清水平均低于治疗前,且观察组患儿更低于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组患儿血清NSE、S-100β水平比较(ug/L, )
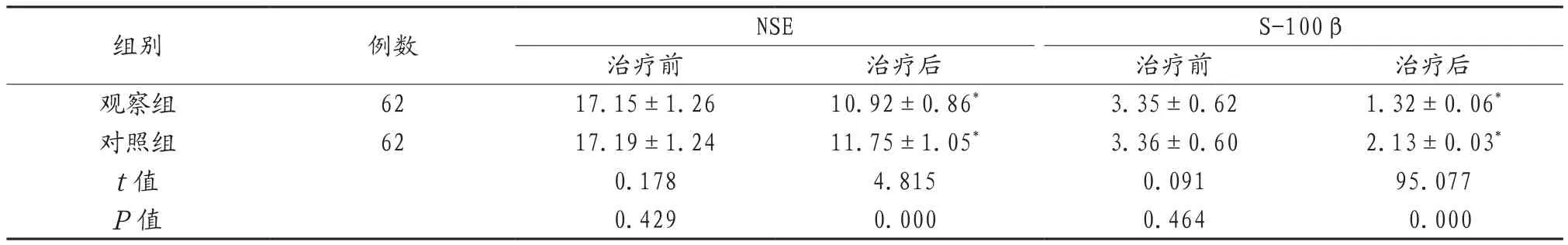
表2 两组患儿血清NSE、S-100β水平比较(ug/L, )
注:与治疗前相比,*P<0.05。NSE:神经元特异性烯醇化酶;S-100β:中枢神经特异蛋白。
组别 例数 NSE S-100β治疗前 治疗后 治疗前 治疗后观察组 62 17.15±1.26 10.92±0.86* 3.35±0.62 1.32±0.06*对照组 62 17.19±1.24 11.75±1.05* 3.36±0.60 2.13±0.03*t值 0.178 4.815 0.091 95.077 P值 0.429 0.000 0.464 0.000
2.3 两组患儿炎症因子水平比较 治疗前,两组患儿TNF-α、IL-6、CRP等炎症因子水平组间比较差异无统计学意义(P>0.05);治疗后,两组患儿TNF-α、IL-6、CRP炎症因子水平均低于治疗前,且观察组患儿更低于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组患儿炎症因子水平比较( )

表3 两组患儿炎症因子水平比较( )
注:与治疗前相比,*P<0.05。TNF-α:肿瘤坏死因子-α;IL-6:白细胞介素-6;CRP:C反应蛋白。
组别 例数 TNF-α(pg/mL) IL-6(ng/L) CRP(mg/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 62 1 683.69±85.68 1 165.89±63.58* 0.59±0.13 0.32±0.06* 13.59±3.51 5.14±0.12*对照组 62 1 684.70±85.69 1 542.85±36.71* 0.60±0.11 0.46±0.09* 13.60±3.50 6.79±0.37*t值 0.066 40.429 0.462 10.191 0.016 33.401 P值 0.948 0.000 0.322 0.000 0.494 0.000
2.4 两组患儿不良反应发生率比较 观察组、对照组患儿并发症发生率分别为11.29%、8.06%,组间比较差异无统计学意义(P>0.05),见表4。

表4 两组患儿不良反应发生率比较[例(%)]
3 讨论
病毒性脑炎为小儿多发疾病,在我国以单纯疱疹病毒与肠道病毒感染为主,随着病情进展,会导致患儿脑血管内皮发生变性坏死,出现神经元水肿,致使神经髓鞘变性,影响脑细胞生成的同时,严重危及患儿生命健康[4]。
纵观临床,针对病毒性脑炎患儿的治疗,仍无特效药物,多以抗病毒、对症支持治疗为主,其中应用范围较广的药物为阿昔洛韦,该药物为嘌呤类似物,属于抗病毒药物,对病毒亲和力及选择性较高(主要抑制水痘带状疱疹病毒、单纯疱疹病毒等),用药后,能竞争性地争夺病毒脱氧核苷合成所需的病毒腺苷激酶;可在体内迅速活化为阿昔洛韦三磷酸酯,有效抑制病毒DNA聚合酶的产生,阻碍病毒复制;此外,其还能结合增长的DNA链,中断病毒DNA链转录过程,达到抗病毒,阻止病情进展,减轻患儿痛苦的目的[5]。
值得注意的是,观察病毒性脑炎病情进展的情况发现,病毒入侵患儿脑组织,大量增殖复制后,会加速神经细胞的破坏,加剧神经系统损害[6]。神经系统受损后,会进一步促使内源性阿片受体大量释放,使细胞中环磷酸腺苷(cAMP)水平显著降低,脑部血流量减少,颅内压显著升高,诱发脑水肿的出现,加重病情[7]。由此提示临床减轻脑水肿改善病情,可从抑制阿片受体方面入手。此次研究,观察组患儿所用药物纳洛酮则为阿片类受体拮抗剂,能高效结合阿片受体,改善脑部神经功能障碍症状,且该药物还能作用于中枢神经系统,促使钠、钾离子与三磷酸腺苷酶(ATP酶)的功能恢复,有效改善患儿血管痉挛、呼吸抑制的症状,并减轻其痛苦[8]。本研究结果显示,联合用药的观察组患儿治疗有效率高于对照组(P<0.05),证实联合用药确能增强疗效。
此外,有研究发现,小儿病毒性脑炎的发病过程中,血清NSE、S-100β等神经细胞损害标志物,与介导炎性反应、脑组织损伤加剧、血脑屏障破坏等生理过程有密切联系,由此可知,通过观察上述指标水平亦可评估病情,并制定相应的治疗方案[9]。本研究结果显示,治疗后,观察组患儿血清NSE、S-100β低于对照组(P<0.05),证实联合用药可减轻疾病对神经细胞的损害。分析原因,纳洛酮在减轻人胚胎大脑神经元缺氧所致的神经细胞损伤中,有积极作用,可最大程度阻止疾病对患儿神经细胞的损害,显著发挥改善缺氧神经元,抑制谷氨酸释放的作用,最终达到减轻兴奋性神经毒性和患儿痛苦的目的[10-11]。分析纳洛酮减轻神经细胞损害的作用机制,可能与纳洛酮可调节神经元细胞内干细胞因子、影响细胞因子受体表达密切相关。
TNF-α为单核巨噬细胞分泌,参与多项生理过程,当血脑屏障受病毒侵犯时,在病毒与炎性因子刺激下,TNF-α水平会显著提升,加速炎症反应进展[12]。IL-6为促炎症反应因子,在调节细胞增殖分化中有重要作用,研究发现,该项指标在病毒性脑炎患儿体内异常高表达[13]。而CRP为炎症反应敏感指标。由此可知,TNF-α、IL-6、CRP均参与病毒性脑炎患儿的病理过程。本研究结果显示,治疗后,观察组患儿TNF-α、IL-6、CRP等炎症因子水平显著低于对照组(P<0.05),说明联合治疗可发挥协同作用,显著减轻患儿机体炎症反应,控制病情。最后观察两组患儿的不良反应发现,组间比较差异无统计学意义(P>0.05),可知联合用药未叠加不良反应,安全性较高。
综上所述,对病毒性脑炎患儿在阿昔洛韦基础上加以纳洛酮治疗,能显著增强疗效、改善血清指标、稳定病情,且不良反应较少,安全性较高,值得临床推广应用。

