人工智能在眼病筛查和诊断中的研究进展
陈健祺 综述 李睿扬,林铎儒,项毅帆,赖伟翊,林浩添 审校
(1.中山大学中山医学院,广州 510080;2.中山大学中山眼科中心,眼科学国家重点实验室,广东省眼科视觉科学重点实验室,广州 510060)
进入2 1 世纪后,人口迅速增长、老龄化逐渐加剧,现有的医疗资源正越来越难以满足日益增长的医疗需求,亟需新型诊疗模式予以补足。鉴于眼睛是易于获取影像数据的体表器官,且眼科诊疗主要依据眼部图像数据[1],眼科人工智能(artificial intelligence,AI)的研究和应用具有明显的学科优势[2]。在白内障、青光眼、糖尿病性视网膜病变(diabetic retinopathy,DR)等领域的筛查诊断中,眼科AI的研究日趋成熟,主要表现为一种“眼部图像数据+AI”的模式。眼科AI应用于眼病的筛查诊断,将减少医疗系统对人工的依赖程度,使眼病相关筛查诊断更快速、更便捷、一致性更高,从而显著提高医疗服务的效率和成本效益[3]。本文将对眼科AI在眼病筛查诊断中的研究进展进行综述。
1 眼科AI 在白内障中的应用
白内障是常见的晶状体疾病,目前在发展中国家,白内障占到了伤残调整寿命年的90%以上[4],在世界范围内,白内障是首位致盲眼病。眼科AI在白内障的研究较为成熟深入,主要应用的是“裂隙灯+AI”的模式。Lin等[5]基于裂隙灯照相资料,使用深度学习算法创建了一个AI诊疗平台CC-Cruiser,主要用于先天性白内障的分诊。该算法包含了用于筛查先天性白内障的识别网络、对先天性白内障严重程度评估的分级网络,以及协助眼科医生进行治疗的辅助决策网络,对先天性白内障的诊断准确率达到了98.25%,治疗建议准确率达到了92.86%,目前已在多家协作医院完成临床试点应用。在进一步的多中心临床验证中,虽然发现CC-Cruiser的诊断和治疗判断准确率(分别为87.4%和70.8%)显著低于专家教授(分别是99.1%和96.7%),但CC-Cruiser诊断平均用时(2.79 min)显著短于专家教授(8.53 min),同时患者也对CC-Cruiser提供的整体医疗服务质量表示满意。对于诊断准确率较低,目前主要认为归因于儿童患者配合度低、眼睑睫毛遮挡镜头、裂隙灯强光使晶状体显像浑浊等,亟需进一步的改良优化。鉴于聚焦特定亚型白内障的人工智能系统可能在真实临床应用中存在局限性,Wu等[6]在进一步的实验室研究中建立并验证了一个通用的AI平台以分诊不同类型的白内障。该平台在初步试验中表现出了较好的性能,接收者操作特征曲线下面积(area under cur ve,AUC)均达到了99%以上。与传统模式相比,眼科医生在AI的辅助下服务的患者人数提高了10.2倍。“裂隙灯+AI”的模式,在白内障相关的AI研究中表现出了一定的应用潜力。
2 眼科AI 在青光眼中的应用
青光眼是世界范围内造成不可逆失明的第二大原因[7]。鉴于其眼底改变的不可逆性,及时、可靠的早期诊断将有助于改善青光眼的预后。然而,青光眼的诊断复杂,需要综合多模态的影像学资料,包括视野、眼底相和光学相干断层扫描(optical coherence tomography,OCT)等,且严重依赖临床医生的经验和专业知识。AI与影像学资料的配合可助力青光眼的筛查诊断,《中国基于眼底照相的人工智能青光眼辅助筛查系统规范化设计及应用指南(2020年)》[8]指出,AI筛查青光眼更符合成本效益比,可极大节省成本,提高眼科医师的效率,从而使筛查覆盖更广泛的人群,避免因早期漏诊而致盲的情况发生。
2.1 青光眼的“视野检查+AI”模式
自动化视野检查是检测青光眼病人视功能的重要手段,特征性的视野改变是诊断青光眼的金标准。然而,患者的主观因素以及长时间的检查引起的视疲劳,可能导致不可靠的检查结果。早在20世纪70年代,研究人员就开始评估如何优化阈值评估策略从而缩短检查时间[9],一系列算法策略如瑞典的交互式阈值分割算法(Swedish Interactive Thresholding Algorithm,SITA)[10]以及变体模型SITA Fast(SFA)[11]应运而生。
然而,视野检查的判读仍然存在主观性强、学习曲线长等问题,“视野检查+AI”的模式有助于补足其缺陷。Li 等[12]基于国际金标准Humphrey视野数据开发了青光眼自动判读系统iGlaucoma。该系统在实验室检验中诊断性能(AUC 0.834~0.877,灵敏度0.831~0.922,特异度0.676~0.709)优于所有6名参与检验的眼科医生,在实际诊所患者样本的检验中准确率达0.99,实际性能令人满意[AUC 0.966(0.953~0.979),灵敏度0.954(0.930~0.977),特异度0.873(0.838~0.908)],是一种视野检查的高效工具。目前,该系统已落地应用于真实世界,初步走向了临床应用,可帮助医生更好的判读视野,提高青光眼的诊断率。
2.2 青光眼的“眼底彩照+AI”模式
特征性的眼底改变是青光眼的标志之一,“眼底彩照+AI”的模式亦是研究的热点。Li等[13]和Liu等[14]报道了利用卷积神经网络训练的基于眼底彩照的深度学习模型,目前该模型尚处于实验室研究阶段。在实验室眼底照片验证中,诊断灵敏度均在95%以上,特异性均在90%以上,具有一定的临床应用潜力。同处实验室研究的还有Cheung等[15]报道的利用眼底彩照预测OCT参数的模型,该研究方向不仅希望能通过“眼底彩照+AI”的模式筛查诊断青光眼,还希望能通过眼底彩照获得更客观定量的病情评估。研究人员利用眼底彩照及其对应的OCT测量参数作为参考标准来训练深度学习模型,验证时,要求模型自主提取眼底图像特征,如视网膜神经纤维层(retinal nerve fibre layer,RNFL)厚度,Bruch's膜开口距离与最小盘沿宽度(Bruch's membrane openingminimum rim width,BMO-MRW)等,依据眼底彩照直接预测OCT参数。Medeiros等[16]研究显示:该预测模型得出的RNFL厚度和真实测量值之间呈现强相关性,预测的平均绝对误差约为7 μm,使用这些预测值区分青光眼和正常眼的AUC(0.944)与使用实际RNFL厚度值的AUC(0.940)几乎相同。Thompson等[17]研究表明预测模型得出的BMOMRW值和观测值之间亦呈强相关性,平均绝对误差为27.8 μm,使用预测值和真实值区分青光眼和正常眼的AUC相近,分别为0.945和0.933。可以设想,对于缺乏OCT等医疗设备的偏远地区以及基层医院,该预测模型可为临床医生提供可参考的OCT预测数据,以帮助临床医生获得更客观定量的病情评估,从而进一步提高眼底图像检测青光眼的应用价值。
2.3 青光眼的“视网膜扫描+AI”模式
王亚星等[18]认为,目前诊断青光眼时主要依据视野、眼底照片、O CT等,这种诊断模式于病变本身而言具有相对滞后性,当结构及相应功能学改变或进展出现时,病变实已进展到严重阶段,鉴于筛查诊断的重要价值是争取在临床前期或疾病早期发现患者,这种滞后性可能会削减眼科AI在青光眼的临床应用价值。基于该现状,Cordeiro等[19]设计出一种利用AI的快速且高敏的测试方法——凋亡视网膜细胞检测(detection of apoptosing retinal cells,DARC),可识别快速进展甚至存在失明风险的青光眼患者,该方法通过静脉注射荧光染色剂使其附着在视网膜细胞上,使凋亡视网膜细胞显影,再通过“视网膜扫描+AI”的模式得到客观的DARC计数,受损细胞越多则DARC计数越高。在二期临床试验中研究者使用AI对参与者进行了随访分析,发现所有DARC计数较高者均为进展性青光眼,相较金标准OCT检测,该技术能提前18个月预测青光眼的进行性损害,可大大提前干预的时间节点。目前,DARC已被英国药品和保健品管理局、美国食品药物管理局批准,纳入抗青光眼药物临床试验的终点指标。在合理的范围内将筛查发现、做出预警的时间提前,将有利于增加眼病的干预时间窗,增强眼科AI实用性。
3 眼科AI 在DR 中的应用
视网膜病变是糖尿病患者的常见并发症[20],鉴于世界范围内糖尿病患病率逐年上升,DR的疾病负担也正逐年加重[21]。研究[22]表明:糖尿病患者定期眼底筛查,早期发现眼底病变并给予及时治疗,可有效降低DR患者的视觉损害及致盲率,而“眼底彩照+AI”的模式正有助于DR筛查诊断的普及。目前,AI在DR的应用主要聚焦在分割和分类[23],分割是为满足定向的需求在指定的眼底图像上发现并标记病变形态,主要包括特征性生物学结构如中央凹、视杯比、渗出和血管瘤等,分类则是进一步进行眼底影像的诊断、分级。通过对数据集的不断训练,可以有效提高AI 筛查DR的准确性。在实验室的研究中,学者们先后建立并验证了相关的AI诊断系统(表1),“眼底彩照+AI”的模式在实验室研究中表现出了优良的工作性能。
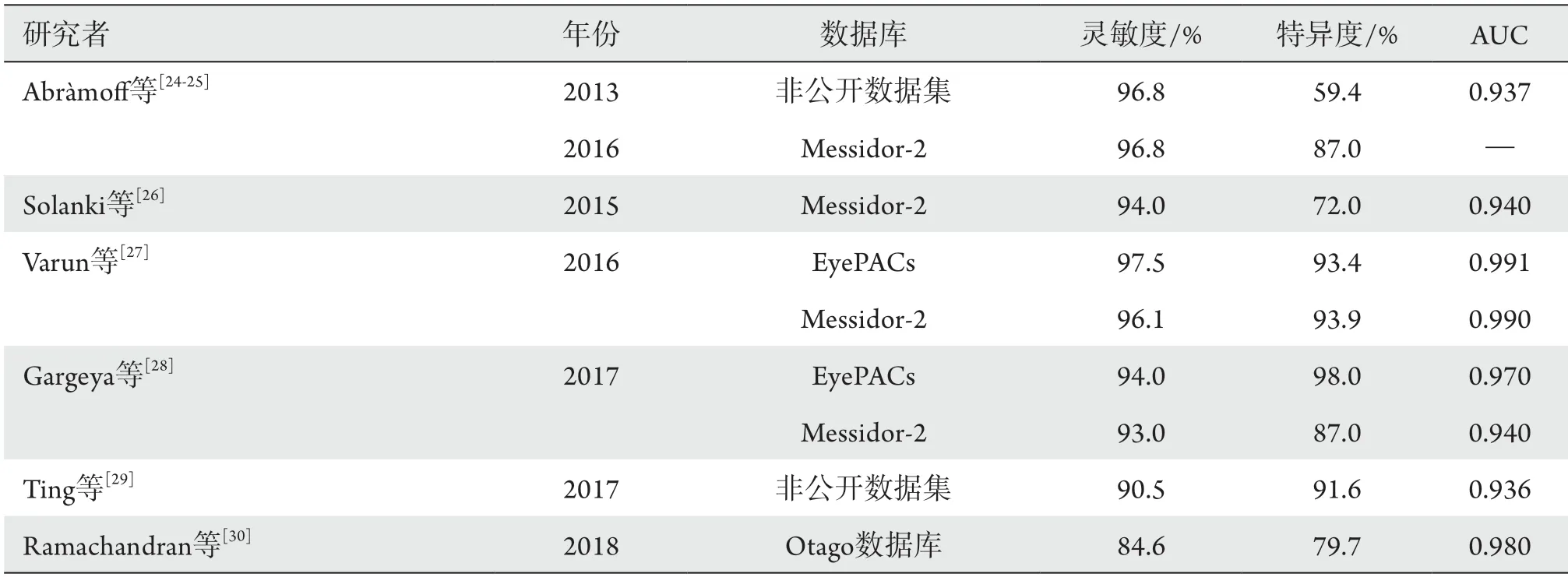
表1 基于眼底彩照筛查DR的AI系统主要研究结果汇总Table 1 Summary of main findings in AI system for screening DR based on fundus photographs
深度学习的进步使得多种检测DR的AI算法快速走向临床,IDx-DR已成为第一个被美国食品和药物管理局批准用于检测DR的AI设备[31]。然而,鉴于基于云的设备都需要高计算力,需要连接网络才能实现实时报告。研究人员进一步开发了Medios——一种基于智能手机的离线AI诊断软件。该软件采用智能手机的非散瞳眼底照相机捕捉双眼视网膜图像,并利用现代智能手机的高性能,直接在图形处理器上完成图像的离线处理,有望成为资源受限地区进行DR大规模筛查的一种理想选择[32]。在DR的识别诊断中其敏感性和特异性分别达到了98.84%和86.73%[33],在印度的前期试验显示灵敏度达100%,并具有较好的稳定性[32]。
由于AI算法高度依赖大量精确数据,何明光等[3]指出,在眼科AI领域,理想的训练数据集应包含疾病表型的所有可能变化,包括严重性、种族、伪影、眼底相机类型及临床表现的混杂变化等。目前,DR领域的大多数AI系统基于的是公共数据集,这些数据集训练得到的算法,可能会不适用于疾病背景和严重程度明显不同的临床环境,这可能为眼科AI在DR的真实应用中带来局限性。
4 结语
眼科学作为临床医学的一部分,自诞生起亦经历了从经验医学到循证医学、转化医学、精准医学的演变,这种演变过程,其本质是将生命不断数字化表述和智能化分析的过程。由眼科AI的飞速发展可知,近年来,眼科的诊疗逐渐走向智慧医学模式——即将互联网、大数据、人工智能等信息技术用于医疗,逐步形成部分人力工作的替代方案。在眼科AI中,深度神经网络在图像识别领域的表现优于传统算法和人类在图像识别领域的辨识能力,这使得“眼部图像数据+AI”的模式体现出了较大的临床应用潜能,尤其是在白内障、青光眼、DR等常见病、多发病中。短期内,眼科AI可能充当的是“智慧助手”的角色,通过分析大量的临床数据帮助人类医生加快判断与分类、发现异常并提供转诊服务,从而减少临床医生的工作量,并降低误诊率,进而成为眼科疾病一线筛查的长期方案。长远来看,眼科AI有望成为“智慧大脑”的角色,随着AI算法的不断改进,数据库的扩充,眼科AI或可进化为具备独立思考和指挥能力的医疗元素,从而更好地为医疗健康服务,其前景可期。
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。详情请访问:https://creativecommons.org/licenses/by-ncnd/4.0/。

