超声法提取橘子皮单宁及其抗氧化研究
陈秋娟,谢微,胡月芳,梁冬梅,黄小英
(1.贺州学院 材料与化学工程学院,广西 贺州 542899;2.贺州学院 食品科学与工程技术研究院,广西 贺州 542899)
单宁是多酚中高度聚合的一种化合物,广泛应用于食品加工中,如食品辅色、调味、酒水的澄清等[1]。近年来,单宁因具有一定的抑菌[2]、抗癌[3]和解毒[4]等作用,被多次应用到食品、果蔬加工、医药、水处理等领域[5],具有十分广阔的开发前景。
现今的单宁物质大多数取于植物,植物中的单宁含量较高,容易提取,来源广,所以很多学者都是优先选择在植物中提取单宁。如李玉巍等[6]从柿子皮中提取的单宁含量达到21.5%;刘涛等[7]从香蕉皮中提取的单宁提取率达到78.11%;章莉娟等[8]研究的核桃果皮单宁提取率达到20.36 mg/g。而目前用橘子皮提取单宁却鲜有报道,相关研究也比较少。
橘子大多是被人们用作新鲜水果来直接食用,或对其进行加工,做成柑橘黄豆酱[9]、柑橘醋等[10-11]。橘子加工后,会剩下大量的橘子皮,部分会加工为陈皮[12]和柑橘皮发酵汁[13],但大多数橘子皮被当作果蔬废弃物丢弃,这导致橘子皮资源遭到浪费,无法得到充分利用,也对环境造成污染。但若能利用橘子皮提取单宁物质,不仅原料丰富,还能废物利用。
采用超声法提取橘子皮中的单宁,探讨其抗氧化性,以期为橘子皮的综合利用提供一些理论依据。
1 材料与方法
1.1 材料、仪器与设备
磷钼酸:合肥巴斯夫生物科技有限公司;无水碳酸钠:成都市科隆化学品有限公司;单宁酸:天津市永大化学试剂有限公司;磷酸、七水合硫酸亚铁:广东省化学试剂工程技术研究开发中心;抗坏血酸(Vc):天津市光复科技发展有限公司;水杨酸:天津市科密欧化学试剂有限公司;30%过氧化氢:广州新建精细化工厂;1,1-二苯基-2-三硝基苯肼(DPPH):福州飞净生物科技有限公司;钨酸钠:广东光华科技股份有限公司;无水乙醇:成都市科龙化工试剂厂;以上试剂均为分析纯。
722型可见分光光度计 上海光谱仪器有限公司;KQ5200DE型数据超声波清洗器 昆山市超声仪器有限公司。
橘子皮购于当地市场,手工剥取橘子皮,清洗干净后,于60 ℃恒温烘干后粉碎,过60目筛后,装袋密封,备用。
1.2 单因素试验
1.2.1 乙醇浓度对橘子皮单宁提取率的影响
分别称取2 g橘子皮粉,加入料液比为1∶20(g/mL),体积浓度分别为30%、40%、50%、60%、70%的乙醇溶液,于功率100 W、温度60 ℃下超声40 min,平行测定3次滤液的吸光度,计算橘子皮中单宁的提取率,取平均值。
1.2.2 料液比对橘子皮单宁提取率的影响
分别称取2 g橘子皮粉,加入料液比为1∶10、1∶15、1∶20、1∶25、1∶30(g/mL),体积浓度为50%的乙醇溶液,于功率100 W、温度60 ℃下超声40 min,平行测定3次滤液的吸光度,计算橘子皮中单宁的提取率,取平均值。
1.2.3 超声时间对橘子皮单宁提取率的影响
分别称取2 g橘子皮粉,加入1∶15(g/mL)且体积浓度为50%的乙醇溶液,于功率100 W、温度60 ℃下分别超声3,5,10,15,20 min,平行测定3次滤液的吸光度,计算橘子皮中单宁的提取率,取平均值。
1.2.4 超声温度对橘子皮单宁提取率的影响
分别称取2 g橘子皮粉,加入1∶15(g/mL)且体积浓度为50%的乙醇溶液,于功率100 W、设温度为40,50,60,70,80 ℃下超声10 min,平行测定3次滤液的吸光度,计算橘子皮中单宁的提取率,取平均值。
1.3 正交试验
正交试验可以获得大量的信息。根据单因素试验结果,设计L9(34)正交试验,因素及水平见表1。
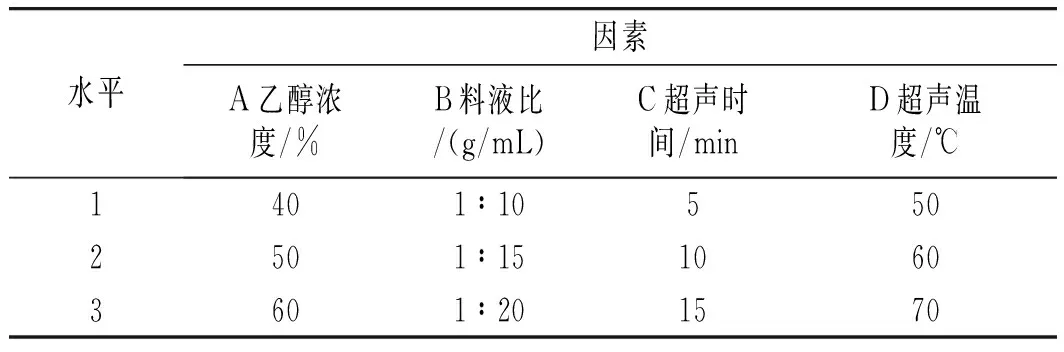
表1 正交试验因素水平表Table 1 The factors and levels of orthogonal test
1.4 橘子皮中单宁含量的测定
参照文献[14]配制Folin-Donis试剂(F-D试剂)。参照文献[15]绘制单宁工作标准曲线:A=90.2c-0.0331,R2=0.9996。橘子皮中单宁含量W的计算公式[16]:W(%)=(A×N×V)/m,式中:A为由标准曲线所得的浓度(mg/mL);N为稀释倍数;V为浸提液体积(mL);m为橘子皮的质量(g)。
1.5 抗氧化试验
参照文献[17]分别进行橘子皮单宁清除羟基自由基与DPPH自由基的能力测定,同时以Vc做对比试验,考察橘子皮单宁的抗氧化性能。
2 结果与讨论
2.1 单因素试验
2.1.1 乙醇浓度对橘子皮单宁提取率的影响
由图1可知,乙醇浓度增大,橘子皮单宁的提取率增大,于50%时达到最大提取率18.89%。乙醇浓度高于50%后,橘子皮单宁提取率下降。原因是增大乙醇浓度后,乙醇含量过高导致醇解反应,使得橘子皮中的醇溶性、脂溶性杂质增加,导致橘子皮中单宁的含量下降[18]。因此,提取橘子皮单宁的最佳乙醇浓度为50%。

图1 乙醇浓度对橘子皮单宁提取率的影响 Fig.1 Effect of ethanol concentration on the extraction yield of tannin from orange peel
2.1.2 料液比对橘子皮单宁提取率的影响
由图2可知,料液比增大,单宁提取率提高,于1∶15(g/mL)达到最大提取率20.62%。料液比的增大可以增大单宁的溶出量。料液比大于1∶15(g/mL)后,橘子皮单宁提取率下降。原因是料液比虽可增大细胞内外的质量浓度差,利于单宁提取,但同时会导致超声能量密度下降[19],提取率降低。因此,提取橘子皮单宁的最佳料液比为1∶15(g/mL)。
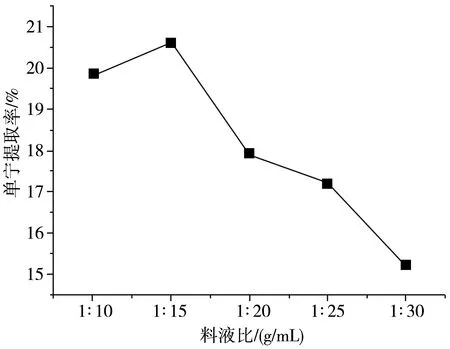
图2 料液比对橘子皮单宁提取率的影响Fig.2 Effect of solid-liquid ratio on the extraction yield of tannin from orange peel
2.1.3 超声时间对橘子皮单宁提取率的影响
由图3可知,超声时间增长,单宁提取率增大,于10 min达到最大提取率21.48%。超声时间多于10 min后,单宁提取率下降。其原因可能是在10 min时,单宁基本被提取出来,继续超声会导致单宁被降解和氧化。因此,提取橘子皮单宁的最佳超声时间为10 min。
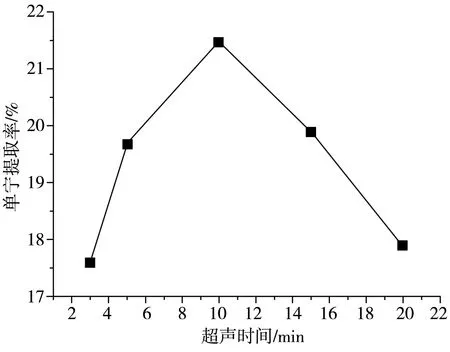
图3 超声时间对橘子皮单宁提取率的影响Fig.3 Effect of ultrasonic time on the extraction yield of tannin from orange peel
2.1.4 超声温度对橘子皮单宁提取率的影响
由图4可知,40~60 ℃温度内,提取率逐渐增大,一旦超过60 ℃,提取率下降。原因是温度过高,导致单宁物质失去活性[20]。由此可知,单宁提取率受超声温度的影响,60 ℃下单宁的最高提取率为19.20%。因此,提取橘子皮单宁的最佳超声温度为60 ℃。
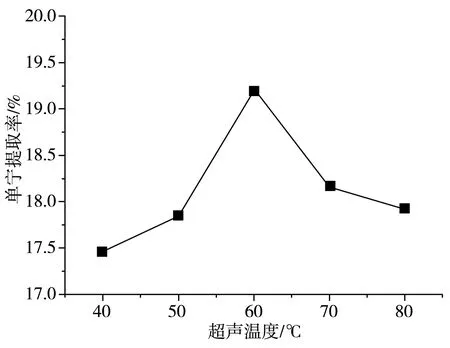
图4 超声温度对橘子皮单宁提取率的影响
2.2 正交试验结果分析
正交试验结果见表2。
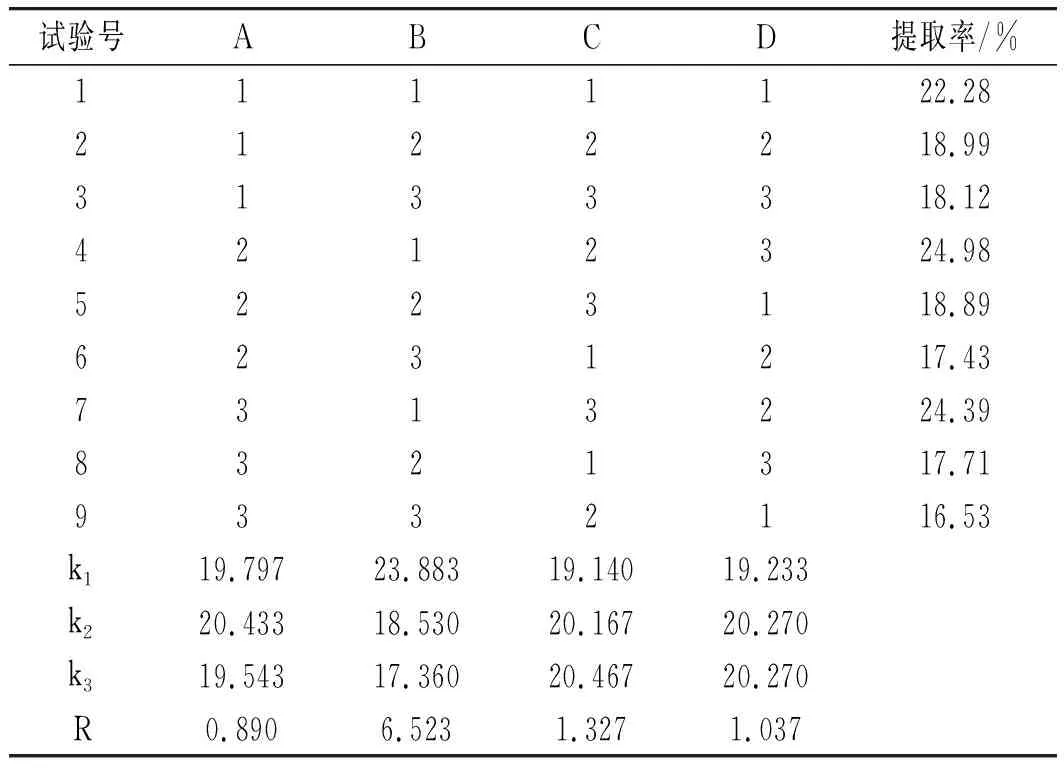
表2 正交试验结果Table 2 The results of orthogonal experiment
由表2可知,影响橘子皮单宁提取率的主次因素为料液比(B)>超声时间(C)>超声温度(D)>乙醇浓度(A),优组合为A2B1C3D2、A2B1C3D3。
2.3 验证试验
对A2B1C3D2和A2B1C3D3进行验证试验,试验重复3次,计算单宁得率,取其平均值,结果见表3。
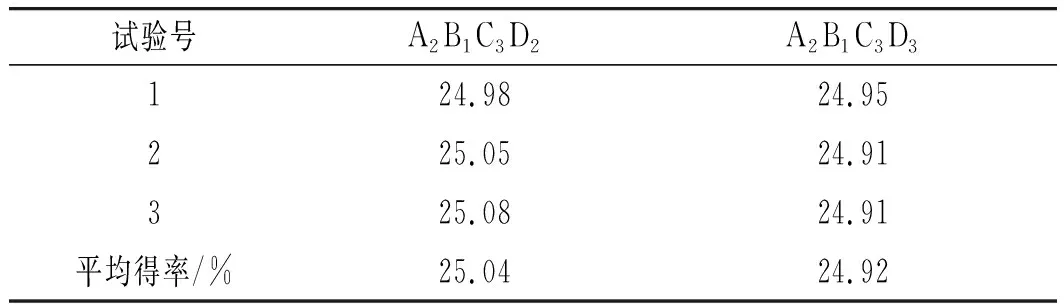
表3 验证实验结果Table 3 The results of verification experiment
由表3可知,A2B1C3D2试验组合优于A2B1C3D3试验组合。由此确定A2B1C3D2为橘子皮单宁的最佳提取工艺条件,即乙醇浓度50%、料液比1∶10 (g/mL)、超声时间15 min、超声温度60 ℃。
2.4 抗氧化性试验
2.4.1 橘子皮单宁清除羟基自由基能力的测定
橘子皮单宁清除羟基自由基的能力的结果见图5。
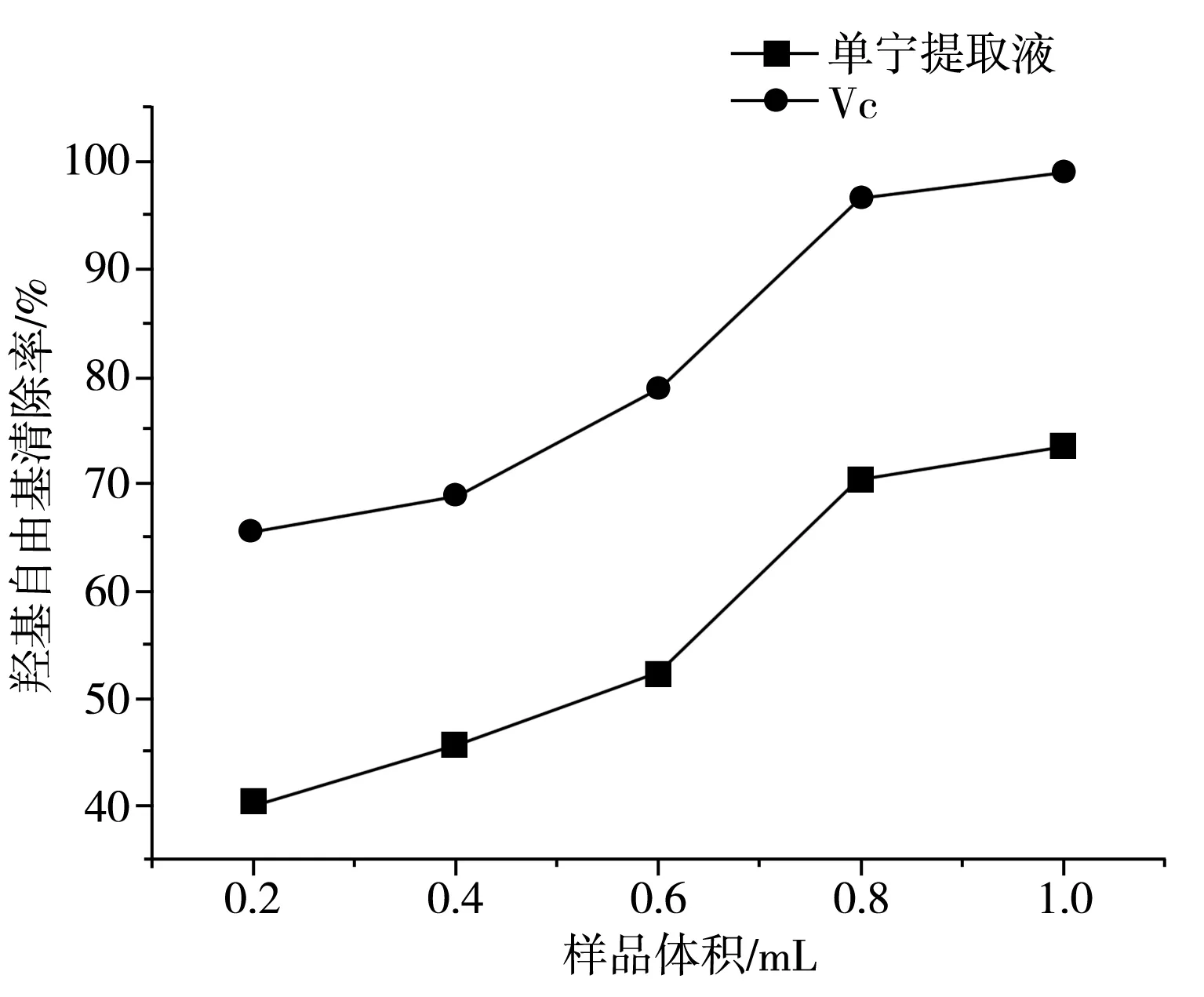
图5 橘子皮单宁清除羟基自由基的效果 Fig.5 Effect of tannin from orange peel on scavenging hydroxyl radical
由图5可知,随着橘子皮单宁提取液体积增大,清除羟基自由基能力增强,最大清除率达73.37%,变化趋势与Vc有着一定的相似性,说明橘子皮单宁提取液有一定的清除羟基自由基能力,且其变化呈现正相关,可作为新型抗氧化剂开发。
2.4.2 橘子皮单宁清除DPPH自由基的能力测定
DPPH法是测定抗氧化活性的一种常用方法,橘子皮单宁清除DPPH自由基能力的结果见图6。
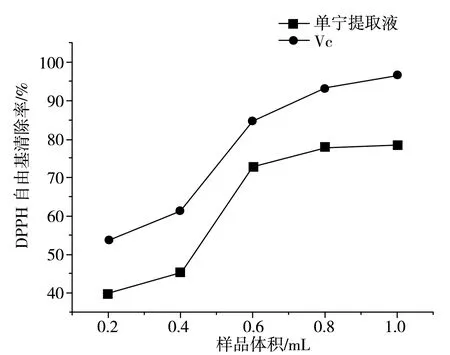
图6 橘子皮单宁清除DPPH自由基的效果Fig.6 Effect of tannin from orange peel on scavenging DPPH radical
由图6可知,随着橘子皮单宁提取液体积的不断增大,其对DPPH自由基的清除能力也在相应地增强,最大清除率达到78.52%,这说明橘子皮单宁提取液对DPPH自由基有着一定的清除能力。
3 结论
本文采用超声波法从橘子皮中提取单宁,试验以乙醇浓度、料液比、超声时间和超声温度4个单因素对橘子皮单宁的提取率进行考察,确定了乙醇50%、料液比1∶10(g/mL)、超声时间15 min、超声温度60 ℃为提取橘子皮单宁的最佳工艺条件,此时橘子皮中单宁的提取率最高,达25.04%。进行抗氧化性测试后,得到清除羟基自由基和DPPH自由基的得率,分别为73.37%和78.52%,表明橘子皮中单宁有着一定的抗氧化能力,可作为天然抗氧化剂的开发来源。

