射频消融与药物治疗对心房颤动合并心力衰竭患者的疗效差异比较
徐尧 蔡衡 李洪仕
(天津医科大学总医院心内科,天津 300052)
心房颤动(房颤)和心力衰竭(心衰)在临床上关系密切,二者可互为因果。房颤和心衰均会对患者预后造成严重威胁,故需系统而优化的管理。既往研究中,无论房颤患者是否合并心衰,采用抗心律失常药(antiarrhythmic drug,AAD)作为节律控制的手段均未显示明显获益[1-3],可能是由于AAD维持窦性心律的益处被其副作用所抵消。而射频消融在能更有效地维持窦性心律的情况下避免AAD的副作用,理论上是一种更加理想的治疗方式。
1 对象与方法
1.1 一般资料
研究对象为2018年1月—2020年4月于天津医科大学总医院住院治疗的房颤伴心衰患者88例(年龄46~90岁)。纳入标准为:(1)阵发性、持续性或长程持续性非瓣膜性房颤;(2)NYHA心功能分级Ⅱ级或Ⅲ级;(3)年龄≥18岁;(4)左室射血分数(left ventricular ejection fracton,LVEF)<50%或欧洲心脏病学会(European Society of Cardiology,ESC)射血分数保留性心衰(heart failure with preserved ejection fraction,HFpEF)评分(见图1)≥5分。排除标准:(1)甲状腺功能亢进引起的房颤;(2)近3个月出现急性心肌梗死;(3)左心耳血栓;(4)既往行房颤射频消融;(5)肝肾功能异常(转氨酶或肌酐水平超过正常上限3倍)。纳入的患者根据治疗策略分为射频消融组和药物治疗组。采用药物治疗的患者纳入药物治疗组,同时选取相同数量的基线资料匹配的采用射频消融的患者纳入射频消融组。

注:e′表示二尖瓣环舒张早期血流速度,E/e′表示舒张早期左室充盈速度/二尖瓣环舒张早期血流速度,NT-proBNP表示N末端脑钠肽前体,BNP表示脑钠肽;1 mm Hg=0.133 3 kPa。
1.2 研究方法
1.2.1 治疗方法
射频消融组:消融前停用所有AAD(胺碘酮除外),并按照指南要求,给予指南指导下的标准心衰治疗。消融前所有患者行经食管超声心动图排除左心耳血栓。患者取平卧位,术前连接多导电生理仪及CARTO3(Biosense Webster Inc,Diamond Bar,CA,USA)或Ensite NavX(St Jude Medical,Minneapolis,MN)三维标测系统。局麻下穿刺股静脉置入鞘管并送入冠状窦电极。成功穿刺房间隔后置入房间隔鞘,给予肝素抗凝。应用SMARTTOUCH® SF导管(Biosense Webster Inc,Diamond Bar,CA,USA)于左心房及各肺静脉内采集,以快速解剖建模模式建立三维解剖模型。行双侧环肺静脉隔离,经验证达传入及传出阻滞。对于持续性房颤,若行双肺静脉隔离后仍未转复则采用消融导管判断心房电压,根据低电压区分布情况酌情行顶部线、前壁线、底部线或二尖瓣峡部线消融,对于仍未转复者,静脉推注依布利特使心率降低从而确定激动顺序,进而对消融缝隙予补点消融,再次验证双侧肺静脉传入及传出阻滞,手术成功[4]。消融后的3个月定义为空白期,空白期内使用AAD控制心律,反复出现的持续房性心动过速/心房扑动/房颤采用电复律转复。在消融后3个月空白期后出现的30 s以上的房性心律失常定义为复发,可酌情给予第二次射频消融。
药物治疗组:所有患者依据个体状况使用胺碘酮或索他洛尔维持窦性心律和/或使用β受体阻滞剂或地高辛控制心室率,使平均心率在休息时≤90次/min,运动时≤110次/min[5]。若基线时未达该标准,则在门诊随访时规律调整用药以实现目标。根据个体状况使用指南推荐药物改善心功能。
1.2.2 随访
所有患者采用住院系统调阅、门诊复诊、电话及微信等方式随访。患者于出院后3、6、9、12个月复查12导联心电图、动态心电图和超声心动图。随访截止日期为2020年10月31日。观察指标包括LVEF、左心房前后径(由超声医师测量3次取平均值),观察预后包括窦性心律维持率、心衰再入院率及生存率。本研究随访12个月时的随访率为77.3%。
1.2.3 亚组分析
根据LVEF是否<50%,患者还被分为射血分数降低性心衰(heart failure with reduced ejection fraction,HFrEF)患者和HFpEF患者,其中HFpEF患者的纳入标准参考了ESC关于HFpEF的最新诊断标准[6],患者须满足评分≥5分(图1)。采用左心室质量指数(left ventricular mass index,LVMI)评估HFpEF患者的心脏舒张功能。
1.3 统计学方法

2 结果
2.1 患者基线资料
研究共纳入88例患者。其中药物治疗组44例,射频消融组44例。两组患者在除年龄、NYHA心功能分级及CHA2DS2-VASc评分以外的一般资料无统计学差异,见表1。
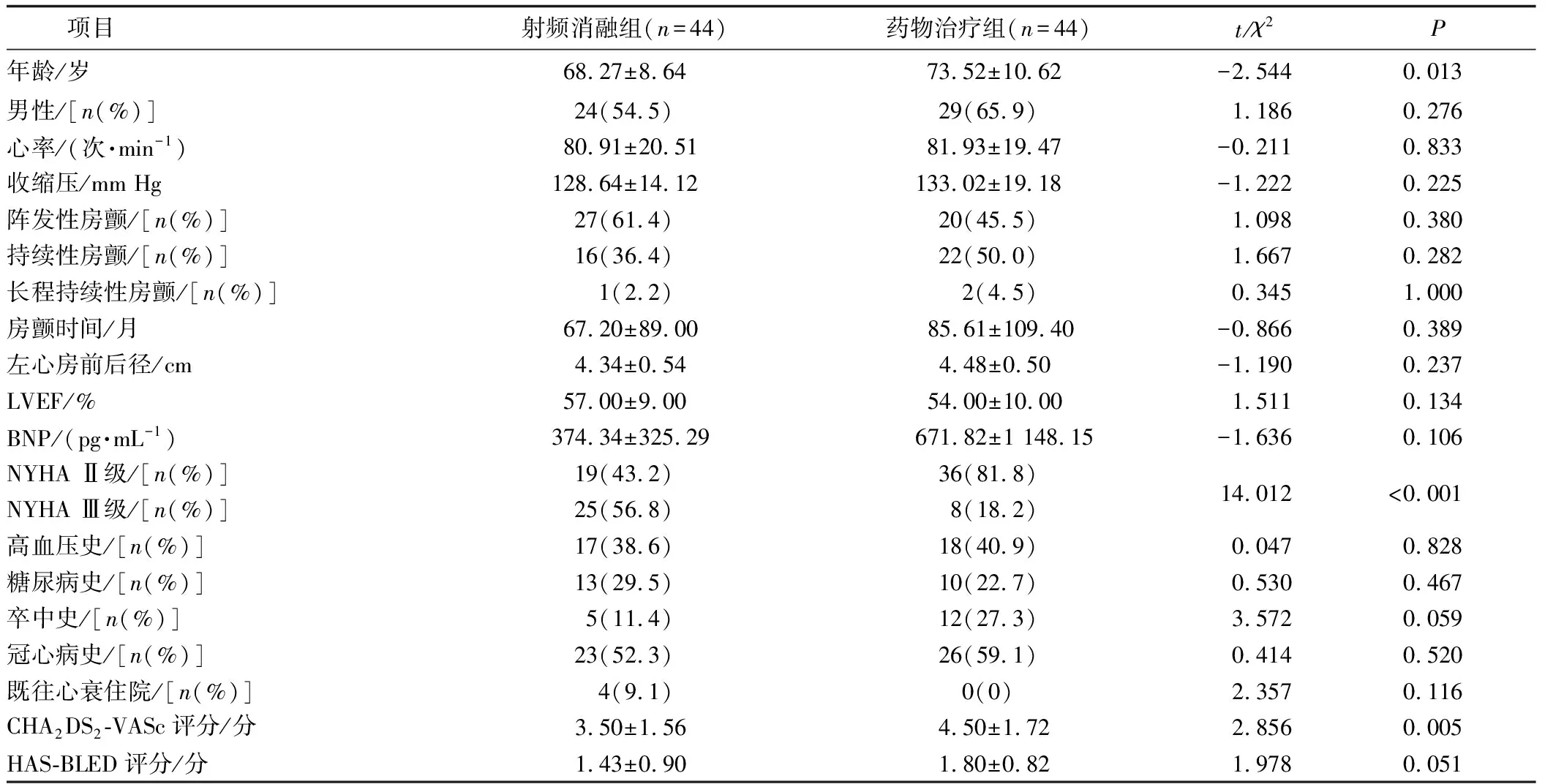
表1 患者基线资料
2.2 观察预后
2.2.1 窦性心律维持率
术后中位时间为12个月的随访显示,射频消融组有13例复发,其中2例予电复律转复,2例行二次射频消融治疗;药物治疗组有31例复发,射频消融组的复发率显著低于药物治疗组(P<0.001),见图2。
2.2.2 心衰再入院次数
两组患者的中位再入院次数均为0,故增加了累计再入院次数的比较。射频消融组的累计次数为7次;药物治疗组的累计次数为18次。组间差异有统计学意义(Z=-2.115,P=0.034),见表2。
2.2.3 生存率
随访显示,射频消融组有1例死亡,药物治疗组有7例死亡,均为心源性死亡。射频消融组患者的生存率显著高于药物治疗组(P=0.007),见图3。
2.3 观察指标
2.3.1 LVEF
由于药物治疗组持续性房颤患者比例高于射频消融组,考虑到房颤负荷对心功能改善的影响,笔者将两组患者按照房颤类型分开进行对比。
对于阵发性房颤患者,治疗前射频消融组(59%±8%)与药物治疗组(53%±11%)的差异有统计学意义(P=0.004)。随访3个月(60%±7% vs 54%±10%,P=0.003)、6个月(60%±7% vs 54%±10%,P=0.001)、9个月(61%±7% vs54%±9%,P=0.013)和12个月(64%±4% vs52%±10%,P=0.001),差异均有统计学意义。在随访时间方面,射频消融组中,时间因素对LVEF的单独效应有统计学意义(P=0.017),药物治疗组中则无统计学意义(P=0.422),见表3和图4。

图2 患者复发情况

表2 心衰再入院情况

图3 生存率

表3 阵发性房颤患者LVEF改善情况
对于持续性房颤患者,在组别方面,治疗前射频消融组与药物治疗组的差异无统计学意义(P=0.943)。随访9、12个月时,差异有统计学意义(59%±8% vs 57%±4%,P=0.020;64%±3% vs 55%±3%,P=0.004)。在随访时间方面,射频消融组中,时间因素在射频消融组(P=0.005)和药物治疗组(P=0.008)均对LVEF的单独效应有统计学意义,见表4和图5。

图4 阵发性房颤患者LVEF改善情况
2.3.2 左心房前后径
由于两组患者不同房颤类型比例不同,持续性房颤患者通常拥有更大的左心房前后径,笔者仍将两组患者根据房颤类型进行比较。

图5 持续性房颤患者LVEF改善情况
在组别方面,治疗前射频消融组[(4.21±0.47)cm]与药物治疗组[(4.32±0.50)cm]的差异无统计学意义(P=0.275)。随访3个月[(3.99±0.29)cm vs (4.34±0.54)cm,P=0.019]、6个月[(3.78±0.33)cm vs (4.46±0.60)cm,P=0.001]、9个月[(3.73±0.36)cm vs (4.56±0.54)cm,P<0.001]和12个月[(3.66±0.32)cm vs (4.73±0.62)cm,P<0.001],差异均有统计学意义。在随访时间方面,时间因素在射频消融组(P=0.006)和药物治疗组(P<0.001)均对左心房前后径的单独效应有统计学意义,见表5和图6。

表4 持续性房颤患者LVEF改善情况
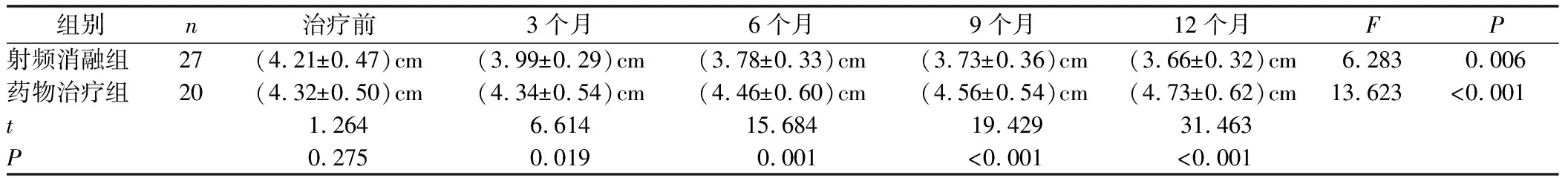
表5 阵发性房颤患者左心房前后径改善情况

图6 阵发性房颤患者左房前后径改善情况
对于持续性房颤患者,在组别方面,治疗前射频消融组[(4.80±0.66)cm]与药物治疗组[(4.65±0.67)cm]的差异无统计学意义(P=0.897)。随访3个月[(4.62±0.46)cm vs (4.78±0.55)cm,P=0.047]、6个月[(4.42±0.46)cm vs (4.98±0.52)cm,P=0.002]、9个月[(4.13±0.45)cm vs (5.08±0.56)cm,P<0.001]和12个月[(3.97±0.50)cm vs (5.23±0.43)cm,P<0.001],差异均有统计学意义。在随访时间方面,时间因素在射频消融组和药物治疗组均对左房前后径的单独效应有统计学意义(P<0.001),见表6和图7。

表6 持续性房颤患者左房前后径改善情况
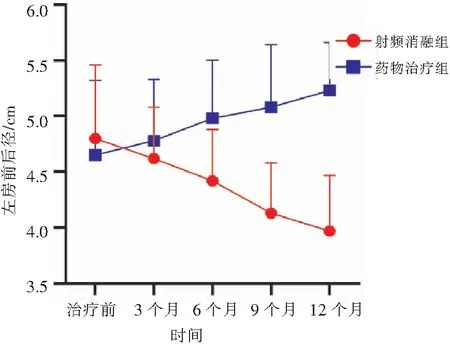
图7 持续性房颤患者左房前后径改善情况
2.4 亚组分析
2016年ESC心衰指南[7]将LVEF为40%~49%的心衰定义为中间范围射血分数心衰(heart failure with mid-range ejection fraction,HFmrEF)。考虑到HFmrEF患者同样以收缩功能受限为主以及样本量的限制,本研究将接受射频消融的HFmrEF患者(2例)归入HFrEF组。接受射频消融的患者中HFrEF组有6例,HFpEF组有38例。在中位时间为12个月的随访中,HFrEF组患者中有1例复发,HFpEF组患者中有12例复发,差异不具有统计学意义(χ2=0.554,P=0.652),见表7。

表7 HFpEF和HFrEF患者的房颤复发情况
在LVEF改善方面,治疗前HFpEF组(61%±6%)与HFrEF组(40%±7%)的差异有统计学意义(P=0.004)。随访3个月(63%±2% vs 47%±8%,P=0.005)、6个月(64%±1% vs 51%±8%,P=0.017)和9个月(64%±2% vs 53%±8%,P=0.021),差异均有统计学意义。在随访时间方面,HFpEF组(P=0.004)和HFrEF组(P<0.001)中,时间因素对LVEF的单独效应均有统计学意义,见表8和图8。HFpEF患者的LVMI由治疗前的102.12%±22.31%降低至随访12个月时的94.51%±20.55%,差异不具有统计学意义(P=0.104),见表9。

表8 HFpEF和HFrEF患者不同时间点的LVEF

图8 HFpEF和HFrEF患者不同时间点的LVEF
3 讨论
3.1 主要发现
射频消融能维持大多数房颤患者的窦性心律,尽管少数患者需接受二次消融或电复律。与药物治疗相比,射频消融能在早期显著改善患者的心功能,降低再入院率和死亡率,这与CASTLE-AF研究和AATAC研究得出的结论一致[8-9]。笔者发现两组患者的生存率从随访12个月后开始出现明显差距,随着随访的进行,差距不断扩大,因此笔者认为射频消融对于房颤伴心衰患者的长期生存率有明显的益处。因为两组患者在伴随疾病方面无明显差异,且所有死亡患者均为心源性死亡,笔者考虑可能仍与消融具有更高的窦性心律维持率从而改善心功能有关。此外虽然药物治疗组患者的心功能分级水平在基线时是优于射频消融组的,但随访12个月时的死亡率(11.4%)反而高于射频消融组(2.3%),进一步说明房颤负荷对心功能的不利影响以及消融对心功能的益处。因此笔者认为持续性房颤患者可能通过消融获益更多。

表9 HFpEF患者的LVMI改善情况
3.2 窦性心律维持率
维持窦性心律意义重大。窦性心律的维持可防止心动过速性心肌病,且能有效地降低卒中风险,还可减少甚至停止抗凝药物的使用,从而降低相关的出血风险[10]。最新公布的AMICA研究[11]认为,在房颤伴心衰患者中,接受射频消融能实现比药物治疗更高的窦性心律维持率。在本研究中,射频消融组的窦性心律维持率(70.5%)同样显著高于药物治疗组(27.3%)。然而,本研究中两组的Kaplan-Meier曲线在随访后期均出现显著下降趋势,笔者认为与后期随访人数较少有关。术后18个月及24个月的随访人数明显低于随访12个月内的,且随着随访的进行,患者房颤复发的可能性也逐渐增加,而这几位复发的患者却大大增加了复发患者在分析中的权重,因此出现了图示的情况,造成一定的偏倚,但这并不妨碍笔者从总体的角度去看待射频消融相对于药物治疗在窦性心律维持率的优势。
3.3 心功能改善
在心功能改善方面,随访显示对于心衰伴房颤患者,射频消融组的左心房前后径随着随访的进行不断缩小,药物治疗组则不断增大。射频消融能有效维持患者的窦性心律,减少患者左心房的无序收缩,从而逆转患者的心房重塑,减小患者的左心房大小。对于心衰伴阵发性房颤患者,射频消融组LVEF均随着随访的进行逐渐升高,而药物治疗组LVEF随时间的改变不明显,术后射频消融组的LVEF均显著高于药物治疗组,但在治疗前射频消融组的LVEF也显著高于药物治疗组,并不能说明射频消融的疗效一定优于药物治疗。对于心衰伴持续性房颤患者,射频消融组和药物治疗组LVEF均随着随访的进行逐渐升高,在术后的9个月以及12个月,射频消融组的LVEF均显著高于药物治疗组,显示出更好的疗效。在NYHA心功能分级方面,随访结束时,射频消融组患者的心功能分级强于药物治疗组(P<0.001),但射频消融组在基线时的心功能分级低于药物治疗组(P<0.001)。总体来说,射频消融能改善房颤伴心衰患者的心功能,但本研究只纳入了心功能Ⅱ级或Ⅲ级的患者,是考虑到心功能过差的患者可能不能耐受射频消融治疗,其疗效也受较多因素的干扰。既往大多数研究均只在心功能Ⅱ级或Ⅲ级的患者中评估改善情况,CASTLE-AF研究[8]虽纳入了心功能Ⅳ级的患者,但在终点事件的亚组分析中也只评估了Ⅱ级和Ⅲ级的患者,CAMERA-MRI研究[12]纳入心功能Ⅱ~Ⅳ级的患者,并认为接受射频消融的患者能更显著地改善心功能分级。因此,心功能较差的患者的治疗策略仍需更加谨慎且系统地评估。
3.4 亚组分析
在本研究中,HFrEF和HFpEF患者的房颤复发率并无显著性差异(P=0.652)。左心室舒张功能障碍是HFpEF的重要特征,可加重左心房重塑,促进房颤基质的发生和发展[13]。因此,在不使用AAD的情况下,HFpEF患者窦性心律的维持可能比无心衰和HFrEF的患者更为困难。对于心室功能受限的HFpEF患者,房颤减少舒张期充盈时间,而有效心房收缩的丧失增加了对左室充盈和血流动力学的不利影响。因此,从理论上讲,HFpEF患者可从节律控制中获得益处,对于伴有房颤的患者,射频消融可能是一种更有效的治疗选择。Kelly等[14]的研究认为对于年龄>65岁的房颤伴HFpEF患者,节律控制可有效降低1年内全因死亡的风险。尽管该研究中大部分接受节律控制策略的患者应用AAD而非射频消融治疗,但良好的预后使笔者相信射频消融作为一种更高效的节律控制手段能为患者带来更大的获益。最近一项meta分析纳入了6项评估射频消融在房颤伴HFrEF或HFpEF患者疗效差异的研究,认为房颤伴HFpEF患者接受射频消融能获得更低的死亡率以及更显著的生活质量改善[15]。本研究中HFpEF和HFrEF患者在接受射频消融后均有较高的窦性心律维持率,而HFpEF患者显示出相比HFrEF患者更高的复发率,笔者考虑与HFrEF患者数量较少所产生的偏倚有关。本研究中,HFpEF和HFrEF患者的LVEF均较前显著增加,且HFrEF患者的改善更加明显,但笔者认为不能仅凭LVEF的改善程度就认为HFrEF患者从射频消融的获益更大。射频消融组和药物治疗组患者在射频消融前均达到了最佳的心率控制(平均心率分别为80.91次/min和81.93次/min),且心率从基线到随访期间无显著变化。因此,射频消融术后心功能的改善可能更多地与窦性心律的维持有关。关于左心室舒张功能,在房颤患者中,存在单独的舒张功能障碍但保留LVEF的患者并不少见。而本研究采用评估左心室肥大的LVMI作为间接评估左心室舒张功能的指标,一方面由于肥厚的心室通常舒张功能受限,另一方面左心室舒张早期血流速度/舒张晚期血流速度(E/A)敏感性较差,且较多患者测量超声心动图时处于房颤状态,无法获得准确的E/A值。虽然术后与术前的差异无统计学意义,但笔者仍能看到下降的趋势,说明HFpEF患者接受射频消融后舒张功能得到改善,或许随着随访的继续,舒张功能的改善会更加明显。
3.5 局限性
本研究尚存在一定的局限性:(1)随访方法有限:虽然患者门诊随访均有心电图资料,但在两次随访期间并无监测设备,只能依赖患者对自身症状的感知,可能会忽略无症状性复发。(2)受限于回顾性研究的性质,评估心功能指标较少,其中NYHA心功能分级受主观因素影响较大,且不够精确,对于心脏舒张功能也需其他精确指标的评估。(3)本研究的超声心动图结果来源于多位操作者,可能造成一定的偏倚。(4)样本量较小,随访时间较短。
4 结论
与药物治疗相比,射频消融能更有效地维持房颤伴心衰患者的窦性心律,改善心功能,降低再入院率及死亡率。且射频消融对于房颤伴HFrEF或HFpEF的患者均有良好的治疗效果。因此,射频消融应在房颤伴心衰患者的治疗中发挥更大的作用。

