基于农用氢能的Ag/Co-B/CTAB催化氨硼烷产氢性能研究
陈 佳,龙 博,郑书河
(福建农林大学机电工程学院,福建 福州 350108)
0 引言
当今社会,化石能源的使用加剧了环境问题,因此,寻求可替代绿色清洁能源已成为研究者广泛关注的问题。现有的新型能源有氢能、风能、潮汐能、太阳能、核能和生物质能(沼气)等。其中,氢能以其来源广泛、成本低廉、燃烧产物清洁、能源效率高及制备工艺简单等优点被广泛关注[1-2]。近年来,氢气在农业上的应用逐步进入人们的视野,研究显示,氢气是一种重要的植物气体信号分子,它通过参与调控植物激素信号的途径影响植物的生长发育与逆境适应;氢水的杀菌效果可替代部分农药,还能促进果蔬成长、改良土壤;它还可应用于种子萌发、花期调控、农作物产品保鲜等方面,有助于提高病虫害抗性和农产品品质,并减少化肥的使用等[3-4]。另外,氢燃料在农业生产中极具潜力,氢能源作为一种新的可再生能源,对于农民来说,可以用氢燃料来发电和驱动引擎,完全可以取代柴油,既保护了环境也节省了成本,这预示着“氢农业时代”的到来[5-9]。相信,在未来,农民可以使用氢水代替或部分代替农药和化肥,让农作物的抗病、抗虫、抗旱和抗盐等能力进一步增强,同时也能带来农产品品质的提升和产量的增加。因此,这也意味着解决如何将氢能源大规模生产和如何将其应用到农业生产上等问题是重中之重[10-14]。目前,制氢的方法有多种,主要包括电解水制氢、水煤气法制氢、矿物燃料制氢、石油热裂解的合成气和天然气制氢、金属与酸反应制氢等,以上方法基本是利用化石燃料来产氢的,缺点是资源消耗过大,也不利于保护环境。因此,探索出一种廉价高效清洁氢气生产方式,有利于氢能作为农业能源的普及[15-16]。
常见的储氢材料有氨硼烷(ammonia-borane,AB)、硼氢化钠、硼氢化钾和腈硼烷,其中AB因其较高的储氢能力(氢含量约为19.6 wt%)、在水中的高溶解度和成本较低而成为极具前景的储氢材料之一,满足当前对清洁能源的要求[17-22]。虽然已经开发出了一些贵金属(Pt、Rh、Ru、Pd等)非均相催化剂来完成AB转化为氢气,且具有良好的活性,但因资源有限、成本昂贵阻碍了其实际应用[23]。到目前为止,开发的用于AB水解的非贵金属催化剂很少,但与贵金属催化剂相比,非贵金属催化剂的转化率仍然不高。因此,开发廉价、高效的非贵金属催化剂,进一步提高常温环境条件下的催化活性(catalytic activity,CA)、选择性和转化率是安全高效储氢的关键,因此对钴硼化物展开了大量的研究[24-26]。
钴硼化物(Co-B)是催化AB水解的一种廉价而有效的催化剂,在文献中大体上可分为非负载型催化剂、负载型催化剂、多元合金催化剂等,改性的钴硼化物催化剂由于硼中缺乏电子,电子很容易从钴转移到硼,从而大大提高了AB水解制氢的效率[27-31]。但由于钴硼化物具有磁性,在催化过程中极容易发生团聚,故而使得其有效面积会显著减小,影响其催化性能。因此,研究如何保证钴硼化合物在催化过程中的比表面积(BET)不会显著减小、提高其催化活性位点成为了研究热点[32]。
本课题组制备了一种基于银/钴硼化物/十六烷基三甲基溴化铵(Ag/Co-B/CTAB)复合结构的新型催化剂,Ag/Co-B/CTAB催化剂催化AB得到的氢气可以应用于农业生产加工中,不仅保护了环境,还具有一定的经济价值。在样品分析时发现金属状态下的Ag作为一个原子势垒,以避免Co-B粒子团聚,有利于粒子更好地分散,从而可以有效增加催化剂的BET。单质银的加入促进了电子的传递,电子转移增强了活性物种之间的相互作用,Ag在Co-B上的高度分散增加了暴露的活性中心的数量,分散了Co的活性位点,从而提高了催化活性。CTAB作为模板剂具有优良的亲水性,可以控制催化剂的形态,使水分子能够快速到达催化剂表面。这可以加速攻击硼-氮键使其断裂,证明自组装形成的复合结构大大提高了催化性能。此外,还比较了Co-B/CTAB和Ag/Co-B/CTAB样品,分析了Ag/Co-B/CTAB样品的优点。
1 材料与方法
1.1 试验材料
试验材料如表1所示。

表1 试验材料Tab.1 List of test materials
1.2 试验设计
试验中采用还原法制备Ag/Co-B/CTAB化合物,在烧杯中加入20 mL去离子水、0.238 g CoCl2·6H2O和0.1 g CTAB进行搅拌,将50 mL去离子水、0.01 g NaBH4、0.01 g NaOH配置成溶液作为还原剂,在不断搅拌中加入上述溶液。反应结束后将溶液中的沉淀物过滤,用去离子水和酒精多次冲洗以去除不必要的离子。洗涤后得到的黑色粉末在60 ℃真空干燥6 h,所得样品记为Co-B/CTAB。之后将得到的Co-B/CTAB样品加去离子水在超声波清洗机中超碎,然后将硝酸银溶液加入上述溶液,重复上述的离心洗涤的步骤,干燥后所得样品记为Ag/Co-B/CTAB。
1.3 催化剂表征
采用傅里叶变换红外光谱(FTIR)对样品进行纯度鉴定,观察特征峰强度的变化。用X射线衍射仪(Cu Kα,λ=1.541 78 Å)在40 kV和40 mA条件下,在10°~80°的2θ范围内,以2°/min的扫描速率对催化剂进行了粉末X射线衍射(XRD)分析。利用X射线光电子能谱(XPS)确定了催化剂的基本元素成分和表面能态分布。使用卡尔·蔡司扫描电子显微镜获得扫描电镜(SEM)图像。使用JEOL 2100F透射电子显微镜(TEM)获得样品的微结构和微区组成。根据美国康塔仪器公司的体积分析仪获得吸附等温线,用Brunauer-Emmett-Teller方法确定比表面积。
1.4 氢气生成速率(HGR)测量
如图1所示,AB的水解反应是在一个小型单颈玻璃烧瓶反应器(50 mL)的水浴加热系统中进行的。样品、AB、NaOH溶液一起放入超声浴反应器中,AB在30 ℃常压下发生水解脱氢反应。在整个测量过程中,通过一个充满水的滴定管测量氢气的体积。此外,还研究了反应温度对AB水解的影响,考虑温度范围为30~60 ℃。
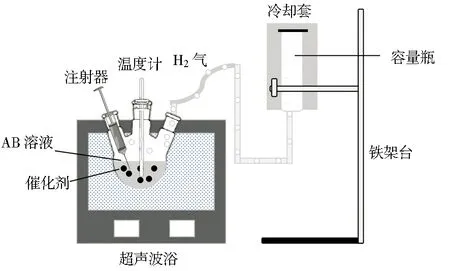
图1 氨硼烷溶液超声水解制氢测试Fig.1 Test of hydrogen production by ultrasonic hydrolysis of AB solution
2 结果与分析
2.1 催化剂物性表征
通过FTIR对制备的Ag/Co-B/CTAB、Co-B/CTAB催化剂的图像进行了分析,如图2所示。由图2a可知,常温下FTIR光谱范围为400~4 000 cm-1,可以在3 450 cm-1处观察到结构O-H的拉伸振动;吸附水的拉伸振动峰值为1 630 cm-1,此时具有H-O-H的形变振动特征,表明制备的样品催化剂在AB水解过程中具有较强的吸附水作用;而在1 398 cm-1附近有一个峰,这是B-O的拉伸振动引起的吸收带(υas(B3-O));另外,B-O振动引起的吸收带(δ(B-O-B))在661 cm-1处也清晰可见[33-35]。
由图2b可知,Ag/Co-B/CTAB粉末具有多晶结构。以Ag/Co-B/CTAB催化剂为例,可以观察到在36.041°、43.038°、46.159°、50.674°、51.911°、57.363°和58.357°的衍射峰,这归因于Co3B2的四方晶系的(200)、(002)、(211)、(112)、(220)、(202)和(310)晶格面(JCPDS:00-045-1182),而在38.115°、44.299°、64.443°和77.397°的衍射峰是Ag的三方晶系的(111)、(200)、(220)和(311)晶格面(JCPDS:01-087-0597),表明了单质银成功的掺杂在Co-B中,电子的转移使得Ag+得到电子被还原成了单质Ag[36]。另外,对于Co-B/CTAB催化剂来说,它与Ag/Co-B/CTAB催化剂的Co3B2具有相同的特征峰,但是Ag/Co-B/CTAB中的Co2+含量明显高于Co-B/CTAB催化剂,这可归因于银的加入促进了电子的转移,使得Co2+含量变高[37-39]。

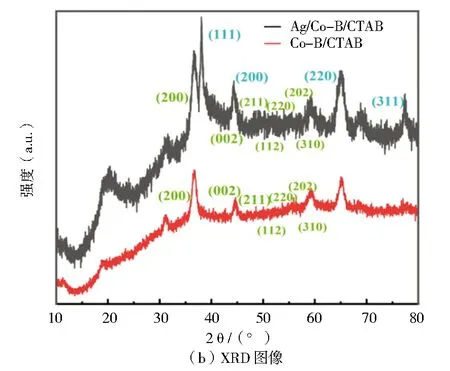
图2 Ag/Co-B/CTAB、Co-B/CTAB催化剂的FTIR图像和XRD图像分析Fig.2 FTIR images and XRD images analysis of catalyst Ag/Co-B/CTAB、Co-B/CTAB
图3为Ag/Co-B/CTAB的XPS全谱图,Ag/Co-B/CTAB纳米颗粒主要由Co、B、Ag、O和C元素组成[40]。Ag/Co-B/CTAB材料的Co 2p区有两个主峰,分别为780.1和794.9 eV,卫星峰分别为782.2、797.9 eV和787.75、803.45 eV,表明元素Co既存在于金属态,也存在于氧化态。与氧化钴峰相关的2+态归因于Co(OH)2,可能是在催化剂制备过程中Co、B、Ag三者间发生了电子的转移。另外,这些复合催化剂的Co峰有不同程度的正位移(有一个较大的结合能),而一个较大的结合能表示Co存在着更多的氧化态。在191.6 eV处也观察到XPS峰,这与Ag/Co-B/CTAB中的B 1s的氧化态水平相对应,也与文献中报道的B 1s水平相似[41]。结合图2b的XRD结果分析表明,与纯硼(187.1 eV)的结合能值相比较,Ag/Co-B/CTAB催化剂中硼的结合能值有明显的4.5 eV的正位移,比已知结果(1.0 eV)要大,这种转移也证明了合金的电子转移,佐证了Co、B和Ag在Ag/Co-B/CTAB晶体结构中电子的转移使得样品的协同效果较好,这提高了催化性能,缩短了反应时间[42-44]。Ag/Co-B/CTAB催化剂得到的Ag 3d XPS光谱在374.2 eV和368.2 eV处有两个峰,可以归为单质银成分。这是由于3d双峰分裂6.0 eV,Ag 3d核心能级谱代表两个强峰,证实了银的金属性质。另外,催化活性取决于金属的电子性质,单质银的加入改变了Co-B结构的电子环境,与未加银的Co-B的比较表明,Ag/Co-B/CTAB催化剂中发生了从Co-B到银的电荷转移,这种转变导致了富电子Ag/Co-B/CTAB样品的电子负值净差异,Ag+得到电子被还原成单质Ag。而金属状态下的Ag作为一个原子势垒,避免了Co-B粒子的团聚,有利于粒子更好地分散,从而保持较高的BET[36,39,45]。
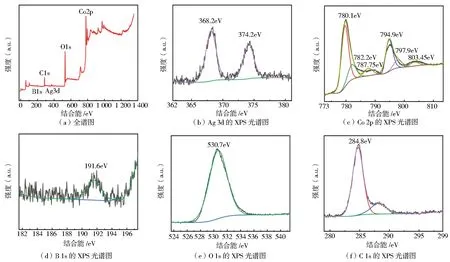
图3 Ag/Co-B/CTAB催化剂的XPS图像分析Fig.3 XPS images analysis of catalyst Ag/Co-B/CTAB
试验制备的催化剂形貌示意如图4所示。由图4a中Ⅰ、Ⅱ和Ⅲ中可以看出,Co-B/CTAB由堆积的球形颗粒组成,而CTAB通常作为模板剂和修饰剂来控制Co-B的形态生长和控制Co2+的络合,因此Co-B/CTAB有更多异常皱纹和卷曲边缘。加入单质Ag后,Ag/Co-B/CTAB的形貌与Co-B/CTAB形貌保持一致,没有明显的改变,为了进一步获得关于样品的结构和元素组成的信息,进行了TEM分析,结果如图4b所示。从图中结果发现,单质Ag被成功地掺杂到催化剂中,这与XRD和XPS的结果相吻合。由图4c可知,在合成的Ag/Co-B/CTAB中可以清晰地观察到Ag纳米颗粒,进一步证实了Ag纳米颗粒掺杂在Co-B中。另外,间距为0.239 nm的特征晶格条纹是Ag的(111)面,它也明确地表明Ag/Co-B/CTAB纳米颗粒由许多结晶良好的晶粒组成[36,39,46-47]。
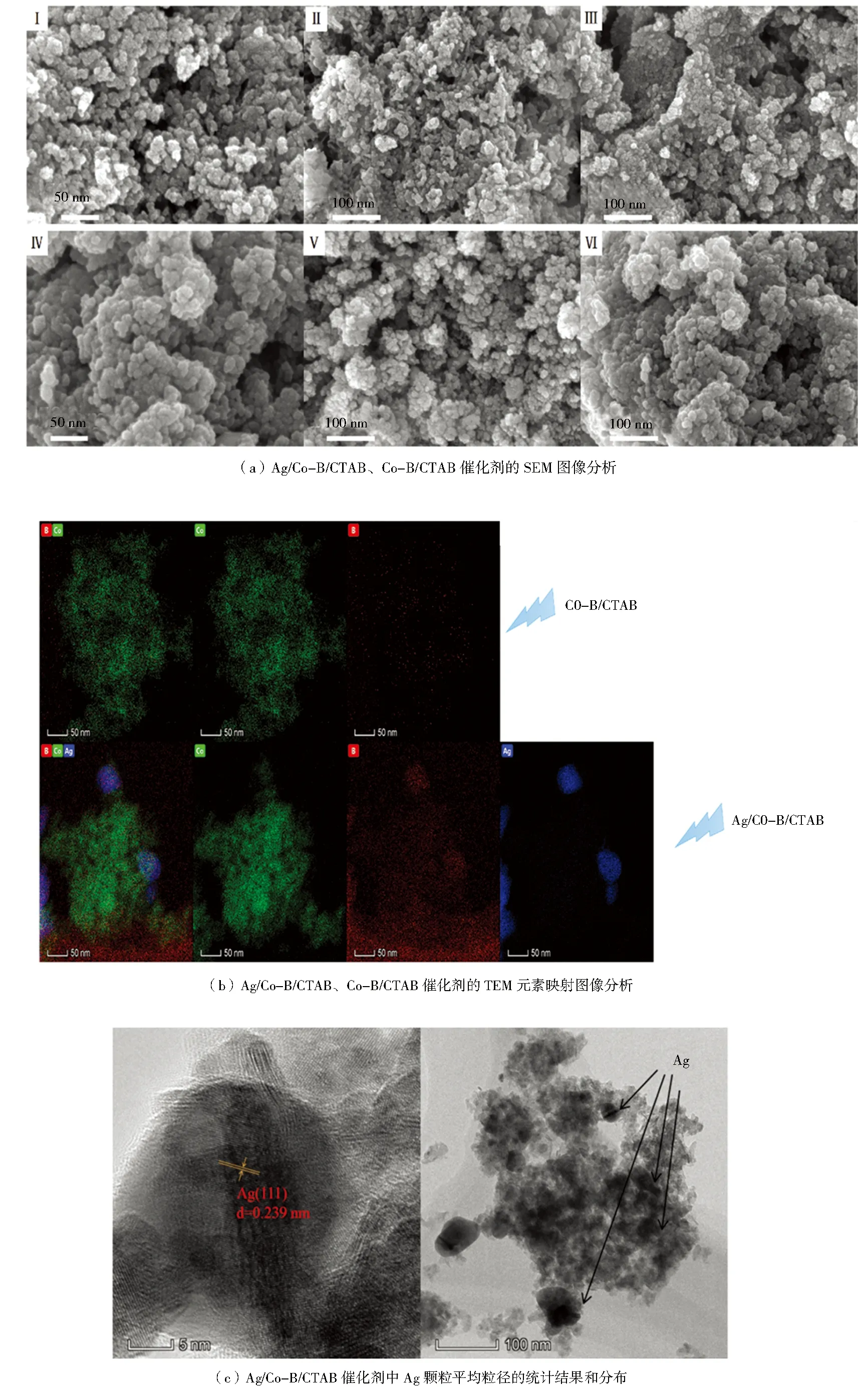
图4 试验制备的催化剂形貌示意Fig.4 Morphology of catalyst prepared in the test
由图5a催化剂的氮气吸附-脱附等温线可以观察到,按照IUPAC分类,催化剂的等温线都表现出典型的类似于IV ADI的H3型滞后回路。表2中总结了Ag/Co-B/CTAB、Co-B/CTAB催化剂详细的结构特性,包括比表面积、平均孔径和孔容。发现Ag/Co-B/CTAB催化剂的BET大于Co-B/CTAB,这也表明了当金属Ag作为掺杂剂加入到Co-B样品中,避免了Co-B粒子的团聚,有利于粒子更好地分散,从而保持较高的BET。图5b显示了Co-B/CTAB、Ag/Co-B/CTAB催化剂样品的吸附孔分布图,对照滞后环的种类发现,这两种催化剂的孔隙是片状粒子堆积形成的狭缝孔,这也从侧面证实了CTAB为模板控制催化剂的形貌,使催化剂拥有大的孔径,从而方便单质银的掺杂[31,48]。
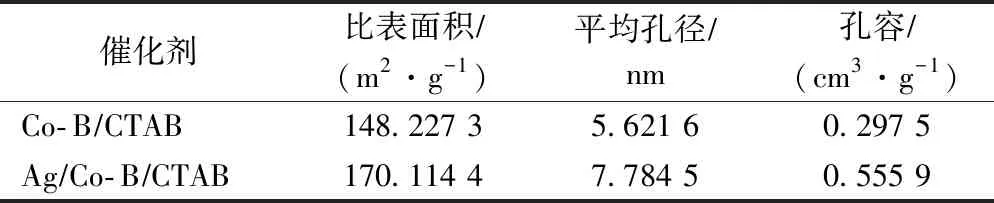
表2 催化剂理化性质Tab.2 Physicochemical properties of catalysts
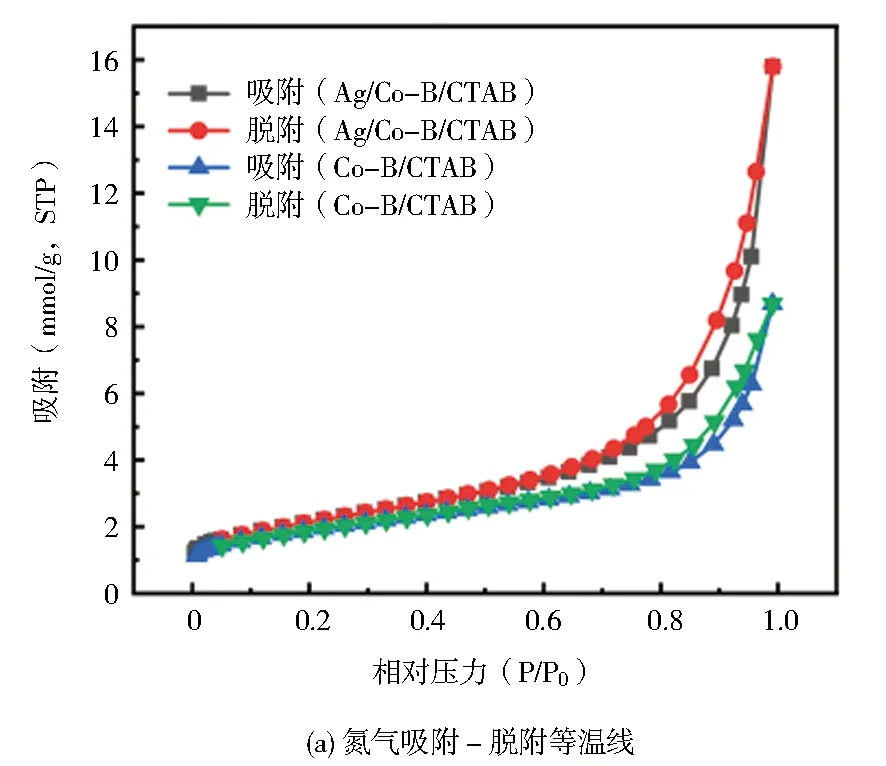
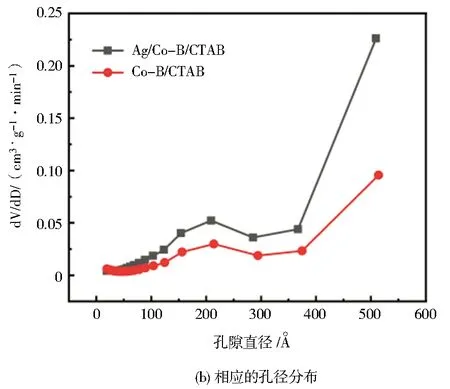
图5 Ag/Co-B/CTAB、Co-B/CTAB催化剂的氮气吸附-脱附等温线和相应的孔径分布Fig.5 N2-adsorption-desorption isotherm and pore size distribution of catalysts Ag/Co-B/CTAB and Co-B/CTAB
2.2 不同因素对催化AB水解产氢速率的影响
试验中为了评价AgNO3浓度对Co-B样品性能的影响,在改性时分别采用了浓度为1%、3%、5%、7%和9%(wt,质量分数,下同)的AgNO3溶液,并比较了制备样品的催化产氢性能,如图6a所示。试验数据采用多次试验的平均数,结果显示Ag/Co-B/CTAB-7%样品的催化产氢效果最佳。这是因为在Co-B样品中加入适量的金属Ag可以提高催化剂的协同效应和电子效应,金属Ag可以分散Co的活性位点;加入过量的Ag,活性部位可能会有一定程度的堵塞,产生相反的作用,同时过量的Ag的负载会影响与催化剂之间的协同效应。因此试验中采用了7%的AgNO3浓度,制备的样品也直接表示为Ag/Co-B/CTAB(代表了Ag/Co-B/CTAB-7%样品)[49-50]。
如图6b所示,对所得到的两种催化剂在AB水解反应中的催化行为进行了估计。AB催化产氢的试验是在超声波震荡的条件下进行的,这两种催化剂的产氢速率(HGR)的大小比较为Ag/Co-B/CTAB[16.185 L/(min·g催化剂)]>Co-B/CTAB[10.76 L/(min·g催化剂)],Ag/Co-B/CTAB粉末催化剂的HGR远远高于未掺杂的Co-B/CTAB的催化剂,这说明了Ag/Co-B/CTAB催化剂具有较高的CA,有利于AB水解。从SEM图也可以证实,单质银的加入有效地阻止了Co-B的团聚,增加了比表面积,从而提高了催化性能[51-53]。
AB的水解温度也是影响HGR催化效率的重要因素之一,通过AB在30~60 ℃不同温度下的水解反应,考察了Ag/Co-B/CTAB样品的催化性能,结果如图6c所示[21]。试验中发现了随着温度的升高,H2的生成率逐渐增强,这证实了Ag、Co、B和CTAB的结合从侧面对催化剂样品有协同作用,促进了催化反应的进展。另外,AB在样品(Ag/Co-B/CTAB)存在下水解的活化能(Ea)值计算为12.581 kJ/mol,与其他文献相比,Ag/Co-B/CTAB催化剂的Ea值低于许多其他Co-B合金催化剂,说明其催化活性高于Co-B催化剂[54-55]。
为了研究Ag/Co-B/CTAB催化剂用量对HGR的影响,试验分别用5、10、15和20 mg 4种不同用量的催化剂对AB(0.15 g)溶液进行水解,并在30 ℃下测定HGR,结果如图6d所示。通过试验得到了催化剂用量的增加会增加液固接触的机会,同时由于AB的水解反应是一级水解动力学,因此产氢效率也会成比例增加。SEM和BET结果表明,催化剂的比表面积有所提高,从侧面证实了接触面积的增加[53,56]。
AB浓度对催化剂CA的影响如图6e所示,试验选择AB溶液浓度分别为0.001 62、0.003 24、0.004 86和0.006 48 mol。结果显示,AB溶液浓度越高,总产氢量也越高,但浓度过高会影响水分子到达催化剂表面的速度,从而降低水解产氢速率,随着时间的推移,AB的水解反应速度也逐渐减慢[57]。在Ag/Co-B/CTAB催化剂催化AB水解产氢反应中也会存在部分单质Ag从Co-B表面脱落,导致单质Ag的负载量下降,从而导致了催化剂活性中心可及性的降低,影响了产氢速率[58-59]。

图6 不同因素对Ag/Co-B/CTAB催化剂催化AB水解产氢速率的影响Fig.6 Effects of different factors on hydrogen production rate of AB hydrolysis catalyzed by catalyst Ag/Co-B/ TAB
进一步研究了Ag/Co-B/CTAB催化剂催化AB水解产氢的机理,发现了催化活性与催化剂中金属的电子性质有关。与未加单质银的Co-B/CTAB的比较表明,Ag/Co-B/CTAB催化剂在制备时电子从Co-B向银转移,这种转变导致了富电子的Ag/Co-B/CTAB样品,Ag+得到电子被还原成单质Ag,而金属状态下的Ag作为一个原子势垒,避免了Co-B粒子团聚,有利于Co-B粒子更好地分散,从而保持高的比表面积。另外,Co、B、Ag元素之间的电子转移也增强了活性物种之间的相互作用,而单质Ag在Co-B上的高度分散增加了暴露的活性中心的数量,分散了Co的活性位点,从而提高了催化活性[60]。单质Ag的加入导致AB在催化位点上的强吸附(AB分子在金属Ag表面的活化以解离吸附的形式进行),有效激活B-N键,促进析氢。在试验中也发现CTAB作为模板剂控制了催化剂的形态,使水分子在水解反应中更容易到达催化剂表面,而在理论上,1 mol的AB可以得到3 mol的氢气,具体的反应方程式如式(1)所示,这都是此试验产氢量高的原因[61]。
(1)
3 结束语
本文研究了一种新型Ag/Co-B/CTAB复合材料催化剂。与未掺杂单质银的Co-B纳米颗粒相比,Ag+得到电子被还原成单质Ag,而金属状态下的Ag作为一个原子势垒,以避免Co-B粒子团聚,这有利于粒子更好地分散,从而保持高的比表面积,而单质Ag的加入导致AB在催化位点上的强吸附(AB分子在金属Ag表面的活化以解离吸附的形式进行),可以有效地激活B-N键(这是由于Ag/Co-B/CTAB催化剂的改性表面与AB相互作用的结果),从而降低反应能位垒,促进析氢。另外在催化过程中电子也得到了传递,最终有望提高催化产氢速率。Ag/Co-B/CTAB催化剂的HGR为16.185 L/(min·g催化剂),进一步提高了AB水解反应的产氢速率。试验所研究的金属促进Co-B合金粉末在AB水解过程中的高产氢率也得到了证实,这种具有低成本效益的催化剂可能会导致氢气大规模生产的应用前景,并为农业的未来指引方向,引领我们走向“氢农业时代”。

