原发性肺淋巴上皮瘤样癌1例并文献复习
郭健,张有志,陈佶,周仲文,陈小东
原发性肺淋巴上皮瘤样癌(primary pulmonary lymphoepithelioma-like carcinoma,PPLELC)是一种罕见的原发性肺恶性肿瘤,在2015 年WHO 肺肿瘤组织学分类中被划分为“其他未分类癌”[1]。它是一种爱泼斯坦巴尔病毒(EBV)相关的上皮性肿瘤,1987 年首次报道该病,后续大多数报告来自东亚国家,罕有病例在西方国家[2-3]。研究表明,PPLELC如能早期诊断,预后优于其他非小细胞肺癌(NSCLC)亚型。然而,PPLELC 常误诊为肺鳞癌,临床医生对该病认识不足。为探讨PPLELC 的临床特点、诊断和治疗方法,现结合近期诊治的1 例PPLELC,并复习国内外相关文献对该病予以分析讨论。
1 临床资料
男,57岁,因“咳嗽伴痰中带血2周”于2021年3月17 日第一次入住复旦大学附属华山医院。病人入院2 周前无明显诱因下出现咳嗽,咳痰,痰中带血,无鼻塞、咽痛,无发热,无胸痛,于2021 年3 月3日就诊当地医院门诊治疗,期间于2021年3月12日行胸部CT 平扫示左下肺前基底段不规则高密度斑片影(图1),考虑肺炎,予以左氧氟沙星治疗1周,咳嗽有所好转,仍有痰血,为进一步诊治而入我院。既往史:否认鼻炎、慢性阻塞性肺疾病、原发性高血压等慢性疾病史;无吸烟、饮酒史。
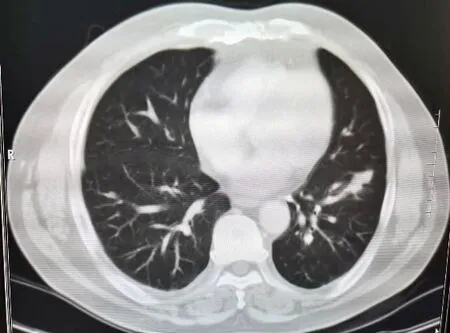
图1 2021年3月12日胸部CT平扫:左下肺前基底段不规则高密度斑片影
查体:体温36.6 ℃,血压125/75 mmHg(1 mmHg=0.133 kPa)。口唇无紫绀,鼻中隔无偏曲,鼻旁窦区无压痛。皮肤黏膜未见黄染及出血点,浅表淋巴结未及肿大。头颈无异常,胸廓无畸形,双肺呼吸音清,未闻及干湿啰音,心率76 次/分,心律齐,无杂音,腹平软,无压痛,肝脾肋下未及,脊柱四肢未见异常。
辅助检查:2021 年3 月18 日血常规白细胞计数为5.10×109/L,中性粒细胞为0.65,红细胞沉降率为12 mm/h,C 反应蛋白为1.60 mg/L,降钙素原为0.02 μg/L;痰涂片和培养阴性,1,3-β-D 葡聚糖检测试验、乳胶凝集试验和半乳甘露聚糖试验阴性,结核感染T细胞检测阴性,支原体、衣原体及军团菌抗体均阴性,血清肿瘤标志物、ANA、ENA、抗dsDNA 正常。气管镜下见左右各级支气管未见明显异常,于左下叶前段行经引导鞘管支气管内超声(EBUS-GS)探及异常回声,活检病理示间质慢性炎症、肺泡间隔增宽,小灶支气管上皮增生;支气管肺泡灌洗液常规和生化正常,mNGS:细菌、真菌、寄生虫、结核分枝杆菌复合群、支原体、衣原体和立克次体均为阴性,人类疱疹病毒4型(EBV)检出序列数4785。
诊治经过:入院完善气管镜等相关检查后予以出院,嘱其继续口服左氧氟沙星治疗1 周及1 月后复查肺CT。于2021 年5 月2 日复查肺CT 见左下叶病灶(图2)较前(2021年3月12日)有所增大。遂再次入院,于2021 年5 月12 日行CT 引导下经皮肺穿刺,组织病理示淋巴细胞中散在异性上皮细胞,免疫组化:细胞角蛋白(CK)(+),EB 病毒编码的小RNA(EBER)(+),突触素(Syn)(-),甲状腺转录因子-1(TTF-1)(-),增殖指数(Ki67)(40%+),肿瘤蛋白63(P63)(+),新天冬氨酸蛋白酶A(Napsin A)(-);特染:过碘酸雪夫氏染色(PAS)(-),抗酸(-),银染(-),结合酶标,符合淋巴上皮瘤样癌(图3)。五官科会诊行鼻窥镜等检查未见鼻咽部异常表现。进一步完善相关检查评估病情后,于2021 年5 月26日行左下叶切除手术。
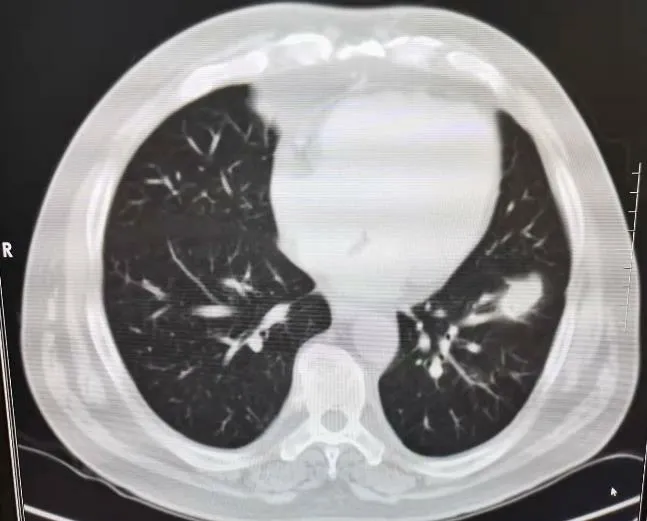
图2 2021年5月2日胸部CT平扫:左下肺病灶范围较前增大,并见空泡征
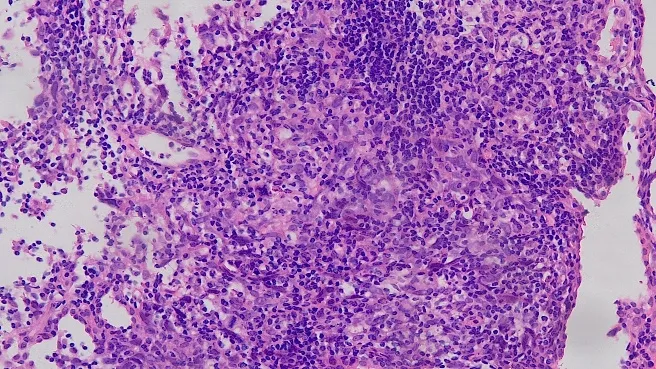
图3 左肺下叶穿刺组织病理(HE×200):肺淋巴上皮瘤样癌,瘤细胞呈巢状排列,伴大量淋巴细胞浸润
2 结果
肺左下叶切除术后切除组织病理报告为“低分化癌伴大量淋巴细胞浸润,鳞癌可能”;切片送至复旦大学附属肿瘤医院病理科会诊,结果为低分化癌伴EBV 感染及大量淋巴细胞浸润,符合淋巴上皮瘤样癌(lymphoepithelioma-like carcinoma,LELC)。病人目前术后恢复良好,紫杉醇和卡铂同时联合免疫检查点抑制剂(ICI)替雷利珠单抗辅助治疗中。
3 讨论
PPLELC 约占NSCLC 的0.7%,通常发病于年轻、不吸烟的亚洲人群,我国报道最多[2],且多集中于华南地区,本病例为华东地区首次报道。众所周知,吸烟是肺癌最重要的危险因素,然而大多数PPLELC 病人无吸烟史。PPLELC 同其他类型肺癌临床表现一致[4],并无特异症状,最常见表现为咳嗽,其他包括咯血、胸痛、体质量减轻等。部分病例于健康体检中被偶然发现。
PPLELC 肺CT 主要表现为结节或肿块,大多数表现为胸膜附近的孤立性肺结节或团块影,直径<3.5 cm,通常不累及淋巴结,晚期常常出现支气管血管周围淋巴结转移、血管包绕和扩张等征象[5]。左下叶是好发部位,病灶内钙化和空洞不常见,这与常伴发空洞的鳞癌有之区别。本例病人发病部位也是在左下叶近叶间胸膜,但其形态不规则,影像学表现类似肺炎。相关报道显示PPLELC 肿瘤细胞摄取FDG 不尽一致,因此PET/CT 在PPLELC 中的鉴别诊断价值存有争议[6]。
PPLELC 特征性病理学表现是间质和癌细胞之间有致密淋巴细胞及浆细胞浸润[7],这是一种反应性增生改变。绝大部分病例组织标本通过原位杂交技术可检测EBV编码RNA[8]。免疫组化显示CK、EMA 为癌细胞表达的最常见分子[7]。由于PPLELC在组织学上与未分化的鼻咽癌无明显区别,需要排除鼻咽部原发的转移性LELC[9]。本例病人经鼻咽内窥镜和影像学检查排除鼻咽癌,结合活检组织病理学和EBV 检测阳性明确诊断为PPLELC。本例病人通过支气管镜于病灶所在叶段行支气管肺泡灌洗术,灌洗液病原微生物二代测序(mNGS)也显示大量EBV,这可能为临床高度怀疑LELC 的病例提供了一种新的诊断思路。
多项研究发现PPLELC 与其他肺癌亚型在突变谱、拷贝数改变和信号通路畸变等方面存在明显差异,在PPLELC 中很少检测到表皮生长因子受体(EGFR)、间变性淋巴瘤激酶(ALK)等驱动基因突变[10-11],本例病人组织标本及血液样本驱动基因检测均为阴性。我国学者通过免疫组化(ISH)和全外显子(WES)检测到所有PPLELC 病例的EBV 编码RNA(EBER)阳性染色和EBV 序列,充分证实EBV感染在PPLELC 中的作用[10],本例病人组织标本基因检测亦显示EBV 阳性。同时,该项研究发现载脂蛋白B mRNA 编辑酶催化多肽(APOBEC)家族基因特征、核因子κB(NF-κB)途径失调和I型IFN基因缺失可能是EBV 诱导PPLELC 形成的原因。此外,发现肿瘤坏死因子受体相关因子3(TRAF3)在PPLELC 中普遍存在突变,包括5%的单体细胞突变和80%的缺失。TRAF3 是一种肿瘤抑制基因,负调控NF-κB 通路[12]。因此,TRAF3 缺失是NF-κB 失调的核心因素,在PPLELC 发生中起着重要作用。以上研究发现可能促进新的治疗策略的发展,如NFκB抑制剂有望成为治疗PPLELC的新方法。
尽管PPLELC 的肿瘤突变负荷较低,但大多数肿瘤的细胞程序性死亡配体1(PD-L1)表达阳性[11,13]。一项来自中国台湾的报告显示PPLELC 中75.8%(50/66)病人PD-L1 阳性[13];另一项研究队列显示69%(20/29)病人的肿瘤表面表达PD-L1,其中14%(4/29)高表达(≥50%),55%(16/29)中度表达(5%~49%)[11]。PD-L1 的高表达通常与细胞程序性死亡受体1/细胞程序性死亡配体1(PD-1/PD-L1)抑制剂的良好反应相关,以上研究提示免疫检查点抑制剂(ICI)可能是治疗PPLELC的重要方法。
PPLELC 尚无标准治疗方案,同其他肺癌亚型类似,根据临床分期选择外科手术、化疗、放疗和免疫治疗等。与氟尿嘧啶或培美曲塞联合顺铂相比,吉西他滨和顺铂可提高转移性或复发性鼻咽癌的生存率[14]。PPLELC 在遗传和组织病理学特征方面与鼻咽癌相似,多项研究同样证实与铂类药物联合化疗的药物中吉西他滨临床疗效优于其他药物,如培美曲塞和紫杉醇[10,15]。在一项研究队列中,对PDL1(+)肿瘤比例得分为15.0%、30.0%和60.0%的三名病人进行免疫治疗,均获得疾病控制[11]。此外,已有研究显示免疫治疗优于化疗[16],这项研究共包括27 名病人,其中ICI 组10 例,化疗组17 例。两组客观缓解率(ORR)分别为80.0% 和70.5%(P=0.678),疾病控制率(DCR)分别为100.0%和88.2%(P=0.516),虽然这两项终点指标差异无统计学意义,但ICI 组病人总体分期更晚,无进展生存期(PFS)明显延长(15.0 m和7.9 m,P=0.005)。
PPLELC 与其他NSCLC亚型比较[7,16],转移率低,预后好,2 年和5 年生存率分别为80.0% 和54.0%。处于疾病早期的病人,肿瘤完全切除后罕有复发[17];晚期病人,化疗和免疫治疗可获得较好的疗效[18-19]。

