利奈唑胺的波谱学特征和结构确证
黄 进,葛永红,朱 琳,袁 磊,罗玉全,高浩凌,*
(1.浙江医药股份有限公司昌海生物分公司,浙江 绍兴 312300;2.浙江医药股份有限公司新昌制药厂,浙江 绍兴 312500;3.浙江医药股份有限公司研究院,浙江 绍兴 312300)
利奈唑胺(Linezolid),化学名为(S)-N-[[3-[3-氟-4-(4-吗啉基) 苯基]-2-氧代-5-噁唑烷基]甲基]-乙酰胺,是Pharmacia &Upijohn 公司研制的第一个噁唑烷酮类抗菌药,于2000 年4 月首次获得美国FDA 批准,商品名为Zyvox,2006 年9月被批准进入中国销售。用于治疗由耐甲氧西林金黄色葡萄球菌(MRSA)引起的院内获得性肺炎、社区获得性肺炎、复杂性皮肤和皮肤软组织感染以及万古霉素耐药的屎肠球菌感染[1-2]。其化学结构见图1。
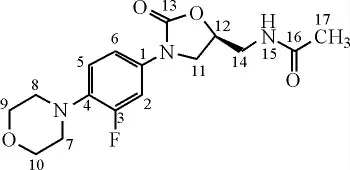
图1 利奈唑胺的化学结构Fig.1 Chemical structure of linezolid
利奈唑胺及其有关物质的合成已有大量报道[3-10],同时也是多晶型药物[11-13]。本研究通过UV、IR、HRMS、NMR、TGA/DSC、PXRD 对利奈唑胺进行较为全面的结构表征,有助于原料药及其杂质的结构研究,对其质量控制和其他药物的分析具有借鉴意义。
1 分析方法与结果
1.1 仪器与材料
仪器:岛津UV-2450 型紫外分光光度计、岛津IRA-1S WL 型傅里叶红外光谱仪、Agilent 1290-G6520B 型液相色谱-质谱联用仪、BRUKER AVANCE Ⅲ400 型超导核磁共振波谱仪、热重分析仪TAQ500、差示扫描量热仪TAQ2000、Brucker D8 Advance X-射线粉末衍射仪。
材料:利奈唑胺(纯度99.99%,浙江医药股份有限公司研究院)。
1.2 紫外光谱(UV)分析
以甲醇为溶剂,将利奈唑胺配制成0.01 mg/mL的溶液,该溶液在258 nm 处有强吸收谱带(图2),为π→π*跃迁,紫外吸收图谱显示了芳香族的特征吸收,显示苯环或杂芳环的存在。

图2 利奈唑胺的紫外吸收光谱Fig.2 UV spectrum of linezolid
1.3 红外光谱(IR)分析
以溴化钾压片法测试IR 光谱(图3),样品红外光谱吸收峰在3361.93 cm-1、1751.36 cm-1、1674.21 cm-1、1516.05 cm-1、1444.68 cm-1、1409.96 cm-1、1357.89 cm-1、1328.95 cm-1、1273.02 cm-1、1236.37 cm-1、1219.01 cm-1、1143.79 cm-1、1114.86 cm-1、1076.28 cm-1、1064.71 cm-1、1049.28 cm-1、906.54 cm-1、850.61 cm-1、756.10 cm-1,与文献[11]报道的晶型Ⅱ基本一致。
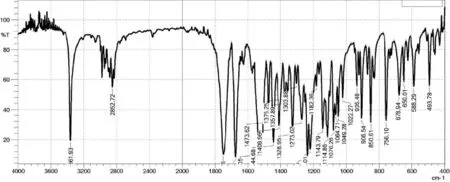
图3 利奈唑胺的红外吸收光谱Fig.3 IR spectrum of linezolid
1.4 高分辨质谱(HRMS)分析
样品的HRMS 结果显示,样品的离子峰[M+H]+的质荷比(m/z)为338.1522,分子式为C16H20FN3O4,与利奈唑胺(其[C16H20FN3O4+H]+理论值为338.1511)一致。
1.5 核磁共振分析
由图4~图8 可知,利奈唑胺供试品的1H NMR谱含有20 个氢,这与利奈唑胺供试品分子中的氢原子个数相符。13C NMR 谱显示样品有21 个碳原子,结合DEPT 135°谱,δC41.83 ppm、δC47.61 ppm、δC50.93 ppm、δC50.96 ppm、δC66.90 ppm 处的碳为仲碳,其中根据HSQC 谱δC66.90 ppm 与δH3.03~3.05 ppm 处4 个氢相关,故δC66.90 ppm为2 个仲碳;δC22.94 ppm 与单峰δH2.02 ppm 处3 个氢相关,DEPT 135°谱显示δC22.94 ppm 向上,故δC22.94 ppm 归属为甲基碳C-17,δH2.02 ppm归属为甲基氢H-17。根据HSQC 谱δC107.37 ppm 与δC107.63 ppm(d 峰,JC-F=26 Hz)、δC113.96 ppm 与δC113.99 ppm(d 峰,JC-F=3 Hz)、δC118.79 ppm 与δC118.83 ppm(d 峰,JC-F=4 Hz)分别为同一叔碳。由于苯环有氟原子,结合HMBC 谱可知:δC132.89 ppm 与δC133.00 ppm(d 峰,JC-F=11 Hz)、δC136.41 ppm 与δC136.50 ppm(d 峰,JC-F=9 Hz)、δC154.16 ppm 与δC156.61 ppm(d 峰,JC-F=202 Hz)分别为同一季碳。综合1H NMR 谱、13C NMR 谱、DEPT 135°谱、HSQC 谱,样品分子中含有16 种碳原子,其中1 个伯碳,6 个仲碳,4 个叔碳,5 个季碳,与利奈唑胺供试品分子结构的伯碳、仲碳、叔碳、季碳个数一致。

图4 利奈唑胺的1H NMR 谱Fig.4 1H NMR spectrum of linezolid

图5 利奈唑胺的D2O 交换谱Fig.5 D2O spectrum of linezolid
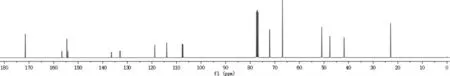
图6 利奈唑胺的13C NMR 谱Fig.6 13C NMR spectrum of linezolid
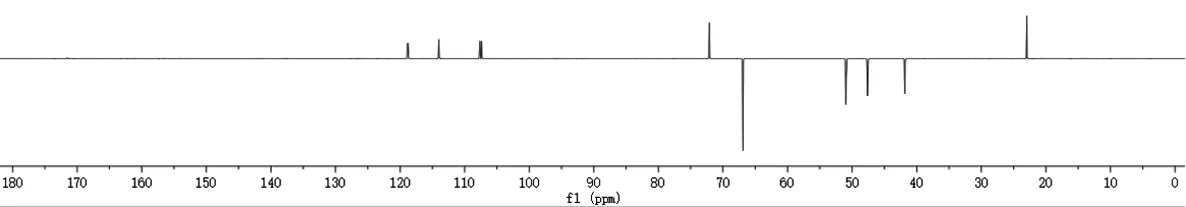
图7 利奈唑胺的DEPT 135°谱Fig.7 DEPT 135° spectrum of linezolid
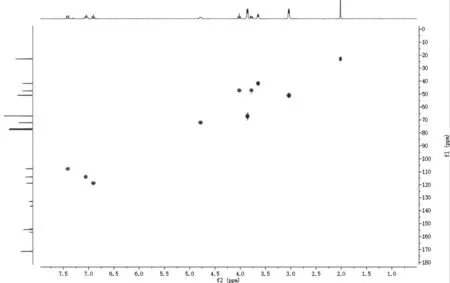
图8 利奈唑胺的HSQC 谱Fig.8 HSQC spectrum of linezolid
HSQC 谱(图8)中δC66.90 ppm 与δH3.85~3.87 ppm 处4 个氢相关,δC50.93 ppm 和δC50.96 ppm与δH3.03~3.05 ppm 处4 个氢相关,HMBC 谱δH3.03~3.05 ppm 与季碳δC136.41 ppm 和δC136.50 ppm 相关,可将δH3.03~3.05 ppm 归属为H-7 和H-8、δH3.85~3.87 ppm 归属为H-9 和H-10、δC50.93 ppm 和δC50.96 ppm 归属为C-7 和C-8、δC66.90ppm归属为C-9和C-10、季碳δC136.41ppm和δC136.50 ppm(d 峰,2JC-F=9 Hz)归属为C-4。
COSY 谱(图9)中低场δH6.88~6.93 ppm 与δH7.02~7.05 ppm 相 关,δH7.39~7.44 ppm 与δH7.02~7.05 ppm 相关(信号较弱),HMBC 谱中δH7.39~7.44 ppm、δH6.88~6.93 ppm 与季碳δC154.16 ppm 与δC156.61 ppm(d 峰,1JC-F=202 Hz)相关,δH7.02~7.05 ppm 与季碳δC154.16 ppm 与δC156.61 ppm(d 峰,1JC-F=202 Hz)相关(信号较弱),可将δH7.39~7.44 ppm、δH7.02~7.05 ppm、δH6.88~6.93 ppm 分别归属为H-2、H-6、H-5,季碳δC154.16 ppm 与δC156.61 ppm 归属为C-3,结合HSQC 谱,可将δC107.37 ppm 与δC107.63 ppm(d 峰,2JC-F=26 Hz)、δC113.96 ppm 与δC113.99 ppm(d 峰,4JC-F=3 Hz)、δC118.79 ppm 与δC118.83 ppm(d 峰,3JC-F=4 Hz)分别归属为C-2、C-6、C-5。HMBC 谱中H-2、H-6、H-5 都与δC132.89 ppm与δC133.00 ppm(d 峰,3JC-F=11 Hz)相关,可将δC133.34 ppm 与δC133.45 ppm 归属为C-1。
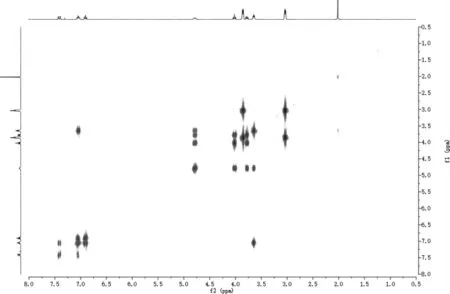
图9 利奈唑胺的1H-1H COSY 谱Fig.9 1H-1H COSY spectrum of linezolid
HMBC 谱(图10)中H-17 和δH3.63~3.66 ppm与低场δC171.49 ppm 相关,可将δC171.49 ppm归属为羰基碳C-16,δH3.63~3.66 ppm 归属为H-14,结合HSQC 谱可将δC41.83 ppm 归属为C-14。COSY 谱中δH3.76~3.80 ppm 与δH4.00~4.04 ppm相关,HSQC谱中δH3.76~3.80ppm和δH4.00~4.04 ppm与δC47.61 ppm 相关(DEPT135°谱显示其为亚甲基碳),可将δH3.76~3.80 ppm 和δH4.00~4.04 ppm 归属为H-11,δC47.61 ppm 归属为C-11。HMBC 谱中H-11 与低场季碳δC154.59 ppm 相关,可将δC154.59 ppm 归属为C-13。COSY 谱中H-11、H-14 分别于δH4.76~4.82 ppm 相关,可将δH4.76~4.82 ppm 归属为H-11,结合HSQC 谱可将δC72.11 ppm 归属为C-12。利奈唑胺的1H NMR 和13C NMR 数据归属见表1。

图10 利奈唑胺的HMBC 谱Fig.10 HMBC spectrum of linezolid
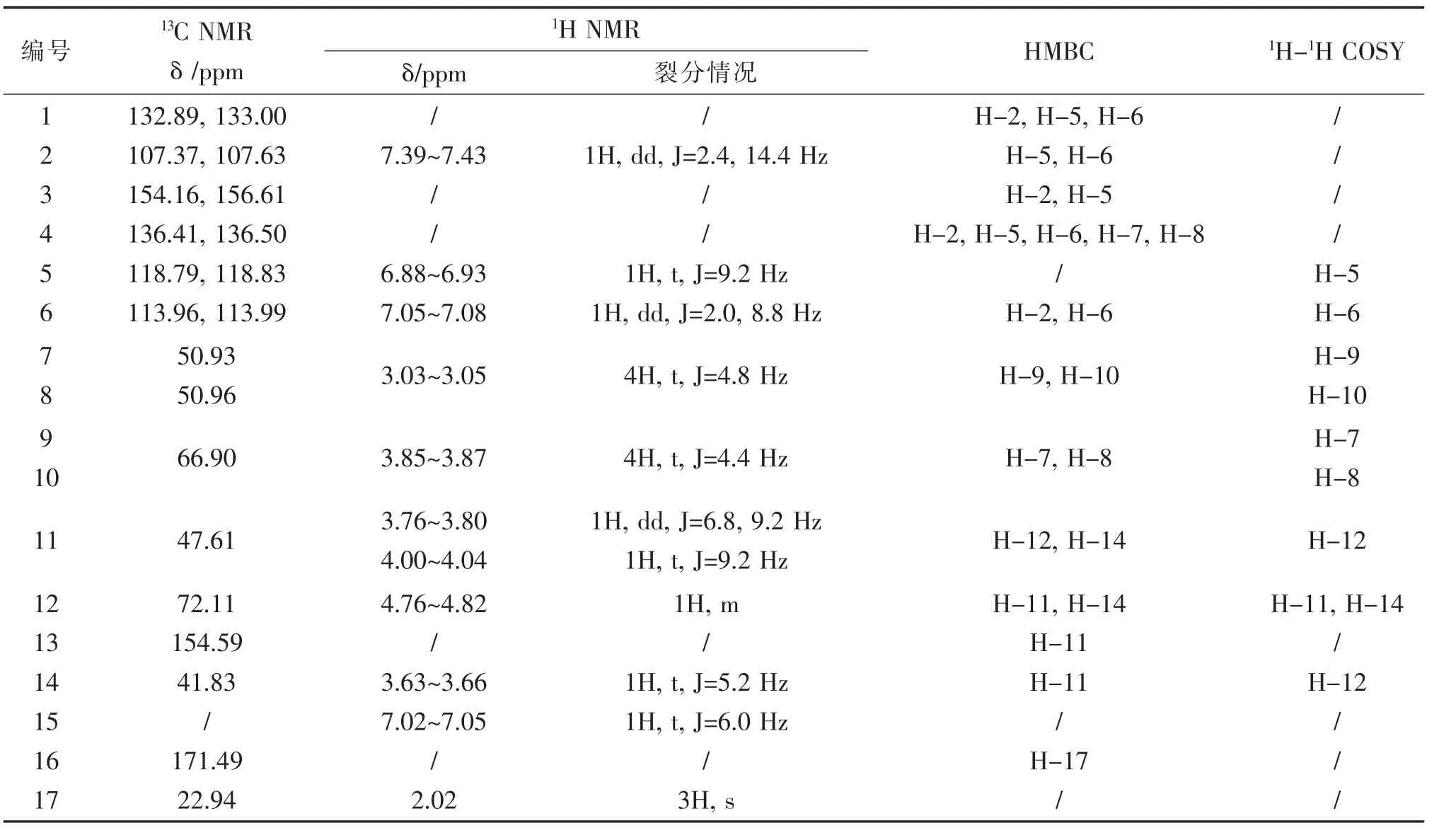
表1 利奈唑胺的1H NMR 和13C NMR 数据归属Tab.1 1H NMR and 13C NMR data assignments of linezolid
1.6 TGA/DSC 谱图分析
对样品进行TGA-DSC 热稳定分析,确定其熔融温度。TGA 用Pt 坩埚,升温范围为25 ℃~400 ℃,升温速率为10 ℃/min 结果显示,样品随温度升高失重变化经历1 个阶段,在约180 ℃以上,样品开始失重(图11)。
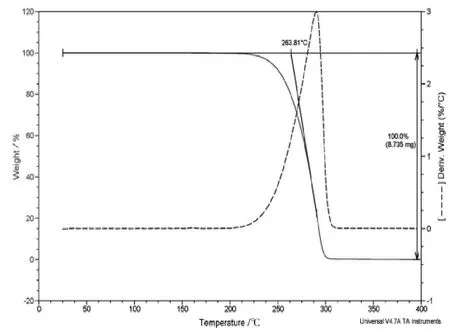
图11 利奈唑胺的TGAFig.11 TGA of linezolid
DSC 用Al 坩埚,升温范围为25 ℃~200 ℃,升温速率为10 ℃/min,结果见图12。图12 显示,样品随温度升高经历2 个吸热峰,外推起点和峰值分别为154.16 ℃、155.60 ℃,为样品的转晶(晶型Ⅱ转变为晶型Ⅳ);外推起点和峰值分别为176.81 ℃、179.44 ℃,为样品的熔融[12]。
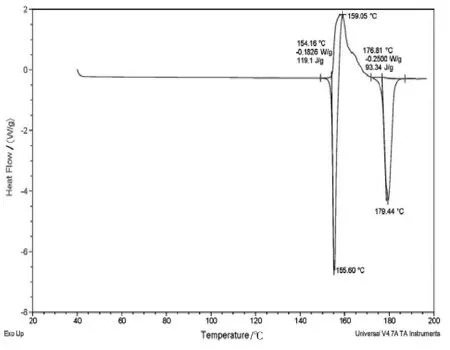
图12 利奈唑胺的DSC 图Fig.12 DSC of linezolid
1.7 粉末X-射线衍射分析
采用X 射线粉末衍射仪对样品进行分析。Cu-Kα 辐射,石墨单色器,管压:40 kV,管流:40 mA,2θ 扫描范围:4°~50°,扫描速率:6 °/min,步长:0.02°。其主要特征峰见表2,与专利[11]衍射峰对比,可确定利奈唑胺样品的晶型为晶型Ⅱ。
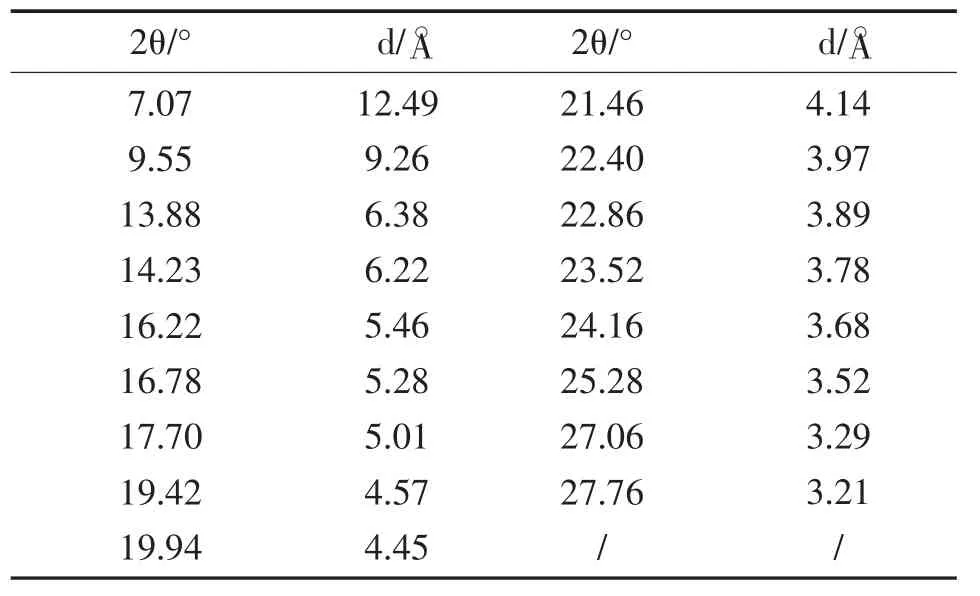
表2 利奈唑胺的X-射线粉末衍射峰Tab.2 X-ray diffraction peak of linezolid
2 结论
通过对样品进行检测分析,样品的甲醇溶液在258 nm 处有强吸收谱带、HRMS 确定样品的分子式为:C16H20FN3O4,NMR 波谱数据表明样品与利奈唑胺分子结构一致;IR、TGA/DSC 和PXRD的检测结果与文献对比,确定样品为晶型Ⅱ。综合各谱数据可确定样品与利奈唑胺分子结构一致,为利奈唑胺的合成研究、制剂开发、质量控制提供了参考依据。

