卵巢成熟型囊性畸胎瘤伴类癌3例临床病理分析
陈荏槐,郑金花,苏小洁,朱新宇,崔小光 (广东省东莞市东华医院病理科,广东东莞 523110)
卵巢成熟型囊性畸胎瘤伴类癌是一种罕见的肿瘤,一般认为卵巢的原发性类癌起源于成熟型囊性畸胎瘤中的胃肠道及呼吸道的神经内分泌细胞[1-3],组织病理学分为岛状类癌、梁状类癌、甲状腺肿类癌及黏液类癌4 种类型,多伴发同侧成熟型囊性畸胎瘤[4-5],临床多无明显症状,多以体检超声发现而就诊。我们收集3 例病例结合文献对其临床病理特征、诊断及鉴别诊断进行分析。
1 一般资料
例1,女性,28岁,因检查彩超发现左侧附件包块1 年余入院,包块大小52 mm×42 mm,考虑卵巢畸胎瘤;子宫及右侧附件区未见异常。妇检:外阴发育正常,阴道通畅,阴道少量黄白色分泌物,无异味;宫颈光滑,无接触性出血,无抬举痛;子宫正常大小,后位,活动好,无压痛;左侧附件区可触及囊实性包块,5 cm×4 cm,光滑,活动可,无明显压痛,右侧附件区未及包块,无压痛。
例2,女性,39岁,因彩超发现左侧附件液实混合性包块9 a 入院,包块大小39 mm×32 mm,回声不均匀,内可见团状强回声,边界欠清,考虑畸胎瘤。妇检:外阴发育正常,阴道通畅,可见少许白色分泌物;宫颈轻度糜烂,无接触性出血,抬举痛;子宫正常大小,质中,无压痛,中位,活动好;阴道左前穹窿触及一直径5 cm 左右包块,活动度欠佳,质中,有压痛,边界清。左侧附件区稍增粗,无压痛,右侧附件区未及异常,无压痛。
例3,女,42 岁,入院前1 年余在当地卫生院体检时行B 超发现盆腔包块,现来我院住院,我院复查B超提示盆腔多发混合性包块,考虑双侧卵巢畸胎瘤。患者平素月经周期规律,经期3~4 d,周期28 d,量中,无痛经,平素患者偶有腰酸不适,平躺时下腹有压迫不适感,妇检:外阴发育正常,阴道通畅;阴道前后穹窿均变浅,宫颈光滑,无接触性出血,无抬举痛;子宫大小正常,无压痛,子宫前位,活动好,子宫偏后方、双侧附件区可触及多个包块,范围约17 cm×11 cm,质软,活动度好,无压痛。
2 病理结果
3 例标本均以10%中性福尔马林固定,常规包埋、石蜡切片、HE染色及光镜观察。免疫组化采用自动免疫组化机检测,一抗所有抗体均购自基因公司。
2.1 大体所见
例1,囊性肿物1个,体积4.5 cm×4.0 cm×1.0 cm,囊内含毛发及皮脂样物,并见头节1 枚,体积2.0 cm×1.5 cm×0.8 cm,囊壁厚0.1 cm,质软,头节旁见一灰白结节,最大径约0.7 cm,边界清。例2,左侧附件(图a):灰白灰红色碎组织多块,体积共计8.4 cm×6.0 cm×2.5 cm,切面灰白灰黄,呈囊实性,实性部分略呈胶冻样,其中可见输卵管样组织1 条,长4.2 cm,直径1.1~1.6 cm,质软。例3,标本1 左侧附件:囊壁样组织4 块,大小8.0 cm×7.5 cm×2.5 cm,内见少量毛发,局部见一头节,大小2.5 cm×2.0 cm×0.6 cm,部分囊内壁附咖啡样物,囊壁厚0.1~0.2 cm。另见输卵管1 条,长7 cm,直径0.5~0.7 cm,伞端不开放。标本2 右侧卵巢肿物:囊壁肿物2 枚,大小分别为3.0 cm×2.8 cm×2.0 cm及5.0 cm×3.0 cm×1.5 cm,囊内均可见头节及皮脂样物,囊壁厚0.1 cm。标本3 全子宫+右侧附件:全子宫1个,体积8.5 cm×5.5 cm×3.5 cm,已被临床从前壁剖开,宫腔深6.5 cm,肌壁厚2.0~2.5 cm,内膜菲薄,宫颈管长3.5 cm,宫颈外口光滑,右侧输卵管长5 cm,最大径0.5~1.0 cm,伞端区域与卵巢粘连,粘连处浆膜呈暗红色,切面灰黄灰红,质软,右侧卵巢体积3.5 cm×3.0 cm×1.5 cm,切面灰黄灰红,质中。
2.2 镜下HE形态
例1 可见鳞状上皮、皮脂腺、汗腺、软骨、神经胶质(图b)等成熟型囊性畸胎瘤的成分,另见甲状腺滤泡与类癌混合增生的区域,类癌细胞呈实性片状、巢团状、梁索状、小管状、假菊形团或缎带样生长,细胞柱状或卵圆形,体积中等或偏大,胞质红染、丰富,胞界不清,核圆形、卵圆形或雪茄形,栅栏状排列,染色质粗,呈胡椒粉样或撒椒盐样,核仁不明显,核分裂不易见。例2主要是肠型腺体与甲状腺肿类癌混合生长的形态,肠型腺体富含杯状细胞,腔内及间质可见多量分泌的黏液,部分类癌形成小梁状结构(图c),部分区域形成黏液湖,湖中可见漂浮的类癌细胞(图e),甲状腺滤泡大小、形状不一,滤泡上皮主要为扁平上皮,部位为柱状细胞,滤泡腔内含多量嗜伊红的胶冻样物。其中输卵管未见明显病变。例3 可见呼吸道纤毛柱状上皮、胃小凹上皮、平滑肌、神经节细胞、脂肪及黏液腺泡等成熟型囊性畸胎瘤的成分,另见岛状或小梁状分布的类癌区域,类癌细胞与例1 描述形态基本一致,未见甲状腺肿成分。
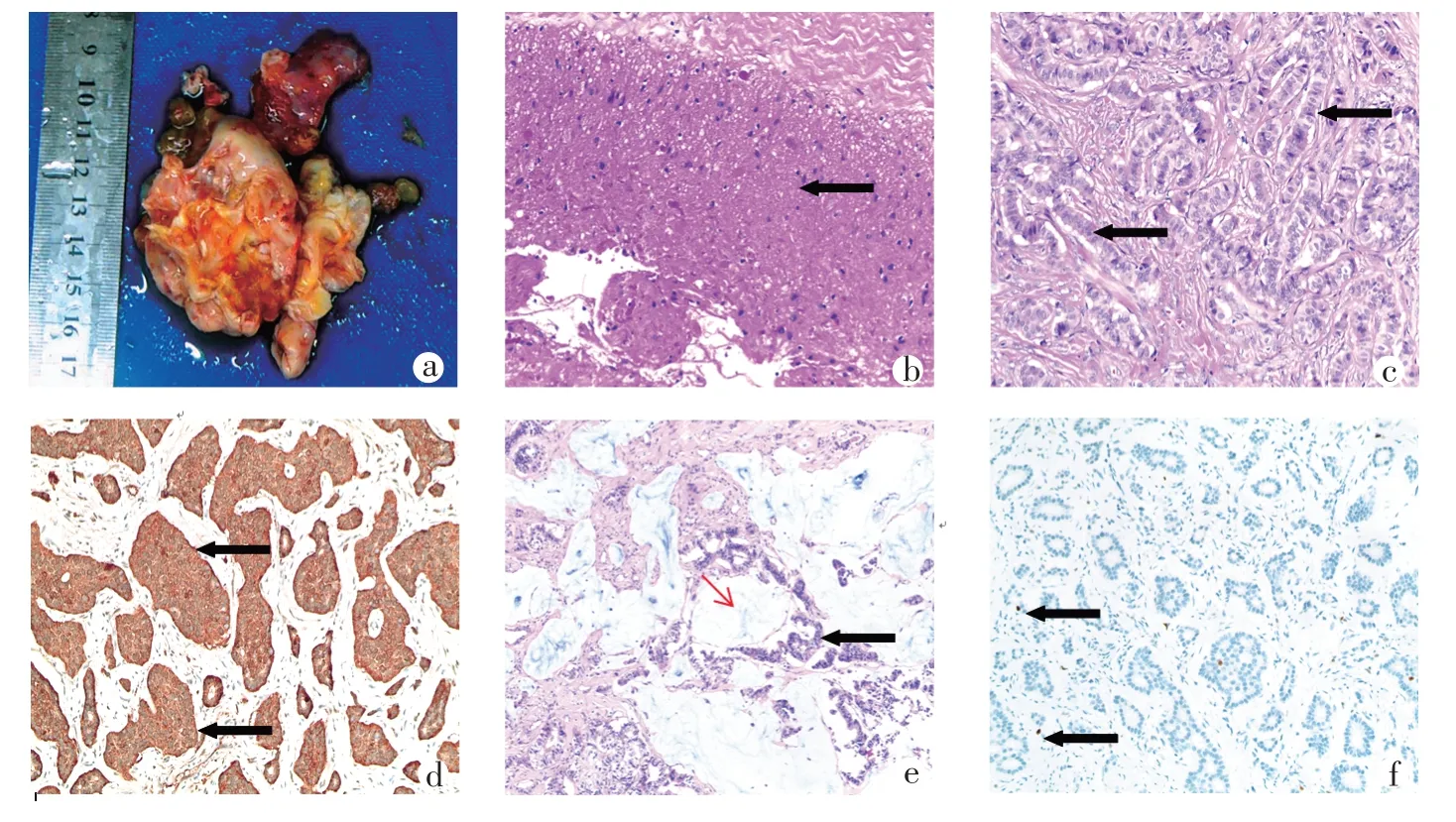
a.例2左附件大体;b.例1成熟型囊性畸胎瘤的神经胶质(200倍);c.例2小梁状生长的类癌区域(200倍);d.例3类癌CgA阳性(200倍);e.例2伴有黏液产生的类癌区域(100倍),红色箭头指黏液,黑色箭头指类癌;f.例3增殖指数(Ki67)约1%~2%(200倍)
2.3 免疫组化结果
3 例类癌区域均Syn(+),CgA(图D)(+),CD56(+),Ki67(图F)(约1%~2%+),CK(+),CDX2(+),Inhibin-α(-),其中2 例甲状腺肿区域均TTF-1(+),CD56(+),CK(+),而Syn(-),CgA(-),CDX-2(-)。
2.4 病理诊断
例1(左侧卵巢)成熟型囊性畸胎瘤伴甲状腺肿类癌(最大径约0.7 cm)。例2(左侧附件)卵巢成熟型囊性畸胎瘤伴甲状腺肿类癌(最大径约1.4 cm),输卵管未见异常。例3(左侧卵巢)成熟型囊性畸胎瘤伴岛状类癌(最大径约0.8 cm),输卵管未见明显病变。(右侧卵巢)成熟型囊性畸胎瘤。(全子宫+右侧附件)慢性宫颈炎;增生期子宫内膜;(右侧)输卵管伴出血坏死,卵巢伴肉芽肿性炎及出血坏死。
3 治疗及预后
例1 行左侧卵巢切除,随访13 个月未见肿瘤复发;例2行左侧附件切除,随访21个月未见肿瘤复发;例3 行全子宫及双侧附件切除及术后化疗,随访9 个月未见肿瘤复发。
4 讨论
卵巢成熟型囊性畸胎瘤伴类癌是非常少见的卵巢肿瘤,由畸胎瘤和类癌两种成分构成,其中畸胎瘤可以分为成熟型和未成熟型两大类,成熟型的相对多见,占卵巢所有肿瘤20%,ICD 编码为0,为良性病变,好发于女性的生育年龄,临床可表现为腹痛、腹部包块或因超声检查而偶然发现。本文3 例均因超声检查偶然发现,极少数年轻女性病例与抗NMDAR脑炎相关[6-8],约10%的病例双侧发生。本文1 例也是双侧卵巢同时并发成熟型囊性畸胎瘤。其发病机制尚未完全明确,被广泛接受的是起源于原始的生殖细胞[9]。肉眼观大部分为囊性,镜下可以看到2 个或3 个不同胚层来源的成熟组织。本文3 例为囊性或囊实性,可见鳞状上皮、神经胶质、软骨、甲状腺、呼吸道上皮等不同胚层的成分,非常罕见的情况下也可以看见前列腺组织[10],但本文3例均未见前列腺组织。
卵巢成熟型囊性畸胎瘤可以发生恶性转化,其中最常见的是鳞状细胞癌,甲状腺乳头状癌、恶性黑色素瘤[11]、类癌及未分化癌[12]也有被报道,本文3例就是成熟型囊性畸胎瘤恶性转化为类癌。有时候恶性转化的成分很少,需要充分取材及全面细致地镜下观察才能发现,必要时须加做免疫组化进一步诊断,因为两者的治疗及预后截然不同。本文例1和例3类癌的成分比较少,若取材不充分或阅片过快则容易漏诊。
卵巢类癌指的是原发性类癌,也就是卵巢本身发生的,不是其他器官类癌的转移,新版WHO 卵巢类癌的定义是与胃肠道类似的分化好的神经内分泌肿瘤[1],归类与2014版的WHO一样,归在单胚层畸胎瘤与体细胞肿瘤中,没有跟随胃肠道及胰腺神经内分泌肿瘤的命名,但级别相当于胃肠道神经内分泌肿瘤的1级。
卵巢类癌的发病率非常低,约占卵巢所有肿瘤的1%[13],发病年龄不定,大部分患者发生在绝经后,平均年龄53 岁,但本文3 例年龄分别为28、39 及42 岁,均为绝经前。约30%的患者具有类癌综合征,不同的激素升高会引起不同的临床表现,如多肽YY 升高会引起慢性便秘[14-15],类固醇激素升高会引起多毛、不规则阴道流血、男性化,甲状腺素升高会引起甲亢等,肿物切除后相应症状会消失。本文3 例均无激素升高引起相应的症状。
卵巢类癌通常在畸胎瘤的取材及镜检中无意发现,体积一般很小,通常为实性,偶然也可为囊性,切面均匀一致黄色或者褐色,如有黏液还会发光[16],本文3 例大小分别为0.7、1.4 及0.8 cm。组织病理学根据其生长方式分4 种类型,即岛状类癌、甲状腺肿类癌、小梁状类癌及黏液类癌,其中最常见的是岛状类癌,其次是甲状腺肿类癌,4 种类型可以单独或混合存在。本文2 例为甲状腺肿类癌,1 例为岛状类癌与小梁状类癌混合,岛状类癌成分占绝大部分(约90%)。其中例2 还可见到甲状腺肿类癌与肠型腺体移行的区域,这提示了类癌可能原发于畸胎瘤肠道腺体的神经内分泌细胞。免疫组化方面,类癌主要表达上皮及神经内分泌的标志,如广谱角蛋白(Pan-CK),CD56、突触素(Syn)、嗜铬素A(CgA)等;另外还有报道其会表达CDX2,但表达程度不一,不表达甲状腺转录因子-1(TTF-1)、抑制素α(Inhibin-α)等。本文3 例均表达CDX2、Pan-CK、CD56、Syn及CgA,不表达TTF-1、Inhibin-α,增殖指数一般很低,1%~2%。
卵巢类癌需与以下肿瘤进行鉴别诊断。⑴转移性类癌:一般双侧卵巢均有病变,位于卵巢表面,呈多结节状,无伴卵巢畸胎瘤,胃肠镜及影像学检查可以发现相应病灶。卵巢外的类癌多位于胃肠道或肺,直肠比较常见,一般体积小且位于肠腔内,极少发生转移,若卵巢与卵巢外同时发现类癌,病变的位置相当重要,因为镜下形态及免疫均无法区分。如直肠、双侧卵巢均有病变且卵巢的病变位于表面时则支持卵巢非原发;如卵巢只有一侧有类癌或类癌伴发畸胎瘤,直肠病灶位于浆膜面则支持卵巢原发;如卵巢一侧或双侧有病变,直肠病变位于肠腔内时则支持卵巢与直肠均为原发,因为类癌几乎不发生转移。尽管没有绝对的指标能解决原发性与转移性类癌这个棘手的问题,但妥善及正确治疗似乎显得更为重要。⑵卵巢甲状腺肿:仅有大小不一的甲状腺滤泡而无类癌成分。⑶卵巢甲状腺肿发生的乳头状癌:组织病理学会出现很多大小不一的乳头结构,癌细胞的核具有典型乳头状癌核的特征,如卵圆形核、核沟、核内假包涵体等,免疫组化弥漫强表达CK19,失表达CD56,不表达Syn、CgA 等神经内分泌标记。⑷Sertoli-Leydig细胞瘤:当类癌主要以小梁状或腺管状生长方式为主时需要加做免疫组化鉴别诊断,Sertoli-Leydig细胞瘤表达Inhibin-α,不表达神经内分泌标记,而类癌则相反。⑸血管周上皮样细胞肿瘤(PEComa):该肿瘤表达HMB45 及Melan-A 等色素细胞标记,不表达神经内分泌细胞标记。⑹转移性黏液腺癌:当类癌为黏液类癌亚型时需排除胃肠道来源的黏液腺癌,转移性腺癌一般累及双侧卵巢而无伴畸胎瘤,表达上皮性标记,一般不表达神经内分泌标记。
由于卵巢成熟型囊性畸胎瘤伴类癌发病率低,目前尚无统一的治疗方案,当患者很年轻、病变为单侧、肿瘤包膜完整、类癌体积很小且局限于畸胎瘤的实性结节时,行单侧卵巢或单侧附件切除即可,术后一般不复发,预后佳。当患者无生育要求或病变为双侧时,最好行全子宫、双侧附件切除及化疗,本文例1 行单侧卵巢切除,例2行单侧附件切除,例3行全子宫及双侧附件切除再加化疗,随访至今均未见复发或转移。

