TiO2负载硅铝陶瓷介孔球对甲基橙吸附和光催化降解的研究
徐 琦 胡伟达, 蔡 舟 陈 磊田 柳 彭承鑫
1.湖南工业大学材料与先进制造学院湖南 株洲 412007
2.湖南工业大学醴陵陶瓷学院湖南 株洲 412007
3.金田铜业(集团)股份有限公司浙江 宁波 315034
1 研究背景
近年来,自然环境中有机污染物所造成的水污染问题引起了人们的高度重视。半导体光催化材料在光能激发条件下具有较强的氧化性能,可对自然环境中大部分有机污染物产生催化降解作用,因而有关半导体光催化材料的水污染治理研究受到广泛关注。在常见半导体光催化材料中,自S.N.Frank首次发现TiO2可以光催化降解水溶液中的有机物以来,研究人员对TiO2在污水治理方面开展了大量的研究工作。TiO2材料因制备工艺简单、成本较低、催化性能较高、重复利用率较好及对环境无二次污染等特点,在商业应用中TiO2成为市场首选的光催化材料[1-2]。
与传统外加氧化剂(如漂白粉、紫外/臭氧/双氧水等)污水治理方法相比,TiO2在吸收特定光波能量后可对H2O进行催化,从而产生具有强氧化能力的羟基自由基,此类羟基自由基可使水中溶解的有机污染物氧化分解,生成CO2、H2O或其它离子类物质。反应过程中TiO2仅起到催化作用,可重复使用,可见TiO2材料催化降解有机污染物的效果较传统工艺更好[3-6]。研究发现,TiO2具有优异的光催化性能需要满足两个条件:一方面其晶体结构为锐钛矿型;另一方面要形成纳米级TiO2颗粒。然而在实际使用过程中,纳米级TiO2在光催化降解有机污染物时极易团聚,从而导致催化性能降低及不易回收的问题。目前,为解决TiO2不易分散的问题,常将TiO2负载于载体表面,如分子筛、多孔陶瓷等,也有直接将TiO2通过掺杂其他物质制备成介孔球状用于水污染治理[7-9]。
基于上述研究内容,本研究拟采用溶胶凝胶法制备TiO2溶胶,再将其与硅铝陶瓷介孔球液相混合,经热处理工艺制备TiO2负载硅铝陶瓷介孔球光催化材料,并研究其对甲基橙溶液的吸附和光催化降解效应,以期将TiO2负载硅铝陶瓷介孔球应用于工业生产体系染料废水的光催化净化治理。
2 实验部分
2.1 实验原料、设备及仪器
1)实验原料
硅铝陶瓷介孔球(以下简称为介孔球),喷雾干燥法自制,平均粒径为120 μm,比表面积为438.2 m2/g,平均孔径为3.752 nm;钛酸丁酯,分析纯,福晨(天津)化学试剂有限公司;三乙醇胺,分析纯,中国医药(集团)上海化学试剂公司;无水乙醇,分析纯,长沙安泰精细化工实业有限公司;甲基橙,分析纯,福晨(天津)化学试剂有限公司。
2)实验设备与仪器
扫描电子显微镜(scanning electron microscope,SEM),JSM-6510型,日本电子株式会社;X射线 衍 射 仪(X-ray diffractometer,XRD),UItima-IV型,日本理学株式会社;傅里叶变换红外光谱仪(Fourier transform infrared spectrometer,FTIR spectrometer),Nicolet is10型, 美国赛默飞世尔科技公司;可见分光光度计,722S型,上海菁华科技仪器有限公司;高速搅拌器,LC-MSH-2L型,上海力辰仪器科技有限公司;超声波清洗仪,KQ-100E型,昆山市超声仪器有限公司;鼓风干燥箱,DHG-9030A型,上海精宏实验设备有限公司;箱式炉,KSL-1400X-A3型,合肥科晶材料技术有限公司。
2.2 TiO2负载介孔球制备
将钛酸丁酯、三乙醇胺和乙醇按体积比为34:10:140混合并搅拌均匀,再逐滴加入10 mL乙醇和去离子水的混合溶液(两者体积比为9:1),高速搅拌2 h后静置48 h,制得TiO2溶胶。将所制TiO2溶胶与介孔球按质量比为1:10混合,静置24 h后超声分散30 min,形成一定黏度的浆料,将其放入120℃烘箱干燥12 h,再经箱式炉450℃热处理,随炉冷却后,即制得所需样品[10]。
2.3 吸附和光催化降解甲基橙实验
室温条件下,在自制的反应装置(见图1)中研究不同条件的介孔球对甲基橙的吸附及光催化性能,并测量反应后甲基橙的吸光度值。具体操作步骤如下:称量5 g介孔球样品加入自制光催化装置中(20 W紫外灯),单次量取5 mL一定浓度的甲基橙溶液加入反应装置中,收集反应后的溶液进行吸光度检测。
2.4 测定与表征
采用扫描电子显微镜分析试样表观形貌,测试前样品需喷金处理。采用X射线衍射仪分析样品晶体结构,测试条件为:CuKα射线,λ=0.154 18 nm,扫描速度10 (°)/min,测量范围20°~90°。采用傅里叶变换红外光谱仪分析样品化学键的变化,检测范围450~4000 cm-1。采用可见分光光度计检测甲基橙的吸光度值,其中分光光度计测定值固定为463 nm,分析甲基橙浓度的变化。
3 结果与讨论
3.1 SEM形貌
图2为介孔球及TiO2负载介孔球的扫描电镜图。图2a为介孔球外部形貌图,介孔球球径为120 μm左右,球表面有较多凹坑及微小气孔;图2b为介孔球截面图,可以清楚发现球内部为微小孔隙结构,经实验前期比表面测试其平均孔径约为3.752 nm;图2c~d为实验所制TiO2负载介孔球及其局部放大形貌图,可见负载于介孔球表面的TiO2物质具有一定孔隙的膜层结构,且TiO2膜断裂层较多,层阶较明显,但整体上对介孔球包覆较完整。

图2 样品SEM形貌分析Fig.2 SEM morphology analysis of samples
3.2 XRD晶体结构分析
图3为介孔球及TiO2负载介孔球的X射线衍射谱图,其中曲线a为原始介孔球的X射线衍射谱图,曲线b为TiO2负载介孔球的X射线衍射谱图。

图3 样品 XRD晶体结构分析Fig.3 XRD crystal structure analysis of samples
图中曲线a在26.18°, 35.44°, 41.10°等处出现较明显晶体结构峰,查阅相关文献此类峰归属于SiO2六方晶系衍射峰(PDF-12-0708)[11];同时在45.69°,60.51°, 67.21°, 75.10°等处出现 Al2O3特征衍射峰(PDF-04-0877)[12]。曲线 b中除有 SiO2、Al2O3晶型衍射峰型出现外,还在25.27°, 37.87°, 48.04°,55.06°, 62.44°等处出现TiO2锐钛矿峰型(PDF-21-1272)[13]。从上述样品XRD晶体结构分析可知,在本实验条件下制备的负载于介孔球表面的TiO2为锐钛矿晶型。
3.3 吸附和光催化性能
3.3.1 甲基橙吸附和光催化降解
为了较好地分析甲基橙的吸附和光催化降解过程,本研究首先测定不同浓度甲基橙标准溶液的吸光度值,检测数据如表1所示。
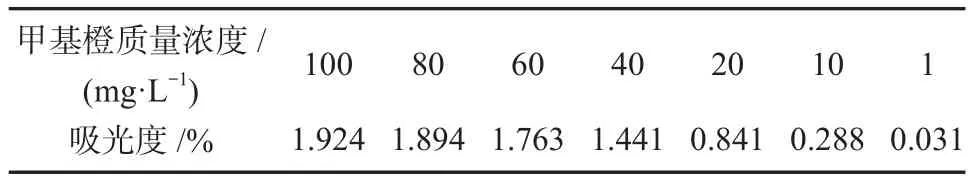
表1 甲基橙标准溶液吸光度Table 1 Absorbance of methyl orange standard solution
再采用对比法分别选用黑暗环境下介孔球、黑暗环境下TiO2负载介孔球以及紫外灯光照条件下TiO2负载介孔球3种实验条件,在反应装置中(图1)对甲基橙吸附和光催化降解效应进行研究。实验中单次量取5 mL甲基橙溶液(质量浓度为100 mg/L)加入反应装置(图1),共收集10批次反应的溶液进行吸光度检测,检测结果如图4~5所示,其中图4为不同实验条件下所收集反应溶液的吸光度值变化图,图5为对应实验条件所收集溶液的颜色变化图。

图4 甲基橙吸光度图Fig.4 Absorbance value of methyl orange

图5 甲基橙颜色变化图Fig.5 Color change diagram of methyl orange

彩图
由图4~5可知,3种实验条件下甲基橙溶液经反应装置所收集的第1, 2批次溶液的吸光度值接近于0,说明此时介孔球对甲基橙吸附或催化作用较强;但从第3批次开始,随着实验次数的增多,所收集溶液的吸光度逐渐增大,黑暗条件下所得溶液的吸光度较紫外光照条件下的大,且介孔球所得溶液的吸光度比TiO2负载介孔球的大。分析其原因:当甲基橙溶液在第1, 2批次经介孔球过滤后,由于介孔球中孔隙率较大,甲基橙在介孔球中吸附量也相对较多,与水溶液分离较彻底;但随着甲基橙加入实验装置批次的增多,介孔球孔隙吸附甲基橙逐渐达到饱和,在浓度和压力的作用下,水溶液经介孔球流出时会溶解部分甲基橙,因此,后续随着甲基橙批次的增多,所得溶液的吸光度值逐渐增大。
进一步对比图4中曲线b与c可知,黑暗条件下TiO2负载介孔球所得溶液的吸光度较未负载介孔球的小,这是因为本实验制备的TiO2成一定粗糙的膜层包覆介孔球,形成的TiO2负载介孔球表面粗糙度较大,增大了其对甲基橙的吸附面积,在黑暗条件下TiO2负载介孔球吸附能力有一定增强。曲线b中,TiO2负载介孔球经10批次实验后,甲基橙的吸光度值为1.688,对应甲基橙质量浓度约为50 mg/L;曲线c中,介孔球经10批次实验后,所得溶液的吸光度值为1.824,对应甲基橙质量浓度约为80 mg/L。曲线a为在紫外灯光照条件下TiO2负载介孔球所得溶液吸光度,经10批次实验后溶液的吸光度值为0.956,对应甲基橙浓度约为30 mg/L左右。与曲线b、c相比,相同条件下曲线a的吸光度大幅降低,分析其原因:本试验制备的TiO2负载介孔球除具有上述相同的吸附作用外,负载于介孔球表面的TiO2经XRD检测为锐钛矿晶型,锐钛矿TiO2在紫外光照射下能表现出良好的光催化性能,可使吸附于其表面的甲基橙进一步发生光催化降解,从而降低整个反应体系中甲基橙的浓度。
3.3.2 红外光谱分析
为了进一步检验TiO2对甲基橙的光催化降解作用,选取上述实验中经10批次反应后,在黑暗环境下TiO2负载介孔球、紫外光照条件下TiO2负载介孔球经室温干燥后进行红外光谱分析,结果如图6所示,其中曲线a为甲基橙红外光谱,曲线b为黑暗环境下TiO2负载介孔球吸附甲基橙后的红外光谱,曲线c为经紫外光照射后TiO2负载介孔球的红外光谱。

图6 不同样品红外光谱图Fig.6 IR spectra of different samples
曲线a甲基橙红外光谱中,1373 cm-1处对应为甲基橙分子结构中苯环上C—N键的伸缩振动峰,817, 745 cm-1处对应为甲基橙分子结构中苯环上C—H键的伸缩振动峰[14]。曲线b黑暗环境下TiO2负载介孔球吸附甲基橙后的红外光谱中,1373 cm-1处同样对应为甲基橙分子结构中苯环上C—N键的伸缩振动峰,1076 cm-1处则为Si—O—Al键的伸缩振动峰,817, 745 cm-1对应为甲基橙分子结构中苯环上两处不同的C—H键的伸缩振动峰,629 cm-1处为Al—O 键伸缩振动,450~490 cm-1为 Si—O、Ti—O键的伸缩振动。对比曲线a与b可知,黑暗环境下TiO2负载介孔球除有Si(Al,Ti)—O等硅铝化学键的基本结构外,还出现了与甲基橙分子结构相似的红外峰。曲线c紫外光照射后TiO2负载介孔球的红外光谱中,1076 cm-1处对应为Si—O—Al键的伸缩振动峰,817 cm-1处为甲基橙分子结构中苯环上C—H键的伸缩振动峰,461 cm-1处为Ti—O键的伸缩振动峰[15-16]。与曲线a对比可知,曲线c在1373 cm-1处甲基橙分子结构中苯环上C—N键的伸缩振动峰没有出现,同时817, 745 cm-1处甲基橙分子苯环上两种C—H键伸缩振动峰仅有817 cm-1处峰存在,这可能是由于在紫外光照实验条件下TiO2对甲基橙起到光催化作用,促使甲基橙苯环上C—N键的断裂,引起苯环上C—H键的改变。从上述红外分析可知,在紫外光照射条件下TiO2对甲基橙分子结构的改变有一定作用,促使甲基橙发生光催化降解。
4 结论
以实验室自制硅铝陶瓷介孔球为基体,以钛酸丁酯为前驱体,采用溶胶凝胶法制备TiO2溶胶并将其负载于介孔球表面,用于甲基橙溶液吸附和光催化降解的应用,得到以下结论。
1)经SEM和XRD等表征分析,TiO2是以多层粗糙度较高的膜层包覆于介孔球表面,且TiO2晶体结构为锐钛矿晶型。
2)在自制反应装置中,采用对比法考察不同介孔球样品对甲基橙的吸附和光催化降解作用。结果表明,黑暗条件下介孔球、TiO2负载介孔球经10批次实验后甲基橙质量浓度分别从原来的100 mg/L降低到80 mg/L、50 mg/L,两者对甲基橙吸附作用较明显;在紫外灯光照射条件下,TiO2负载介孔球经10批次实验后甲基橙质量浓度从100 mg/L降低到30 mg/L,表现出更优异的吸附作用。
3)红外光谱分析表明,在紫外光照射条件下TiO2对甲基橙有一定的光催化降解作用。
4)实验制备的TiO2负载介孔球对甲基橙吸附和光催化降解性能良好,吸附饱和后的介孔球有望通过烧结工艺重复利用,在染料废水治理中具有良好的应用前景。

