五味子属植物木脂素类化学成分及其药理作用研究进展
刘媛媛,黄仕其,李玉泽,樊 浩,张化为,邓 翀,宋小妹,张东东,王 薇
五味子属植物木脂素类化学成分及其药理作用研究进展
刘媛媛,黄仕其,李玉泽,樊 浩,张化为,邓 翀,宋小妹,张东东*,王 薇*
陕西中医药大学药学院,陕西 咸阳 712046
五味子属隶属于五味子科,主要含有木脂素类、三萜类、多糖类以及挥发油等化学成分,临床上常用于治疗肝炎、肝肾移植、阿尔茨海默症和失眠等疾病。现代研究表明五味子属中木脂素类成分为该属植物的主要活性成分,具有保肝、抗肿瘤、抗病毒、抗氧化和神经保护等药理作用。对五味子属植物中木脂素类化学成分及其药理作用的研究进展进行综述,为后续该属植物的相关研究开发和综合应用提供参考。
五味子属;木脂素类;联苯环辛烯型木脂素;保肝;抗肿瘤;抗氧化
五味子科(Schisandracea)包含五味子属Michx和南五味子属Kaemp f. ex Juss,分布于亚洲东南部和北美东南部[1],我国是五味子科植物资源最为丰富的国家,其中五味子属植物约有30种,我国有19种(表1),集中分布于西南部和东南部地区[2]。目前对于五味子属的研究主要集中在五味子、华中五味子、阿里山五味子、二色五味子、金山五味子、翼梗五味子、兴山五味子、滇藏五味子、合蕊五味子、毛叶五味子、红花五味子、绿叶五味子和鹤庆五味子等。五味子属植物具有收敛固涩、益气生津、补肾宁心等功效,《神龙本草经》《本草纲目》《中药大辞典》等医药著作对该属植物均有收录,《中国药典》2020年版对五味子(北五味子)和华中五味子(南五味子)的质量标准有详细记载[3]。该属植物化学成分丰富,其中木脂素是最主要的一类化学成分,联苯环辛烯类是五味子属特有的化合物类型,是五味子属中最有潜力的一类化合物,在开发免疫调节和抗癌药物方面具有十分广阔的前景,以华中五味子酮为例的环木脂素具有很好的神经保护作用,单环氧木脂素在抗肿瘤和抗炎作用方面表现最为突出,双环氧类木脂素药理活性广泛,尤其是抗炎和抗菌作用显著,并且还具有一氧化氮抑制作用。
近年来,对于五味子属植物的开发应用,重点体现在保健品、食品饮料、红酒和日用化妆品等方面。五味子乙醇提取物在免疫抑制方面的临床研究已成为研究热点,对于单体化合物的研究,在五味子丙素的化学结构基础上合成了治疗肝炎的新药联苯双酯,不仅如此,华中五味子中分离得到的华中五味子酮具有显著的抗氧化活性,尤其针对于阿尔茨海默症的研究进行了大量的药理实验。五味子属植物化学成分丰富,药理活性多样,五味子作为我国著名中药,临床应用广泛。目前对于五味子属植物化学成分及药理活性的研究依然是国内外植物化学领域关注的热点。木脂素作为五味子属植物最为重要的一类化学成分,也是其主要的药理活性成分,近些年来,因其免疫抑制作用突出在临床上用于治疗器官移植而被频繁报道,同时研究还发现五味子众多药理活性的基础物质皆是木脂素类成分。然而对于五味子属中木脂素类成分却少有系统的梳理和总结。因此本文围绕五味子属中木脂素类成分及其药理作用展开综述,对该属19种植物中木脂素类化学成分及其碳骨架类型进行详细的分类总结,对该属木脂素的药理活性进行全面的整理,旨在为该属植物的进一步研究和开发利用提供科学依据。
表1 五味子属植物的名称
Table1 NamesofSchisandraplants
编号植物名称 a阿里山五味子S. arisanensis Hayata b二色五味子S. bicolor Cheng c五味子S. chinensis (Turcz.) Baill d金山五味子S. glaucescens Diels e大花五味子S. grandiflora (Wall.) Hook. f. et Thoms f翼梗五味子S. henryi Clarke g兴山五味子S. incarnata Stapf h狭叶五味子S. lancifolia (Rehd. et Wils.) A. C. Smith i小花五味子S. micrantha A. C. Smith j滇藏五味子S. neglecta A. C. Smith k重瓣五味子S. plena A. C. Smith l合蕊五味子S. propinqua (Wall.) Baill m毛叶五味子S. pubescens Hemsl. et Wils n红花五味子S. rubriflora (Franch). Rehd. et Wils o球蕊五味子S. sphaerandra Stapf p柔毛五味子S. tomentella A. C. Smith q绿叶五味子S. viridis A. C. Smith r鹤庆五味子S. wilsoniana A. C. Smith s华中五味子S. sphenanthera Rehd. et Wils
1 化学成分
近年来,国内外学者从五味子属植物中分离出多种有效成分,发现五味子属果实、茎、叶和根中主要含有木脂素类、三萜类、挥发油、有机酸及多糖类等成分。其中木脂素类为主要化学成分,目前从五味子属植物中分离得到的木脂素类成分有239种,从结构上可分为联苯环辛烯木脂素、环木脂素、单环氧木脂素、简单木脂素、7,8-开环木脂素、双环氧木脂素和新木脂素。早在1978年,Liu等[4]从华中五味子中分离出5种木脂素schisantherins A~E,张孟亭[5]从台湾阿里山五味子中提取分离得到4个新木脂素arisantetralones A~D和7个新的联苯环辛烯型木脂素arisanschinins F~L,Liu等[6]从二色五味子中分离出9个新的木脂素schibitubins A~I,除此之外,Gao等[7]从滇藏五味子中发现新木脂素neglignans A~G,马文辉[8]从鹤庆五味子中分离得到10个木脂素schisanwilsonins A~J。
1.1 联苯环辛烯型木脂素
联苯环辛烯型木脂素是五味子属特有的化学成分。此类木脂素的结构中既有联苯的结构,又有联苯与侧链环合成的八元环状结构,其结构两侧苯环的1~3、12~14位主要被羟基、亚甲基二氧基或甲氧基取代。C6位的取代基通常是苯甲酸酯、乙酸酯、当归酸酯或顺芷酸酯等酯基。联苯环辛烯型木脂素含有多个手性碳原子,其绝对构型主要依据联苯之间的阻转异构、环辛烯的立体构象以及取代基的立体构型判断。通过圆二色光谱上235~255 nm内的科顿效应(cotton effect,CE)推断,CE为正,联苯为构型,CE为负,联苯为构型;通过氢谱和奥弗豪塞尔核效应(nuclear overhauser effect,NOE)来确定化合物环辛烯上取代基的绝对构型。五味子属植物中的联苯环辛烯木脂素(1~143)见表2,化学结构见图1和表3。
1.2 环木脂素
环木脂素是由1个苯丙素单位中苯环的6位和另1个苯丙素的7位环合形成。红外光谱中,该类木脂素常见的特征性吸收基团有羟基(3600~3100 cm−1)、亚甲二氧基(940~920 cm−1)和羰基(1700~1660 cm−1)。五味子属植物中环木脂素(144~157)的化学结构见图2和表4,化合物名称、植物来源及其部位见表5。
表2 五味子属中的联苯环辛烯型木脂素
Table 2 Dibenzocyclooctene lignans in Schisandra
续表2
A-果实 B-茎 C-叶 D-种仁 E-根 F-藤茎,下表同
A-fruit B-stem C-leaf D-kernel E-root F-ratan, same as below tables

图1 五味子属中联苯环辛烯型木脂素的化学结构
表3 五味子属中联苯环辛烯型木脂素的取代基
Table 3 Substituent groups of dibenzocyclooctadienes lignans in Schisandra
编号R1R2R3R4R5R6R7R8R9R10 1OHOCH3OCH3OHOCH3OCH3 α-CH3α-CH3 2OHOCH3OCH3OHOCH3OCH3 β-CH3β-CH3 3OCH2O OCH3OHOCH3OCH3 β-CH3α-CH3,β-OHα-OAng 4OCH2O OCH3OHOCH3OCH3α-OAngα-CH3,β-OHβ-CH3 5OHOCH3OCH3OCH3OCH3OCH3β-OAngα-CH3,β-OHβ-CH3 6OCH2O OCH3OCH3OCH3OCH3β-OBZα-CH3, β-OHα-CH3 7OCH2O OCH3OCH3OCH3OCH3β-OTigα-CH3,β-OHα-CH3 8OCH3OCH3OCH3OCH3OCH2O β-OAngα-OH, β-CH3α-CH3 9OCH3OCH3OCH3OCH3OCH2O β-OBZα-OH,β-CH3α-CH3 10OCH2O OCH3OCH3OCH3OCH3α-OHα-CH3α-CH3 11OCH3OCH3OHOCH3OCH3OCH3 α-CH3α-CH3 12OCH2O OCH3OCH3OCH3OHβ-OBZα-CH3α-CH3 13OCH2O OCH3OCH3OCH3OHα-OACα-CH3α-CH3 14OCH2O OCH3OCH3OCH3OCH3β-OACα-CH3,β-OHβ-CH3α-OCin 15OCH2O OCH3OCH3OCH3OCH3β-OBZα-CH3β-CH3α-OAc 16OCH2O OCH3OCH3OCH3OCH3 α-CH3α-CH3OCH3 17OCH2O OCH3OCH3OCH3OCH3β-OBZα-OH, β-CH3α-CH3 18OCH2O OCH3OCH3OCH3OCH3β-OAngα-OH, β-CH3α-CH3 19OCH2O OCH3OCH3OCH3OCH3β-OAngα-OH,β-CH3β-CH3α-OAc 20OCH2O OHOCH3OCH3OCH3 α-CH3β-CH3α-OAc 21OCH2O OCH3OCH3OCH3OCH3 α-CH3α-CH3α-OAc 22OCH2O OCH3OHOCH3OCH3 α-CH3α-CH3α-OAng 23OCH2O OCH3OHOCH3OCH3 α-CH3α-CH3α-OAc 24OCH2O OCH3OCH3OCH3OCH3β-OBZα-OH,β-CH3α-CH3α-OAc 25OCH2O OCH3OCH3OCH2O β-OBZα-CH3α-CH3, β-OH 26OCH2O OCH3OHOCH3OCH3 α-CH3α-CH3α-OH 27OCH2O OCH3OHOCH3OCH3β-OAngoxiraneα-CH3α-OAng 28OCH2O OCH3OCH3OCH3OCH3β-OAngα-CH3,β-OHα-CH3 29OCH2O OCH3OCH3OCH3OCH3 α-CH3α-CH3 30OCH2O OCH3OCH3OCH2O α-CH3α-CH3 31OCH2O OCH3OCH3OCH3OCH3β-OBZα-CH3,β-OHα-CH3 32OCH3OCH3OCH3OHOCH3OCH3 α-CH3α-CH3 33OHOCH3OCH3OCH3OCH3OH α-CH3α-CH3 34OCH3OCH3OCH3OCH3OCH3OCH3 β-CH3β-CH3 35OCH3OCH3OCH3OCH3OCH2O α-CH3α-CH3 36OCH3OCH3OCH3OCH3OCH3OCH3 α-CH3α-CH3 37OCH2O OCH3OCH3OCH3OCH3β-OAngα-CH3α-CH3 38OCH2O OCH3OCH3OCH3OCH3β-OBZα-CH3α-CH3 39OCH2O OCH3OCH3OCH3OCH3 α-CH3α-CH3α-OCH3 40OCH2O OCH3OCH3OCH3OH α-CH3α-CH3α-OCH3 41OCH2O OCH3OCH3OCH3OH α-CH3α-CH3α-OAc 42OCH3OHOCH3OCH3OCH3OCH3 α-CH3, β-OAng α-CH3 43OCH2O OCH3OCH3OCH2O β-OAngoxiraneα-CH3
续表3

编号R1R2R3R4R5R6R7R8R9R10 44OCH3OCH3OCH3OCH3OCH3OHHα-CH3,β-OHα-CH3 45OCH2O OCH3OCH3OCH2Oβ-OBZα-CH3α-CH3 46OCH2OOCH3OCH3OCH3OCH3α-OBZα-CH3,β-OHα-CH3 47OCH2OOCH3OCH3OCH3OCH3α-OTigα-CH3,β-OHα-CH3 48OCH2OOCH3OCH3OCH2Oβ-OHα-CH3α-CH3 49OCH2OOCH3OCH3OCH3OCH3β-OHα-CH3α-CH3 50OCH3OCH3OCinOCH3OCH3OCH3 α-CH3,β-OHα-CH3 51OCH3OCH3OBZOCH3OCH3OCH3 α-CH3α-CH3 52OCH3OHOCH3OCH3OCH3OH α-CH3α-CH3 53OCH3OCH3OCH3OHOCH3OH α-CH3α-CH3 54OCH3OCH3OHOCH3OCH3OH α-CH3α-CH3 55OCH2OOCH3OCH3OCH3OCH3α-OHα-CH3α-CH3 56OCH2OOCH3OCH3OCH3OCH3β-OBZα-CH3α-CH3 57OCH2OOCH3OCH3OCH3OCH3β-OAngα-CH3,β-OHα-CH3 58OCH2OOCH3OCH3OCH3OCH3β-OBZα-CH3,β-OHα-CH3 59OHOCH3OCH3OCH3OCH3OCH3 α-CH3,β-OHα-CH3 60OAcOCH3OCH3OCH3OCH3OCH3 α-CH3α-CH3 61OCH3OCH3OHOCH3OCH2O α-CH3α-CH3 62OHOCH3OCH3OCH3OCH3OHβ-OBZα-CH3α-CH3 63OCH2OOCH3OCH3OCH3OCH3 α-CH3α-CH3α-OH 64OCH3OCH3OCH3OCH3OCH3OCH3β-OAngα-OH,β-CH3α-CH3 65OCH3OCH3OCH3OHOCH3OCH3β-OAcα-CH3,β-OHβ-CH3α-OBZ 66OCH2OOCH3OCH3OCH3OCH3β-OAngα-CH3α-CH3α-OAc 67OCH3OCH3OAngOCH3OCH3OCH3 α-CH3,β-OHα-CH3 68OCH3OCH3OHOCH3OCH3OCH3 α-CH3,β-OHα-CH3 69OCH3OCH3OTigOCH3OCH3OCH3 α-CH3,β-OHα-CH3 70OCH3OCH3OBZOCH3OCH3OCH3 α-CH3,β-OHα-CH3 71OHOCH3OCH3OAngOCH3OCH3 α-CH3α-CH3 72OCH3OCH3OAngOCH3OCH3OCH3C7=C8α-CH3α-CH3 73OCH2OOHOHOCH3OCH3β-OAngα-OH,β-CH3α-CH3α-OAng 74OCH3OCH3OCH3OAngOCH3OCH3 β-CH3α-CH3α-OH 75OHOCH3OCH3OCH3OCH3OCH3β-OAngα-OH,β-CH3α-CH3α-CO(CH2)4CH3 76OHOCH3OCH3OHOCH3OCH3β-OBzα-OH,β-CH3α-CH3α-CO(CH2)4CH3 77OCH2OOHOCH3OCH3OCH3β-OAngα-OH,β-CH3α-OH, β-CH3α-COCH2CH3 78OHOCH3OCH3OAngOAngOAngβ-OAcβ-CH3α-CH3α-OH 79OHOCH3OCH3OCH3OCH3OCH3β-OBzα-OH,β-CH3α-OAngα-CO(CH2)4CH3 80OCH2OOCH3OCH3OCH3OCH3β-OAngβ-CH3α-CH3α-CO(CH2)4CH3 81OCH3OCH3OBzOCH3OCH3OCH3 α-CH3α-CH3 82OCH3OCH3OAngOCH3OCH3OCH3 α-CH3α-CH3 83OHOCH3OCH3OCH3OCH3OCH3α-OHα-CH3α-CH3 84OCH3OCH3OHOCH3OCH2O α-CH3α-CH3 85OCH2OOHOCH3OCH3OCH3β-OHα-CH3α-CH3 86OCH2OOCH3OCH3OCH3OCH3 α-CH3α-CH3 87OCH2OOCH3OCH3OCH3OCH3β-CH3Oα-CH3α-CH3 88OCH2OOCH3OCH3OCH3OCH3β-OBZα-CH3,β-OHα-CH3
续表3

图2 五味子属中环木脂素的化学结构
表4 五味子属中环木脂素的取代基
Table 4 Substituent groups of cyclolignans in Schisandra
编号R1R2R3R4R5R6 144OHOCH3OHOCH3β-CH3β-CH3 145OCH3OHOHOCH3β-CH3β-CH3 146OHOCH3OCH3OCH3β-CH3β-CH3 147OHOCH3OCH3OCH3α-CH3β-CH3 148OCH3OCH3OHOCH3β-CH3β-CH3 149OCH3OHOHOCH3β-CH3α-CH3 150OHOCH3OHOCH3β-CH3α-CH3 151OHOCH3OHOCH3β-CH3β-CH3 152OHOCH3OCH3OCH3β-CH3α-CH3
表5 五味子属中的环木脂素
Table 5 Cyclolignans in Schisandra
编号化合物名称来源部位文献 144arisantetralone AaA5 145arisantetralone BaA5 146arisantetralone CaA5 147arisantetralone DaA5 148(−)-holostyligoneaA5 149wulignan A2f, nA, B13,27 150epiwulignan A1f, nA, B13,27 151wulignan A1f, rA, B8,27 152epischisandronefB27 153(−)-galcatindA35 154(+)-isootobaphenol dA35 1554′,5-O-didemethylcyclogalgravindA35 156henricines BfB27 1574,4-di(4-hydroxy-3-methoxyphenly)- 2,3-dimethylbutanol lB36
1.3 单环氧木脂素
单环氧木质素结构的特征在于在简单木质素的基础上存在四氢呋喃结构,如7--7′、9--9′或7--9′等结构类型,五味子属中该类成分主要是7--7′型最为常见,该类结构常具有对称性结构,在氢谱中,可见2个d峰的甲基信号重叠。在1.78左右有2个m峰的氢信号。五味子属植物中的单环氧木脂素(158~193)见表6,化学结构见图3和表7。
1.4 简单木脂素
简单木脂素是由2分子苯丙素仅通过β位的碳原子(C8-C8′)连接而成,该类木脂素可用EI-MS测定,多数木脂素可得到分子离子峰,木脂素因有苄基基团,从而可以发生苄基裂解。且这类化合物也是其他一些类型木脂素的生源前体。五味子属植物中的简单木脂素(194~226)见表8,化学结构见图4和表9。
1.5 7,8-开环木脂素
7,8-开环木脂素的骨架是芳基四氢呋喃木脂素C7-C8键的氧化裂解。从五味子属的果实、茎和叶中共分离出9种化合物。五味子属植物中的7,8-开环木脂素(227~235)见表10,化学结构见图5。
1.6 双环氧木脂素
双环氧木脂素是一种由2分子苯丙素相互连接形成具有双骈四氢呋喃环结构的木脂素,并且骨架中多具有4个手性碳的旋光异构体,在核磁共振碳谱上C7和C7′位的化学位移可达到85.0以上,因其结构的对称性,氢谱和碳谱也常会出现重叠信号。(+)-pinoresinol(236)、(+)-syringaresinol(237)和prinsepiol(238)均来自金山五味子的茎[25,39],化学结构见图6。
1.7 新木脂素
新木脂素是由2个苯丙素通过侧链、苯环或氧连接形成,且在C8和C8′之间没有化学键。C9位为羟甲基时,碳谱上89.0、55.5、65.0为苯骈呋喃型新木脂素C7、C8、C9的典型特征。此外,新木脂素还包括2个以氧键形式通过氧醚键连接的C6-C3单体,因此也称为氧新木脂素。vladinol F(239)可以从金山五味子、小花五味子的茎中分离得到[30,39],化学结构见图7。
表6 五味子属中的单环氧木质素
Table 6 Monoepoxylignans in Schisandra
编号化合物名称来源部位文献 158zuihonins EbB37 159zuihonins FbB38 160ganschisandrinbA6 1613′,3″-dimethoxylarreatricinbA6 162(+)-9′-hydroxygalbelginbA6 163schiglaucin AdB39 164schiglaucin BdB39 165(+)-zuihonin AdB25 166(–)-zuihonin CdB25 167(+)-chicaninedA35 168henricines AfB27 169ganshisandrinefB27 170(+)-henricin f, gA11 171(+)-zuihonin Cd, gA, B11,39 172d-表加巴辛rF8 173galgravinbA6 174(–)-nectandrin AbA6 175(–)-futokadsurin AbA6 176schisanpropininlB40 177(–)-machilusinsB37 178ganschisandrinesA, B37,41 179(+)-neoolivilsB18 180schisphenlignan HsB42 181veraguensinsA43 182(7S,8S,7′R,8′S)-7-methoxyl-7-(3,4-methylenedioxyphenyl)-8-hydroxyl-7′-(5′-hydroxy-3′-methoxyphenyl)-8′-methyl-tetrahydrofuransE44 183(7S,8S,7′R,8′S)-7-methoxyl-7-(3,4-methylenedioxy-phenyl)-8-hydroxyl-8′-methyl-7′-(3′,4′,5′-trimethoxyphenyl)-tetrahydrofuransE44 184(7S,8S,7′R,8′S)-7-methoxyl-7-(3,4-methylenedioxyphenyl)-8-hydroxyl-8′-methyl-7′-(3′,4′-methylenedioxyphenyl)-tetrahydrofuransE44 185schiglaucin BsE44 186schiglaucin AsE44 187(7S,8S,7′R,8′S)-(7,8-trans-8,8′-trans-7′,8′-trans)-7-methoxyl-7-(3,4-methylenedioxy-phenyl)-8-methyl-8′-methyl-7′-(3′,4′-dimethoxyphenyl)-tetrahydrofuransE44 188(7S,8S,7′R,8′S)-7-methoxyl-7-(3,4,5-trimethoxyphenyl)-8-methyl-8′-methyl-7′-(3′,4′- methylenedioxyphenyl)-tetrahydrofuransE44 189(7S,8S,7′R,8′S)-7-(3,4-methylenedioxyphenyl)-8-methyl-8′-methyl-7′-(3′,4′-dihydroxy-phenyl)-tetrahydrofuransE44 190talaumidinsE44 191(7S,8S,7′R,8′S)-7,8-epoxide-7-(3,4-methylenedioxyphenyl)-8-methyl-8′-methyl-7′-(3′,4′-dimethoxyphenyl)-tetrahydrofuransE44 192(7S,8S,7′R,8′S)-7,8-epoxide-7-(3,4-methylenedioxyphenyl)-8-methyl-8′-methyl-7′-(4′-hydroxy-3′-methoxyphenyl)-tetrahydrofuransE44 193epoxyzuonin AsE44

图3 五味子属中单环氧木脂素的化学结构
表7 五味子属中单环氧木脂素的取代基
Table 7 Substituent groups of monoepoxylignans in Schisandra
编号R1R2R3R4R5R6R7R8R9R10 158β-CH3α-OH, β-CH3OCH2O OCH2Oα-OCH3 159β-CH3α-OH, β-CH3OCH2O OCH2Oα-OH 160β-CH3β-CH3 OCH3OCH3OCH3OCH3 161β-CH3β-CH3 OHOCH3OCH3OH 162β-CH2OHα-CH3 OCH2OOCH2O 163β-CH3α-CH3, β-OH OCH2OOCH3OCH3 α-OCH3 164β-CH3α-CH3, β-OH OCH3OCH3OCH2O α-OCH3 165α-CH3α-CH3 OCH2OOCH2O 166α-CH3α-CH3 OCH3OCH3OCH2O 167α-CH3α-CH3OCH2O OHOCH3 168β-CH3α-CH3, β-OH OCH3OCH3 OCH3OCH3α-OCH3 169β-CH3β-CH3 OCH3OCH3 OCH3OCH3α-OCH3 170β-CH3β-CH3 OCH2OOCH3OCH3OCH3 171α-CH3α-CH3 OCH3OCH3OCH2O 172β-CH3β-CH3 OCH2OOCH2O 177β-CH3α-H,β-CH3HOCH3OCH3OCH2OH 178β-CH3α-H,β-CH3HOCH3OCH3OCH3OCH3H 179β-CH2OHα-CH2OH,β-HHOCH3OHHOHOCH3 180β-CH3α-CH3, β-OHOCH2OHOCH3OCH3OHα-OCH3 181α-CH3α-H,β-CH3HOCH3OCH3OCH3OCH3H 182α-OH, β-CH3α-CH3,β-HOCH3HOHOCH2OH β-OCH3 183α-OH, β-CH3α-CH3,β-HOCH3OCH3OCH3OCH2OH β-OCH3 184α-OH, β-CH3α-CH3,β-HHCH2OCH2OH β-OCH3 185α-OH, β-CH3α-CH3,β-HHOCH2OCH3CH3H β-OCH3 186α-OH, β-CH3α-CH3,β-HHOCH3OCH3OCH2OH β-OCH3 187β-CH3α-CH3,β-HHOCH3OCH3OCH2OH β-OCH3 188β-CH3 α-CH3,β-HHOCH2OOCH3OCH3OCH3 β-OCH3 189β-CH3 α-CH3,β-HHOHOHOCH2OH 190β-CH3 α-CH3,β-HHOCH3OHOCH2OH
表8 五味子属中的简单木脂素
Table 8 Simple lignans in Schisandra
编号化合物名称来源部位文献 194pre-gomisinaA5 195austrobailignan-6bA6 196oleiferin FbA6 197(+)-dihydroguaiaretic acid bA6 1985-[(2S,3R)-4-(3,4-dimethoxyphenyl)-2,3-dimethylbutyl]-1,3-benzodioxoledA35 199meso-dihydroguaiaretic aciddA35 200(+)-anwulignandA35 201华中五脂素gA11 202longipedunrin CnA, B, C20 203pubinerlignan EnA, B, C20 2042,3-bis[(4-hydroxy-3-methoxyphenyl)methyl]butanlolnA, B, C20 205schibitubin A bA6 206schibitubin BbA6 207schibitubin CbA6 208schibitubin DbA6 209schibitubin EbA6 210schibitubin FbA6 211tetracentronside BdA35 212(−)-secoisolariciresinol-9-O-β-D-xylopyranosidedB39 213arisanschinin EaA17 214schibitubin GbA6 215tetracentronside BdA35 216(8R,8′R)-9-O-β-D-glucopyranosylpiperphilippinin VIdA35 217(8R,8′R)-9′-O-β-D-glucopyranosylpiperphilippinin VIdA35 218sphenanlignansA45 219myristargenol AsA, D37,44 220schisphenlignan FsB43 221前戈米辛sA, B43 222(–)-secoisolariciresinol-O-α-L-rhamnopyranosidsB18 223(7,8-trans-8,8′-cis)-7-(3,4-dihydroxyphenyl)-7′-(3,4-methylenedioxyphenyl)-8,8′-dimethylbutan-7-diolsD44 224schisphenin AsA46 225erythro-1-(3,4-dimethoxyphenyl)-4-(3,4-methylenedioxyphenyl)-2,3-dimethylbutanesA47 226erythro-austrobailignan-6sA47
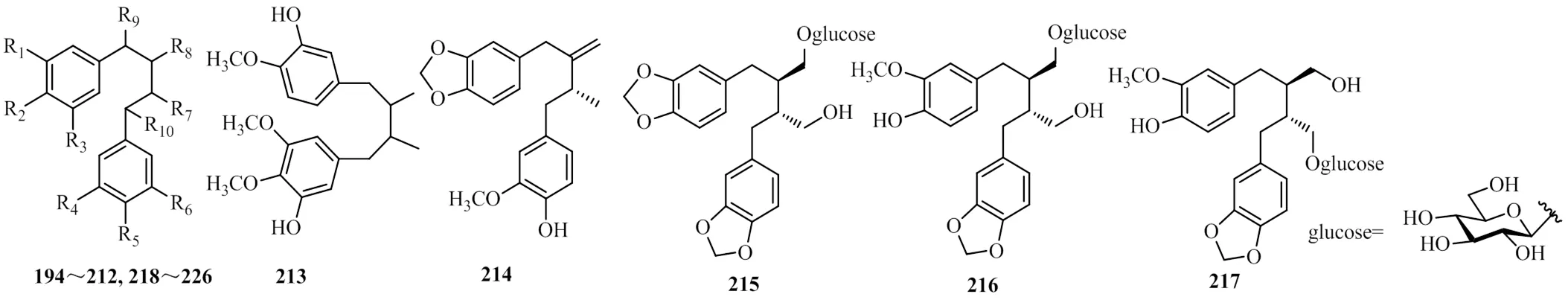
图4 五味子属中简单木脂素的化学结构
表9 五味子属中单环氧木脂素的取代基
Table 9 Substituent groups of monoepoxylignans in Schisandra
编号R1R2R3R4R5R6R7R8R9R10 194OCH3OCH3OHOHOCH3OCH3β-CH3β-CH3 195OCH2O OCH3OH α-CH3β-CH3 196OCH2O OCH3OH α-CH3β-CH3α-OH 197OCH3OH OCH3OH α-CH3β-CH3 198OCH2OOCH3OCH3 199OCH3OH OHOCH3α-CH3α-CH3 200OCH3OH OCH2Oα-CH3α-CH3 201OCH2O OCH3OCH3OHβ-CH3β-CH3 202OCH3OCH3OHOCH3OH β-CH3β-CH3 203OCH3OCH3OHOCH3OCH3 β-CH3β-CH3 204OCH3OH OCH3OH β-CH3β-CH2OH 205OCH3OH OCH2O α-CH3α-CH2OH 206OCH3OH OCH3OH α-CH3α-CH2OH 207OCH2O OCH3OH β-CH3β-CH2OH 208OCH2O OCH3OH β-CH3β-CH2OH 209OCH3OH OCH2O β-CH3β-CH2OAc 210OCH3OH OCH3OH β-CH3β-CH2OAc 211OCH2O OCH2O α-CH2OHβ-CH2Oglucose 212OCH3OH OCH3OH α-CH2OHβ-CH2Oxylosyl 219OCH2OHOCH3OCH3OHβ-CH3β-CH3 220OCH3OHHHOCH2Oα-CH3α-CH3 221OHOCH3OCH3OCH3OHOCH3α-CH3H 222OHOCH3OCH3OCH3OCH3OHβ-CH3H 223OCH3OHHHOHOCH3α-CH2OHβ-CH2Orhamnoyl 224HOCH2OOHHOCH3β-CH3β-CH3 β-OH 225HOCH2OHOHOCH3β-CH3β-CH3 β-OH 226OCH2OHHOCH3OCH3β-CH3β-CH3
表10 五味子属中的7,8-开环木脂素
Table 10 7,8-Seco-lignans in Schisandra
编号化合物名称来源部位文献 227schibitubin IbA 6 228(7′R,8′S)-3,4-dimethoxy-3′,4′-methylenedioxy-7,8-seco-7,7′-epoxylignan-7,8-dionedA35 229(7′R,8′S)-3,4-methylenedioxy-3′,4′-dimethoxy-7,8-seco-7,7′-epoxylignan-7,8-dionedA35 230neglectahenols AjB, C48 231neglectahenols BjB, C48 232neglectahenols CjB, C48 233neglectahenols DjB, C48 234marphenol B jB, C48 2357,8-secoholostylone BjB, C48

图5 五味子属中7,8-开环木脂素的化学结构
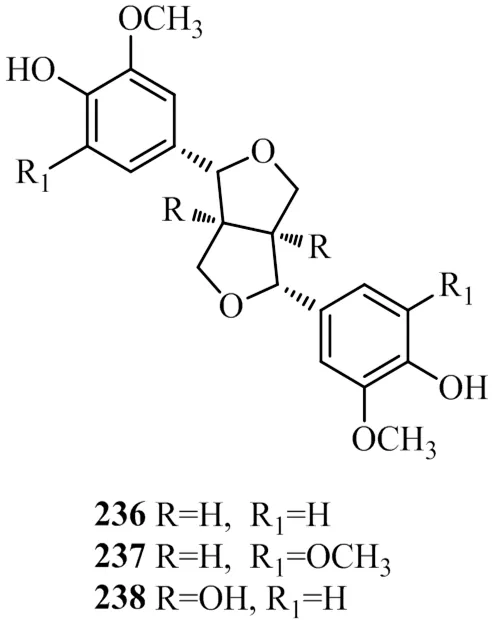
图6 五味子属中双环氧木脂素的化学结构

图7 五味子属中新木脂素的化学结构
2 药理作用
2.1 保肝
Chen等[49]研究发现阿里山五味子中(+)-戈米辛K3(11)有显著的抗肝纤维化活性。王菊平等[50]通过大鼠急性肝内胆汁淤积造成的肝损伤实验,发现deoxyschisandrin(36)能通过降低丙氨酸氨基转移酶(alanine aminotransferase,ALT)、谷氨酸氨基转移酶(aspartate aminotransferase,AST)、碱性磷酸酶(alkaline phosphatase,ALP)活性及总胆红素(total bilirubin,TBIL)水平,升高肝脏中Na+, K+-ATP酶活性而发挥肝脏保护作用。此外,五味子药渣提取物中木脂素类成分对CCl4所致大鼠急性肝损伤具有保护作用[51]。关于华中五味子中木脂素保肝作用的研究最为广泛,Gao等[52]发现化合物(+)-anwulignan(200)可以降低肝脏外周血液中的AST和ALT活性,其机制可能与激活p38丝裂原活化蛋白激酶通路的抗氧化能力,增加受损细胞的生存能力有关;单体化合物schisandrol B(16)具有显著的保肝作用,研究人员发现其能够降低对乙酰氨基酚诱导的肝毒性,其作用机制是通过激活核因子E2相关因子2(nuclear factor NF-E2-related factor 2,Nrf2)/抗氧化反应元件(anti-oxidant response element,ARE)途径和调节靶基因,从而诱导排毒[53]。此外,schisandrol B还具有促小鼠肝脏再生功能[54]。
2.2 抗肿瘤
张孟亭[5]研究发现阿里山五味子中单体化合物arisanschinin F(1)对人髓母细胞瘤Daoy细胞、结肠癌WiDr细胞、人喉表皮样癌HEp-2细胞、人乳腺癌MCF-7细胞具有明显的细胞毒活性,半数有效量分别为6.23、6.08、4.12、4.09 μg/mL。二色五味子中分离得到的新木脂素zuihonins E~F(158~159)能够抑制人肝癌HepG2细胞、人肺癌A549细胞和MCF-7细胞的生长[39]。Chen等[21]发现neglschisandrins F(72)对A549细胞具有较好的抑制作用,同时该单体化合物对于人结肠癌HCT-8细胞表现出中度的细胞毒性。Gao等[55]从合蕊五味子中分离得到化合物schisantherin F(71),研究表明schisantherin F可通过抑制半胱氨酸天冬氨酸蛋白酶-3(cystein-asparate protease-3,Caspase-3)和Caspase-9的活性,下调B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)和上调凋亡相关因子Bcl-2相关X蛋白(B-cell lymphoma-2/Bcl-2 associated X protein,Bax)的表达从而诱导人黑色素瘤A375细胞的凋亡;乳腺癌为现今多发疾病,对于此疾病的研究,五味子属绿叶五味子具有显著的药理活性,研究报道其抗肿瘤活性成分有angelylgomisin H(67)和戈米辛H(68)[56-57]。Yang等[58]发现化合物(+)-戈米辛M2(111)能够抑制乳腺癌干细胞BCSCs增殖;除此之外,戈米辛J(33)对MCF-7细胞、乳腺癌MDA-MB-23细胞以及其他11种癌细胞都具有显著的细胞毒活性[59]。对于三阴性乳腺癌的研究发现schisandrin A(34)可能成为其治疗的潜在候选药物[60]。
2.3 抗病毒
现代药理学研究表明五味子属植物具有显著的抗病毒作用,孙汉董课题组对五味子属植物进行了广泛的研究,发现五味子属中多种植物具有该药理活性。Chen等[61]发现红花五味子中木脂素戈米辛J、戈米辛M2、(±)-戈米辛M1(61)具有抗人类免疫缺陷病毒(human immunodeficiency virus,HIV)活性,(±)-戈米辛M1表现出最有效的抗HIV活性。Xue等[62]从五味子的果实中分离出的methylgomisin O(87)具有很强的抗乙型肝炎病毒(hepatitis B virus,HBV)病毒活性,其半数抑制浓度为5.49 μg/mL。从阿里山五味子中分离出的戈米辛B(28)和戈米辛G(9)在抗HBsAg和HBeAg测试中显示出中等活性[63]。Ma等[64]从鹤庆五味子果实部位分离得到抗HBV木脂素活性成分schisanwilsonins A~G,其中schisanwilsonins C抗HBV活性最显著。
五味子属中木脂素成分除了对人类HIV、HBV等病毒有作用外,对于植物病毒也有一定的研究报道。Wang等[65]研究发现红花五味子中schisanhenol(32)对烟草花叶病毒具有防治作用,且抗病毒效果强于宁南霉素。此外还发现滇藏五味子中木脂素neglectahenols E~F同样具有抗烟草花叶病毒活性[66]。
2.4 抗氧化
研究者从阿里山五味子醋酸乙酯部位分离的arisanschinins E具有明显的1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl radical,DPPH)自由基清除活性[67]。Wang等[68]通过研究不同产地五味子和华中五味子中木脂素抗氧化活性,发现其主要抗氧化活性成分为schisanhenol和schisandrin B(29)。同时Jiang等[44]对华中五味子根部进行了化学成分的分离和抗氧化活性研究,所分离得到的木脂素均具有不同程度的清除DPPH自由基能力,其中化合物190抗氧化活性与维生素C相当,并且对人红细胞寿命具有显著的抗氧化溶血作用。此外,五味子总木脂素也具有良好的清除超氧阴离子自由基能力[69]。
2.5 神经保护
二色五味子中所分离出的schiglaucin A(163)、(+)-chicanine(167)、d-表加巴辛(172)、galgravin(173)在淀粉样β蛋白片段25-35(Aβ25-35)诱导的人神经母细胞瘤SH-SY5Y细胞损伤模型中显示具有很好的神经保护活性[6]。此外,从金山五味子茎中分离出的2个新四氢呋喃木脂素schiglaucin A和schiglaucin B(164)对SH-SY5Y细胞损伤同样具有明显的神经保护作用[35,39]。通过大鼠Morris水迷宫实验,于方等[70]发现华中五味子酮通过影响大鼠海马区核因子-κB信号转导通路而对阿尔茨海默症发病起到保护作用。此外,有研究发现提高大鼠脑内抗氧化系统活性和促进氧自由基清除,可能是华中五味子酮治疗阿尔茨海默症模型大鼠新的作用机制[71]。
3 结语与展望
我国五味子属资源丰富,集中分布于西南部和东南部地区,随着对该属植物成分不断深入的研究,其现代药理研究也取得了较大进展,尤其是其主要活性成分木脂素,具有广泛的药理活性,在保肝、抗肿瘤、抗氧化、神经保护方面效果突出。目前对五味子属植物中南北五味子的研究有较详尽的综述,而该属其他植物化学成分和药理作用的报道都相对较少。此外,该属植物仍然没有完整的质量标准可供参考,不同产地五味子指标性成分有一定的差异。
值得注意的是,对于单体化合物的研究与开发,以华中五味子酮、五味子酯甲、五味子醇乙、五味子丙素和五味子酚的研究最为广泛,其中五味子丙素具有很好的治疗肝炎作用,在此结构基础上研发了我国首个治疗肝炎的新药联苯双酯,2004年治疗肝炎的I类新药双环醇的上市更加证明了五味子独具的保肝作用。因此从五味子属植物天然产物中寻找新的具有开发新药价值的先导化合物依然具有十分重要的意义。此外抗氧化作用突出的木脂素类成分有望成为新的抗氧化剂,为研发心脑血管疾病药物奠定基础。用于器官移植免疫抑制效果突出的乙醇提取物,仍然需要不断深入地研究其药理作用机制。五味子属植物具有很好的增强免疫力、改善记忆力和改善睡眠效果,可用于开发更广泛的保健品。红酒、果糖饮料、护肤品等也需要进一步开发和推广。在临床应用研究方面,有报道称华中五味子叶对骨损伤有一定的治疗作用,应引起重视。
利益冲突 所有作者均声明不存在利益冲突
[1] 许利嘉, 刘海涛, 彭勇, 等. 五味子科药用植物亲缘学初探 [J]. 植物分类学报, 2008, 46(5): 692-723.
[2] 中国科学院中国植物志编辑委员会. 中国植物志 [M]. 北京: 科学出版社, 1996: 243.
[3] 中国药典 [S]. 一部. 2020: 69, 263.
[4] Liu C S, Fang S D, Huang M F,. Studies on the active principles ofRehd. et Wils. The structures of schisantherin A, B, C, D, E, and the related compounds [J]., 1978, 21(4): 483-502.
[5] 张孟亭. 阿里山五味子果实活性木酚素成分之研究[D]. 台湾: 台湾大学, 2009.
[6] Liu Y, Yu H Y, Wang Y M,. Neuroprotective lignans from the fruits ofvar.[J]., 2017, 80(4): 1117-1124.
[7] Gao X M, Wang R R, Niu D Y,. Bioactive dibenzocyclooctadiene lignans from the stems of[J]., 2013, 76(6): 1052-1057.
[8] 马文辉. 毛南五味子和鹤庆五味子的化学成分及其抗病毒活性 [D]. 上海: 复旦大学, 2007.
[9] 刘叶. 绿叶五味子果实化学成分及神经保护作用研究[D]. 武汉: 华中科技大学, 2014.
[10] 张明晓, 黄国英, 白羽琦, 等. 南、北五味子的化学成分及其保肝作用的研究进展 [J]. 中国中药杂志, 2021, 46(5): 1017-1025.
[11] 田添. 两种五味子属药用植物的化学成分及生物活性研究[D]. 武汉: 华中科技大学, 2015.
[12] 陶媛媛, 杨建红, 张燕, 等. 翼梗五味子木脂素成份的分离与鉴定 [J]. 云南师范大学学报: 自然科学版, 2007, 27(1): 65-68.
[13] Xiao W L, Wang R R, Zhao W,. Anti-HIV-1 activity of lignans from the fruits of[J]., 2010, 33(5): 697-701.
[14] 徐秀梅, 廖志华, 陈敏. 滇藏五味子化学成分研究 [J]. 中国药学杂志, 2009, 44(23): 1769-1773.
[15] Yang G Y, Li Y K, Wang R R,. Dibenzocyclooctadiene lignans fromand their anti-HIV-1 activities [J]., 2010, 73(5): 915-919.
[16] Luo X, Pu J X, Fan P,. Four new dibenzocyclooctadiene lignans from[J]., 2011, 9(3): 167-172.
[17] 刘金城. 阿里山五味子活性木脂素成分之研究[D]. 台湾: 台湾大学, 2008.
[18] Huang S Q, Zhang D D, Li Y Z,.: A comprehensive review of its botany, phytochemistry, pharmacology, and clinical applications [J]., 2021, 49(7): 1577-1622.
[19] 刘嘉森, 黄梅芬, 高耀良. 翼梗五味子的研究Ⅱ翼梗五味子酯和翼梗五味子酸的结构[J]. 上海: 中国科学院上海药物研究所, 1980, 38(4): 361-370.
[20] 刘嘉森, 马玉廷. 神农架地区五味子科植物成分的研究II.五味子酯F的分离与结构研究 [J]. 化学学报, 1988(5): 460-464.
[21] Chen M, Xu X M, Xu B,. Neglschisandrins E-F: Two new lignans and related cytotoxic lignans from[J]., 2013, 18(2): 2297-2306.
[22] 李磊. 毛叶五味子化学成分的研究 [D]. 重庆: 西南大学, 2008.
[23] Mu H X, Li X S, Fan P,. Dibenzocyclooctadiene lignans from the fruits ofand their anti-HIV-1 activities [J]., 2011, 13(5): 393-399.
[24] Tian T, Liu Y, Yu H Y,. Dibenzocyclooctadiene lignans from the fruits of[J]., 2015, 51(6): 1046-1048.
[25] Cai N N, Wang Z Z, Zhu X C,. Schisandrin A and B enhance the dentate gyrus neurogenesis in mouse hippocampus [J]., 2020, 105: 101751.
[26] 刘小霞, 刘芳, 顾蔚. 秦岭地区四种五味子果实木脂素检测 [J]. 中药材, 2013, 36(7): 1053-1055.
[27] Liu H T, Xu L J, Peng Y,. Two new lignans from[J]., 2009, 57(4): 405-407.
[28] Yang G Y, Fan P, Wang R R,. Dibenzocyclooctadiene lignans fromand their anti-human immunodeficiency virus-1 activities [J]., 2010, 58(5): 734-737.
[29] 李蓉涛. 五种五味子属药用植物及东紫苏化学成分研究[D]. 昆明: 中国科学院昆明植物研究所, 2003.
[30] Huang S Q, Liu Y Y, Li Y Z,. Dibenzocyclooctadiene lignans from the root bark of[J]., 2021, 45: 137-141.
[31] 王洪洁, 陈延镛. 红花五味子中木脂素成分的化学研究 [J]. 药学学报, 1985, 20(11): 832-841.
[32] Chen M, Liao Z, Xu X,. Neglschisandrins C-D: Two new dibenzocyclooctadiene lignans from[J]., 2008, 13(5): 1148-1155.
[33] Xu L J, Huang F, Chen S B,. New lignans and cytotoxic constituents from[J].,2006, 72(2): 169-174.
[34] 罗纲, 刘嘉森. 粤北产五味子科植物风沙藤的化学成分研究(II) [J]. 化学学报, 1992, 50(5): 515-520.
[35] Yu H Y, Chen Z Y, Sun B,. Lignans from the fruit ofwith antioxidant and neuroprotective properties [J]., 2014, 77(6): 1311-1320.
[36] Huang F, Xu L J, Ganggang S. Antioxidant isolated from(Wall.) Baill [J]., 2009, 42(3): 351-356.
[37] 任荣. 华中五味子的化学成分及其抗炎活性研究 [D]. 昆明: 昆明理工大学, 2009.
[38] Huang R M, Huang H J, Zhang N L,. Two new lignans from the stems of[J]., 2012, 14(12): 1116-1121.
[39] Yu H Y, Hao C, Meng F Y,. Neuroprotective lignans from the stems of[J]., 2012, 78(18): 1962-1966.
[40] Liu M, Hu Z X, Luo Y Q,. Two new compounds fromvar.[J]., 2017, 7(3): 257-262.
[41] Li Y F, Jiang Y, Huang J F,. Four new lignans from[J]., 2013, 15(9): 934-940.
[42] Liang C Q, Hu J, Luo R H,. Six new lignans from the leaves and stems of[J]., 2013, 86: 171-177.
[43] Huang H C, Lin Y C, Fazary A E,. New and bioactive lignans from the fruits of[J]., 2011, 128(2): 348-357.
[44] Jiang K, Song Q Y, Peng S J,. New lignans from the roots of[J]., 2015, 103: 63-70.
[45] 蒋司嘉. 五味子和华中五味子的木脂素类化学成分研究 [D]. 上海: 复旦大学, 2003.
[46] 陈聿桢. 红花八角果实和阿里山五味子果实活性成分的研究 [D]. 台湾: 台湾大学药学研究所, 2010.
[47] 宋秋艳. 秦岭两种五味子属植物化学成分结构及其抗病毒活性研究 [D]. 兰州: 兰州大学, 2013.
[48] Gao X M, Mu H X, Wang R R,. 7,8-secolignans fromand their anti-HIV-1 activities [J]., 2012, 23(10): 1853-1857.
[49] Chen Y C, Liaw C C, Cheng Y B,. Anti-liver fibrotic lignans from the fruits ofand[J]., 2013, 23(3): 880-885.
[50] 王菊平, 李小芹, 李永春. 五味子甲素对急性肝内胆汁淤积大鼠肝功能的保护作用研究 [J]. 亚太传统医药, 2018, 14(6): 32-33.
[51] 陶小芳, 宿树兰, 江署, 等. 五味子药渣提取物中木脂素类成分分析及其对急性肝损伤模型大鼠的保护作用 [J]. 中草药, 2016, 47(17): 3051-3057.
[52] Gao J Q, Yu Z P, Jing S,. Protective effect of anwulignan against-galactose-induced hepatic injury through activating p38 MAPK-Nrf2-HO-1 pathway in mice [J]., 2018, 13: 1859-1869.
[53] Jiang Y M, Wang Y, Tan H S,. Schisandrol B protects against acetaminophen-induced acute hepatotoxicity in mice via activation of the NRF2/ARE signaling pathway [J]., 2016, 37(3): 382-389.
[54] Li X, Sun J, Fan X,. Schisandrol B promotes liver regeneration after partial hepatectomy in mice [J]., 2018, 818: 96-102.
[55] Gao D, Qu Y, Wu H. Inhibitory effects of schisantherin F fromsubsp.on human melanoma A375 cells through ROS-induced mitochondrial dysfunction and mitochondria-mediated apoptosis [J]., 2020, 34(10): 1486-1489.
[56] Zhang J, Shi L L, Zheng Y N. Dibenzocyclooctadiene lignans fromimprove glucose uptake[J]., 2010, 5(2): 231-234.
[57] Hou X T, Deng J G, Zhang Q,. Cytotoxic ethnic Yao medicine Baizuan, leaves ofA. C. Smith [J]., 2016, 194: 146-152.
[58] Yang Y G, Hao E W, Pan X L,. Gomisin M2 from Baizuan suppresses breast cancer stem cell proliferation in a zebrafish xenograft model [J]., 2019, 11(19): 8347-8361.
[59] Jung S, Moon H I, Kim S,. Anticancer activity of gomisin J fromfruit [J]., 2019, 41(1): 711-717.
[60] Xu X, Rajamanicham V, Xu S,. Schisandrin A inhibits triple negative breast cancer cells by regulating Wnt/ER stress signaling pathway [J]., 2019, 115: 108922.
[61] Chen M, Kilgore N, Lee K H,. Rubrisandrins A and B, lignans and related anti-HIV compounds from[J]., 2006, 69(12): 1697-1701.
[62] Xue Y B, Li X F, Du X,. Isolation and anti-hepatitis B virus activity of dibenzocyclooctadiene lignans from the fruits of[J]., 2015, 116: 253-261.
[63] Wu M D, Huang R L, Kuo L M,. The anti-HBsAg (human type B hepatitis, surface antigen) and anti-HBeAg (human type B hepatitis, e antigen) C18dibenzocyclooctadiene lignans frommatsudai and[J]., 2003, 51(11): 1233-1236.
[64] Ma W H, Lu Y, Huang H,. Schisanwilsonins A-G and related anti-HBV lignans from the fruits of[J]., 2009, 19(17): 4958-4962.
[65] Wang Q Y, Deng L L, Liu J J,. Schisanhenol derivatives and their biological evaluation against tobacco mosaic virus (TMV) [J]., 2015, 101: 117-124.
[66] Wang H, Yang J X, Lou J,. 7,8-Secolignans from the fruits of[J]., 2015, 17(1): 27-32.
[67] Liu C C, Abd El-Razek M H, Liaw C C,. Arisanschinins A-E, lignans fromhay [J]., 2010, 76(14): 1605-1610.
[68] Wang X T, Yu J H, Li W,. Characteristics and antioxidant activity of lignans inandfrom different locations [J]., 2018, 15(6): e1800030.
[69] 马莹慧, 冯波, 朱鹤云, 等. 北五味子中总木脂素类成分的抗氧化及抗炎活性研究 [J]. 食品研究与开发, 2019, 40(11): 25-30.
[70] 于方, 拓西平, 吕建勇, 等. 华中五味子酮对阿尔茨海默病样大鼠学习记忆功能及海马区核因子κB、诱导型一氧化氮合酶表达的影响 [J]. 第二军医大学学报, 2007, 28(12): 1351-1355.
[71] 吕建勇, 拓西平, 于方. 华中五味子酮对阿尔茨海默病模型大鼠学习记忆的影响及其机制的研究 [J]. 山西医药杂志, 2007, 36(1): 27-29.
Research progress on lignans and pharmacological activities in plants of
LIU Yuan-yuan, HUANG Shi-qi, LI Yu-ze, FAN Hao, ZHANG Hua-wei, DENG Chong, SONG Xiao-mei, ZHANG Dong-dong, WANG Wei
College of Pharmacy, Shaanxi University of Chinese Medicine, Xianyang 712046, China
belongs to the Schisandracea family. It mainly contains chemical components such as lignans, triterpenes, polysaccharides and volatile oils and is widely used in treatment of hepatitis, liver and kidney transplantation, Alzheimer’s disease, insomnia and other diseases. Modern studies have shown that lignans are the main active components of, with pharmacological effects such as liver protection, antitumor, antivirus, anti-oxidant and neuroprotection. Research progress on lignans and pharmacological activities in plants ofare summarized in this paper, in order to provide references for the research and development and comprehensive application of.
Michx; lignans; dibenzocyclooctadienes lignans;liver protection; antitumor; anti-oxidant
R282.710.5
A
0253 - 2670(2022)06 - 1903 - 16
10.7501/j.issn.0253-2670.2022.06.034
2021-09-18
国家自然科学基金资助项目(82174111);陕西省科技厅自然科学基础研究计划项目(2021JQ-744);陕西省重点研发计划项目(2019ZDLSF04-03-02);陕西中医药大学学科创新团队项目(2019-YL12)
刘媛媛(1996—),女,硕士研究生,研究方向为中草药药效物质基础。E-mail: 763019058@qq.com
王 薇(1972—),女,博士,教授,研究方向为中药药效物质基础及中药炮制。E-mail:2051003@sntcm.edu.cn
张东东(1990—),男,博士,讲师,研究方向为中药药效物质基础。E-mail: zhangnatprod@163.com
[责任编辑 崔艳丽]

