菲并咪唑磺酸(羧酸)衍生物的合成与表征
李秋林,谢鹏,李书纬,乔鹏程,柒鑫,赵冰,2
菲并咪唑磺酸(羧酸)衍生物的合成与表征
李秋林1,谢鹏1,李书纬1,乔鹏程1,柒鑫1,赵冰1,2
(齐齐哈尔大学 1. 化学与化学工程学院,2. 黑龙江省表面活性剂与工业助剂重点实验室,黑龙江 齐齐哈尔 161006)
尽管菲并咪唑衍生物具有优良的光化学性能,但其较差的水溶性在一定程度上限制了其应用范围.将磺酸(羧酸)基团引入到菲并咪唑结构,旨在设计和合成水溶性菲并咪唑衍生物.以9,10-菲醌、乙酸铵、对氨基苯磺酸(甲酸)、苯甲醛为原料,采用“一锅法”将磺酸(羧酸)基团引入到菲并咪唑结构中,合成了菲并咪唑磺酸(羧酸)衍生物.通过优化反应物的物质的量比、催化剂种类和用量、反应溶剂等因素,确定了合成菲并咪唑磺酸(羧酸)衍生物的较佳反应条件,产物收率在75%~89%.采用熔点、红外光谱、核磁氢谱和碳谱对所合成的菲并咪唑磺酸(羧酸)衍生物的结构进行表征和确认.
菲并咪唑;磺酸(羧酸)衍生物;合成;条件优化;结构表征
咪唑类衍生物广泛存在于DNA和蛋白质等物质中,表现出重要的生物活性.而且,咪唑结构中含有2个共振的氮原子,具有特殊共轭结构,使咪唑类化合物兼具酸性和碱性的结构特征,并可以与强碱作用成盐,这些结构特征使咪唑类衍生物在化工产品中间体的生产中起到重要的作用.因此,近年来对于咪唑衍生物的设计、合成及应用受到广大研究者的普遍关注.其中,菲并咪唑是咪唑类衍生物的重要一类,其良好的刚性结构和发光性能被广泛应用于荧光传感领域[1-5].
文献[6]报道了通过硼氟化合物修饰菲并咪唑环上1号位的氮原子,使咪唑环的荧光发射峰由450 nm红移到600 nm,实现了荧光发射光谱的红移及裸眼观测.文献[7]报道了通过亚胺键链接合成了荧光素-菲并咪唑双荧光团的荧光探针分子,并应用于pH的检测.该探针分子通过分子内氢键向去质子化作用的转化过程实现了分子内电子的定向流动,导致了荧光信号的变化.此外,文献[8]报道了菲并咪唑-噻吩的衍生物在有机发光半导体(Organic Electroluminescence Display,OLED)中的应用.文中指出该类菲并咪唑衍生物具有良好的光性能,并且随着电压的增加,器件的电致发光强度增加,并且此类化合物相对于其它发光材料具有更高的光量子产率.在生物领域,咪唑衍生物也表现出有一定性能.近期,文献[9]报道了临床观察甲巯咪唑联合比索洛尔可以通过下调甲状腺激素及糖代谢水平具有显著疗效.文献[10]报道了含肼基基团的Schiff碱类菲并咪唑衍生物的良好抗菌性能.这说明咪唑类衍生物,尤其菲并咪唑衍生物在发光材料和抗菌材料领域具有广阔的应用空间.因此,设计和合成结构多样的菲并咪唑衍生物具有重要的研究意义.
由于菲并咪唑的刚性结构,大部分文献报道菲并咪唑衍生物的水溶性较差,在一定程度上限制了菲并咪唑衍生物的应用范围.因此,本文将磺酸(羧酸)基团引入到菲并咪唑结构中,设计和合成了菲并咪唑磺酸(羧酸)衍生物,旨在提高菲并咪唑衍生物的水溶性,拓展菲并咪唑衍生物的应用领域.
1 实验部分
1.1 仪器与试剂
X-6精细显微熔点测试仪(北京泰克仪器有限公司);Spectrum GX型傅里叶变换红外光谱仪(KBr压片,北京华海恒辉科技有限公司);Bruker AV400/600型超导核磁共振仪(TMS为内标,美国Bruker公司);Vario EL元素分析仪(德国Elementar公司).
9,10-菲醌,取代的苯甲醛,对氨基苯磺酸,对氨基苯甲酸(AR,上海阿拉丁试剂有限公司);乙酸铵,碳酸钠,冰乙酸,乙酸乙酯,石油醚,乙醇(AR,天津市富宇精细化工有限公司).实验中采用的试剂和溶剂均未进行预处理.
1.2 目标产物的合成与表征
1.2.1 菲并咪唑磺酸衍生物的合成 菲并咪唑磺酸衍生物的合成路线见图1.依次将0.624 g 9,10-菲醌(3 mmol)、0.519 g对氨基苯磺酸(3 mmol)、0.94 g乙酸铵(6 mmol)、0.6 mL苯甲醛(6 mmol)加入到三口烧瓶中,再加入0.5 mL冰乙酸为催化剂,25 mL乙醇作为溶剂.搅拌,并将反应混合物加热至回流,反应2 h左右.反应结束后降温,将混合物加入到200 mL的蒸馏水中.采用5%的Na2CO3水溶液调节混合物的pH至7左右,析出大量固体.过滤,滤饼反复用蒸馏水洗涤,得到粗产物.粗产物用乙酸乙酯重结晶得到目标产物4-(2-苯基-[9,10-]-1-菲并咪唑-2-)苯磺酸,收率86%,熔点>300 ℃.IR(KBr,cm-1):3 396,3 014,1 654,1 546,1 458,1 180,1 036,863,754,719;1H NMR(600 MHz,DMSO-6):8.889(,=4.8 Hz,2H,ArH),8.876(,2H,ArH),8.818(,=5.0 Hz,1H,ArH),8.529(,=4.2 Hz,2H,ArH),7.765(,=4.2 Hz,2H,ArH),7.665~7.784(m,2H,ArH),7.401~7.649(m,4H,ArH),7.390(,=5.6 Hz,2H,Ar).
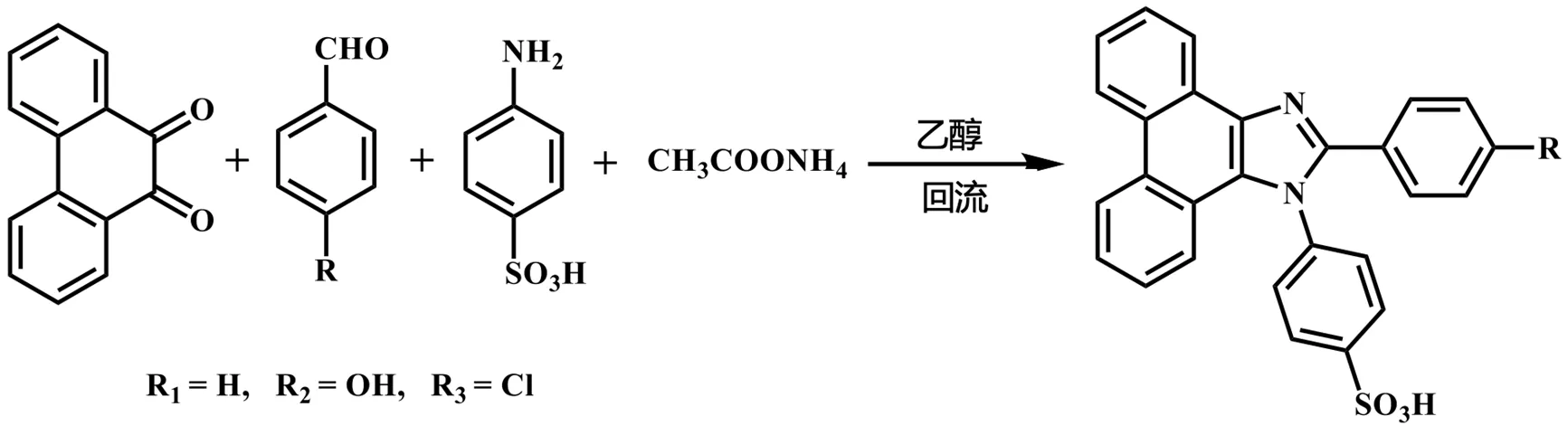
图1 菲并咪唑磺酸衍生物的合成路线
采用0.624 g 9,10-菲醌(3 mmol)、0.519 g对氨基苯磺酸(3 mmol)、0.94 g乙酸铵(6 mmol)、0.732 g对羟基苯甲醛(6 mmol)为原料,合成目标产物4-[2-(4-羟基苯基)-[9,10-]-1-菲并咪唑-2-]苯磺酸,收率89%,熔点>300 ℃.IR(KBr,cm-1):3 375,3 134,1 652,1 608,1 505,1 033,754,722;1H NMR(600 MHz,DMSO-6):10.41(s,1 H,OH),8.836(,=5.4 Hz,2H,ArH),8.718(,=4.8 Hz,2H,ArH),8.299(,=4.8 Hz,2H,ArH),7.759~7.804(m,4H,ArH),7.664(,=4.8 Hz,2H,ArH),7.371(,=4.8 Hz,2H,ArH),7.074(,=5.4 Hz,2H,ArH).
采用0.624 g 9,10-菲醌(3 mmol)、0.519 g对氨基苯磺酸(3 mmol)、0.94 g乙酸铵(6 mmol)、0.842 g对氯苯甲醛(6 mmol)为原料,合成目标产物4-[2-(4-氯苯基)-[9,10-]-1-菲并咪唑-2-]苯磺酸,收率80%,熔点>300 ℃.IR(KBr,cm-1):3 205,1 602,1 557,1 495,1 102,1 021,803,746;1H NMR(600 MHz,DMSO-6):8.892(,=4.8 Hz,2H,ArH),8.675(,=5.0 Hz,2H,ArH),8.346(,=5.0 Hz,2H,ArH),8.529(,=4.2 Hz,2H,ArH),8.315(,=4.5 Hz,2H,ArH),7.665~7.784(m,2H,ArH),7.401~7.649(m,2H,ArH),7.390(,=5.6 Hz,2H,Ar).
1.2.2 菲并咪唑羧酸衍生物的合成 菲并咪唑羧酸衍生物的合成路线见图2.依次将0.624 g 9,10-菲醌(3 mmol)、0.411 g对氨基苯甲酸(3 mmol)、1.024 g乙酸铵(6 mmol)、0.6 mL苯甲醛(6 mmol)加入到三口瓶中,再加入0.5 mL冰乙酸为催化剂,25 mL乙醇作为溶剂.搅拌,加热至回流.反应过程中采用TLC监测跟踪反应情况(展开剂为石油醚∶乙酸乙酯=7∶3),溶液逐渐变浅,反应2 h后,停止反应.将反应混合物倒入烧杯中,并加入200 mL蒸馏水.采用5%的Na2CO3水溶液调节混合物的pH至7左右,有大量固体析出,过滤,滤饼用水洗涤,干燥后得到粗产物.粗产物经乙酸乙酯重结晶后得到目标产物4-(2-苯基-[9,10-]-1-菲并咪唑-1-)苯甲酸,收率75%,熔点>300 ℃.IR(KBr,cm-1):3 588,3 104,1 521,1 486,1 179,775,719;1H NMR(600 MHz,DMSO-6):13.079(s,1H,COOH),8.798(,=4.8 Hz,2H,ArH),8.512(,=4.2 Hz,2H,ArH),8.035(,=4.2 Hz,4H,ArH),7.744~7.780(m,3H,ArH),7.630(,=4.2 Hz,2H,ArH),7.002~7.126(m,4H,ArH).

图2 菲并咪唑羧酸衍生物的合成路线
采用0.624 g 9,10-菲醌(3 mmol)、0.411 g 4-氨基苯甲酸(3 mmol)、1.024 g乙酸铵(6 mmol)、0.732 g对羟基苯甲醛(6 mmol)为原料,合成目标产物4-[2-(4-羟基苯基)-[9,10-]-1-菲并咪唑-1-]苯甲酸,收率80%,熔点>300 ℃.IR(KBr,cm-1):3 609,3 043,1 527,1 475,1 238,1 175,756,724;1H NMR(600 MHz,DMSO-6):13.168(s,1H,COOH),9.916(,=4.2 Hz,1H,OH),8.810(,=4.8 Hz,2H,ArH),8.545(,=4.2 Hz,2H,ArH),8.158(,=4.2 Hz,4H,ArH),7.744(,=4.8 Hz,2H,ArH),7.612(,=4.2 Hz,2H,ArH),6.977~6.992(m,4H,ArH).
采用0.624 g 9,10-菲醌(3 mmol)、0.411 g对氯苯甲酸(3 mmol)、1.024 g乙酸铵(6 mmol)、0.842 g对氯苯甲醛(6 mmol)为原料,合成目标产物4-[2-(4-氯苯基)-[9,10-]-1-菲并咪唑-1-]苯甲酸,收率82%,熔点>300 ℃.IR(KBr,cm-1):3 608,3 343,1 671,1 455,1 175,756,724;1H NMR(600 MHz,DMSO-6):13.073(s,1H,COOH),8.826(,=4.8 Hz,2H,ArH),8.731(,=4.2 Hz,2H,ArH),8.204(,=4.2 Hz,4H,ArH),7.852(,=4.8 Hz,2H,ArH),7.690(,=4.2 Hz,2H,ArH),6.961~6.983(m,4H,ArH).
2 结果与讨论
2.1 菲并咪唑磺酸衍生物的结构表征
采用红外光谱和核磁氢谱对所合成的菲并咪唑磺酸(羧酸)衍生物进行了结构表征.4-(2-苯基-[9,10-]-1-菲并咪唑-2-)苯磺酸的红外光谱见图3a.由图3a可见,在3 396 cm-1出现一个尖峰,可归属为游离羟基O-H的伸缩振动峰,在3 000 cm-1以上存在明显的羟基缔合的宽峰,这些结构说明目标产物中存在游离和缔合的羟基.此外,在1 180,1 036 cm-1处出现强吸收尖峰,可归属为S-O键的伸缩振动.1 654 cm-1处的中强峰为C=N双键的伸缩振动.1 594,1 457 cm-1处的中强峰可归属为苯环的骨架振动.红外光谱的结果初步说明目标产物为菲并咪唑修饰的苯磺酸衍生物.
4-(2-苯基-[9,10-]-1-菲并咪唑-2-)苯磺酸的核磁氢谱见图3b.由图3b可见,所有的质子峰的化学位移均出现在7~9之间,共17个质子(分子式为C27H18N2O3S).核磁氢谱中没有出现苯磺酸羟基O-H氢质子,可能是由于活泼氢被氘代试剂取代的原因.这些结果符合化合物4-(2-苯基-[9,10-]-1-菲并咪唑-2-)苯磺酸的结构特征,说明目标化合物为4-(2-苯基-[9,10-]-1-菲并咪唑-2-)苯磺酸.
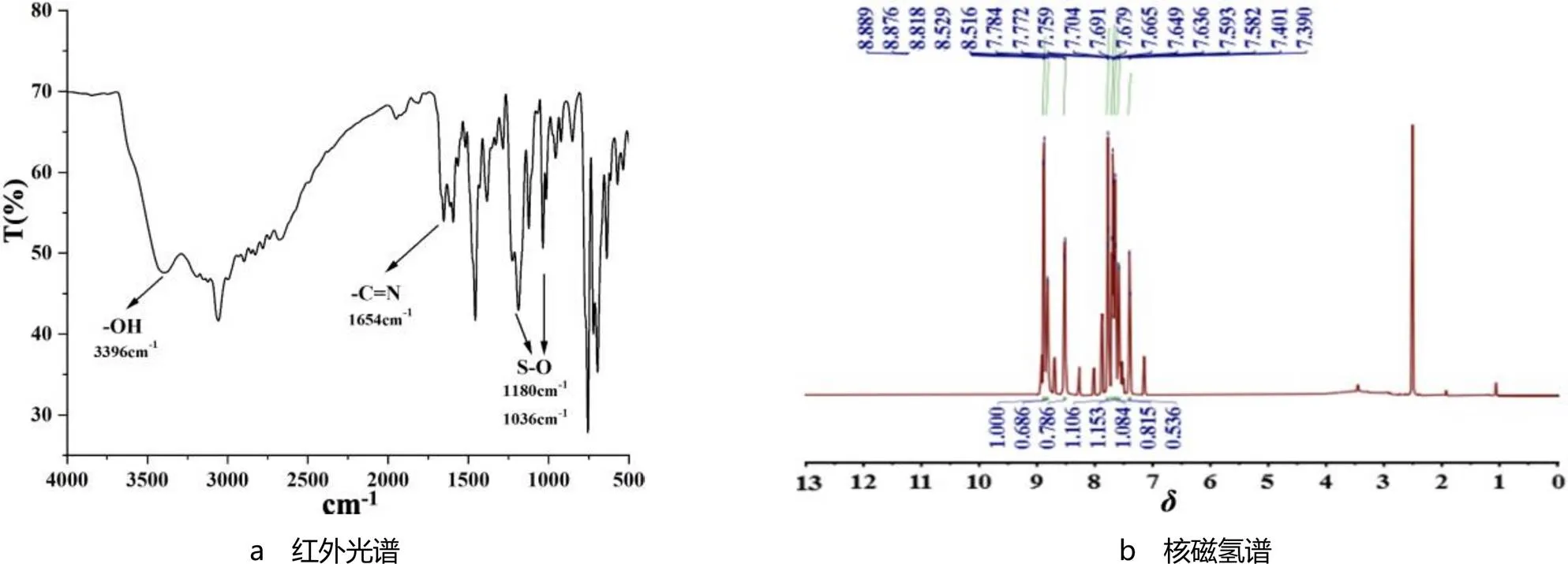
图3 4-(2-苯基-[9,10-d]-1H-菲并咪唑-2-)苯磺酸的红外光谱和核磁氢谱
2.2 菲并咪唑羧酸衍生物的结构表征
4-[2-(4-羟基苯基)-[9,10-]-1-菲并咪唑-1-]苯甲酸的红外光谱和核磁氢谱见图4.由图4a可见,3 609 cm-1处的尖峰为游离羟基O-H的伸缩振动峰,3 000 cm-1的宽峰为羟基缔合峰,1 611 cm-1的强峰为C=N双键的伸缩振动峰,1 237,1 175 cm-1为C-O的伸缩振动.根据红外光谱数据初步判断,该化合物结构为4-[2-(4-羟基苯基)-[9,10-]-1-菲并咪唑-1-]苯甲酸.同样采用核磁氢谱进一步对化合物的结构进行表征和确认(见图4b).由图4b可见,化学位移值为13.23处的质子峰归属为羧酸上的氢质子,化学位移值9.92为羟基O-H氢质子,7~9之间为芳香氢质子.所有氢质子数量和裂分与4-[2-(4-羟基苯基)-[9,10-]-1-菲并咪唑-1-]苯甲酸的结构一致.因此,红外光谱和核磁氢谱数据的结果表明,所合成的化合物为目标产物4-[2-(4-羟基苯基)-[9,10-]-1-菲并咪唑-1-]苯甲酸.

图4 4-[2-(4-羟基苯基)-[9,10-d]-1H-菲并咪唑-1-]苯甲酸的红外光谱和核磁氢谱
2.3 菲并咪唑磺酸(羧酸)衍生物的合成工艺优化
以4-(2-苯基-[9,10-]-1-菲并咪唑-2-)苯磺酸为模型化合物,探讨了反应物的物质的量比、反应时间、反应温度等条件对反应收率的影响.采用9,10-菲醌、对氨基苯磺酸、乙酸铵和苯甲醛为原料,通过“一锅法”四组分偶联反应制备目标产物4-(2-苯基-[9,10-]-1-菲并咪唑-2-)苯磺酸.首先,探讨了4种反应物的物质的量比对反应收率的影响.以无水乙醇为溶剂,加入0.5 mL冰醋酸作为催化剂,回流反应2 h后,反应物的物质的量比对产率的影响见表1.由表1可见,为了保证反应充分进行,反应过程中乙酸铵的用量为9,10-菲醌的2倍.当对氨基苯磺酸和苯甲醛用量与9,10-菲醌相同时,产物收率为65%;只提高对氨基苯磺酸的用量,产物的收率没有发生明显变化,为67%;只提高苯甲醛用量时,产物的收率明显上升,为85%;对氨基苯磺酸和苯甲醛用量同时增加时,产物收率与只提高苯甲醛用量时没有明显变化,为86%.结果表明,苯甲醛用量对反应产率的影响较大.适量增加苯甲醛用量有利于提高产物的收率.原因可能是因为苯甲醛挥发性较强,随着反应的进行,反应体系中有效的苯甲醛浓度逐渐减少,如果投料量过少,无法保证其反应充分进行.因此,后续合成菲并咪唑磺酸(羧酸)衍生物的过程中采用9,10-菲醌、乙酸铵、对氨基苯磺酸、苯甲醛的物质的量比为1∶2∶1∶2.

表1 反应物的物质的量比对产率的影响
在确定了反应物的物质的量比的基础上,进一步讨论了反应中催化剂种类和用量对反应的影响.9,10-菲醌、乙酸铵、对氨基苯磺酸、苯甲醛的物质的量比为1∶2∶1∶2,以无水乙醇为溶剂,回流反应2 h后,不同催化剂种类和用量对产物收率的影响见表2.由表2可见,反应不加催化剂时,反应10 h后,产物的收率仅为25%.加入质子酸(浓盐酸和浓硫酸)时,反应收率有所增加;以冰醋酸为溶剂时,反应2 h后,收率即可达到85%;改用三氟乙酸和对甲苯磺酸时,反应收率均不理想.由此可见,采用冰醋酸为催化剂时反应收率较高,即冰醋酸更能有效促进反应进行.质子酸、三氟乙酸、对甲苯磺酸均不能达到理想的催化效果.因此,后续反应采用冰醋酸为催化剂.
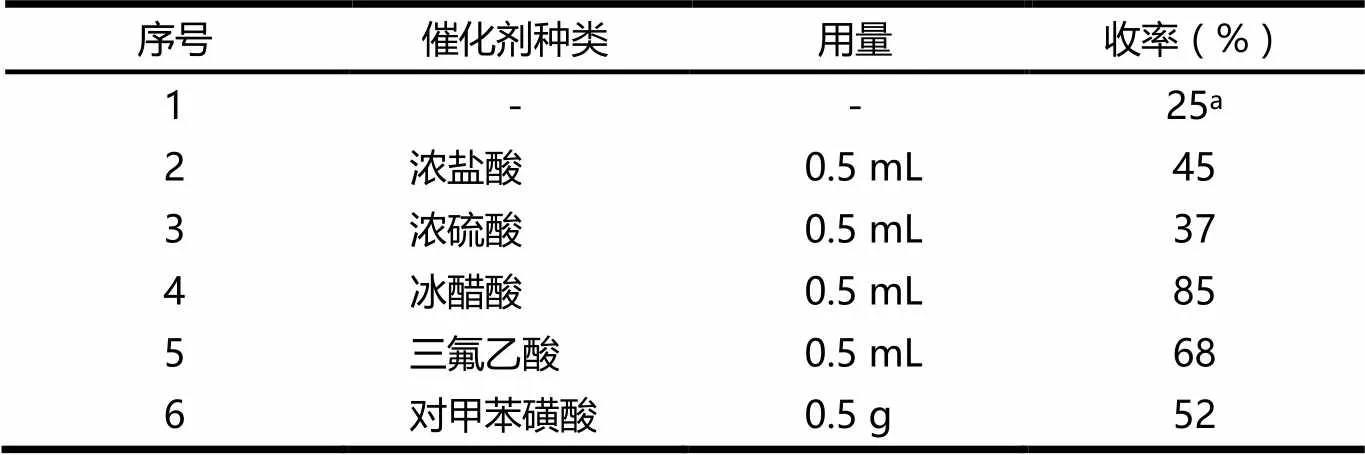
表2 不同催化剂种类和用量对产率的影响
注:a为反应时间10 h.
在上述结果的基础上,9,10-菲醌、乙酸铵、对氨基苯磺酸、苯甲醛的物质的量比为1∶2∶1∶2,以冰醋酸为催化剂,对反应溶剂的选择进行了优化,分别采用甲醇、乙醇、冰乙酸、N,N-二甲基甲酰胺和四氢呋喃为溶剂,回流条件下,反应结果见表3.由表3可见,采用甲醇为溶剂反应2 h,通过TLC观察几乎未见到有产物生成;继续延长反应时间至10 h,TLC上发现少量产物点,原因可能是由于反应温度较低,无法提供反应所需的热量.采用乙醇为溶剂时,反应2 h时分离产率为85%;延长反应时间(4 h),产率没有显著增加.采用冰乙酸为溶剂时,分离产率为72%,收率适中.以N,N-二甲基甲酰胺和四氢呋喃为溶剂时,反应均能进行,但产率较低.在冰乙酸、N,N-二甲基甲酰胺和四氢呋喃中反应时,虽然反应能够进行,但是后处理过程需要加水处理,产物损失严重,对产物的收率影响较大.

表3 不同反应溶剂比对收率的影响
综上,通过优化反应条件,确定了合成4-(2-苯基-[9,10-]-1-菲并咪唑-2-)苯磺酸的较佳反应条件应为:9,10-菲醌、乙酸铵、对氨基苯磺酸、苯甲醛的物质的量比为1∶2∶1∶2,冰醋酸为催化剂,在乙醇为溶剂的条件下,反应2 h时,产物的分离产率为85%.4-[2-(4-羟基苯基)-[9,10-]-1-菲并咪唑-2-]苯磺酸、4-[2-(4-氯苯基)-[9,10-]-1-菲并咪唑-2-]苯磺酸、4-(2-苯基-[9,10-]-1-菲并咪唑-1-)苯甲酸、4-[2-(4-羟基苯基)-[9,10-]-1-菲并咪唑-1-]苯甲酸、4-[2-(4-氯苯基)-[9,10-]-1-菲并咪唑-1-]苯甲酸均参考上述条件合成,产率在75%~89%之间.说明该反应条件对菲并咪唑磺酸(羧酸)衍生物的合成具有一定的普遍性.
3 结语
采用9,10菲醌、乙酸铵、对氨基苯磺酸和取代苯甲醛为原料,“一锅法”合成了3个菲并咪唑磺酸衍生物;采用9,10菲醌、乙酸铵、对氨基苯甲酸和取代苯胺为原料,“一锅法”合成了3个菲并咪唑羧酸衍生物.通过优化模型反应的物质的量比、催化剂种类和用量、反应溶剂等因素,确定了合成菲并咪唑磺酸(羧酸)衍生物的较佳反应条件为,9,10-菲醌、乙酸铵、对氨基苯磺酸、苯甲醛的物质的量比为1∶2∶1∶2,冰醋酸为催化剂,乙醇为溶剂,产物产率在75%~89%之间.通过熔点、红外光谱、核磁氢谱和碳谱对所合成的6个菲并咪唑磺酸(羧酸)衍生物的结构进行了表征,确认了合成的化合物为目标产物.通过本文的研究,为设计和合成水溶性菲并咪唑衍生物提供了新的思路和方法.
[1] Huang W,Lin J,Chien C,et al.Highly phosphorescent biscyclometalated iridium complexes containing benzoimidazolebased ligands[J].Chemistry of materials,2004,16(12):2480-2488.
[2] Matsumoto S,Abe H,Akazome M,et al.Fluorescence of Diimidazol[1,2–a:2′,1′-c]quinoxalinium Salts Under Various Conditions[J].The Journal of organic chemistry,2013,78(6):2397-2404.
[3] Liu S,Wu S.New watersoluble highly selective fluorescent chemosensor for Fe(III)ions and its application to living cell imaging[J].Sensors and Actuators B:Chemical,2012(171-172):1110-1116.
[4] Ji S,Meng X,Ye W,et al.A rhodaminebased“turnon”fluorescent probe for Fe3+in aqueous solution[J].Dalton Trans,2014,43(4):1583-1588.
[5] Zhu J,Zhang Y,Wang M,et al.A Fluorescent Iron Ion(Ⅲ)Probe Based on Diphenyl Ketonebased Schiff Base[J].FINE CHEMICALS,2016,12(33):1321-1326.
[6] Li W,Lin W,Wang J,et al.Phenanthro[9,10-d]imidazole-quinoline Boron Difluoride Dyes with Solid-State Red Fluorescence[J].Org Lett,2013,15(7):1768-1771.
[7] Li S,Kan W,Zhao B,et al.A fluorescent pH probe for an aqueous solution composed of 7-hydroxycoumarin,Schiff base and phenanthro[9,10-d]imidazole moieties(PICO)[J].Heterocyclic Communications,2018,24(2):93-97.
[8] Kulaa S,Szlapa-Kula A,Kotowicz S,et al.Phenanthro[9,10-d]imidazole with thiophene rings toward OLEDs application[J].Dyes and Pigments,2018,159:646-654.
[9] 耿坡,张劲草,张鹤,等.甲巯咪唑联合比索洛尔治疗甲状腺功能亢进症的效果及其对甲状腺激素和糖脂代谢的影响研究[J].临床合理用药,2021,9(14):114-116.
[10] Slassi S,Aarjane M,Yamni K,et al.Synthesis,crystal structure,DFT calculations,Hirshfeld surfaces,and antibacterial activities of schiff base based on imidazole[J].Journal of Molecular Structure,2019,1197:547-554.
Synthesis and characterization of sulfonic acid(carboxylic acid)derivatives based on phenanthroimidazole
LI Qiulin1,XIE Peng1,LI Shuwei1,QIAO Pengcheng1,QI Xin1,ZHAO Bing1,2
(1. School of Chemistry and Chemical Engineering,2. Heilongjiang Provincial Key Laboratory of Surface Active Agent and Auxiliary,Qiqihar University,Qiqihar 161006,China)
Although phenanthroimidazole derivatives have manifested excellent optical properties,most of their solubility in water were relatively poor which restrained their applications in the many fields.The sulfonic and carboxylic groups were functionally introduced into the moiety of phenanthroimidazole in order to design,synthesize and improve the solubility of phenanthroimidazole derivatives.Sulfonic acid and carboxylic acid derivatives based on phenanthroimidazole were synthesized by the“one-pot”reaction of 9,10-phenanthraquinone,ammonium acetate,-aminobenzene sulfonic acid(carboxylic acid) and benzaldehyde through the introduction of sulfonic and carboxylic groups.The optimized reaction conditions were obtained by the adjustment of the quantity ratio of raw materials,the type and amount of catalyst,and solvents with the moderate yield from 75% to 89%.The structures for synthesized sulfonic acid(carboxylic acid)derivatives based on phenanthroimidazole were characterized and determined by the method of melting point,IR,1H and13C NMR.
phenanthroimidazole;sulfonic and carboxylic acid derivatives;synthesis;optimization;structural characterization
O69
A
10.3969/j.issn.1007-9831.2022.02.009
1007-9831(2022)02-0047-06
2021-10-29
黑龙江省大学生创新创业训练计划项目(202010232004)
李秋林(1999-),女,四川绵阳人,在读本科生.E-mail:1685953216@qq.com
赵冰(1977-),女,辽宁辽阳人,教授,博士,从事荧光探针的合成及性能研究.E-mail:zhao_submit@aliyun.com

