阿帕替尼联合替莫唑胺在复发高级别胶质瘤治疗中的应用效果
许柯炎 矫阳 王俊宽 刘学友 孙红卫 罗文正 赵海彪
郑州大学第一附属医院神经外科 郑州 450052
胶质瘤是一种高度恶性的脑肿瘤,亦是脑肿瘤患者死亡的主要原因[1]。几乎所有患者都会在手术切除、放疗和化疗后因为肿瘤的耐药性及侵袭性出现复发[2],并且复发后的预后更差。理想的治疗方案是最大限度手术切除肿瘤,然后辅助放化疗。但是部分高级别复发胶质瘤患者并不适用于手术治疗,因此急需建立新的治疗策略。其中阿帕替尼联合替莫唑胺治疗复发性肿瘤是一个较新的治疗方案,但关于其对放化疗后复发高级别胶质瘤的治疗效果均为散在报道[3]。本研究通过对阿帕替尼联合替莫唑胺在复发高级别胶质瘤治疗中的应用效果进行探讨,旨在为临床对复发胶质瘤患者的诊治积累经验。
1 资料与方法
1.1一般资料回顾性分析2016-01—2020-09我院神经外科收治的79例术后复发高级别胶质瘤患者的临床资料。均给予阿帕替尼联合替莫唑胺治疗。纳入标准:(1)年龄15~70岁,健康状况(KPS)评分≥70分。(2)原发胶质瘤已全部切除,病理结果证实为高级别胶质瘤(WHO Ⅲ~Ⅳ级),术后初期根据STUPP方案进行放化疗。(3)MRS和PWI显示肿瘤复发信号。(4)由资深神经外科医师评估患者无法耐受再次手术,或患者拒绝二次手术治疗。(5)除甘露醇和皮质激素外,未接受控制脑水肿的其他治疗。排除标准:(1)骨髓造血功能、肾功能及肝功能不全。(2)依从性差或不足以完成化疗联合靶向药的治疗。(3)复发前接受过抗血管生成药物治疗。(4)除原发胶质瘤外存在其他部位肿瘤。男51例,女28例;年龄(46.13±15.21)岁(范围:15~70岁)。WHOⅢ级20例,Ⅳ级59例。端脑复发70例,其他部位9例。研究方案经郑州大学第一附属医院伦理委员会批准;知情同意书从患者的法定监护人或患者本人处获得。
1.2治疗方案阿帕替尼起始剂量500 mg/d,如果患者出现≥3级药物相关不良事件,则将剂量改为250 mg/d。替莫唑胺以100 mg/m2/d(服用7d,休息7d)的剂量服用,周期为14 d。
1.3评估指标由资深神经外科医生对患者服药前后相关状态进行评估(MRI、体检、精神状态、常见毒性)。MRI检查中,以T1增强像测量肿瘤体积,以T2像测量水肿宽度,使用多田公式计算具体数值。以患者治疗前最新MRI影像为基线,以RANO标准评估肿瘤水肿宽度、肿瘤体积。使用KPS评估健康状况,简易精神量表(MMSE)评估精神状态。常见毒性通过不良事件通用术语标准(CTCAE)5.0版评估。无进展生存期(PFS)定义为从登记到病情进展或死亡的时间,以先到者为准,或报告患者没有疾病进展的最后随访日期。总生存期(OS)定义为从开始服药到死亡的时间,或患者报告存活的最后随访日期。

2 结果
2.1近期疗效按照阿帕替尼联合替莫唑胺方案治疗4周后,完全缓解(CR)0例(0.00%),23例(29.11%)部分缓解(PR),46例(58.23%)肿瘤稳定(SD),10例(12.66%)肿瘤有进展(PD)。23例(29.11%)客观缓解(ORR),66例(83.54%)肿瘤控制(DCR)。患者典型治疗影像见图1。治疗后水肿宽度、肿瘤体积、KPS评分、MMSE评分较治疗前显著改善,差异均有统计学意义。见表1。
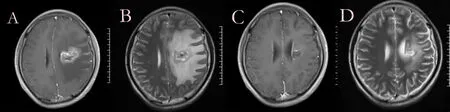
注:A.治疗前T1增强像 B.治疗前T2像 C.治疗4周后T1增强像 D.治疗4周后T2像
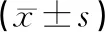
表1 服药前后的近期疗效比较
2.2远期疗效患者6个月无进展生存率为36.8%,12个月总生存率为19.8%,中位无进展生存时间为4.9(95%CI 3.91~5.89)个月。复发后中位生存时间为6.4(95%CI 5.34~7.46)个月。
2.3药物相关不良反应药物相关不良反应主要为高血压、手足综合征、白细胞减少等,见表2。其中10例因出现药物不良反应减药,其他患者通过对症和支持治疗后不良反应得以控制。

表2 药物相关不良反应事件(例)
3 讨论
目前对于复发高级别胶质瘤尚没有标准的治疗策略[4]。临床多选用替莫唑胺的剂量密集方案治疗不能耐受二次手术,或拒绝二次手术的复发高级别胶质瘤患者。但替莫唑胺的治疗效果多与患者的MGMT启动子甲基化、1p/19q缺失状态,以及IDH-1突变状态相关联,且远期疗效较差[5]。
新血管是为肿瘤提供营养和氧气的途径,抑制血管生成可以抑制肿瘤生长、发展和转移。有研究发现,通过抑制血管内皮生长因子(VEGF)和血管内皮生长因子受体(VEGFR)的结合来阻止下游通路的激活,从而限制肿瘤的生长[6]。阿帕替尼是一种新型的小分子选择性血管内皮生长因子受体-2(VEGFR-2)酪氨酸激酶抑制剂,可抑制VEGFR-2的激活,以阻断VECG,介导信号转导,并抑制血管生成以控制肿瘤生长。相关文献资料亦显示[7],其在恶性胶质瘤患者治疗中显示出积极作用。
贝伐珠单抗(BEV)是治疗复发性胶质母细胞瘤最广泛使用的抗血管生成药物,但相关研究显示,贝伐珠单抗治疗失败后肿瘤浸润性会增强,易引发肿瘤颅内播散转移[8]。且阿帕替尼可通过细胞内自分泌VEGF信号促进肿瘤细胞凋亡,而贝伐珠单抗不能。此外,阿帕替尼可通过抑制多种ABC转运蛋白的功能来逆转多药耐药性。
胶质瘤的组织学特征表现为VEGF的过度表达引起显著的微血管增生和血脑屏障破坏,最终导致复发肿瘤周围严重水肿[9],这是导致患者肢体运动障碍、神经认知功能下降,以及死亡的重要原因[10]。本研究结果显示,阿帕替尼联合替莫唑胺可在减小肿瘤体积的同时减少瘤周水肿的宽度,推测阿帕替尼可能在影响肿瘤生长的同时,减少肿瘤的占位效应和水肿;同时通过改善血管通透性和减少糖皮质激素依赖性,以获得更好的脱水治疗效果。临床观察发现,部分胶质瘤患者肿瘤体积不大,但瘤周水肿更为严重,容易导致颅内压升高和严重的神经损伤。因此,减少脑水肿有利于改善患者的神经功能。与相同或更大尺寸的缓慢生长病变相比,水肿迅速增加的快速生长病变可能导致剩余的功能性脑组织没有更多的时间适应,从而产生更快的神经认知功能下降和更严重的神经功能缺损。因此,阿帕替尼对这些患者的影响更为显著。
与既往单用替莫唑胺的研究比较[11],联合用药研究显示了相对满意的结果。但值得注意的是,靶向治疗的增加并未显示任何生存结果改善的迹象,可能与本次研究纳入患者病情进展后使用的治疗方案及IDH突变状态、MGMT甲基化状态等与既往研究不同有关,因此患者的生存获益与剂量密集方案治疗复发高级别胶质瘤无明显差异,更多的相关因素等待更一步的前瞻性研究去完善。与既往研究相比[12],本研究结果显示阿帕替尼联合替莫唑胺的药物不良反应事件略高于替莫唑胺的剂量密集方案。主要差异表现在患者的蛋白尿、手足综合征、高血压和贫血发生频率。
本研究是回顾性设计,病情较重的患者存在放弃治疗的可能性,故存在一定的局限性和选择偏倚。此外,阿帕替尼的最佳给药方案尚不清楚,低剂量阿帕替尼可能仍然是一个有吸引力的治疗方案,需在今后进一步开展前瞻性研究,以分析阿帕替尼联合替莫唑胺治疗复发高级别胶质瘤患者的影响因素。
综上所述,阿帕替尼联合替莫唑胺治疗复发高级别胶质瘤患者的效果优于单独使用替莫唑胺,且安全性较高,不良反应患者容易耐受。具有临床参考应用价值及进一步研究的意义。

