高校实验动物中心动物质量控制研究与创新实践
张志妮 ,杨力衡 ,严 楚 ,蔡卫斌∗
(1.中山大学实验动物中心,广州 510006;2.广州市白云区畜牧兽医站,广州 510550)
实验动物作为“活的精密仪器”,是生命科学研究中必须具备的四大基本条件之一,涉及疾病机制研究、治疗方法研究、疫苗研究与评价等多个领域。截止至2019 年7 月,在过去30 年里,涉及实验动物论文中,PubMed 论文数据库论文154 万篇,占生物医学论文的79%,药学尤其是毒理、安全性评价论文 占85%,Nature、Science、Cell、Nature Medicine、Nature Genetics、Nature Cell Biology、Nature Biotechnology、Jouranl of Experimental Medicine 等国际一流学术杂志有22 万篇、占77%,而我国在2013~2015 年间则有32844 篇、占7%,从1901~2018 年的81 年度(占颁奖年度的75%)诺贝尔生理学或医学奖涉及25 种动物,被应用了168 次[1]。
实验动物质量直接关系着研究和评价数据的准确性、可靠性和可重复性,动物感染烈性传染病后极易集体死亡、实验中断,且携带人畜共患传染病菌动物不仅威胁实验人员健康,一旦扩散还将产生严重的公共卫生安全。如实验室源性感染事件有2019 年某研究所布鲁氏菌感染、2011 年某高校教学山羊布氏杆菌感染[2],实验动物获得性病原感染事件有2006 年某高校流行性出血热感染[3]、2004年实验室人员感染流行性出血热[4]、20 世纪末全国各地实验大鼠和工作人员流行性出血热高阳性率[5]等。
高校实验动物中心,为集教学、科研及生产三位一体的公共服务性平台,支撑了学校及附属医院的医学、药学、生命科学、化工、农学、材料等多学科教学和科研的重要技术服务。随着新技术、新研究方法的不断发展,基因修饰动物亦被作为重要、常用的研究对象,多从不同国家、研究机构引入。动物来源复杂,高校科研多学科、多方向,实验类型复杂,实验时间不确定性,学生为主体的实验人员流量大、流动性强等等,均易造成病原菌的传入、交叉感染和传播扩散[6]。本研究旨在总结和探讨近年来的病原控制制度和检测工作成效和心得。
1 建立了病原控制制度
建立并执行了《实验动物准入制度》,从制度方面加强实验动物来源管理和质量控制,规范实验动物进入动物设施。具体措施如下。
1.1 规范动物来源
切断传染源,是传染病控制最有效措施,安全、可靠的动物来源,是实验动物病原控制的源头和关键。据监测病原检出率将动物来源分等级:一级(最高级):即至少连续暗检3 次,病原检测均为阴性的生产设施动物来源;二级:不满足一级、三~五级来源的生产设施动物来源;三级:自检、暗检、抽检和常规检疫中出现非人蓄共患病病原、非动物烈性传染病病原、一般为条件致病菌阳性的生产设施动物来源,动物退出设施,6 个月内不接收相同来源动物;四级:动物烈性传染病病原阳性的生产设施动物来源,1 年内禁止该来源动物进入设施;五级:人蓄共患病病原阳性的生产设施动物来源,按国家相关法规法律处理。
进入动物设施的常规动物(含突变系),需提供实验动物质量合格证明,销售清单、送货单/签收单、近3~6 个月内的实验动物质量检测报告(包含实验动物国家标准要求的相应等级单位病原检测项目,结果均为合格),境外来源需提供来源机构的兽医报告(标明病原检测项目及结果)和海关认可的入关隔离检疫场所隔离检疫报告;基因修饰动物原则上均需通过生物净化(一般是经典的剖宫产代乳净化技术或体外受精及胚胎移植技术)达SPF级,或达国标清洁级+SPF 级必须检测和必要时检测病原检测合格(以下称“活检”) 的相关证明材料[7-9]。
1.2 动物实验设施功能分区和检疫管理
高校动物中心可能因历史原因、不同校区的需求、转基因动物繁育保种、科研多学科和多方向、实验类型和来源复杂、学生流动性大等情况,动物设施分布于不同校区、不同楼宇,可按功能进行分区并执行针对性管理措施:
1.2.1 屏障环境繁育区
繁育区使用于基因修饰动物的保种繁育,不涉及动物实验。进入该区的基因修饰动物必须执行生物净化或活检(动物不适用于活检时,可用同笼饲养至少30 d 以上的哨兵动物活检替代);进入该区的野生型动物,一级来源的常规动物(含突变系)需经检测证实监测病原为阴性(监测病原项目详见表1,每年综合检测成本、病原菌的致病性、对常见动物实验的干扰程度及过往检测数据,及时持续更新监测病原谱。);二级来源动物则执行活检。其余情况执行“1.1 规范动物来源”的内容。
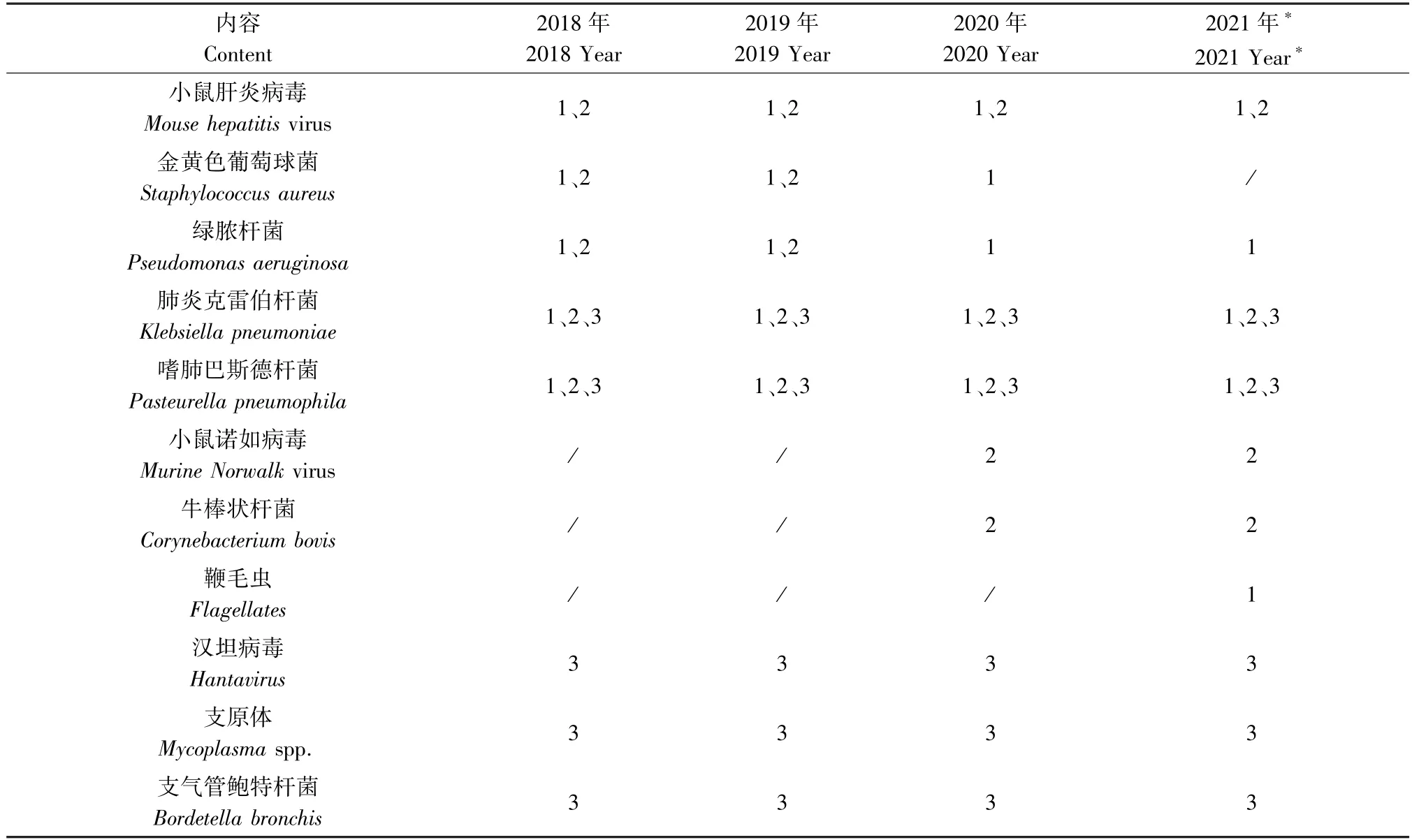
表1 2018~2021 年大、小鼠监测病原谱Table 1 Objective monitoring pathogen genealogy of rat and mouse form 2018 to 2021
1.2.2 屏障环境实验区
该区仅开展动物实验,禁止繁殖。执行“边检疫、边实验、重防范”原则,动物进入该区前,一级来源动物需经检疫期的健康观察;二级来源动物经检测证实监测病原为阴性。其余情况执行“1.1 规范动物来源”的内容。
1.2.3 普通环境实验区
该区仅开展动物实验,禁止繁殖。进入该区的动物需经检疫期的健康观察。其余情况执行“1.1规范动物来源”的内容。
1.2.4 暂养区
该区执行屏障设施的硬件及管理要求,仅用于动物经影像检测、手术、行为学观察或其他屏障外操作后,需短期饲养、但又无法返回屏障设施的情况,管理人员严格把控实验动物的饲养规模和周期。
1.3 在养动物的病原监测
1.3.1 病原监测
繁殖区采用哨兵动物监测(脏垫料法)[10-12],监测现行国标清洁级+SPF 级病原,增添国内外流行且对动物实验影响较大的病原,如小鼠诺如病毒、牛棒状杆菌等,据监测结果,提供快速预警从而控制病原微生物感染和扩散,并为检疫期监测病原谱的更新提供数据支持;其他区域主要执行个性化的兽医护理[13]。
1.3.2 兽医护理
在兽医指导、培训下,每位饲养工作人员、设施管理人员执行日常兽医护理、巡房工作,观察动物日常健康状况,发现异常动物及时上报兽医,经检测诊断后执行相应的防控、处理措施。兽医则对设施进行定期的巡视检查、兽医护理工作现场指导、病原控制和动物福利措施的落实情况监督等[13]。
1.4 实验动物的“点对点”运输
1.4.1 动物进入设施
因动物来源复杂、实验者流动性大等情况,动物的运输除符合国标要求外[9],执行“点对点”动物转运管理制度,即实验者联系供应商订购动物后,供应商与待进入设施的管理人员执行实验动物交接,实验者与设施工作人员将动物接收入设施内。
1.4.2 动物离开设施
屏障设施内待移出的动物,应满足包装规范、保障生存环境、有专用通道、不被周围人群直视等要求,用专用包装盒,在屏障设施内包装后方可移出,普通环境移出的动物,需于运输笼具上覆盖透气遮布[9]。
1.5 动物相关用品的监测
应根据国标要求,需定期监测的项目可有:设施环境技术因子、动物相关用品如动物饮用水和垫料、高压炉的灭菌效果和饲料等[9,14]。
2 病原检测工作
2018 年以来,在检测了1481 批次非活体检实验动物样本中,包括动物粪便、皮肤拭子、鼻咽拭子、血清、毛发等,有106 批次病原阳性,其中的15批小鼠肝炎病毒(Mousehepatitisvirus,MHV)阳性小鼠立即撤场,动物执行安乐死后经高压灭菌器灭菌,动物尸体装入专用尸体袋存放于尸体冷藏柜,集中作无害化处理。检疫饲养区域处理如下:管制进出,封闭送风、排风口;使用杀灭病原菌浓度的消毒 液(如 0.13~ 0.26 mol/L 过氧乙酸按0.008 L/m3)对饲养空间、角落、缝隙和物品表面进行喷雾消毒,密封24 h 后,开启送风、排风口;移出的动物笼具、相关物品及废弃物等先行高压灭菌或杀灭病原菌浓度消毒液浸泡消毒后,执行实验废弃物相关规定处理;管制进出至少3 个月,重新启用前,封闭送风、排风口执行区域净化处理,空气洁净度和落下菌数合格后方可投入使用。同时,严密监控饲养区域的其他动物,并一年内禁止同来源的实验动物进入;检测了395 份活体动物样本,其中38例病原阳性,检疫期病原检测阳性动物均立即退出了设施。非活体动物样本的监测病原阳性批次比例至2021 年达17.72%,说明动物入场前的病原监测是非常必要的。活体检测的阳性率自2019 年出现下降,则主要是部分基因修饰动物执行了生物净化。具体情况详见表2。

表2 2018~2021 年病原检测Table 2 Pathogen detection form 2018 to 2021
从动物来源方面看,2018 年监测的动物来源有12 家,2021 年已达27 家,呈逐年上升趋势,动物来源愈趋复杂、多样,动物质量良莠不齐,但总体质量水平有所提高。详见表3。

表3 2018~2021 年供应单位来源Table 3 Supply units form 2018 to 2021
3 讨论
在上述实验动物的病原检测和质量控制过程中,我们发现病原监测是保障实验动物质量的有效防线。首先,能有效地切断传染源,通过设施的功能分区,不同功能区域执行了不同的检疫制管理度、监测病原谱的及时更新、动物相关用品等的定期检测,杜绝了携带阳性病原的动物和动物用品的进入,使得设施规避了污染风险;检疫期严密监控小鼠肝炎病毒,将数批阳性动物排除在设施之外,哨兵动物的检测结果也证实了此举的必要性;鞭毛虫为阳性检出率较高的寄生虫之一,而检疫期的检测排除、哨兵动物的监测、在养动物的粪便排查和抽查工作,也是控制该寄生虫的有效措施;动物饮用水的定期无菌检测、高压炉灭菌效果和环境技术因子的定期监测,为设施的水机和高压炉使用效果是否合格、维护措施是否得当、日常消毒管理工作是否到位等做出客观的数据支持。其次,阳性病原的检出,为设施消除了病原传播隐患,中心曾在老旧设施的动物粪便中,检出MHV、鞭毛虫阳性,尔后返回至其饲养区域进行合并样本排查,发现阳性后,对阳性样本的覆盖区域的课题组信息梳理、归类后,进行课题组合并样本检测或单笼检测,均发现病原阳性动物集中于某一课题组、甚至于同一品系,经综合分析后考虑,病原为课题组违规操作携带进入设施所致。随之进行的全面排查、定点抽查和哨兵动物监测结果均提示,该病原阳性动物转入设施的时间较短,发现及时,均未造成扩散传播。可见有效的病原检测措施,在阻止病原于设施内的传播隐患方面效果显著。
随着时代的发展,各领域基础研究突飞猛进,产业发展异常迅猛,各学科交叉融合,国内实验设施呈井喷状建设,实验动物需求量更是暴增,高校实验动物中心作为重要的基础性支撑服务平台,保障实验动物质量和生物安全防控是平台核心工作,通过有效的病原控制、优质的科研服务,以期为学校“双一流”建设和国家相关学科领域发展做出更大的贡献。

