基于基因毒性和对单抗聚集影响的聚山梨酯中醛限度的控制
王 珏,江 颖,肖新月,杨 锐,孙会敏*,涂家生
(1中国食品药品检定研究院,国家药品监督管理局药用辅料质量研究与评价重点实验室,北京 100050;2上海市医疗器械化妆品审评核查中心,上海 200020);3中国药科大学,国家药品监督管理局药物制剂及辅料研究与评价重点实验室,南京 210009;
在药用辅料中,甲醛和乙醛通常是经降解产生的小分子杂质,尤其在聚氧乙烯类或包含聚氧乙烯链段的药用辅料(如聚山梨酯20、聚山梨酯80等)中可能存在,其降解途径如图1 所示[1]。甲醛和乙醛分别被世界卫生组织国际肿瘤研究机构(International Agency for Research on Cancer,World Health Organization,WHO IARC)列为致癌物和可能致癌物。按照《人用药品注册技术国际协调会议指南:诱变性杂质的评估和控制》(ICH M7)要求,二者属于基因毒性杂质,因此无论在制剂还是辅料中均需要将其控制在可接受限度以下。
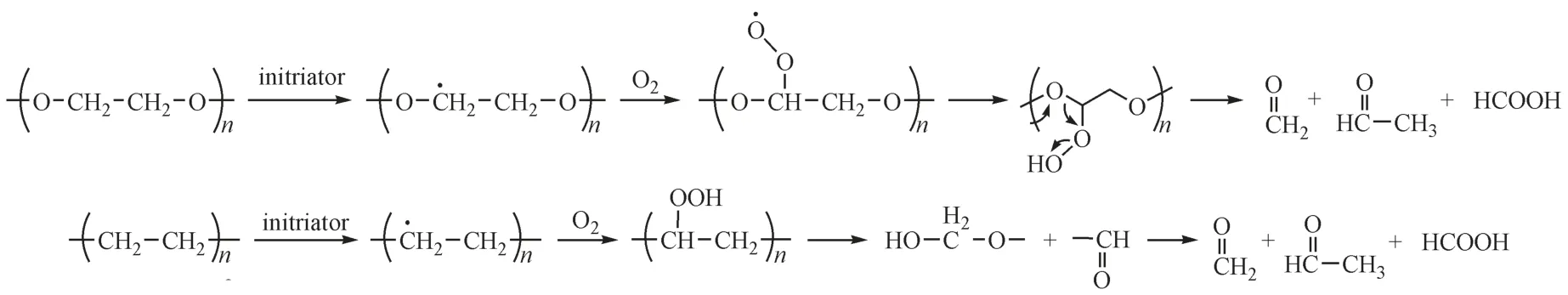
Figure 1 Schematic diagram of aldehyde generation in polysorbates
聚山梨酯80 和聚山梨酯20 作为生物制品中常用的稳定剂,通过竞争机制或分子伴侣机制[2-5]保护蛋白分子在整个生命周期中的稳定性。但其降解产生的醛类小分子不仅会带来安全性风险,而且由于具有较强的反应活性还会对蛋白药物稳定性造成影响。以甲醛为例,它可以与蛋白质分子中的氨基或亚胺基等基团发生亲核加成反应,经偶联邻近的伯胺,使蛋白质分子之间通过共价键而交联,即Mannich 反应。这种反应有可能导致蛋白质聚集体的形成。
然而,目前各国药典聚山梨酯80 和聚山梨酯20 标准中均没有对醛类检查作出相关要求。本研究参考ICH M7 的相关要求,对蛋白制剂用聚山梨酯80 和聚山梨酯20 中甲醛和乙醛的杂质限度进行了合理估算,同时结合甲醛和乙醛对阿达木单抗稳定性的影响对控制限度的制订提出了建议。采用已建立的聚山梨酯80 和聚山梨酯20 中甲醛和乙醛含量测定的HPLC 柱前衍生化法并进行了优化[6-8],运用该方法对市售的多个厂家、多个批次及多个应用级别的聚山梨酯80 和聚山梨酯20 样品进行测定,发现市售产品有部分批次甲醛和乙醛超出了建议限度。
1 材 料
1. 1 样品与试剂
聚山梨酯80 分别购自英国禾大Croda 公司、Ewnik 公司、南京威尔有限公司、江苏保易有限公司、Sigma-Aldrich 公司、日本NOF 公司和上海弘顺生物科技有限公司。聚山梨酯20分别购自南京威尔有限公司、国药集团化学试剂有限公司、J. T.Baker 公司、化夏试剂有限公司和上海一基实业有限公司。阿达木单抗注射液(规格:0. 8 mL:40 mg,国内某制药公司);PBS 缓冲液[赛默飞世尔科技(中国)有限公司];甲醛(中国计量科学研究院,BW3450,9. 67 mg/mL);乙醛(阿拉丁生化科技股份有限公司);甲醛2,4-二硝基苯腙(甲醛-DNPH,默克化工有限公司);乙醛2,4-二硝基苯腙(乙醛-DNPH,德国Dr. Ehrenstorfer GmbH 公司);2,4-二硝基苯肼(上海麦克林生化科技有限公司,98%,HPLC级);盐酸为市售分析纯;乙腈为色谱纯。
1. 2 仪 器
Agilen1260 高效液相色谱仪[安捷伦科技(中国)有限公司]。
2 方法与结果
2. 1 样品中甲醛和乙醛的含量测定
2. 1. 1 溶液配制及衍生化
(1)2,4-二硝基苯肼的纯化 称取2,4-二硝基苯肼4 g,置于烧瓶中,加乙腈200 mL,混匀,于90 ℃水浴中加热30 min,趁热过滤至锥形瓶中。滤液自然冷却后用布氏漏斗抽滤,用乙腈冲洗剩余晶体即得纯化后的2,4-二硝基苯肼。如空白干扰仍可检出,需重复该纯化过程。
(2)衍生化试剂的配制 取纯化后的2,4-二硝基苯肼0. 25 g,精密称定,置于50 mL 量瓶中,加乙腈40 mL,完全混匀后再加入浓盐酸3 mL,超声至完全溶解,用乙腈稀释至刻度,将溶液转移至棕色瓶中,临用新制。
(3)对照品储备液的配制 取甲醛-DNPH 和乙醛-DNPH 适量,精密称定,加乙腈溶解并定量稀释成每毫升约含30 μg 的甲醛-DNPH 对照品储备液和每1 mL 约含200 μg 的乙醛-DNPH 对照品储备液。
(4)供试品溶液的配制 取样品0. 5 g,精密称定,置于10 mL 量瓶中,加乙腈1 mL 溶解样品,再加入衍生化试剂2 mL,混匀。在黑暗处于室温下衍生化30 min 后,加乙腈稀释至刻度,即得供试品溶液。
2. 1. 2 高效液相色谱条件 色谱柱:CAPCELL PAK DD-C8柱(4. 6 mm × 150 mm,5 μm);进样量:20 μL;流动相:A(水)-B(乙腈),流速:1. 0 mL/min;检测波长:360 nm;柱温:30 ℃。流动相梯度:0 ~ 11 min:65% A ~ 20% A;11 ~ 15 min:80% B ~100% B;15 ~ 16 min:100% B ~ 35% B。
2. 1. 3 衍生化反应效率的测定 精密称取甲醛和乙醛对照品适量,用乙腈稀释,分别配制成50 μg/mL 的甲醛对照品溶液和乙醛对照品溶液,各取1 mL 于10 mL 量瓶中,按供试品溶液的配制同法处理,照下式分别计算甲醛和乙醛的反应效率:甲醛反应效率=m甲醛-DNPH/(210 × 50) × 30 ×100%;乙醛反应效率=m乙醛-DNPH/(224 × 50) × 44 ×100%。
其中,m甲醛-DNPH和m乙醛-DNPH分别为样品中甲醛-DNPH和乙醛-DNPH的检出量(μg)。
结果表明,在该反应条件下,甲醛和乙醛的衍生化反应效率分别为100%和98%。
2. 1. 4 线性标准溶液的配制 取甲醛-DNPH 对照品储备液和乙醛-DNPH 对照品储备液用乙腈稀释为每毫升含甲醛-DNPH 分别为0. 15,3,10,20,24,30 μg,含乙醛-DNPH 分别为1,5,60,80,150,200 μg的溶液作为线性标准溶液。
2. 1. 5 测定结果 精密量取线性标准溶液20 μL注入液相色谱仪中,记录色谱图,以浓度与对应峰面积计算回归方程;另精密量取供试品溶液20 μL注入液相色谱仪中,记录色谱图,代入回归方程,并按公式(1)和公式(2)计算供试品中甲醛和乙醛的含量。
采用上述方法对来自8 个厂家共20 批聚山梨酯80 样品、5 个厂家共11 批聚山梨酯20 样品中的甲醛和乙醛进行测定,结果如表1 和表2 所示。本文隐去厂家名称并用大写字母表示,用数字代替批号。级别表示厂家标明的普通级或注射级、未精制或精制、低纯度或中等纯度原料合成产品。结果表明,不同厂家的聚山梨酯80 和聚山梨酯20在甲醛或乙醛含量上存在较大差异,同一厂家不同批次的含量也有所不同;注射级别的产品并不意味着醛类含量低,甚至精制后的产品表现出了较高的乙醛含量(>600 μg/g)。然而精制加工可能有利于聚山梨酯80中的甲醛含量保持在较低水平(<3 μg/g);而较高的原料纯度有可能产生较高含量的甲醛。以上结果提示,原料纯度、精制或提纯工艺与聚山梨酯80 或聚山梨酯20 的含醛量有关,控制醛含量对保证产品质量稳定来说具有重要意义。
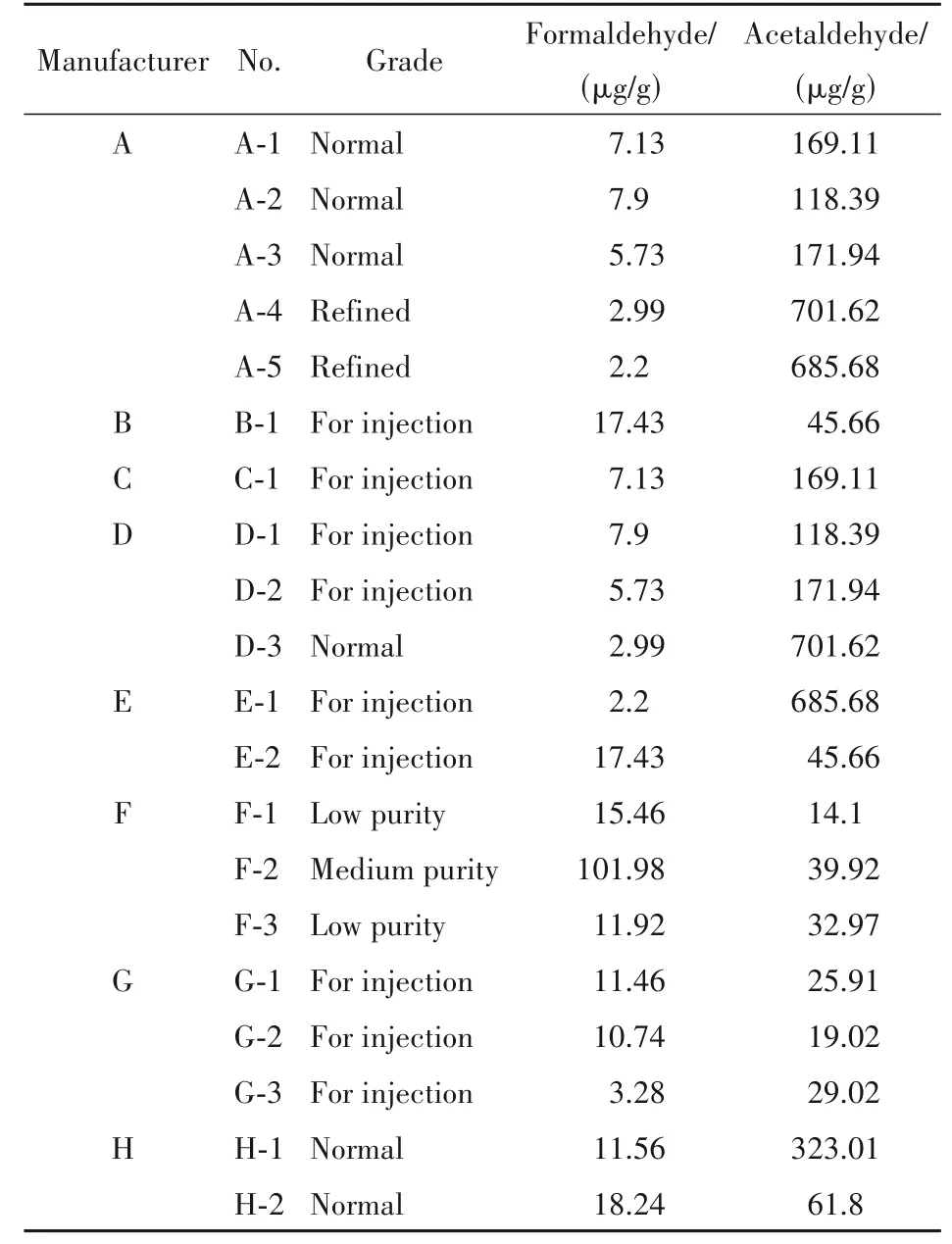
Table 1 Assay of formaldehyde and acetaldehyde in different batches of polysorbate 80 determined by HPLC
2. 2 方法学验证
2. 2. 1 精密度 精密量取3 μg/mL 甲醛-DNPH 对照品溶液和10 μg/mL 乙醛-DNPH 对照品溶液各20 μL,连续进样6 次,记录色谱图,以峰面积计算RSD。结果表明,甲醛-DNPH 和乙醛-DNPH 峰面积的RSD 分别为0. 8% 和0. 9%,均小于2%,表明仪器进样精密度良好。
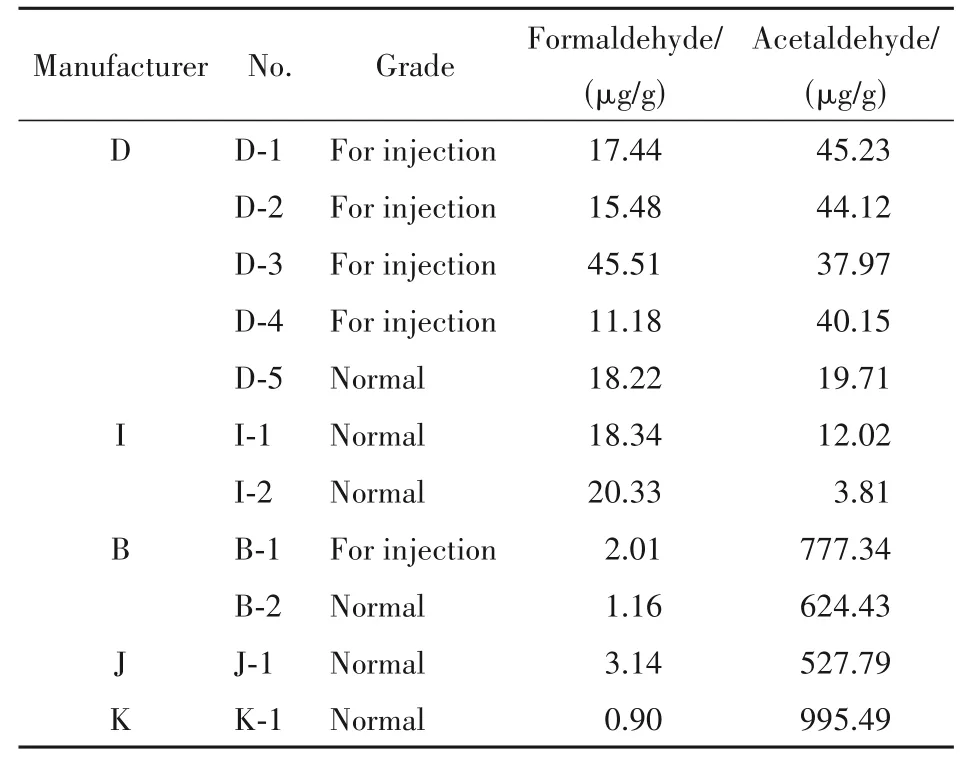
Table 2 Assay of formaldehyde and acetaldehyde in different batches of polysorbate 20 determined by HPLC
2. 2. 2 检出限和定量限 将甲醛-DNPH 和乙醛-DNPH 对照溶液逐级稀释,精密量取各溶液20 μL注入液相色谱仪,以信噪比S/N = 3 对应的溶液浓度作为检出限,S/N = 10 对应的溶液浓度作为定量限。结果表明,甲醛-DNPH 和乙醛-DNPH 的检出限均为0. 005 μg/mL,定量限均为0. 01 μg/mL。
2. 2. 3 线性和范围 分别取甲醛-DNPH 对照品储备液和乙醛-DNPH 对照品储备液,用乙腈稀释为每毫升含甲醛-DNPH 分别为0. 15,3,10,20,24,30 μg,含乙醛-DNPH 分别为1,5,60,80,150,200 μg 的溶液作为系列对照品溶液。精密量取上述对照品溶液20 μL注入高效液相色谱仪中,记录色谱图,以对照品溶液浓度(c,μg/mL)与对应的峰面积(A)进行线性回归,得到甲醛-DNPH 和乙醛-DNPH线性回归方程分别为A= 101. 33c- 1. 244 3(r=0. 999 9),A= 99. 799c+ 65. 509(r= 0. 998 7)。结果表明甲醛-DNPH 在0. 14 ~ 28. 65 μg/mL,乙醛-DNPH在0. 99 ~ 198. 45 μg/mL范围内线性良好。
2. 2. 4 日内精密度 精密量取3 μg/mL 甲醛-DNPH 对照品溶液和10 μg/mL 乙醛-DNPH 对照品溶液各20 μL,分别于0,6,12,24 h 各进样1 次,记录色谱图,以峰面积计算RSD。结果表明,甲醛-DNPH 和乙醛-DNPH 4 次进样峰面积的RSD 分别为1. 39% 和1. 22%,均小于2. 0%,表明日内精密度良好。
2. 2. 5 日间精密度 精密量取3 μg/mL 甲醛-DNPH 对照品溶液和10 μg/mL 乙醛-DNPH 对照品溶液各20 μL,分别于1,2,3,4,5,6 d 各进样1 次,记录色谱图,以峰面积计算RSD。结果表明,甲醛-DNPH 和乙醛-DNPH 6 次进样峰面积的RSD 分别为1. 10% 和0. 81%,均小于2. 0%,表明日间精密度良好。
2. 2. 6 准确度 取已知甲醛和乙醛含量的聚山梨酯80 样品,分别精密加入甲醛6,9,12 μg,乙醛20,25,30 μg,按“2. 1. 1”项方法处理,制成低、中、高3 个浓度的加样回收率测定溶液,每个浓度各3份,按“2. 1. 2”项中色谱条件测定,用外标法以峰面积计算加样回收率,甲醛和乙醛的平均回收率分别为108. 8% 和98. 4%,RSD 分别为3. 7% 和3. 3%。根据《中华人民共和国药典》(2020 年版)四部通则9101 中回收率限度的相关规定,表明本法准确度良好。
2. 3 甲醛和乙醛对阿达木单抗聚集的影响考察
2. 3. 1 共孵育处理 用PBS 配制甲醛和乙醛母液,分别加入到5 mg/mL 经PBS 稀释的阿达木单抗注射液中,使终浓度分别为0,0. 6,6 和60 μg/g。分别在4 ℃和40 ℃条件下静置孵育,于2,4,7 d 时将溶液直接进样,用分子排阻色谱法(size exclu⁃sion chromatography,SEC)测定阿达木单抗的聚集体含量。
2. 3. 2 分子排阻色谱法(SEC)测定 色谱柱:Mab⁃Pac SEC-1(300 Å,7. 8 mm× 300 mm,5 μm);进样量:20 μL;流动相:A:磷酸盐缓冲液(50 mmol/L,pH = 6. 8),B:水(300 mmol/L NaCl),A∶B = 1∶1 等度洗脱;流速:0. 8 mL/min;紫外检测器波长:360 nm;柱温:30 ℃,运行时间:20 min。
精密量取“2. 3. 1”项共孵育处理后的溶液20 μL 注入液相色谱仪,记录色谱图,分别对聚集体和单体色谱峰积分,按照面积归一化法计算聚集体含量。
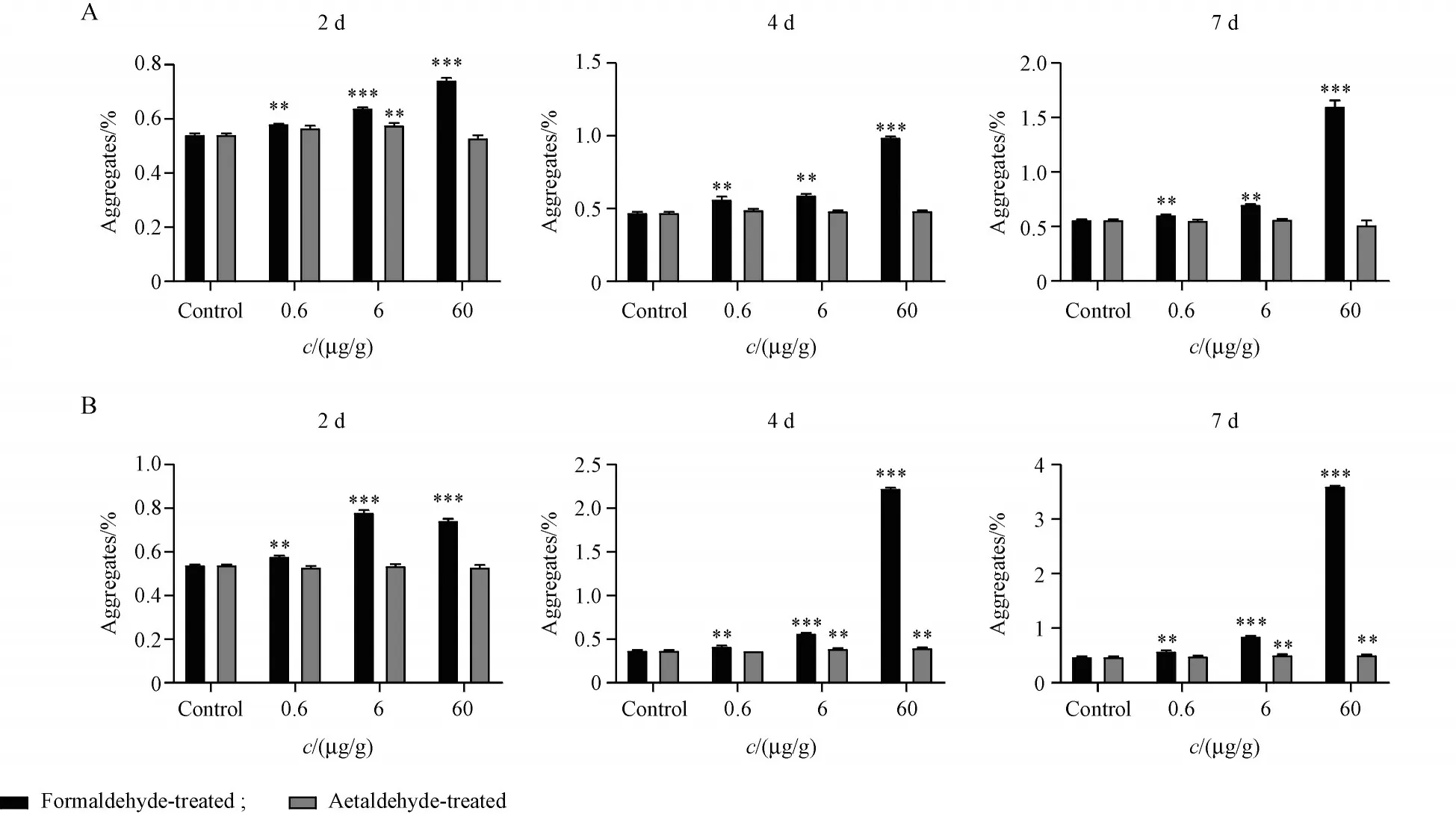
Figure 2 Aggregate assay of adalimumab treated by formaldehyde or acetaldehyde respectively at 4 °C (A) and 40 °C (B) using size exclusion chro⁃matography (SEC) (±s, n = 3)
2. 4 阿达木单抗聚集体含量监测
分别在0. 6,6,60 μg/g 3个浓度条件下、于4 ℃和40 ℃考察了甲醛和乙醛对阿达木单抗聚集的影响。如图2 所示,结果表明,甲醛对阿达木单抗的聚集作用更为显著。甲醛对阿达木单抗的聚集作用具有浓度依赖和温度依赖性,在相同温度下,高浓度(60 μg/g)甲醛相较于中、低浓度(6 μg/g 和0. 6 μg/g)更易导致阿达木单抗聚集;同时,提高温度也可促进甲醛对单抗的聚集诱导作用,即甲醛在4 ℃条件下,4 d 内即可引起1% 以上的单抗聚集,而在40 ℃条件下放置4 d 即可引起2% 以上的阿达木单抗聚集。乙醛对阿达木单抗的聚集效果不论在4 ℃还是40 ℃条件下与对照组相比差异均不十分显著,且浓度增大后也并未对阿达木单抗显示出明显的聚集效应。分子排阻色谱法测定阿达木单抗聚集体的典型色谱图见图3。
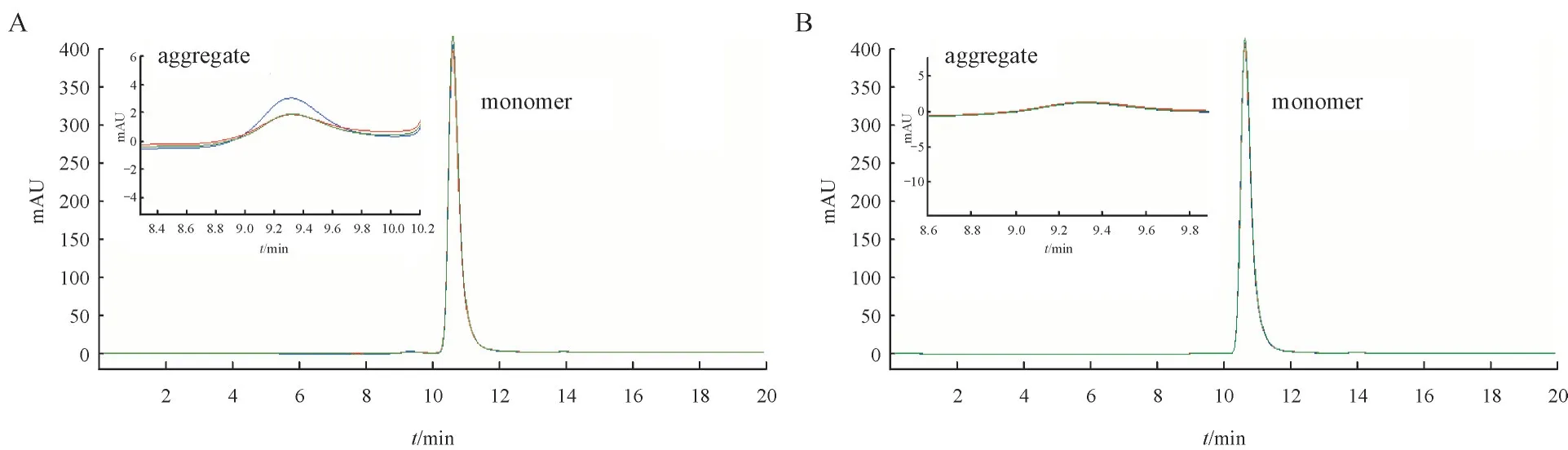
Figure 3 Typical SEC chromatogram of adalimumab respectively treated by formaldehyde (A) and acetaldehyde (B)
3 讨 论
由辅料聚山梨酯80 和聚山梨酯20 引入的甲醛和乙醛杂质不仅经人体摄入时存在安全性风险,而且会对蛋白类药物的稳定性造成影响。本研究采用两种方法对蛋白制剂中聚山梨酯80和聚山梨酯20的甲醛、乙醛含量限度进行了评估。
参考美国非活性物质数据库(IIG)注射剂中聚山梨酯80 和聚山梨酯20 的处方使用量分别为0. 000 2 ~ 0. 585 g/mL 和0. 01 ~ 0. 02 g/mL,将0. 02 g/mL 作为常用处方用量;以国家药品监督管理局网站公布的市售单抗注射液(11 个品规)的规格为参考,将每日给药量10 mL 作为每日摄入体积,按照美国食品药品管理局(FDA)和欧洲药品管理局(EMA)规定的毒理学关注阈值(TTc):长期用药时,潜在毒性杂质每日摄入量不能超过1. 5 μg/d。因此计算得出甲醛和乙醛的限度(估算)均为7. 5 μg/g。另外,按照ICH M7 的要求,采用基于化合物特异性风险评估的可接受摄入量可计算可摄入量(AI)。 根据CPDB(Carcinogenic Potency Database)数据库所报道的甲醛TD50:1. 35 mg/(kg·d)(大鼠)和乙醛TD50:153 mg/(kg·d)(大鼠),得到聚山梨酯80 和聚山梨酯20 中甲醛和乙醛限度(估算)分别为6. 75 和765 μg/g。需要说明的是,以上仅是本研究从杂质安全性评估的角度对注射用单抗制剂中聚山梨酯80和聚山梨酯20的甲醛和乙醛含量限度的粗略估算,是否准确、全面和合理仍有待更进一步的毒理学风险评估。
结合本研究中甲醛和乙醛对阿达木单抗稳定性的实验结果,当甲醛浓度为60 μg/g 时已经可以对单抗聚集产生很大影响,而6 μg/g时对单抗聚集的影响并不显著,因此可以推断,按照以上过程估算得出的甲醛杂质限度(约7 μg/g)条件下对保证单抗稳定性是有利的。而乙醛在本研究实验条件下对阿达木单抗的聚集效应并不显著,因此限度设定应首先考虑其安全性。
此外,在本研究中为了说明小分子杂质对单抗稳定性的影响,给制定单抗中聚山梨酯80和聚山梨酯20中醛类小分子检查提供依据,本研究只关注了两个杂质本身对阿达木单抗稳定性的影响,而未对辅料本身对单抗聚集的直接作用作出考察,将在以后的研究中进一步完善。
4 结 论
本研究不仅建立了适用于聚山梨酯80和聚山梨酯20 中甲醛和乙醛微量杂质检测的HPLC 柱前衍生化检测方法,而且从基因毒性杂质控制和对生物制剂稳定性影响两方面综合考量,初步得出二者的控制限度,并根据实测多批次样品的甲醛乙醛残留量,对辅料质量进行总体评价,对其中甲醛和乙醛限度控制策略进行建议,为辅料质量标准的提高提供了理论支撑。

