CT血管造影在延期DIEP皮瓣乳房重建术中的应用研究
徐 华,刘 莺,张 亦,王庭亮,王 涛,何金光,罗 杰,董莉萍,王海蓉,董佳生,徐元兵,2
1.上海交通大学医学院附属第九人民医院整复外科,上海 200011;
2.武汉科技大学附属孝感医院甲状腺乳腺外科,湖北 孝感 432100
乳腺癌发病率在女性恶性肿瘤中居首位,其中,欧美国家发病率最高,但近年来中国乳腺癌发病率也呈现上升趋势[1]。随着早期筛查普及和治疗手段多样化,乳腺癌患者的预后已得到极大改善。在肿瘤安全的前提下,乳房重建手术应用越来越广泛,乳腺癌术后即刻或延期重建手术较前明显增加。目前,国内数据显示,乳房全切术后约10.7%的患者选择重建手术,其中30%为自体皮瓣乳房重建[2]。而在自体乳房重建中,由于较低的供区并发症和较大的腹部外形改善,腹壁下动脉穿支(deep inferior epigastric perforator,DIEP)皮瓣已成为自体乳房重建的金标准[3]。尽管DIEP皮瓣修复目前已成为常规手术,但腹壁下动脉穿支的解剖变异很大,皮瓣穿支选择仍然具有较高的挑战性[4]。彩色多普勒超声是最早用于DIEP术前皮瓣穿支评估的检查手段,但由于其主观性强、耗时、术前穿支评估假阳性率高以及缺乏局部解剖细节等因素,一定程度上限制了其应用[5]。截止目前,CT血管造影(computed tomography angiography,CTA)检查已成为DIEP手术前必不可少的评估手段[3,6]。CTA较彩色多普勒超声检查能提供更加详细的术前解剖信息,可以更好地进行术前皮瓣优势穿支的选择,明确穿支血管管径、肌肉内走行特点及穿出点位置,整体评估穿支血管的特点,从而有效地指导手术过程[7]。
本研究纳入上海交通大学医学院附属第九人民医院近5年来行延期DIEP乳房重建手术患者298例,以2018年1月为时间节点,通过对比分析,探讨CTA技术在延期DIEP皮瓣乳腺癌术后乳房重建中的应用价值。
1 资料和方法
1.1 一般资料
选取2016年1月—2021年1月于上海交通大学医学院附属第九人民医院就诊拟行延期DIEP皮瓣乳腺癌术后乳房重建手术的298例患者的临床资料。患者均为女性,年龄为25~67岁,平均年龄(42.20±8.28)岁。所有患者均诊断为乳房恶性肿瘤,经肿瘤规范化治疗后,疾病处于稳定期内接受重建手术治疗。其中2016年1月—2018年1月收集的92例患者设定为对照组(US组),术前以彩色多普勒超声检查评估腹部血管穿支(超声仪器为GE Logiq 700,探头频率为10~13 MHz,彩色多普勒频率为7.5 MHz,彩标最高值通常为2 cm/s),超声检查的重点为探测目标穿支血管穿出深筋膜进入皮下脂肪层的精确位置.然后在该穿出点的体表投影处进行标记。2018年1月—2021年1月收集206例患者为观察组(CTA组),术前以CTA检查评估腹部穿支血管,CTA检查仪器为荷兰Philips公司生产的Brilliance 256i CT。造影过程:在手背静脉或肘前静脉通过静脉团注的方式.应用单筒高压注射器,以4 mL/s的速度注入非离子型碘造影剂(安射力350)90~100 mL。利用造影剂示踪剂术触发扫描。CTA参数:120 kVp,250 mA,探测器128 mm×0.625 mm,螺距0.977,512×512 矩阵,350 mm 视野。将CTA数据DICOM文件导入HOROS软件进行处理,分析、定位穿支血管位置、走行等特征,并将穿支的定位标记于患者体表。两组病例资料进行术前基线资料比较,纳入指标包括:年龄、体重指数(body mass index,BMI)、基础疾病史(术前合并原发性高血压史或糖尿病病史)、肿瘤化疗史、胸壁放疗史、腹部手术史、吸烟史及皮瓣血供方式(单/双蒂)。同时对两组病例术中、术后评估指标进行统计学分析。纳入术中评估的指标包括:术前定位穿支数量、术中采用穿支数量、决策穿支时间、穿支解剖时间、供区皮瓣获取时间、皮瓣总重量、总手术时间。术后评估指标包括:腹部切口感染率、脂肪坏死率、二次手术探查率、皮瓣完全坏死率。本研究经过本医院伦理委员会审核通过。
1.2 手术方法
①术前1天患者进行US/CTA检查,US组直接在彩色多普勒超声引导下行穿支血管体表标记;CTA组于CT室进行CT血管造影检查,手术医师自行拷贝DICOM文件,导入术者手机或电脑HOROS软件中,通过影像学成像处理系统计算优势穿支,并以脐平面为中心计算选择优势穿支的位置,进行体表标识。② 术前依据患者健侧乳房形态,重塑患侧乳房下皱襞、内外侧分离区域,进行体表标记画线。③手术时,患者仰卧位,先处理胸壁瘢痕组织,分离胸部皮瓣腔隙。常规切除第3肋软骨,显露胸廓内血管作为受区血管。④ 供区准备:按DIEP皮瓣乳房重建手术常规游离腹部皮瓣,在靠近标记处穿支部位,调低电刀功率,以脐为中心重新测量并于前鞘表面标识目标穿支血管,小心解剖分离,获取DIEP皮瓣。上下分别游离腹壁组织,腹壁整形,脐孔重建,腹部伤口闭合。⑤ 显微血管吻合、乳房重建:解剖分离预留受区动脉和静脉,远端结扎,近端血管夹阻断,修剪胸廓内血管断端。将皮瓣移至乳房缺损处临时固定,修剪腹壁下动静脉。以9-0 或 10-0 prolene血管缝合线进行显微镜下血管吻合,检查吻合口通畅性。皮瓣血运建立后,塑造乳房外形。
1.3 术后处理
所有患者术后常规采取折刀位制动5~7 d,留置导尿管3 d,鼓励术后早期进食,加强皮瓣护理。术后常规给予抗感染、抗痉挛、补液及保温等对症支持治疗。术后严密观察皮瓣的颜色、皮纹、质地、皮温及毛细血管反应来监测皮瓣血运情况,一旦发生血管危象,及时对症处理,必要时手术探查。胸部及腹部负压引流保持引流通畅,观察负压引流的量、性状和颜色,待引流量小于20 mL/d时拔除引流管。
1.4 统计学处理
2 结果
2.1 两组人群术前基线资料比较
298例延期DIEP皮瓣乳房重建手术中,总体皮瓣存活率99.33%(296/298),两组人群在年龄、BMI、基础疾病史、肿瘤化疗史、胸壁放疗史、腹部手术史、吸烟史及皮瓣血供(单/双蒂)方面的差异均无统计学意义(P>0.05,表1)。
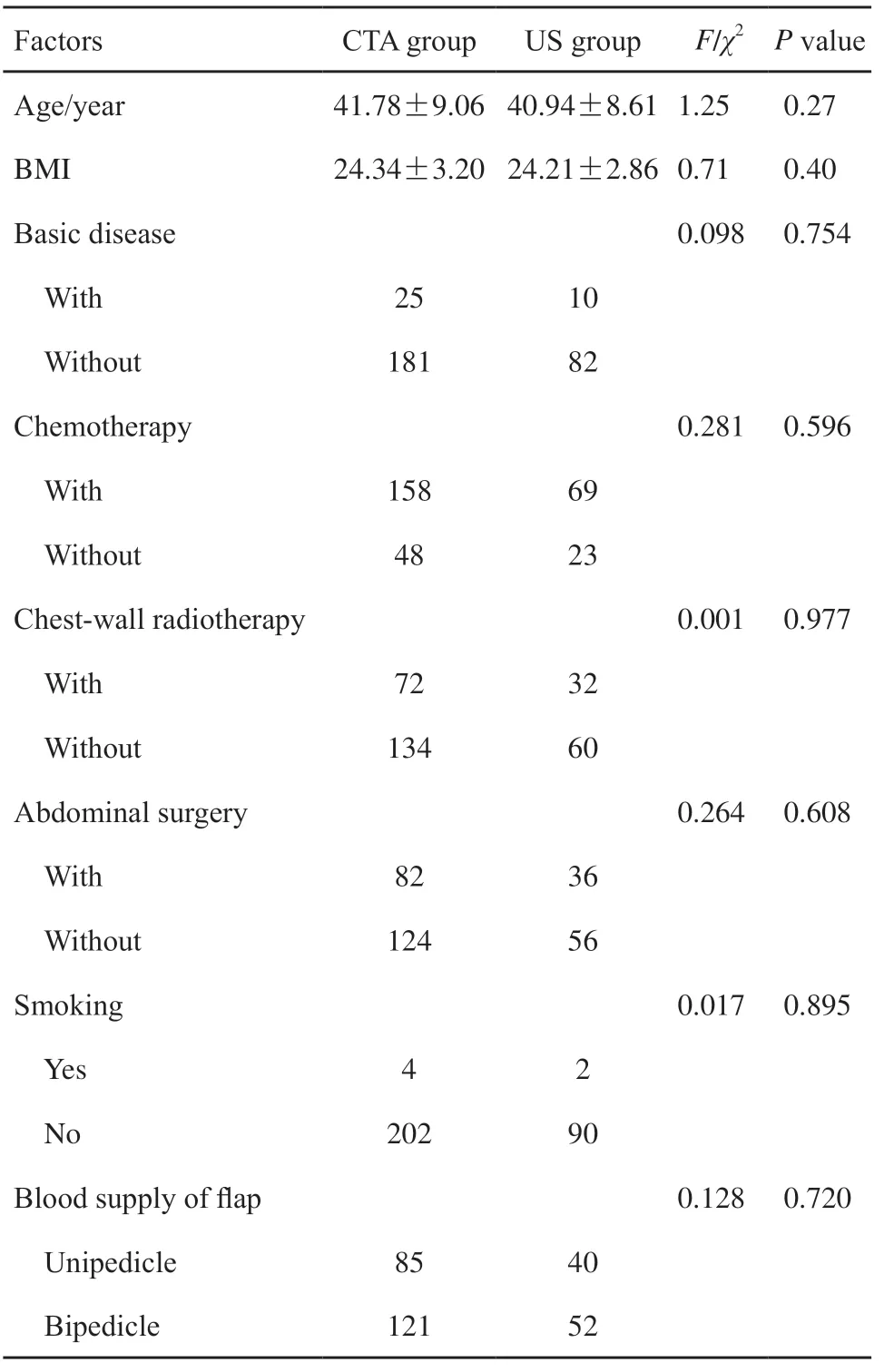
表1 两组人群基线资料比较Tab.1 Comparison of baseline data between two groups
2.2 两组病例的术中、术后结局指标比较
观察组中,术前定位穿支数量为(2.90±1.13)支,对照组为(3.21±1.46)支,两者比较差异有统计学意义(P<0.05)。但两组病例在术中最终采用的穿支数量比较中差异无统计学意义(P=0.342)。在穿支决策时间及穿支解剖时间中,观察组短于对照组(P<0.001,表2)。观察组中供区皮瓣获取时间为(50.05±10.94)min,对照组为(84.8±15.44)min,观察组皮瓣获取时间更短,差异有统计学意义(P<0.001)。在总手术时间比较中,两组差异无统计学意义(P=0.809,图1)。在获取皮瓣总重量中,观察组为(730.62±127.31)g,对照组为(718.25±129.36)g,两者相比差异无统计学意义(P>0.05)。两组术后并发症的比较中,腹部切口感染率、脂肪坏死率、皮瓣完全坏死率差异无统计学意义(P均>0.05)。二次手术探查率比较中,CTA组低于US组(P<0.001,图2)。

图1 术中重点指标比较Fig.1 Comparison of key intraoperative indicators

表2 两组病例术中、术后指标比较Tab.2 Comparison of intraoperative and postoperative indicators between two groups
2.3 两组病例按照是否伴有腹部手术史进行分层比较
按照是否有腹部手术史进行分层比较。将实验数据分为4组:①CTA+无腹部手术组(non-abdominal surgery,NAS);② CTA+腹部手术组(abdominal surgery,AS);③US+NAS;④ US+AS。结果显示,无论CTA组或US组,有腹部手术史患者皮瓣切取时间和总手术时间均增加(P<0.05),对于有腹部手术史患者CTA组的皮瓣切取时间及总手术时间均低于US组(P<0.05)。对于无腹部手术史患者,CTA组皮瓣切取时间低于US组(P<0.05)。总手术时间比较差异无统计学意义(P>0.05,表3)。

表3 两组病例按照腹部手术史进行分层比较Tab.3 Stratification analysis according to the history of abdominal surgery between two groups
2.4 影像手术一致率分析
观察组206个皮瓣中,200个皮瓣术中穿支选择与CTA相关,影像手术一致率为97.09%,对照组92个皮瓣中,40个皮瓣术中穿支选择与US相关,影像手术一致率为43.48%,差异有统计学意义(P<0.001,表4)。

表4 两组病例影像手术一致率比较Tab.4 Comparison of the consistency rate of imaging surgery between two groups
2.5 典型病例
患者女性,65岁,因“左乳癌术后10年,左侧乳房缺损”入院,入院专科查体:胸部:左乳癌术后改变,左侧乳房缺如,左侧胸壁可见一长约15.0 cm×1.0 cm手术瘢痕,愈合情况良好,无皮肤破溃、结节等异常。右侧乳房轻度下垂,其内未及明显异常结节,双侧腋窝及锁骨上下区域未及明显肿大淋巴结。腹部:患者腹部稍隆起,下腹部可见长约10.0 cm×1.0 cm纵向手术瘢痕。术前图片见图3A。入院后完善全身状况评估,未见明显手术禁忌证,遂于全身麻醉下行DIEP皮瓣左侧乳房重建术。术前患者首先进行CTA检查,后进行腹部超声检查,分别于盲态下进行优势穿支体表标识(图3B)。术前分别于水平位、冠状位、矢状位以脐水平为中心,计算左右两侧优势穿支的具体定位(图4)。术中结合CTA导航技术,精确找到对应穿支血管(图5)。完整游离两侧皮瓣穿支血管及DIEP皮瓣,进行皮瓣塑形、乳房成形(图6)。患者手术顺利,术后3 d拔除胸部引流管,5 d拔除腹壁引流管,痊愈出院。

图3 术前患者胸腹部图像Fig.3 Preoperative thoracic and abdominal images of the patient

图4 穿支血管CTA影像图Fig.4 CTA images of perforator vessels

图5 穿支血管影像-实景对比图Fig.5 Perforator vessel image-real comparison

图6 DIEP皮瓣全貌及术后即刻图像Fig.6 A panoramic view of DIEP flap and immediate postoperative images
3 讨论
DIEP皮瓣在乳房重建中具有巨大优势,如组织获取量大,供受区组织相似性、腹直肌及前鞘组织完整保留等,对于腹部脂肪堆积患者同时可起到腹壁整形作用。目前,DIEP已成为自体组织乳房再造的首选皮瓣[8]。但由于其操作技术难度大、手术耗时长、术中环节繁杂、术后并发症多等因素,在一定程度上制约着DIEP皮瓣手术的开展[9-10]。其中,皮瓣穿支血管的抉择和无损伤解剖是DIEP手术中的关键。但皮瓣穿支血管在不同个体之间,或者同一个体不同侧穿支的起点位置、直径、肌内走行等均存在显著差异。传统手术中,医师通过对术中解剖探查各穿支进行综合评估选择优势穿支,手术耗时长,效率较低,且对术者个人经验要求极高。另外,穿支血管由于其管径较细、走行及位置变异性大的特点,进一步增加了手术的难度和风险[11]。
在30多年的DIEP皮瓣发展中,临床上出现了多种用于探测定位皮瓣穿支血管的方法[12]。常用的方法包括:①便携式超声多普勒检查:1975年首次被应用于皮瓣手术中的血管穿支定位,其操作简便、携带方便、价格低廉的优点可以用来进行手术前的血管初步评估,但有研究[13]表明,其较高的假阳性率降低了实际临床使用价值。② 彩色多普勒超声检查:相较于便携式超声多普勒,彩色多普勒超声检查能够提供更为详细的血流动力学信息,如穿支血管的起源、口径、肌内走行、峰值流速、阻力指数等,从而判断血管质量[14]。研究[15]报道,彩色多普勒超声检查可探测到直径约0.7 mm的穿支血管,准确率与CTA相当。如联合超声造影检查,可进一步提高血管显影效果。③高分辨率磁共振血管成像(magnetic resonance angiography,MRA)检查,常规MRA分辨率低,尽管随着高分辨率MRI及相应序列的出现,MRA可以显示直径1 mm的穿支血管,甚至能部分替代CTA检查,但在其经济性、实用性及扫描时长等方面值得考虑[16]。④ CTA检查:2006年,Masia等[17]首先采用CTA术前定位下腹部穿支血管,并选择优势穿支进行了乳房再造手术,CTA的影像学一致率达100%。CTA可以对DIEP皮瓣穿支血管的穿出点、数目、口径及走行等提供精确的解剖信息,与其他检查比较,CTA不易受患者体型、血管变异畸形等方面影响。
目前,国外CTA影像技术越来越广泛地应用于皮瓣修复领域,尤其在腹部DIEP皮瓣乳腺癌术后乳房重建中的应用日趋成熟[18-20]。而国内对于乳腺癌术后延期乳房重建中CTA临床应用的研究报道较少。传统的DIEP乳房重建手术一般采用彩色多普勒超声进行术前穿支评估,而超声检查的假阳性及操作者的主观性在一定程度上影响了穿支定位的准确性。随着影像学技术的广泛应用,CTA能在术前清晰地显示直径>0.3 mm的穿支血管的解剖信息,其作为手术前“彩排预演”,术者可以准确地按图索骥进行术前临床手术模拟[7]。近年来,本中心对于拟行延期DIEP乳房再造患者进行术前影像学评估,结合我院2018年前后影像学评估手段的不同,分析CTA在延期DIEP乳房重建手术中的应用价值。
CTA检查作为一种无创、快速、图像分辨率较高、准确性和特异性较高的术前穿支血管成像方法,目前已广泛应用于DIEP皮瓣穿支血管的术前定位[18,21]。本研究比较了CTA组与US组基线数据、术中观测指标、术后并发症发生率。其中,CTA组在抉择穿支时间及穿支解剖时间方面,明显优于术前超声定位组。在获取相同质量皮瓣中,CTA组所需时间明显短于超声组(P<0.001),这一结论与大部分国外研究相一致[5-6,18]。本组实验中所有CTA数据均为外科医师通过手机或电脑中HOROS软件进行DICOM文件识别、读取。既往研究显示外科医师和放射科医师之间的一致性为67.3%,且外科医师拥有更高的术前穿支定位准确率[3,20,22]。所有进行CTA检查的病例,外科医师可以对拟手术治疗病例随时随地提前进行阅览、测量、画图、标记,而不受时间、空间的限制,尤其方便临床医师的远程会诊手术的方案制定。CTA组能在获取皮瓣时,节省一定手术时间。Haddock等[3]的研究结果显示,皮瓣获取时间及总手术时间均更长。但在本研究总手术时间对比中,CTA组与US组比较差异无统计学意义(P>0.05)。分析这种原因可能是由于:首先,本研究以时间节点为界,2016年1月—2018年1月病例采用超声定位穿支评估,2018年1月—2021年1月采用CTA进行穿支血管评估,在早期(US组)术者团队的精力更多地集中于皮瓣切取过程,随着手术技能进一步提高以及手术器械的改进,术者在后期(CTA组)将更多的精力耗费在皮瓣塑形过程中,故一定程度上降低了两组总手术时间的差异。其次,本研究中US组纳入病例92例,CTA组206例,病例数的不匹配,可能导致实验结果出现偏倚。本研究中CTA组平均净手术时间缩短了34 min,但差异并无统计学意义,可能随着病例数的匹配或增加会出现不同的结果。此外,本研究中CTA组较US组包含了更多的双蒂重建患者(58.7%vs56.5%),一定程度增加了手术时间。
既往腹部手术瘢痕的存在可能会影响DIEP皮瓣重建的效果,这是因为瘢痕组织可能影响腹部皮瓣血供的正常分布,严重时影响穿支血管正常走行,从而加大手术难度[23-24]。而术前CTA检查可以清晰地显示腹壁下深血管、穿支血管的完整性及其走行,对于具有手术史的患者参考价值更大。本研究按照是否伴随腹部手术史进行了分层比较,结果显示,对于具有腹部手术史的患者,CTA组的皮瓣切取时间及总手术时间均低于US组(P<0.05)。对于无腹部手术史患者,CTA组皮瓣切取时间低于US组(P<0.05),总手术时间比较差异无统计学意义(P>0.05)。所以,对于伴有腹部手术史患者加强术前CTA检查具有重要意义。
两组病例术后并发症的比较虽然差异无统计学意义,但CTA组可能拥有更高的皮瓣存活率。为此,本研究再次比较了两组人群的二次手术探查率,US组为13.04%(12/92),CTA组为2.91%(6/206),差异有统计学意义(P<0.001)。显而易见,CTA可以降低二次手术探查风险。而在术中采用穿支与基于影像学资料评估优势穿支的一致性比较中,CTA组影像手术一致率为97.09%(200/206),US组一致率为43.48%(40/92),差异有统计学意义(P<0.001)。因此,CTA检查可以更为准确地进行术前优势穿支的选择、测量及定位。
CTA检查不仅局限于腹部皮瓣穿支的应用,术前如进行胸腹部联合检查时,可以进一步评估胸部受区血管(胸廓内动静脉),尤其对于一些合并放射性溃疡患者,合理的受区血管选择能进一步增加手术成功概率[25-26]。在一些伴有腹部手术史的患者中,可以更好地利用CTA评估腹部穿支血管条件,从而指导手术方式。腹部CTA检查有利于乳房重建手术中供区皮瓣的选择,对于拟进行SIEA皮瓣手术的患者,术前CTA评估尤为重要。然而,CTA检查也存在一些不足之处:患者需暴露在放射线下,这样可能诱发癌变;另外碘造影剂使用可能引起过敏反应、肾损伤等。
综上所述,CTA技术可以准确地提供穿支血管的详细解剖信息,便于手术设计,减少术中穿支抉择及解剖时间,降低二次手术探查风险,具有较高的影像手术一致率,尤其对于既往合并腹部手术史患者,CTA价值更高。
利益冲突声明:所有作者均不存在利益冲突。

