感兴趣体积IVS技术在腹部肿瘤配准范围的研究
赵利荣,周一兵
陆军军医大学第二附属医院 肿瘤科,重庆 400037
引言
随着适形放疗、调强放疗等复杂技术在临床上的推广应用,对射野精度的要求越来越高[1-3]。为解决上述问题,将加速器与成像设备结合在一起,在治疗时采集相关的图像信息,进行位置和剂量的校准,称为图像引导放射治 疗(Image-Guided Radiation Therapy,IGRT)[4-5]。IGRT为精准放疗的先决条件[6-8],目前临床应用的图像引导设备包括电子射野影像装置(Electronic Portal Imaging Device,EPID)和 KV或MV锥形束CT等[9]。KV级CBCT是目前国内外应用最广泛和成熟的影像引导设备[10],该系统采集的图像具有接近诊断标准的CT图像,放疗医生可以很方便以此为依据进行软件自动配准,或选择手动配准,对图像配准结果的审核提供可信赖的方法。
然而,于国产加速器来说,单独配置进口的CBCT会大大增加经济成本。国内很多三甲医院放疗中心面临放疗病人数量较多、工作量繁杂的现状[11]。若每次治疗前都执行CBCT影像引导,显然会付出巨大的时间成本,苏州雷泰公司的电子射野影像系统(Image Verification System,IVS)解决了经济性和时效性问题。然而,实际运用这套国产的EPID系统IVS的图像配准问题中,应该考虑感兴趣体积(Volume of Interest,VOI)配准数值以及不同VOI的选择对配准结果的影响。
基于以上现状,本研究采用德国博医来的盆腔仿真模体作为研究对象,通过开展不同 VOI 的选择对于定位 CT图像与每次放疗前的EPID图像自动配准结果的影响。分别获取 CT 定位图像和位置偏差已知的 20 组EPID 图像,采用IVS系统自带的医学图像配准软件,选择不同的 VOI得到三组不同的配准结果,并对该配准结果与已知真实误差值进行对比分析。
1 材料与方法
1.1 CT图像获取
用铅点标记盆腔模体,并使用飞利浦大孔径CT模拟定位机Bigbore对盆腔仿真模体进行扫描,扫描条件为:电压 120 kV,325层厚 2 mm,层间距2 mm,分辨率为512×512,像素大小为0.88 mm×0.88 mm。
1.2 盆腔模体图像处理
将盆腔模体的CT扫描图像传入Oncentra计划系统,利用Oncentra计划系统在图像上勾画出虚拟的靶区(约5 cm×6 cm),将计划中心设置为虚拟靶区的中心,制定0°和90°的验证野后传入IVS 位置验证系统。
1.3 盆腔模体位置验证
利用盆腔模体的体表标记和激光灯系统进行摆位,使等中心与盆腔模体的计划中心一致后行IVS位置验证扫描,以检验x、y、z三个方向上的位置吻合情况,然后进行模体位置微调,进一步确保摆位的精确性。调整好中心原点坐标后,分别在x、y、z方向上移动治疗床,并保证其另外两个方向位置不变。再对x、y、z三个方向同时移床并进行 IVS 扫描,移动距离依次为 0.2、0.5、1.0 cm,得到 20 组IVS 图像。将所有IVS图像与计划 CT 图像进行在线匹配,匹配范围分别是以靶区为中心的默认的范围35 cm×35 cm×35 cm、适中范围25 cm×25 cm×25 cm、较小的适应靶区的范围10 cm×10 cm×10 cm,分别记录匹配结果并进行统计分析。IVS软件系统操作流程图如图1所示:① 参考图像的传输与接收[与照射计划同中心的数字重建射线影像(Digitally Reconstructed Radiograph,DRR)];② 患者在加速器治疗床进行摆位;③ 启动EPID非晶硅图像采集板,设置参数,分别获取0、90°(或270°)的正交图像;④ 图像配准分析、纠正摆位误差、必要时重新标记等中心的位置;⑤ 定期采集图像查看治疗的位置精度,适时纠正误差。
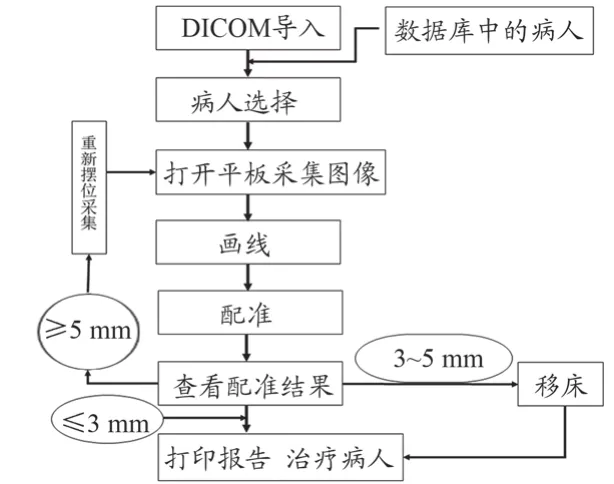
图1 IVS软件操作流程图
1.4 治疗前质量保证
为保证结果的准确性,必须在实施影响引导之前采用合适的质量保证措施,以消除或者尽量减少与影像引导放疗设备无关的系统误差。采用Winston-Lutz Test方法校准加速器的等中心位置后,参照YYT0890-201标准[12],对IVS位置验证系统进行质控(图2),确保影像引导设备的等中心和加速器的等中心重合,保证等中心的偏差不超过0.1 mm。对医科达加速器治疗床的旋转精度也进行了校准,保证床的旋转精度<±0.1°。对IVS图像质量也进行了质量保证措施,包括:图像的线性、成像延迟、图像的畸变、低对比度、空间分辨率等方面。

图2 IVS中心位置验证
1.5 EPID图像引导系统IVS 系统
IVS是通过加速器和图像处理技术的结合,使得物理师能够在放疗之前甚至病人固定在治疗床上接收放疗期间,立刻获得肿瘤图像。IVS位置验证系统属于EPID的一种,图像采集系统采用非晶硅平板探测器,分辨率为2688×2688,物理探测范围为41 cm×41 cm,它是利用加速器治疗射束成像,一般仅需要1~2 MU。利用 IVS计算机软件,可以将采集图像和CT重建的DRR图像进行对比,从而调节病人的位置或者射野摆位,以便更精确地照射目标肿瘤并避开周围的正常组织。
1.6 统计学分析
应用软件Origin 8.0 pro软件计算盆腔模体3D方向误差的平均值、标准偏差和方均根偏差值。应用软件SPSS 20.0软件,分别对三种不同的VOI 选取区域进行了两两间的配对样本t检验,以P<0.05表示有统计学差异。
2 结果
本实验选取盆腔模体,预设20组误差值已知的摆位偏差。IVS位置验证系统扫描的盆腔模体的位置验证(图3)。人为预设的20组不同的摆位误差值分别在0和90°进行了IVS系统的拍片,图3上为0的正位片,图3下为90°的侧位片,将IVS系统影像板采集的DR和CT重建的DRR进行配准。
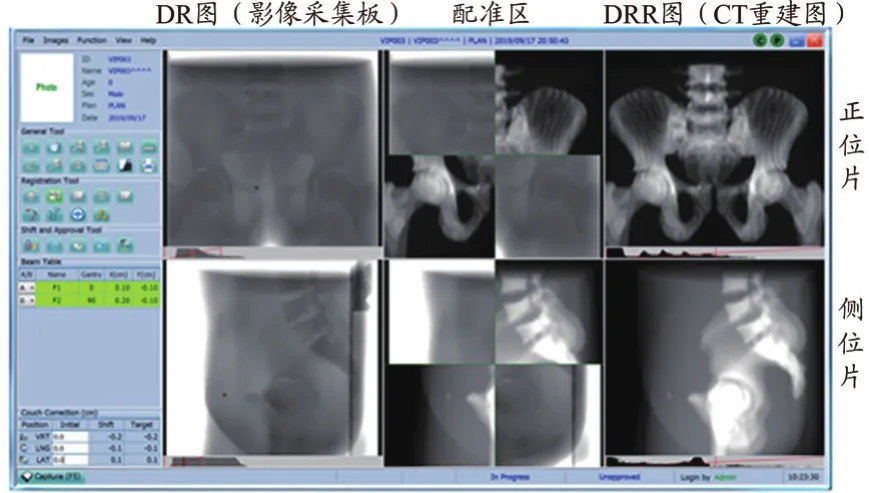
图3 IVS 系统扫描的盆腔模体的位置验证图
对于实验结果处理方法,本研究设定了标准:首先在坐标为(x,y,z)为(0,0,0)时,配准结果设为(x0,y0,z0),计算两组图像配准结果的相对偏差并计算绝对偏差。设原始移动坐标为(x,y,z),配准后坐标为(x1,y1,z1),则三维方向的绝对偏差X、Y、Z,见式(1)。
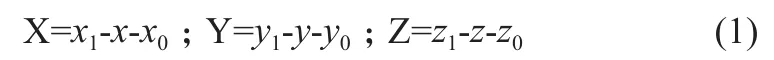
20组盆腔模体摆位误差结果分别减去相对应的已知误差值,结果用箱式误差分析图显示,如图4所示。从图中可以看出选择不同的VOI配准范围,对配准结果有较大影响。三种不同VOI配准范围的统计误差如表1 所示:对于20组不同的摆位偏差,VOI为35 cm×35 cm×35 cm时3D方向的平均值(M)分别为1.0、0.3、0.4 mm;统计的标准差(SD)分别为 0.3、0.6、0.4 mm;而对于VOI为25 cm×25 cm×25 cm和10 cm×10 cm×10 cm时,3D方向的均值均大于VOI为35 cm×35 cm×35 cm的均值,并且通过配对样本t检验的分析可以看出,VOI为35 cm×35 cm×35cm与VOI为25 cm×25 cm×25 cm和10 cm×10 cm×10cm相比,x、y、z三个方向的摆位误差差异均具有统计学意义(P<0.05);而对于VOI为25 cm×25 cm×25 cm与10 cm×10 cm×10 cm相比,x、y、z三个方向的摆位误差无统计学意义(P>0.05)。
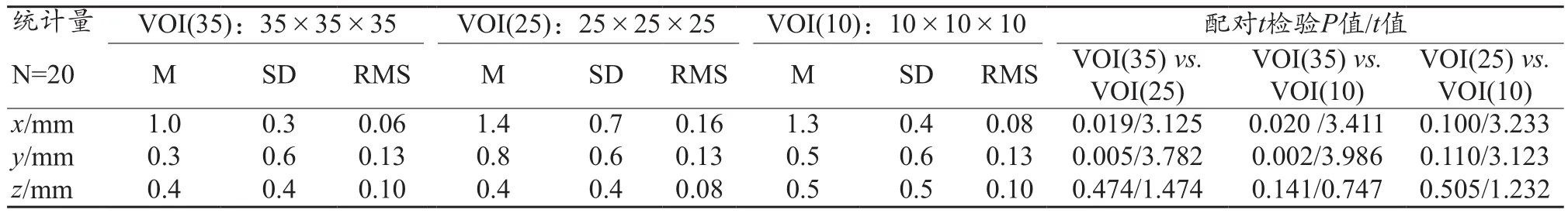
表1 不同VOI 3D方向误差统计
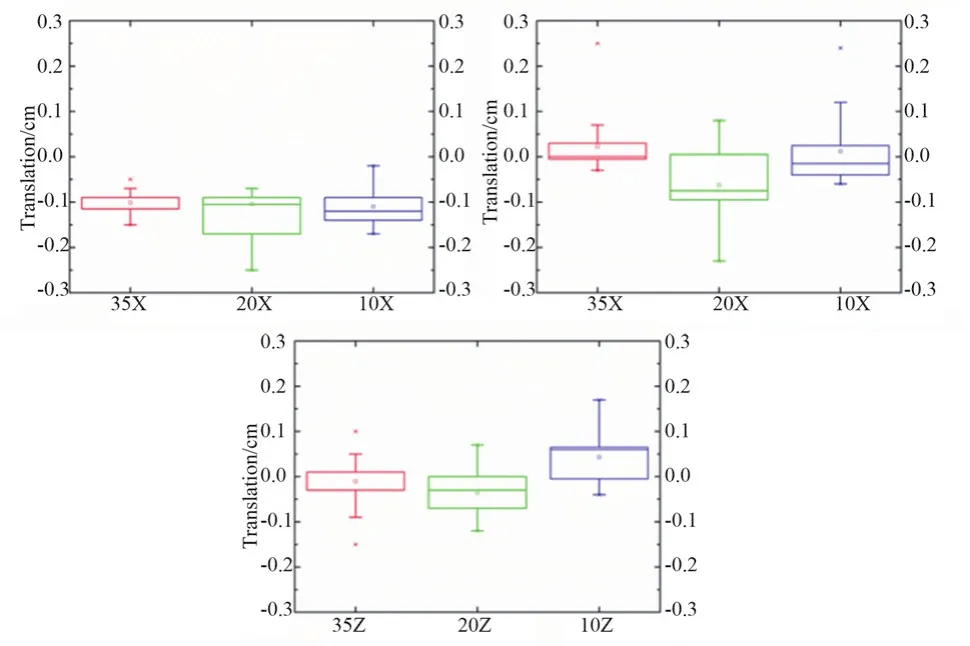
图4 盆腔模体20摆位误差的箱式误差分析图
3 讨论
IGRT是在患者进行治疗前、治疗中利用各种影像设备,对肿瘤及正常器官进行监控,并根据器官位置的变化调整治疗位置、治疗条件,使照射野紧随靶区。最终目的使剂量的实际投射区域与计划投射区域相一致。
EPID验证是IGRT的常用形式[13],利用加速器治疗射束成像,对软组织分辨率相对较低,通常以骨性标记作为参考与计划系统重建的DRR图像进行配准,是治疗实施过程中最为直接快速的验证方式之一。主要特点包括:① 利用加速器治疗射束成像,减少机械误差;② 软组织分辨率相对较低,建议在配准时以骨性标记为主要参考;③ 配准的参考图像是与DRR图像基于等中心进行配准,靶区位置比较直观;④ 整个图像采集、配准、移床、治疗的时间比较短,提高了患者的舒适度。
本科室安装的国产EPID影像引导系统IVS采用全自动支撑架,可以实现快速配准和一键移床的功能,和KV级CBCT相比优势为:拍摄每幅射野影像仅需1~2 MU,患者接受的额外剂量低;只需要拍摄正位、侧位两幅影像,直观高效;患者的舒适度提高。通过对盆腔模体实验的研究,总结出了科室安装的国产EPID影像引导系统IVS的配准的一些原则:对于盆腔部位建议选取腰椎、尾椎、骨盆或者髂骨中两到三处为骨性标记画线,腹部盆腔正位验证,配准主要依据为:腰椎边缘、小骨盆、耻骨联合、闭孔,主要观察图像左右方向误差,头脚方向只做参考;对于腹部盆腔侧位验证,配准主要依据为:腰椎边缘、骶尾椎边缘、耻骨联合等,主要观察图像头脚、腹背方向误差。
本研究采取仿真模体为研究对象,我们可以预设模体的摆位误差,在已知误差的情况下,通过三种不同的VOI选取,逆向分析哪种条件下的结果更可靠[14-15]。如果是真实的而患者,引起摆位误差的因素很多,很难评估单因素对摆位误差的影响。此外,仿真模体具有非常接近真实模体的解剖结构,可以更加逼真地模拟真实患者的图像配准,并且模体作为一个刚性物体,实验中避免了呼吸运动等运动对实验结果的影响。
然而本文选取的是盆腔体部模体进行研究,相关结果对于其他体部肿瘤,尤其是靶区较小的肿瘤,如体部立体定向放射治疗,可能不具备太大的参考意义,相关研究还需深入[16-17]。主要有以下两个方面的原因:① 相对而言盆腔部位基本属于刚体,靶区相对位置固定,较大的配准区域有助于提供更多信息使得图像配准更加准确;② 盆腔模体是静态模体,无法提供与真实患者治疗时类似的动态信息,而实际体部图像配准容易受到外轮廓变化以及体内各种器官运动的影响,选择太大的配准区域可能导致干扰信息远远大于有用信息,选择太小的配准区域又可能导致信息量的不够,导致配准结果的不准确。本研究采用盆腔模体比较研究不同配准范围对于配准结果的影响,具有一定的临床意义。
4 结论
通过对仿真盆腔模体的研究,对于腹部肿瘤而言,IVS系统的配准范围VOI 建议选取35 cm×35 cm×35 cm,配准结果的误差最小。这和图像配准时信息量的多少有关系,就本研究的结果表明感兴趣区域选取太小会导致配准时图像信息的不完全,进而会导致患者治疗时位置误差增加。

