显微血管减压术治疗舌咽神经痛的疗效观察
邬 立 潘 轲 汪 逵 谭雪瑛 谭高峰 田仁富
舌咽神经痛(glossopharyngeal neuralgia,GPN)是一种罕见的颅神经疼痛综合征[1],表现为舌咽神经分布区(下颌角、耳、扁桃体窝和舌根)或迷走神经分布区(咽部和耳)反复剧烈、电击样疼痛。吞咽、说话、咳嗽或咀嚼均可诱发疼痛,严重影响病人的生活质量[1]。GPN 的一线治疗是药物治疗[1],手术治疗适用于难治性GPN[2,3]。2014 年1 月~2021 年3 月显微血管减压术(micro-vascular decompression,MVD)治疗GPN共25例,现报道如下。
1 资料与方法
1.1 病例选择标准 纳入标准:符合《中国显微血管减压术治疗三叉神经痛和舌咽神经痛专家共识(2015)》中的诊断标准[4],保守治疗难以长期、有效控制疼痛,术前影像发现责任血管,病人有手术意愿。排除标准:存在严重系统性疾病不能耐受全麻手术;继发性GPN。
1.2 一般资料25例中,男11例,女14例;年龄34~76岁,中位年龄54岁;左侧15例,右侧10例;病程1~96个月,中位病程12个月。症状分布:咽喉部11例,下颌角+耳部5 例,舌根+扁桃体窝7 例,外耳道深部2例。保守治疗服药种类:1 种1 例,2 种11 例,3 种及以上13 例。术前巴罗神经学研究所(Barrow Neurological Institute,BNI)疼痛分级Ⅳ级14 例,Ⅴ级11 例[5]。术前常规行头颅岩尖部MRI 薄层扫描(3D-TOF序列,层厚2 mm)发现责任血管,主要责任血管为小脑后下动脉、椎动脉及小脑前下动脉。
1.3 手术方法 全麻下,采取侧卧位,通过常规乙状窦后入路行MVD。采用肌电图和诱发电位装置,使用针刺激器,针电极作为记录和参考电极。接地电极放置在一侧肩部。在口外环甲肌放置迷走神经记录电极。骨窗位于横窦下1 cm,显露乙状窦后缘。硬膜切开后,在手术显微镜下剪开蛛网膜、缓慢释放脑脊液,待小脑塌陷之后深入到桥小脑角,解剖桥小脑角蛛网膜并轻轻撑开小脑后,在手术显微镜下完全显露后组颅神经。对后组颅神经周围局部蛛网膜粘连或增厚情况,尽可能充分松解蛛网膜。用刺激器刺激后组颅神经根,以识别迷走神经运动根,术中有意识规避损伤。探查舌咽神经及迷走神经根出脑干区(root exit zone,REZ)至全长,以识别责任血管。将适量浸湿的Teflon 棉垫于血管和神经之间。术中尽可能减少对舌咽神经和迷走神经的牵拉,并再次确认责任血管已完全垫开且各神经张力适中,冲洗术野后,关颅。
1.4 随访及疼痛评估 通过电话或门诊随访,应用BNI分级评估疗效[5]。
2 结果
2.1 责任血管 术中发现责任血管:小脑后下动脉伴/不伴其分支17 例(68.0%),小脑后下动脉+椎动脉4例(16.0%),椎动脉2(8.0%),小脑前下动脉伴分支1(4.0%),无名小动脉1例(4.0%)。
2.2 手术疗效 术后疼痛均立即缓解,BNI 分级Ⅰ级。术后出现轻微吞咽困难1 例,1 个月后消失;出现局部脑脊液瘘1例,缝合瘘口、局部加压包扎联合腰大池置管引流治疗后痊愈;出现术侧面部麻木1例,3个月后好转,无颅内感染及手术死亡病例。术后随访6个月至7年,中位数4年,未见复发。
2.3 典型病例
病例1:54岁女性,因左侧下颌部疼痛1年入院,每天发作5~10 次,洗脸、吃饭、喝水、说话等均可诱发疼痛,口服普瑞巴林、加巴喷丁以及奥卡西平,症状控制差。术前MRI发现责任血管,完善术前准备,在全麻下行MVD。术后疼痛立即缓解,术后6 个月无复发。见图1。

图1 舌咽神经痛微血管减压术前影像及术中情况
病例2:49岁男性,因咽喉部疼痛1个月余入院,每天发作4~6次,吞咽诱发疼痛明显,口服卡马西平及其他药物(具体不详),症状控制差。术前MRI 发现责任血管,完善术前准备,在全麻下行MVD。术后疼痛立即缓解,术后随访1 年4 个月,无复发。见图2。
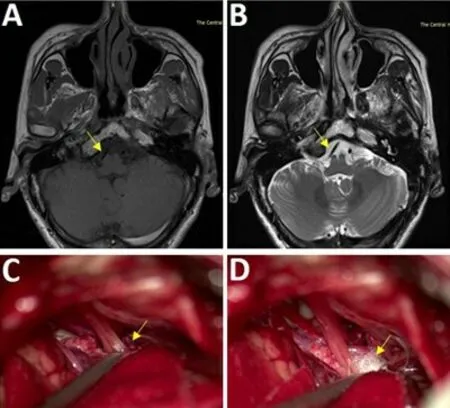
图2 舌咽神经痛微血管减压术前影像及术中情况
3 讨论
GPN 占所有颅神经痛的0.2%~1.3%[1]。Katusic等[6]研究显示,GPN 的发病率约为0.7/10 万,男女发病率近似,总体发病率随着年龄的增长而增加。临Amthor和Eide[7]认为,GPN的发病机制是由于小脑后下动脉或椎动脉等血管压迫,加上蛛网膜局部增厚、粘连,导致舌咽神经和迷走神经根脱髓鞘,使局部形成神经纤维回路而触发疼痛发作。
目前,GPN 的一线治疗是药物治疗。但对于一些药物难治性GPN,手术可能是最有效的治疗方案,而且MVD 相对于舌咽神经根切断术或伽玛刀放射治疗具有较高的治愈率,随着手术技术的提高,并发症的发生率和复发率逐渐降低[3,5,8]。本文病例术前药物控制不佳,BNI 分级Ⅳ、Ⅴ级,出现不同程度的药物耐受,需要加大药物服用剂量或联合用药,联合用药比例为96%;术前MRI 3D-TOF 序列报道24 例具有明显的责任血管,1例责任血管不明确;术中证实责任血管与术前MRI 3D-TOF序列所示血管的一致性。这表明3D-TOF序列在术前责任血管的判定及手术设计具有重要的应用价值[9]。本文GPN 最常见的责任血管是小脑后下动脉(68.0%),部分病例其分支也参与压迫神经;另外,责任血管为小脑后下动脉+椎动脉及单纯椎动脉的比例为24%。这与文献报道一致[3]。
迷走神经的运动纤维损伤会导致吞咽困难和发音困难[10]。文献报道神经切断术后运动并发症发生率高达19%[11]。术中识别这些运动神经纤维且有意识地规避这些神经的损伤是预防这些并发症的关键。我们通过术中电生理监测识别迷走神经运动纤维[12],避免术中损伤。取乙状窦后入路术中,骨窗常规显露乙状窦后缘。部分病例后组颅神经周围存在粘连紧密或增厚的蛛网膜。Yu 等[5]研究表明,局部蛛网膜增厚和粘连是GPN 的一个重要的致病因素,并且认为蛛网膜粘连导致可能血管受压更严重。我们术中对于存在蛛网膜粘连紧密或增厚的病例,尽可能充分松解蛛网膜,操作轻微,避免撕裂血管或周围组织。同时,在显露舌咽神经及迷走神经REZ,探查神经全长,避免遗漏责任血管。
我们的经验:术中电生理监测识别迷走神经运动纤维,规避其损伤,减少术后吞咽和发音困难等并发症;由于后组颅神经处蛛网膜粘连紧密或增厚、穿支血管复杂且变异度大、操作空间小等因素,术者应具备丰富的MVD经验和解剖知识;全长探查舌咽神经以防止遗漏责任血管,特别需要观察舌咽神经和迷走神经的REZ;脑神经周围的蛛网膜粘连尽量充分松解,但操作必须轻微,避免撕裂血管或周围组织;入路不必显露横窦,而应显露乙状窦后缘。

