一维氮掺杂碳包覆Fe3O4和Fe7S8纳米棒复合材料的制备及其储锂、储钠性能研究
梁 正, 吴家豪, 王 畅, 尚振领, 王逸飞, 刘 严, 姜付义, 周艳丽
(烟台大学 环境与材料工程学院,山东 烟台 264005)
锂离子电池作为二次储能体系,已经被广泛应用于生活中的各个领域,但是,锂资源分布不均,价格高昂,直接限制了锂离子电池的发展。与金属锂相比,钠元素在地壳中储量丰富,价格便宜,因此,钠离子电池作为下一代电化学储能系统,逐渐引起研究者们的广泛关注[1-3]。
负极材料作为二次电池的主要构成,直接影响电池性能。虽然锂离子电池与钠离子电池相似,但由于钠离子具有较大的半径,很难嵌入到电极材料,导致其在电极材料中扩散缓慢,直接影响其电化学性能[4]。比如,石墨是传统的锂离子电池负极材料,但其却不能作为钠离子电池负极材料[5]。除了碳类负极材料,其他具有转换机制的负极材料,由于其可逆的储锂、储钠电化学特性,备受关注[6-10]。其中,铁基氧化物和铁基硫化物,由于其较高的理论比容量、元素地壳储量丰富、以及对环境友好等优点,已经被用作负极材料,探索其在锂离子电池以及钠离子电池的应用[11-15]。但是,在深度充放电时,该类负极材料存在很多问题,第一,其本身固有的较低的电子电导率,直接影响其电子传输效率;第二,循环过程中较大的体积变化会引起体相电极材料严重粉化,从导电基底脱离,直接造成容量衰减。目前,有两种手段改善铁基负极材料的电化学性能。一种方法是将电极制备成特殊的纳米结构,其较小的颗粒尺寸,能够缩短Li+或者Na+的扩散路径,提高其扩散动力学,同时纳米结构能够缓冲活性材料的结构破坏[16-17]。另一种方法是采用导电碳材料对其进行表面修饰,制备相应的复合材料,改善其储锂、储钠性能[18-19]。如何将上述策略有机的结合,制备出高性能的铁基复合电极材料,仍然值得深入研究。
以水热法制备的FeOOH纳米棒为反应原料,以聚多巴胺(PDA)作为有机碳源,通过简单的聚合反应和后续的高温煅烧,我们成功制备出了Fe3O4@NC和Fe7S8@NC纳米棒复合材料。将上述两种复合材料分别作为锂离子电池和钠离子电池负极材料,组装成的纽扣半电池,都呈现出了良好的储锂和储钠性能。
1 实验部分
1.1 实验药品及试剂
六水合氯化铁(FeCl3·6H2O,分析纯,阿拉丁试剂(上海)有限公司),十六烷基三甲基溴化铵(分析纯,国药集团化学试剂有限公司),三羟甲基氨基甲烷(超级纯,上海麦克林生化科技有限公司),盐酸多巴胺(分析纯,阿拉丁试剂(上海)有限公司),升华硫(分析纯,国药集团化学试剂有限公司),去离子水(Elix Essen型超纯水制备机自制)。
1.2 氮掺杂碳包覆Fe3O4和Fe7S8纳米棒复合材料的制备
1.2.1 羟基氧化铁的制备
称取1.08 g六水合氯化铁(FeCl3·6H2O)和1.0 g十六烷基三甲基溴化铵(CTAB)置于烧杯中,加入40 mL去离子水,磁力搅拌30 min直至完全溶解。然后将溶液转移到聚四氟乙烯内衬反应釜中,80 ℃下反应12 h。待反应釜冷却至室温后,收集沉淀物,并采用乙醇或去离子水反复离心清洗多次后,置于60 ℃真空干燥箱中真空干燥6 h,得到黄色固体羟基氧化铁(FeOOH)。
1.2.2 聚多巴胺包覆羟基氧化铁的制备
首先称取0.30 g三羟甲基氨基甲烷(Tris)于烧杯中,加入50 mL去离子水,磁力搅拌20 min配制0.05 mol·L-1的Tris缓冲溶液。称取0.1 g的FeOOH置于烧杯中,向烧杯中加入50 mL的Tris缓冲溶液混合,超声20 min使其分散均匀。然后向烧杯中加入0.04 g盐酸多巴胺,在30 ℃油浴下搅拌6 h后,使用去离子水或者乙醇离心清洗产物,并将获得的黑色沉淀置于真空干燥箱中于60 ℃下烘干6 h,得到聚多巴胺包覆的羟基氧化铁复合材料(FeOOH@PDA)。
1.2.3 氮掺杂碳包覆Fe3O4和Fe7S8纳米棒复合材料的制备
Fe3O4@NC的制备:0.1 g FeOOH@PDA细粉置于瓷舟,封装在石英管式炉中,在Ar气气氛中500 ℃下煅烧3 h(升温速率为5 ℃·min-1),冷却后获得黑色的氮掺杂碳包覆的Fe3O4复合材料(Fe3O4@NC)。
Fe7S8@NC的制备:0.1 g的FeOOH@PDA和0.4 g升华硫粉混合均匀后转移至瓷舟中,封装在石英管式炉中,在Ar气气氛中,先150 ℃下煅烧2 h后560 ℃下煅烧3 h(升温速率为5 ℃·min-1)。冷却后获得黑色的氮掺杂碳包覆的Fe7S8复合材料(Fe7S8@NC)。
1.3 材料表征
采用X射线粉末衍射仪(XRD-7000X,Cu-Kα,λ= 0.154 06 nm)和激光拉曼光谱分析仪(LabRAM HR 800,法国)对样品的物相进行表征。采用X射线光电子能谱仪(XPS,Thermo Fisher Sci,USA,ESCALAB250)检测样品的元素价态以及元素组成。采用透射电子显微镜(TEM,JEOL-2100,日本)和场发射扫描电子显微镜(FESEM,JSM-7610F,日本)对样品的微观形貌进行表征。采用热分析(TGA,德国耐驰 Sta 449F3)分析复合材料的含碳量。
1.4 电池组装和电化学性能测试
工作电极的制备:活性物质,导电炭黑(Super P)以及羟甲基纤维素钠(CMC)按照7∶2∶1均匀混合,以去离子水作为分散剂进行充分研磨,获得均匀的浆料。然后将其刮涂于清洁的铜箔上,在真空干燥箱中60 ℃下干燥6 h。最终将所得铜箔冲压成所需极片。
CR2032纽扣电池的组装:以制备的Fe3O4@NC或Fe7S8@NC作为工作电极,金属Li/Na片为对电极,Celgard 2400 隔膜和玻璃纤维(GF/F)分别作为锂/钠电隔膜,锂离子电池的电解液为 1 mol/L 的LiPF6的碳酸亚乙酯(EC)和碳酸二甲酯(DMC)(体积比为1∶1),钠离子电池电解液为1 mol/L NaPF6的二乙二醇二甲醚。
电化学性能测试:使用电化学工作站(CHI660E,上海辰华)进行CV曲线测试,电压窗口为0.01~3 V。电池的充放电曲线、循环性能和倍率性能均通过武汉市Land CT2001A蓝电测试系统进行测试。所有数据均是在25 ℃的恒温条件下测得。
2 结果与讨论
Fe3O4@NC和Fe7S8@NC采用三步法制备 (图1)。首先,我们以FeCl3·6H2O作为反应原料,以CTAB作为表面活性剂,采用水热法,制备出一维FeOOH纳米棒。然后,采取室温聚合反应,以多巴胺作为有机碳源,采用Tris溶液调节溶液pH,在恒温条件下,实现聚合多巴胺(PDA)在FeOOH纳米棒的均匀包覆,制备出PDA包覆的FeOOH纳米棒复合材料(FeOOH@PDA)。最后,将FeOOH@PDA直接在Ar气氛、500 ℃下煅烧,制备Fe3O4@NC复合材料,在此过程中,表面的PDA热解为氮掺杂的碳,FeOOH同时发生分解反应形成Fe3O4。如果将FeOOH@PDA和过量的升华硫粉混合,然后再煅烧处理,则可获得Fe7S8@NC复合材料。煅烧过程中,150 ℃下煅烧2 h,能够确保硫粉在FeOOH表界面的充分扩散,560 ℃煅烧3 h后,由PDA热解生成的氮掺杂碳作为还原剂,能够部分参与FeOOH与硫粉的反应,生成Fe7S8。多余的氮掺杂碳层则包覆在Fe7S8表面,最终生成Fe7S8@NC复合材料。
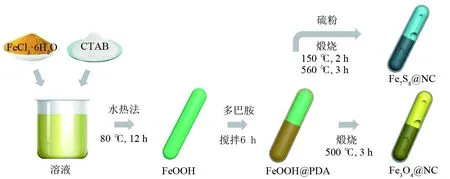
图1 Fe3O4@NC和Fe7S8@NC纳米棒复合材料的制备流程图Fig.1 Schematic illustration for preparation of Fe3O4@NC and Fe7S8@NC nanorods composite materials
2.1 结构及形貌表征
图2a展示出了制备过程中涉及到的四种产物的XRD图,如图2a所示,四种产物均出现明显的衍射峰,其中,FeOOH和FeOOH@PDA的所有衍射峰均与FeOOH的标准卡片号PDF#34-1266相对应,表明包覆PDA后,物相没有发生改变。直接煅烧获得的产物Fe3O4@NC的衍射峰能够与Fe3O4的标准卡片PDF#19-0629相匹配。与硫粉混合煅烧形成的产物Fe7S8@NC的衍射峰与Fe7S8标准卡片PDF#24-0220相匹配,四个主要的衍射峰分别对应于Fe7S8的 (200)、(203)、(206)以及(220)晶面。由于碳的无定形特性,图谱中未发现碳的衍射峰。除此之外,没有发现其他杂质峰,表明已经成功制备出了纯度较高、结晶度良好的FeOOH、FeOOH@PDA、Fe3O4@NC以及Fe7S8@NC复合材料。为了进一步验证碳的存在,采用拉曼光谱对获得的Fe3O4@NC以及Fe7S8@NC进行分析。如图2b所示,位于大约1 309 和1 584 cm-1的两个拉曼散射峰,分别归属于碳的D带和G带,600 cm-1之前的衍射峰分别归属于Fe3O4和Fe7S8。其中,位于206和275 cm-1的两个明显的拉曼峰是由于Fe3O4的骨架振动引起的[20],位于223和288 cm-1的两个主要的拉曼峰对应于Fe7S8的面外Fe-S 振动模式 (Ag) 和面内的Fe-S 振动模式 (Eg)[21]。由热重曲线(图2c和图2d)可知,Fe3O4@NC和Fe7S8@NC的含碳量分别17.24%和18.35%,展现出相似的含碳量。
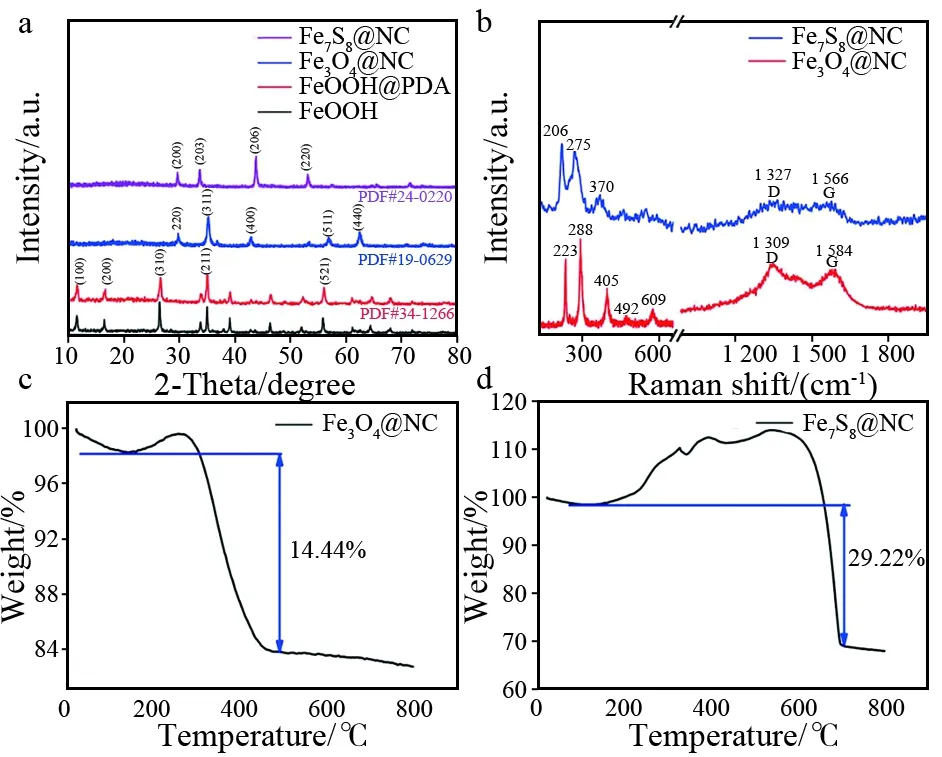
图2 (a) FeOOH、FeOOH@PDA、Fe3O4@NC以及Fe7S8@NC复合材料的XRD图谱;(b) Fe3O4@NC以及Fe7S8@NC复合材料的拉曼光谱; (c) Fe3O4@NC和(d) Fe7S8@NC复合材料的热分析曲线Fig.2 (a) XRD patterns of FeOOH, FeOOH@PDA, Fe3O4@NC and Fe7S8@NC composites; (b) Raman spectra of Fe3O4@NCand Fe7S8@NC composites; (c) and (d) TG curves of Fe3O4@NC and Fe7S8@NC composites
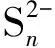
通过SEM和TEM技术表征FeOOH和FeOOH@PDA的形貌。由图4a可知,FeOOH呈现出纳米棒状结构,分散性良好。由TEM图可以看出,FeOOH的平均长度约为200 nm,平均直径约为50 nm,长径比约为4。由图4d和4e可知,FeOOH在包覆完PDA后仍然保持纳米棒状结构,其长径比没有明显变化。由图4f可以清楚的观察到位于FeOOH表面厚度约为7.5 nm的包覆层,证实PDA已经成功地包覆在FeOOH的表面。
进一步地,我们对煅烧处理获得的Fe3O4@NC和Fe7S8@NC两种复合材料进行形貌表征(图5),经过煅烧处理后,由于表面PDA的有效包覆,两种复合材料仍能保持良好的纳米棒状结构。与FeOOH不同的是,煅烧以后,由于FeOOH的分解,Fe3O4@NC和Fe7S8@NC内部的Fe3O4和Fe7S8的微观形貌稍有变化,变成非连续的多孔结构。该多孔结构有利于缓冲Fe3O4和Fe7S8在循环过程中的体积变化,维持结构稳定。由放大的TEM图,仍然可以观察到衬度较浅的碳层,厚度大约为4~5 nm,其作为高电导率的保护包覆层,不仅能够抑制内部活性材料的粉化问题,而且能够提高电子电导率,提升整个电极的储能性能。
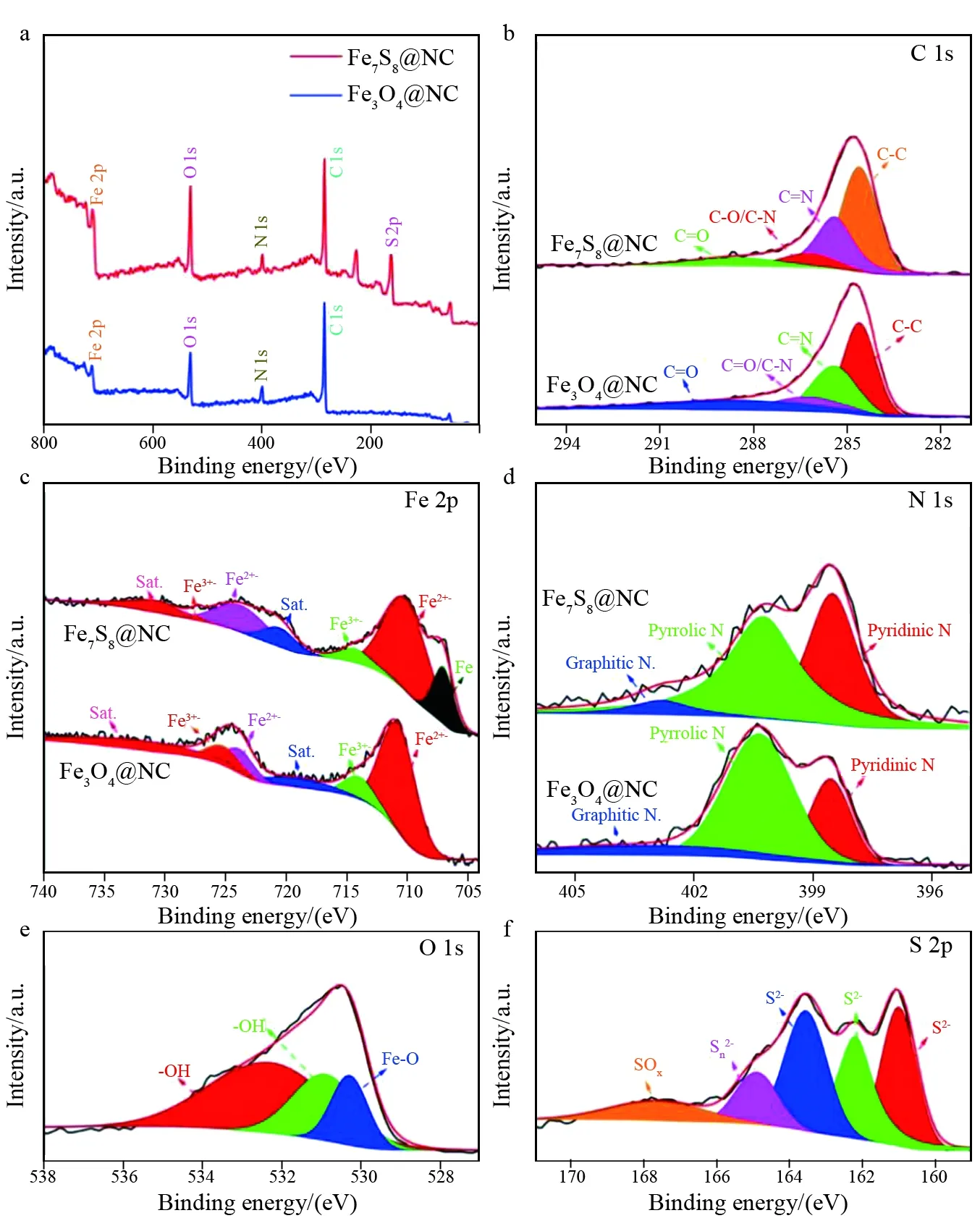
图3 Fe3O4@NC和Fe7S8@NC的XPS谱图:(a) 全谱;(b) C 1s, (c) Fe 2p, (d) N 1s, (e) O 1s, 和 (f) S 2p高分辨谱图Fig.3 XPS spectra of Fe3O4@NC and Fe7S8@NC: (a) survey spectrum;high resolutionspectra of (b) C 1s, (c) Fe 2p, (d) N 1s, (e) O 1s, and (f) S 2p

图4 FeOOH的(a) SEM图像,(b)和(c)TEM图像;FeOOH@PDA的(d) SEM图像,(e)和(f) TEM图像Fig.4 (a) SEM image, (b) and (c) TEM image of FeOOH;(d) SEM image, (e) and (f) TEM image of FeOOH@PDA

图5 Fe3O4@NC的(a) SEM图像,(b)和(c) TEM图像;Fe7S8@NC的(d) SEM图像,(e)和(f) TEM图像Fig.5 (a) SEM image, (b) and (c) TEM image of Fe3O4@NC; (d) SEM image, (e) and (f) TEM image of Fe7S8@NC
2.2 电化学性能研究
得益于Fe3O4@NC和Fe7S8@NC的特殊结构,我们对其储锂、储钠性能进行研究(图6和图7)。图6a展示出了Fe3O4@NC的CV曲线,位于第一圈阴极端的0.54 V的强还原峰主要归属于Fe3O4的还原过程以及SEI膜的形成。位于1.67和1.91 V左右的宽氧化峰主要归属于单质Fe和Li2S逐渐氧化生成Fe3O4。从第二圈开始,阴极峰发生明显的偏移,主要还原峰正偏移至0.79 V左右,可能归因于结构重排。位于1.39 V的宽峰归因于Li+嵌入Fe3O4形成LixFe3O4的过程。相比第一圈,后两圈氧化峰的位置没有发生明显的偏移,展现出较小的电极极化,CV曲线较好的重叠证实了Fe3O4@NC优异的可逆特性[15,23]。图6b展示出了Fe7S8@NC的CV曲线,位于第一圈阴极端1.18 V的强还原峰归因于Fe7S8还原成Fe和Li2S的过程,0.73 V的小峰归结于SEI膜的形成。位于第一圈阳极端1.96 V的强氧化峰归因于Fe和Li2S被氧化为Fe7S8。从第二圈开始,阳极峰和阴极峰的主峰位置都发生正偏移,分别位于2.03和1.31 V,此外,位于阴极端大约为1.85 V的宽峰对应于Li+插入Fe7S8形成LixFe7S8的过程[13]。所有氧化峰的较好重叠表明了Fe7S8@NC电极的可逆特性。图6c和6d展示出了Fe3O4@NC和Fe7S8@NC的充放电曲线,由图可知,其充放电平台与CV曲线的结果保持一致。其中,Fe3O4@NC的首次放电/充电比容量分别为1 415和1 015 mAh·g-1,首次库仑效率为71.7%,而Fe7S8@NC的放电/充电比容量分别为1 375和1 082 mAh·g-1,库仑效率比Fe3O4@NC高,约为78.7%。其不可逆容量损失主要来自于有机电解液分解引起的SEI膜的形成。图6e~g展示了Fe3O4@NC和Fe7S8@NC的储锂性能。在0.5 A·g-1的电流密度下,循环50圈,两种复合材料可逆容量分别维持在1 128和1 032 mAh·g-1,展现出了十分优异的高容量和循环稳定性。由倍率性能可知,Fe3O4@NC的倍率性能明显优于Fe7S8@NC,但在5 A·g-1的倍率下,Fe3O4@NC呈现出明显的容量衰减。图6g展示出了Fe3O4@NC和Fe7S8@NC的大倍率循环性能,如图所示,在2 A·g-1的电流密度下,循环300圈,其可逆比容量可分别维持在1 083和859 mAh·g-1,呈现出优异的循环稳定性。由上述电化学数据可知,与Fe7S8@NC相比,Fe3O4@NC呈现出了更高的可逆储锂容量和容量上升的趋势,可能是由于Fe3O4本身固有的较高的储锂容量以及高比例的赝电容行为引起的[12]。
除了对储锂性能的探索,我们还对Fe3O4@NC和Fe7S8@NC复合材料的储钠性能进行研究,如图7所示,相比锂离子电池,两种复合材料的CV曲线的峰强度明显减弱。对Fe3O4@NC而言,位于0.81 V的首次阴极峰归结于SEI膜的生成以及Fe3O4向Fe的转变过程,位于0.01 V的阴极峰为碳材料的插层反应。阳极端的0.08 V的尖锐的氧化峰对应于碳的还原,位于0.69、1.37 以及2.03 V的三个宽峰归结于单质Fe向高价铁的逐步氧化过程[23]。对Fe7S8@NC而言,位于1.46 V的氧化峰归结于Na+插层至Fe7S8晶格,位于0.87 V的首次阴极峰可归
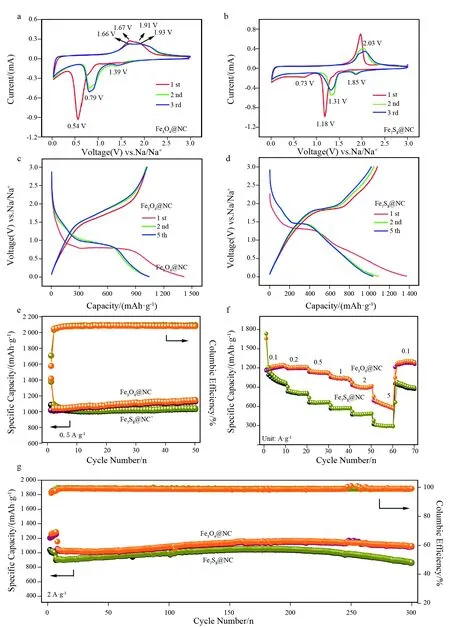
图6 Fe3O4@NC和Fe7S8@NC的储锂性能:(a、 c) Fe3O4@NC和 (b、 d) Fe7S8@NC的CV曲线和充放电曲线,Fe3O4@NC和Fe7S8@NC的(e)循环性能,(f)倍率性能以及(g)大倍率长程循环性能对比Fig.6 Lithium storage performances of Fe3O4@NC and Fe7S8@NC: (a,c) and (b,d) CV curves and discharge/charge profilesof Fe3O4@NC and Fe7S8@NC, respectively, (e) cycle performances at 0.5 A·g-1, (f) rate performances and (g) long term cycle performances at 2 A·g-1 of Fe3O4@NC and Fe7S8@NC
结于SEI膜的生成,位于0.61和0.29 V的阴极峰对应于NaxFe7S4向Fe的转变。位于阳极端1.41 以及1.83 V的两个宽峰归结于单质Fe向高价铁的逐步氧化[11,13]。其充放电曲线与CV结果基本一致。图7e展示了两种复合材料在0.5 A·g-1的电流密度下的循环性能,由图可知,Fe3O4@NC在起始的前几圈,容量缓慢上升,而 Fe7S8@NC的容量出现明显的衰减,但大约50圈后,容量又缓慢上升,循环200圈后,Fe7S8@NC的容量值明显高于Fe3O4@NC,其可逆比容量高达264 mAh·g-1。Fe3O4@NC电极起始的容量上升主要取决于聚合凝胶膜形成和电解液缓慢渗透到电极材料引发的逐步的活化过程[24],而Fe7S8@NC电极的快速容量衰减可能是由于聚硫离子的溶解和结构破坏导致的,随后的容量上升主要取决于颗粒细化导致的赝电容行为[11,15]。由倍率性能可观察到,在不同电流密度下,Fe3O4@NC展示出平稳的容量,而Fe7S8@NC出现明显的容量波动,特别是在初始小电流密度0.1 A·g-1时,容量衰减严重。图7g展示出两种复合材料在1 A·g-1的大倍率循环性能,350圈后,Fe3O4@NC的可逆容量维持在100 mAh·g-1,而Fe7S8@NC的可逆容量高达259 mAh·g-1,展现出良好的循环稳定性。两种复合材料优异的电化学性能主要取决于其精心设计的一维纳米结构以及氮掺杂碳层与内部高容量活性材料间的协同效应。一维纳米棒结构有利于电子和电荷传输,表面碳层能够缓解Fe3O4和Fe7S8的体积变化,抑制结构坍塌,同时提高电导率。碳中氮掺杂能够引入更多的活性位点,提升电极材料的容量。
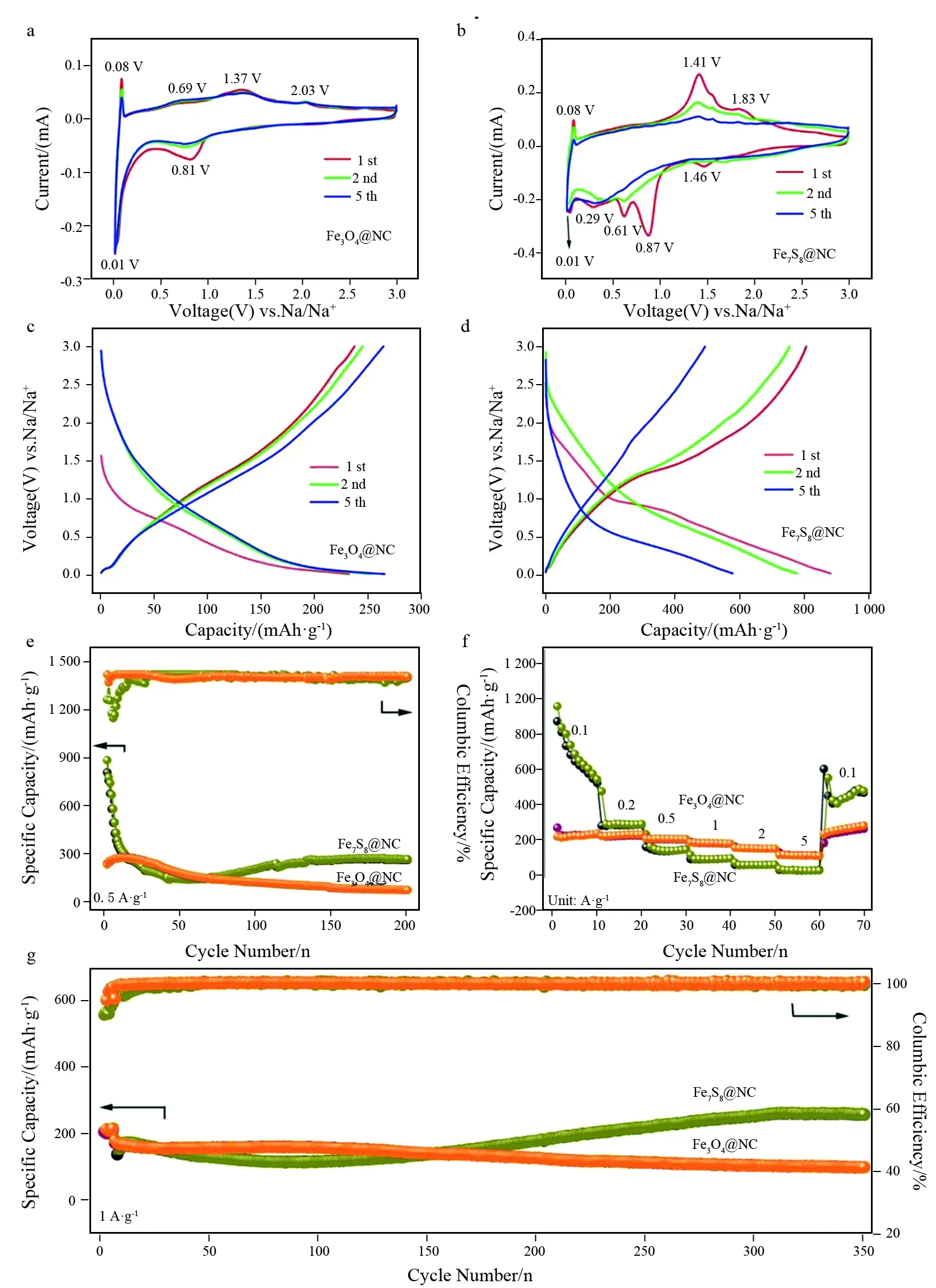
图7 Fe3O4@NC和Fe7S8@NC的储钠性能:(a、 c) Fe3O4@NC和 (b、 d) Fe7S8@NC的CV曲线和充放电曲线,Fe3O4@NC和Fe7S8@NC的(e)循环性能,(f)倍率性能以及(g)大倍率长程循环性能对比Fig.6 Sodium storage performances of Fe3O4@NC and Fe7S8@NC: (a,c) and (b,d) CV curves and discharge/charge profilesof Fe3O4@NC and Fe7S8@NC, respectively, (e) cycle performances at 0.5 A·g-1, (f) rate performances and (g) long term cycle performances at 1 A·g-1 of Fe3O4@NC and Fe7S8@NC
3 结论
以一维FeOOH纳米棒作为反应模板,以聚合多巴胺作为有机碳源,采用简单的三步合成策略,成功制备出了氮掺杂碳包覆的Fe3O4和Fe7S8复合材料。得益于Fe3O4@NC和Fe7S8@NC独特的多孔纳米结构以及氮掺杂碳保护层和内部高容量铁基活性材料的协同效应,上述两种复合材料作为碱金属离子(Li+/Na+)电池负极材料时,组装成的纽扣半电池都展现出优异的储锂/储钠性能。其中,用于锂离子电池负极,Fe3O4@NC显示出了极高的可逆比容量和循环稳定性,其性能优于Fe7S8@NC。而作为钠离子电池负极时,相比Fe3O4@NC,Fe7S8@NC展示出了较高的可逆比容量。上述复合电极材料优异的储锂/储钠性能有望作为下一代潜在的负极材料取代传统的石墨负极。

