喜树碱衍生物N- 乙酰- Asp- Gly- CPT 的药代动力学研究
姜永红
(东北林业大学生命科学学院,黑龙江 哈尔滨 150040)
喜树碱(Camptothecin,CPT)是一种单萜类的吲哚生物碱,从我国珙桐科植物喜树(Camptotheca acuminata)的提取物中分离获得。喜树碱是拓扑异构酶Ⅰ的抑制剂,具有广谱抗肿瘤活性[1-5]。体内研究显示,喜树碱具有严重的副作用,包括会抑制骨髓的活力、刺激胃肠道引起不适以及延迟性腹泻[6,7],而且不经修饰的喜树碱存在溶解性差、体内吸收差、活性结构不稳定等问题。为了获取活性更高、毒副作用更小的喜树碱衍生物,研究人员对喜树碱进行结构修饰,已经应用于临床癌症治疗进程的有伊立替康(CPT-11)[8,9]、拓扑替康(Topotecan, TPT)[10]及9- 氨基喜树碱(9-amino- camptothecin,9-AC )[11,12]等。
N- 乙酰-Asp-Gly-CPT 是本实验室在喜树碱的-20 位羟基引入了甘氨酸和天冬氨酸所合成的喜树碱衍生物(图1),使用甘氨酸酯的空间位阻效应提高了内酯环的稳定性,提高母体喜树碱的溶解性及可吸收性,对于喜树碱的肠道吸收具有积极作用。

图1 喜树碱和N- 乙酰-CPT-Gly-Asp 的结构式
1 实验部分
1.1 实验材料与仪器仪器
高效液相色谱(美国Waters 公司);Sorvall Legend Micro 17 型离心机(美国Thermo 公司);WH-986 静音混合器和WH-861 漩涡混合器(江苏省太仓市科教器材厂);Luna C18 柱色谱柱(美国phenomenex 公司)。Sorvall Legend Micro 17 型离心机(美国Thermo 公司);WH-986 静音混合器 和WH-861 漩涡混合器(江苏省太仓市科教器材厂)等。喜树碱(纯度99%),购自哈尔滨峰源高科技开发有限公司。N- 乙酰-Asp-Gly-CPT 为实验室合成(纯度99%)。SPF级大鼠(300 ± 30 g),购于长春亿斯动物技术有限责任公司。
1.2 实验方法
1.2.1 血浆样品的采集
精确称取N- 乙酰-Asp-Gly-CPT 和CPT 各10 mg,分别溶解于10 mL DMSO 中,并用乙腈稀释到400、200、100、80、40、20、10 ng/mL 的工作溶液,置于-40℃冰箱中保存。其中,四个浓度的质量控制样品(QC)分别为 5 ng/mL、10 ng/mL(低浓度)、100 ng/mL(中浓度)和300ng/mL(高浓度)。
给药前,称取适量N- 乙酰-Asp-Gly-CPT,使用注射溶液(DMSO/PEG-400/0.01 mol/L H3PO4= 5/45/50,v/v/v)溶解混匀,获得浓度为2 mg/mL 的N- 乙酰-Asp-Gly-CPT 悬浊液。
选取3 只健康雄性Wistar 大鼠,体重(300±30)g,使用10%的水合氯醛腹腔麻醉后进行颈脉插管。次日实验前称量大鼠的体重,以3mg/kg 剂量进行尾静脉注射,于给药后0.03、0.08、0.25、0.5、1、2、3、4、6、8、10、12、24 和48 h 取血,将血液置于预先用肝素处理过的离心管中,于4℃、3000 rpm·min-1离心30 min,取上清,并向上清血中加入等体积的0.1M HCl 溶液,混合均匀后置于-80℃冷冻保存。
1.2.2 样品处理
向50 μL 血 浆 样 品 中 依 次 加 入50 μL 0.1M HCl、100μL 乙腈和50μL 内标溶液(CZ44, 100 ng/mL),混合均匀后加入100μL 的1% 乙酸乙腈和500μL 乙酸乙酯,涡旋10 min,13000 rpm/min 离心10 min。取600μL 上清液置于新的离心管内,于氮吹仪中吹干。加入200μL 乙腈复融,室温涡旋10 min,13000 rpm/min 离心,取上清190μL 加入到进样瓶中检测。
1.2.3 标准曲线的制备
按照“1.2.2”样品制备方法制备标准曲线样品,以测得的N- 乙酰-Asp-Gly-CPT 的峰面积与内标比值为纵坐标(y),N- 乙酰-Asp-Gly-CPT 的浓度为横坐标(x),使用最小二乘法进行回归运算。
1.2.4 血药浓度测定
根据标准曲线计算各时间点样品的血药浓度,得到药物浓度- 时间曲线。使用药代动力学软件Kinetica 5.0 计算药代动力学参数。
2 结果与讨论
2.1 色谱条件
使用Waters 高效液相色谱系统(HPLC),1525 梯度泵、2475 型荧光检测器、717 型自动进样器。所用色谱柱为Luna C18 柱。流动相A 为0.1% 的乙酸水,流动相B 为ACN,高效液相色谱系统的流速为1.2 mL·min-1,样品进样体积为30μL,系统的运行时间为25 min。梯度洗脱条件见表1。2475 荧光检测器激发波长为 380nm,发射波长为418 nm。
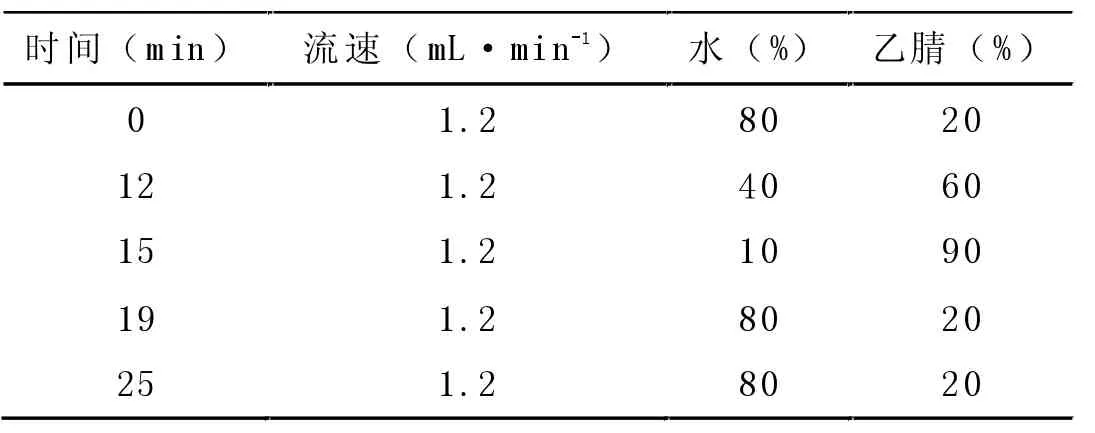
表1 HPLC 法测定N- 乙酰-Asp-Gly-CPT 流动相梯度洗脱条件
2.2 标准曲线的制备
求得标准曲线回归方程为y=0.0053x+0.0017,R2=0.9984,浓度范围为10~400ng/mL。
2.3 血药浓度测定
图 2 是大鼠尾静脉给药 3 mg/kg N- 乙酰-Asp-Gly-CPT (2mg/mL) 后,N- 乙酰-Asp-Gly-CPT 及其主要代谢产物CPT 在血浆中的分布情况,如图所示,尾静脉给药后,血浆样品中可立即检测到N- 乙酰-Asp-Gly-CPT 和CPT,且给药后,N- 乙酰-Asp-Gly-CPT 立即达到最大浓度;但在随后迅速下降,在8h 之后基本检测不到。CPT 的血药浓度呈现先上升后下降的趋势,并且浓度明显低于N- 乙酰-Asp-Gly-CPT。

图2 N- 乙酰-Asp-Gly-CPT(左)和CPT(右)的血药浓度- 时间曲线
使用药代动力学软件Kinetica 5.0 计算药代动力学参数,结果见表2。药物在大鼠体内的药动学过程参照非房室模型。尾静脉给药后,N- 乙酰-Asp-Gly-CPT 的药峰浓度Cmax 是69.75±4.66 ng/mL,约是CPT(2.69±0.54ng/mL)的27 倍;N- 乙酰-Asp-Gly-CPT 在给药后立即达到峰值,这可能是由于N- 乙酰-Asp-Gly-CPT 进入体内后迅速代谢,导致采集血液样品时已经达到最大血药浓度。N- 乙酰-Asp-Gly-CPT 和CPT 的半衰期T1/2 分别为2.93±0.93h 和5.39±0.27 h,平均驻留时间MRT 分别是5.43±1.05 h 和6.95±0.40 h,这说明N- 乙酰-Asp-Gly-CPT 和CPT 在大鼠血浆中的较为稳定,不会快速代谢;尾静脉给药后N- 乙酰-Asp-Gly-CPT 的AUC0-24和AUC0-∞分别为 101.77±55.16 h·ng·mL-1和159.87±71.62 h·ng·mL-1,相应CPT 的分别为26.34±15.73 h·ng·mL-1和34.29±23.96 h·ng·mL-1。

表2 大鼠尾静脉给药3mg/kg N- 乙酰-Asp-Gly-CPT 后N- 乙酰-Asp-Gly-CPT 和HCPT 的药代动力学参数(n=5)
3 结论
本文建立了一种同时测定大鼠血浆中N- 乙酰-Asp-Gly-CPT 及其代谢产物CPT 的HPLC 方法,并将这种测定方法应用于Asp-Gly-CPT 在大鼠体内的药代动力学研究分析中。经考察大鼠尾静脉给药后的药代动力学参数,得出N- 乙酰-Asp-Gly-CPT 进入体内后迅速达到最大血药浓度。N- 乙酰-Asp-Gly-CPT 和CPT 的T1/2和MRT 均较长,说明N- 乙酰-Asp-Gly-CPT 和CPT 在大鼠血浆中的较为稳定,不会快速代谢。

