替诺福韦抗乙型肝炎病毒应答临床相关因素分析*
李松龙,茹仁萍,王 琦,许海生,余丽霞
(浙江省杭州市西溪医院药剂科,浙江 杭州 310023)
富马酸替诺福韦二吡呋酯(TDF)属无环核苷(酸)类似物,对乙型肝炎病毒(HBV)具有强效低耐药的特点,是慢性乙型肝炎(CHB)患者抗病毒治疗的常用药物[1-2]。据报道,健康受试者体内的TDF 血药浓度存在明显差异[3-12],服用TDF后乙型肝炎e抗原(HBeAg)阴性CHB 患者的临床疗效优于HBeAg 阳性的CHB 患者[1-2],提示TDF 的临床应答与血药浓度和HBeAg 水平可能相关。本研究中结合临床治疗实际,纳入晚间服用TDF 的CHB 患者,回顾性评价TDF 抗HBV 应答与患者代谢相(服药后约12 h)血药浓度、性别、年龄及HBeAg、乙型肝炎表面抗原(HBsAg)、HBV DNA、丙氨酸氨基转移酶(ALT)等指标的相关性,为患者的TDF优化治疗和后续治疗方案的调整提供参考。
1 资料与方法
1.1 一般资料
纳入标准:CHB,予TDF治疗时HBV DNA >103IU/mL;晚间服药,无漏服;有治疗初始HBeAg,HBsAg,HBV DNA,ALT 数据,并定期(相距不超过3 个月)复查HBV DNA,接受TDF 治疗后3 个月的血生化样品可获取。本研究经医院医学伦理委员会审核,并豁免签署知情同意书。
排除标准:合并肾功能不全;妊娠期。
病例选择与分组:选取2017年至2019年收治的接受TDF 原研片剂300 mg/d 进行抗HBV 治疗48 周以上的CHB患者87例,其中男59例,女28例;年龄21~65岁,平均(37.1 ± 10.6)岁。按HBeAg 水平分为阴性组(<1 IU/mL)、低水平组(1~<50 IU/mL)、中水平组(50~1 000 IU/mL)和高水平组(>1 000 IU/mL),各组患者一般资料见表1。
表1 各组患者一般资料比较()Tab.1 Comparison of the patients′ general data in each group()

表1 各组患者一般资料比较()Tab.1 Comparison of the patients′ general data in each group()
1.2 方法
根据分组和检验系统查询,收集入组患者符合要求的生化血清样品,供血药浓度监测用。以替诺福韦-D7 为内标,采用超高效液相色谱-串联三重四极杆质谱仪测定血清中TDF 的浓度。统计患者服用TDF 后,HBV DNA 水平从103IU/ mL 降至<30 IU/ mL 水平所需时间(月数),不足1 个月的按1 个月计,24 个月未达标的按24个月计。分析患者HBV DNA 达标月数与血药浓度、HBeAg水平、组别、性别、年龄间的相关性。
1.3 统计学处理
2 结果
2.1 HBsAg、HBeAg、代谢相血药浓度及HBV DNA达标情况
87例患者代谢相血药浓度为(125.29±35.06)ng/mL;HBV DNA 水平由103IU/ mL 降至<30 IU/ mL 所需的时间为(8.71 ± 6.95)月,各组相应检测数据见表2。组内及组间不同血药浓度水平下HBV DNA 6个月达标情况见表3。由表3可见,血药浓度越高,HBeAg水平越低,HBV DNA 6个月达标率越高。
表2 各组患者HBsAg、HBeAg、代谢相血药浓度及HBV DNA达标月数比较(,n=87)Tab.2 Comparison of HBsAg level,HBeAg level,blood drug concentration of metabolic phase and the months of HBV DNA reaching standard in each group(,n=87)
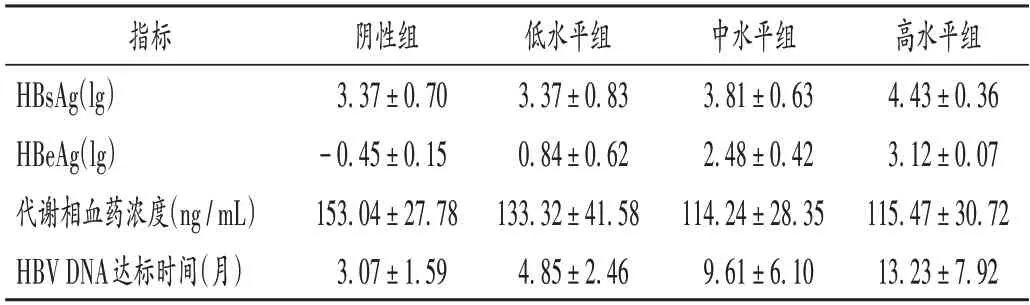
表2 各组患者HBsAg、HBeAg、代谢相血药浓度及HBV DNA达标月数比较(,n=87)Tab.2 Comparison of HBsAg level,HBeAg level,blood drug concentration of metabolic phase and the months of HBV DNA reaching standard in each group(,n=87)

表3 不同血药浓度下HBV DNA 6个月达标情况比较(n=87)Tab.3 Comparison of the percentage of HBV DNA reaching the standard within six months in patients with different blood drug concentrations(n=87)
2.2 不同起始HBV DNA 水平降至103IU/mL 的情况
把起始HBV DNA >105IU/mL 的患者(共57例)纳入分析,结果显示,不同起始水平HBV DNA 2个月内降至103IU/mL的例数,除105级组内外,其余组的组内、组间均无显著差异(P>0.05),详见表4。提示TDF抗HBV临床应答与治疗起始时的HBV DNA水平无明显相关。

表4 不同起始HBV DNA水平2个月内降至103 IU/mL例数比较(n=57)Tab.4 Comparison of the cases of patients with different initial HBV DNA levels decreasing to 103 IU/mL within two months(n=57)
2.3 抗HBV 病毒学应答与影响因素的相关性
Pearson相关性分析结果见表5。可见,患者HBV DNA达标月数与血药浓度呈负相关(P<0.001),与HBsAg和HBeAg 的lg 值及组别呈正相关(P<0.001),而与治疗起始的HBV DNA 水平(lg 值)、起始ALT 水平、性别、年龄无关(P>0.05)。

表5 HBV DNA达标月数与患者影响因素的相关性(n=87)Tab.5 Correlation between the months of HBV DNA reaching standard and influencing factors of patients(n=87)
3 讨论
初期调查发现,多数CHB 患者在睡前服用抗HBV药物,晨时服药的患者相对较少,纳入病例困难,且多为长效干扰素和核苷类药物经治患者,故纳入睡前服用TDF 的CHB 经治患者进行回顾性研究。研究留取的血样为患者自主检测的生化残余血样,均为早晨8:00左右采集,故研究检测到的血药浓度为代谢相浓度。与晨时服药的病例相比,此类病例较易收集,可纳入病例更多,在临床实际治疗的患者中更具代表性,研究结果可能更具参考价值,但缺点是血药浓度受采血时间的影响更大,误差更大,结果可靠性相对降低。后续研究可采用主动采样,纳入起始指标相似的患者队列进行前瞻性研究,所得结果会更具参考价值。
本研究结果表明,CHB 患者服用TDF 抗HBV 的临床治疗实践中,患者抗HBV 病毒学应答欠佳。因此,除进行必要的基因检测和抗病毒药物敏感度检测外,还可开展血药浓度检测。
另有文献报道,食物对富马酸替诺福韦二吡呋酯片的吸收和血药浓度也有明显影响[6-12]。对于血药浓度偏低患者,临床或可尝试通过饮食干预方式增加体内的血药浓度,以提高疗效。对于HBeAg 水平高且服用TDF 后血药浓度过低的CHB 患者,临床医师可提前调整和优化给药方案,进行个体化治疗,以便更早地使血清HBV DNA水平降至检测限以下,获得更好的疗效。

