富硒堇叶碎米荠中硒化合物的形态分析与鉴定
叶 梅,虞锐鹏,丛 欣,陈尚卫,朱 松*
(1.江南大学 食品科学与技术国家重点实验室,江苏 无锡 214122;2.恩施德源健康科技发展有限公司,湖北 恩施 445000)
硒是一种人体必需的微量元素,参与机体许多重要的代谢过程,适量的硒能起到抗氧化防御、维持氧化还原平衡作用,有效改善免疫系统功能[1-2],降低患癌风险[3];然而其不能在人体内自主合成,须通过外界摄入维持正常水平。硒在自然界中分为有机硒和无机硒:无机硒主要为Se(Ⅳ)和Se(Ⅵ),对机体的安全阈值较低;有机硒包括硒蛋白、硒肽、硒代氨基酸等经代谢产生的一系列含硒化合物,对机体的安全阈值较高,生物利用度好[4]。因此,对于72%国土面积有不同程度缺硒的中国,科学安全高效地利用有机硒尤为重要[5]。
堇叶碎米荠是一种典型的富硒植物,能通过自身代谢途径将无机硒高效地转化为有机硒[6-7],2020年国家卫生健康委员会已将堇叶碎米荠列为新食品原料。然而,目前对有机硒化合物的检测手段大多是通过高效液相色谱-电感耦合等离子质谱(HPLC-ICP-MS)[8-9]和高效液相色谱-氢化物原子荧光光谱(HPLC-HG-AFS)分析几种常见的硒代氨基酸[10-11],这主要是受限于硒化合物标准品的数量与种类[12]。除此之外的未知硒化合物,必须采用液相色谱-高分辨质谱联用方法进行结构鉴定[13-14]。
液相色谱-高分辨质谱联用时常用的离子源为电喷雾电离(ESI)源,不受多原子干扰,可用于硒的特异性检测,且高分辨质谱能很好地解决ICP-MS 受色谱分辨率限制而产生的共洗脱问题[13]。但随着分辨率的提高,由于许多伴生的易电离物质产生干扰,使得硒化合物的信号受到强烈抑制,而背景值逐渐升高(相较于ICP-MS 高2 个数量级),导致灵敏度下降。这就需要通过多维色谱分离纯化、冻干浓缩等步骤获得较高浓度和纯度的含硒化合物[15]。常用的高分辨质谱分析器主要包括飞行时间质谱(TOF MS)、轨道离子阱质谱(Orbitrap MS)和傅里叶变换质谱(FT-ICR-MS),其中Orbitrap MS 有利于对大分子量(500~1 000 Da)化合物的分析,但鉴定的硒化合物不够全面[16-17]。FT-ICR-MS虽然具有极高的同位素保真度,但与液相色谱的兼容程度需进一步改善[13]。TOF MS在色谱模式下的高数据采集速度使其能与超高效液相色谱(UPLC)耦合,从而在相对复杂的样品中检测大量的含硒化合物,一定程度上弥补了ESI 离子源的不足,是有利于鉴定低分子量硒化合物的质谱仪器[13,18-19]。如Ward 等[20]将不同富硒酵母的硒化合物,经超滤膜过滤截取、冻干复溶后,直接进高效液相色谱-电喷雾电离源高分辨串联质谱(HPLC-ESI Q-TOF MS),测定了超过100 种含硒化合物。目前运用液相色谱-高分辨质谱联用鉴定的富硒样品绝大多数是蛋白含量较高,研究较为透彻的富硒酵母,对富硒植物中硒化合物的研究较少。本文以富硒堇叶碎米荠为研究对象,在HPLC-ICP-MS 定量分析常见硒化合物的基础上,通过3 kDa 超滤离心管去除大分子杂质、冻干浓缩等方法,采用超高效液相色谱-电喷雾电离源高分辨串联质谱(UPLC-ESI-Triple TOF MS)实现了对富硒堇叶碎米荠中未知硒化合物的鉴定。
1 实验部分
1.1 仪器与试剂
U3000 高效液相色谱仪、iCAP TQ 三重四极杆电感耦合等离子质谱仪(美国Thermo Fisher 公司);SCIEX ExionLC™AC超高效液相色谱、X500R Triple TOF MS 高分辨质谱(美国AB SCIEX 公司);恒温金属浴磁力搅拌器(德国IKA 公司);5804R 台式冷冻离心机(德国Eppendorf公司);Mars6 微波消解仪(美国CEM 公司);LE204E 分析天平、FiveEasy Plus pH 计(上海梅特勒-托利多仪器有限公司);3 kDa 超滤离心管(15 mL,美国Millipore 公司);冷冻干燥机(宁波新芝生物科技股份有限公司);TechMate C18-ST 反相色谱柱(4.6 mm×250 mm,5 μm,日本Shiseido 公司);Kinetex F5 超高效液相五氟苯基柱(100 mm×2.1 mm,2.6 μm,美国Phenomenex公司)。
标准溶液:硒代胱氨酸(SeCys2)、甲基硒代半胱氨酸(MeSeCys)、硒代蛋氨酸(SeMet)、Se(Ⅵ)、Se(Ⅳ)(中国计量科学院国家标准物质研究中心);富硒堇叶碎米荠干粉(恩施德源健康科技发展有限公司);碱性蛋白酶(诺维信生物技术有限公司);胰蛋白酶、蛋白酶K(合肥博美生物科技有限责任公司);磷酸氢二铵、10%四丁基氢氧化铵水溶液(国药集团化学试剂有限公司);硝酸、甲醇、乙腈、甲酸(均为色谱纯,美国Tedia公司)。实验所用超纯水由Milli-Q系统(电阻率为18.2 MΩ·cm,美国Millipore公司)制备。
1.2 实验方法
1.2.1 ICP-MS 测定总硒 取0.15 g富硒堇叶碎米荠干粉于微波消解管中,加3 mL 硝酸,冷消化过夜后加入5 mL 水,于微波消解仪中消解2 h。将消解后的溶液用水定容至相应体积,充分摇匀。取约15 mL,过0.22 μm尼龙膜,于4 ℃保存待测。样品平行实验3次,同时做试剂空白。
1.2.2 HPLC-ICP-MS 测定硒形态 混合硒标准溶液的配制:分别准确吸取466.5 μL Se(Ⅳ)、482.0 μL Se(Ⅵ)、575.0 μL MeSeCys、452.5 μL SeCys2、507.5 μL SeMet溶液,用水定容于10 mL容量瓶中,得质量浓度为2.0 mg/L的硒化合物储备液(以硒计)。混合配制成200 μg/L的混合标准溶液(以硒计),置于4 ℃冰箱保存。
样品前处理:称取0.1 g 富硒堇叶碎米荠干粉,经5%碱性蛋白酶-胰蛋白酶-蛋白酶K 酶解后,400 r/min磁力搅拌4 h。4 ℃下以4 000 r/min离心30 min,上清液经0.22 μm微孔滤膜过滤后进样。
HPLC条件:色谱柱为TechMate C18-ST反相色谱柱(4.6 mm×250 mm,5 μm);流动相为30 mmol/L磷酸氢二铵、0.5 mmol/L四丁基氢氧化铵、3%甲醇,以10%甲酸调流动相pH为6.0。柱温为30 ℃,流速为1.0 mL/min。进样量为10 μL,分析时间为10 min。
ICP-MS条件:射频功率为1 550 W,冷却气流量为14 L/min,辅助气流量为0.8 L/min,雾化气流量为1.025 L/min,O2流量为0.326 mL/min,泵转速为40 r/min,测定模式为TQ-O2模式,Q1设置分析质量数为m/z=80,Q3设置质量数为m/z=96。
1.2.3 UPLC-ESI-Triple TOF MS 测定未知硒化合物 样品前处理:将0.5 g 富硒堇叶碎米荠干粉经酶解后,离心取上清液过15 mL 3 kDa 超滤离心管,4 000 r/min 离心2 h,-20 ℃冷冻干燥后,以1 mL初始流动相复溶,4 ℃下以14 000 r/min高速离心5 min,取上清液待检测。
UPLC 条件:Kinetex F5 超高效液相五氟苯基柱(100 mm×2.1 mm,2.6 μm),柱温为40 ℃,进样盘温度为4 ℃。流动相:A 为0.1%(体积分数,下同)甲酸-水溶液,B 为0.1%甲酸-乙腈溶液。梯度洗脱程序:0~1 min,3% B;1~15 min,3%~95% B;15~18 min,95% B;18.1~20 min,95%~3%B。流速为0.3 mL/min,进样量为10 μL。
ESI-Triple TOF MS 条件:电喷雾(ESI)正离子源,气帘气(CUR)为241 kPa;雾化气(GS1)为379 kPa;辅助气(GS2)为379 kPa;喷雾电压(ISVF)为5 500 V;离子源温度(TEM)为550 ℃,IDA 模式下设置去簇电压(DP)为60 V,碰撞电压(CE)为35 V,碰撞电压差(CES)为15 V。
2 结果与讨论
2.1 富硒堇叶碎米荠中总硒及已知硒形态的含量
采用ICP-MS 测得富硒堇叶碎米荠的总硒含量为2 853.5 mg/kg;经复合蛋白酶酶解后,采用HPLC-ICP-MS进行形态分析,外标法定量计算该堇叶碎米荠中5种硒形态SeCys2、MeSeCys、Se(Ⅳ)、SeMet、Se(Ⅵ)的含量分别为2 154.1、18.5、225.8、4.5、52.3 mg/kg。结果表明,该堇叶碎米荠中主要硒形态为有机硒(以SeCys2为主),有机硒含量达到总硒含量的76.3%。混标和富硒堇叶碎米荠的HPLC-ICP-MS 图如图1所示,可见该堇叶碎米荠中存在多种微量的未知硒化合物,需进一步采用高分辨质谱分析鉴定。

图1 200 μg/L混标(以硒计)(A)和富硒堇叶碎米荠(B)的HPLC-ICP-MS图Fig.1 HPLC-ICP-MS chromatograms of 200 μg/L(as Se)mixed standard solution(A)and Se-enriched C. Violifolia(B)peak:1. SeCys2;2. MeSeCys;3. Se(Ⅳ);4. SeMet;5. Se(Ⅵ)
2.2 富硒堇叶碎米荠中未知硒化合物的鉴定
2.2.1 数据依赖型扫描和动态背景扣除
Triple TOF 高分辨系统的采集速度高达100 Hz,采用数据依赖型扫描(IDA)[21]和动态背景扣除(DBS)的数据采集模式,能够使浓缩复溶后的堇叶碎米荠样品经一次进样后同时获得高质量的全扫描TOF MS谱图和全面的TOF MS/MS谱图。其中TOF MS谱图的扫描范围为m/z100~1 000;IDA模式选择获得15个产物离子的TOF MS/MS 谱图,扫描范围为m/z50~1 000。DBS可以过滤干扰杂质,在通过高分辨和精确质量数全扫描发现主要化学成分的同时,保证目标物得到高质量的TOF MS/MS 谱图,这些高分辨率和精确质量数谱图可用于对目标物的主要化学成分进行结构阐明与确证。
2.2.2 同位素过滤和质量亏损过滤
硒是一种同位素分布特征明显的元素。本实验结果显示,硒有6个同位素峰,74Se同位素峰的丰度非常小,仅占最高丰度80Se 的1.79%。而76Se、77Se、78Se、80Se、82Se 同位素的丰度比约为19∶15∶48∶100∶18,可利用该特征通过同位素过滤方法挖掘数据,找到符合硒同位素分布的质谱图,进而找到可能的含硒有机物。对于可能含有2~3个硒的有机小分子物质,则须先通过元素组成计算工具Mass Calculators得到不同的硒同位素分布情况,再进行同位素过滤。需要注意的是,由于有时谱图干涉或同位素强度比缺乏保真度,须通过人工处理进行再次确认[13]。
另外,硒的质量亏损约为921 mDa,与常见元素有一定差异,因此也可利用特征质量亏损过滤进行含硒有机物的确认[18]。
2.2.3 硒化合物分子式的确认及结构鉴定
依据上述步骤,除HPLC-ICP-MS 形态分析的5 种硒化合物外,本实验通过UPLC-ESI-Triple TOF MS 鉴定[22]出15 种硒化合物,其中有7 种已被报道(如表1)。在8 种未报道的硒化合物中,提出了3 种硒化合物的结构式,分别为C4H7NO2Se([M +H]+的m/z为181.971 5)、C5H8O2Se([M +H]+的m/z为180.976 2)、C7H9NO2Se([M+H]+的m/z为219.987 4),详细的质谱和结构特征信息见表2。以下是3种硒化合物结构的鉴定过程。
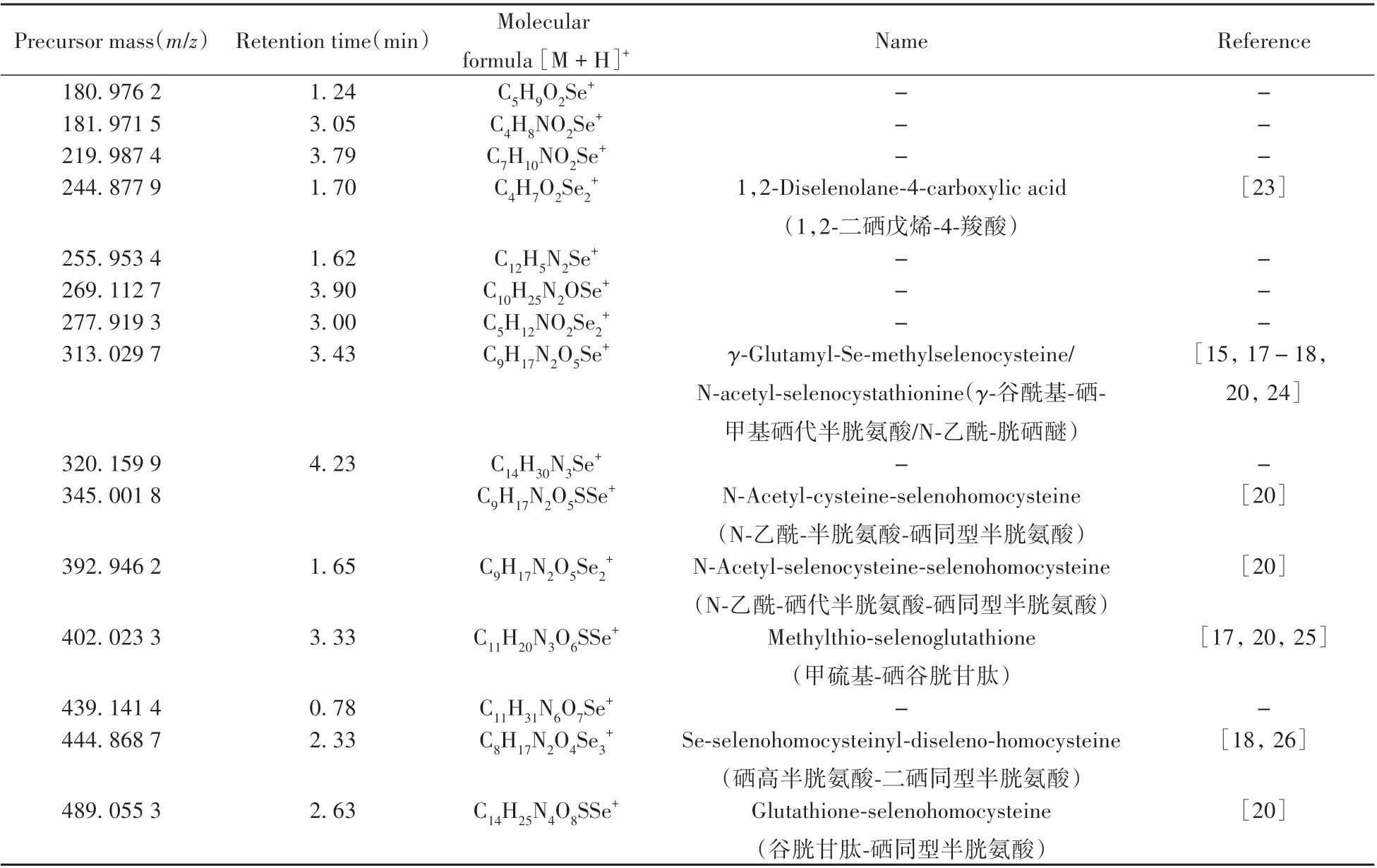
表1 富硒堇叶碎米荠中鉴定的15种硒化合物Table 1 Se compounds identified in Se-enriched C. Violifolia

表2 富硒堇叶碎米荠中鉴定出的硒化合物的一级和二级质谱信息Table 2 MS and MS/MS informations of Se compounds identified in Se-enriched C. Violifolia
2.2.3.1 C4H7NO2Se 通过同位素过滤和质量亏损过滤,在保留时间3.05 min 位置,找到m/z为181.971 5 的化合物加氢母离子,其同位素分布和质量亏损符合硒化合物的特征,提取离子流(XIC)图和TOF MS 谱图分别见图2A、B。为进一步确认该化合物的元素组成,将其TOF MS 谱图与Formular Finder的MS Details相链接,基于其精确质量去除大量元素组成,设置最大元素组成为C50H200N10S5Se5以过滤最大和最小的潜在原子数量和原子类型,留下可能的元素组成形成元素组成列表。根据MS Rank 和Δppm(化合物母离子的精确质量数和理论质量数的偏差)对所有可能的结果进行排序,Δppm 越小,表明提出的m/z与精确的单同位素质量越接近,元素组成的可信度越高。另外,还需考虑元素组成的不饱和度(RDB值)是否符合组成化合物的规律。结果表明,该化合物的分子式仅有1 种元素组成为C4H7NO2Se,Δppm 为0.1 ppm,RDB 值为3,可信度较高,又由于该化合物的m/z值相对较低,分子组成简单,其元素组成可以确定。根据Far等[15]的报道,该化合物的M+H 峰在富硒酵母中被鉴定为某些化合物的裂解产物,对应于硒同型半胱氨酸(SeHCys)的源内片段,如图2C的结构图所示。TOF MS/MS谱图(图2C)通过Formular Finder拟合得到的分子组成与一级质谱完全一致,MS Rank 和MS/MS Rank 均为1 时,其一级质谱Δppm 为0.6 ppm,RDB 值为3,二级质谱Δppm 为3.8 ppm。TOF MS/MS 谱图中响应值最高的m/z135.966 4 峰对应的裂解片段为C3H6NSe,为母离子失去羧基(—COOH)后形成碳碳双键(C====C)所得,与Far[15]和Ouerdane[16]的报道一致。且二级质谱拟合出的其他可能的碎片CHSe、C2H5Se等也证实了该结构的合理性。

图2 硒化合物C4H7NO2Se的XIC图(A)、MS图(B)、MS/MS图和结构式(C)Fig.2 Extracted ion chromatogram(XIC,A),MS spectrum(B),MS/MS spectrum and putative chemical structural formula(C)of Se compound C4H7NO2Se
2.2.3.2 C5H8O2Sem/z为180.976 2的峰经同位素过滤和质量亏损过滤后,通过人工验证确认为硒化合物,其保留时间为1.24 min,XIC图和相应TOF MS谱图如图3A、B所示。通过Formular Finder模式,发现该峰为某含硒化合物的M+H 峰,基于该M+H 峰的精确质量数和最大元素组成拟合形成其所有可能的元素组成列表。根据MS Rank 和Δppm 对所有可能的元素组成进行排序,当元素组成为C5H8O280Se时,其MS Rank 为1,Δppm 为-0.2 ppm,RDB 值为3;当元素组成为C5H8O278Se 时,其MS Rank 为1,Δppm 为0.5 ppm。该化合物的母离子在同位素80Se 和78Se 的精确质量数与理论质量数偏差均小于5 ppm,同位素丰度之比为100∶45.3,与理论离子比例偏差小于10%,表明该化合物的元素组成很可能为C5H8O2Se,但由于其元素组成列表还有其他可信度较高的可能性,最终分子式须通过TOF MS/MS谱图进一步确证。

图3 硒化合物C5H8O2Se的XIC图(A)、MS图(B)、MS/MS图和结构式(C)Fig.3 Extracted ion chromatogram(A),MS spectrum(B),MS/MS spectrum and putative chemical structural formula(C)of Se compound C5H8O2Se
该前体离子(m/z为180.976 2)相应的TOF MS/MS谱图如图3C所示,其多数碎片离子符合硒同位素分布模式,为含硒裂解碎片。将TOF MS/MS 谱图与Formula Finder 的MS/MS Details 相链接,基于二级质谱拟合出可能的母离子分子式和碎片分子式。结果表明,MS Rank 和MS/MS Rank 均为1 时,其一级质谱Δppm 为-0.2 ppm,RDB 值为3,二级质谱Δppm 为5.5 ppm,分子式与一级质谱拟合出的分子式完全一致,可以推测该化合物的分子式极有可能为C5H8O2Se。
该化合物的前体母离子进一步裂解后可能产生的碎片离子如表2 所示,根据Ward 等[20]的报道和SeMet 标样的二级谱图,相似的裂解碎片CH3Se、C2H5Se、C4H7Se 表明该化合物很可能为SeMet 的前体离子(C5H12NO2Se+)失去NH4+后的产物。其次,裂解碎片C4H7O2为Ouerdane 等[24]报道的2 种甲基硒碳水化合物M+H 峰的前体母离子C5H11O3Se+、C6H13O3Se+的裂解碎片,推测该硒化合物的母离子C5H9O2Se+为甲基硒碳水化合物的母离子C5H11O3Se+中性丢失H2O 分子,产生的一种新的甲基硒碳水化合物(Methylseleno carbohydrate),进一步验证了该化合物的结构。将该化合物的结构式导入ChemDraw,通过Show Analysis Window 分析可能的裂解碎片与TOF MS/MS谱图是否一致,结果表明该结构式满足该化合物的多数裂解碎片,如CH3Se、C2H5Se、C4H7Se、C4H5O2、C4H7O2,最后通过Check Structure 功能验证了该化合物结构式的合理性。该甲基硒碳水化合物可能的化学结构式及裂解过程如图3C所示。
2.2.3.3 C7H9NO2Se MS 质谱图中,在m/z为219.987 4 处,发现符合硒同位素分布特征的硒化合物母离子,在总离子流(TIC)图中,其保留时间为3.79 min。该硒化合物母离子在m/z219.987 4 处的同位素分布XIC 图及相应TOF MS 谱图见图4A、B。经Formula Finder 进行分子拟合后,结果表明元素组成为C7H9NO2Se 时,其MS Rank 为1,Δppm 为1.2 ppm,RDB 值为5,符合基本的化合物元素组成规律。该母离子经二级裂解后产生的TOF MS/MS 谱图如图4C 所示。基于TOF MS/MS 进行Formula Finder分子拟合,拟合出的分子式中,MS Rank 为1,MS/MS Rank 为1 的元素组成与TOF MS 谱图拟合结果一致,其一级质谱Δppm 为1.2 ppm,二级质谱Δppm 为1.6 ppm,RDB 值为5,是一个多不饱和硒化合物。

图4 硒化合物C7H9NO2Se的XIC图(A)、MS图(B)、MS/MS图和结构式(C)Fig.4 Extracted ion chromatogram(A),MS spectrum(B),MS/MS spectrum and putative chemical structural formula(C)of Se compound C7H9NO2Se
在TOF MS/MS 谱图中,m/z173.981 7 为响应强度最高的碎片,其响应强度达到2×104,符合硒的质量亏损特征,表明该硒化合物经二级裂解最可能形成m/z173.981 7 的含硒裂解碎片离子,其拟合出的分子式为C6H8NSe,与硒化合物C7H9NO2Se相比,质量数减少了46 Da,表明该化合物很可能含有1个羧基(—COOH),通过中性丢失失去1 个CO 和1 个H2O,由于该化合物的不饱和度较高(RDB 值为5),存在C6H9NSe、C4H5Se、C3H7Se等裂解碎片,表明该硒化合物存在1个环状结构且含有2个C====C键;其次,许多裂解碎片的m/z值较大,表明该硒化合物的硒存在于环状结构中。据此,通过ChemSpider 找出最可能的硒化合物为硒代苯基丙氨酸(Seleno-phenyl-alanine),导入ChemDraw,尝试断裂可能的键,通过Show Analysis Window 得到可能的碎片并与TOF MS/MS谱图拟合出的碎片相匹配,推测硒代苯基丙氨酸可能的结构及裂解途径如图4C所示。
3 结 论
本文采用HPLC-ICP-MS对富硒堇叶碎米荠酶解液中的5种硒形态进行了定量分析;将酶解液通过3 kDa 超滤管去除大分子物质和纯化后,冷冻干燥浓缩样品中的硒化合物,避免了复杂的多维色谱纯化过程;结合UPLC-ESI-Triple TOF MS 高分辨质谱鉴定出富硒堇叶碎米荠中15 种未知硒化合物,包括7种已报道和8种未报道的硒化合物,提出了3种未报道硒化合物的可能结构式。鉴定策略为:通过硒的同位素分布和质量亏损特征发现含硒化合物后,利用含硒化合物的MS、MS/MS 谱图和Formula Finder 拟合出可能的含硒化合物分子式,再通过ChemSpider 及文献搜索,找到可能的含硒化合物结构式,最后根据硒化合物的MS、MS/MS 谱图和裂解碎片采用ChemDraw 验证硒化合物结构式的可靠性。本研究为富硒植物中硒形态分析及未知硒化合物鉴定提供了思路。

