合成大麻素类新精神活性物质AB-CHMINACA的体内与体外代谢研究
李 静,彭慧飞,花镇东,王优美
(1.公安部禁毒情报技术中心,北京 100193; 2.中国刑事警察学院法化系,辽宁 沈阳110854)
近年来,多种合成大麻素和卡西酮类衍生物在全球范围内被报道发现,并在世界多地引起了社会公共安全问题。新兴的毒品较之前药效更强,并多次导致死亡案例发生。 AB-CHMINACA 为吲唑-3-甲酰胺类合成大麻素类新精神活性物质,合成大麻素原体曾被发现存在固体组织,然而因合成大麻素的广泛代谢性致其母药在尿液中罕见,故尿液中代谢产物的鉴定对临床和法庭科学分析起着至关重要的作用。 然而,因国内尚未进行有关其药理学、毒理学、安全性及代谢的相关研究,给检测吸食后尿液中的标志物带来困难,又因开展人体体内实验受限等客观因素,开展体外代谢从成本及便捷性方面来讲均更有利于评价其代谢产物及代谢途径。 本研究旨在通过体外人肝微粒体模型模拟人体代谢环境,从而确定AB-CHMINACA 的I 相代谢产物,并将其结果与1 例真实滥用者的尿液样本比对,从而确定合适的生物标志物,以进一步为临床和法庭科学鉴定提供技术依据。
1 材料与方法
1.1 仪器与试剂
戴安超高压液相系统(Thermo Scientific Dionex Ultimate 3000 RSLC)串联带有热电离喷雾离子化源(HESI)的 Q Exactive Plus 质谱仪。 待分析物 ABCHMINACA(CHNO:m/z 356.2212,由国家毒品实验室缴获物纯化)。 还原型酰胺腺嘌呤二核苷酸磷酸(NADPH)再生系统溶液A5 mL,CorningGentest,NADPH 再生系统溶液B 1 mL,CorningGentest,0.1 mol·L磷酸钾缓冲液100 mL[汇智泰康生物技术有限公司 (北京)]。混合男性肝微粒体(pHLM;蛋白质量浓度:20mg·mL)。 微粒体送达后于 37 ℃解冻、分装并储存于-80 ℃直至使用。
液质级乙腈(CHCN)、甲醇(CHOH)和甲酸(FA)(德国 Merck 公司);超纯水(德国 Merck 公司的Milli-Q Advantage A10 自动蒸馏水机制备);其他所有试剂和溶剂均为分析纯。
1.2 仪器工作条件
色谱柱为ACQUITY UPLCHSS T3色谱柱(100 mm×2.1 mm,1.8 μm),柱温为35 ℃,样品盘温度为4 ℃;流动相为乙腈(B)-0.1%(体积分数,下同)甲酸溶液(A),梯度洗脱,流量和洗脱程序如下:0.0 ~7.0 min时,70%A降至40%A;7.0 ~7.2 min时,40%A降至10%A;7.2 ~9.0min时,保持10%A;9.0~9.1min 时,10%A升至70%A;9.1~12.0 min 时,保持70%A;流量持续保持在0.4 mL·min(表1)。

表1 流动相梯度洗脱程序
超高压液相系统(Thermo Scientific Dionex Ultimate 3000 RSLC)串联带有热电离喷雾离子化源(HESI)的 Q Exactive Plus 质谱。 仪器在使用前进行正离子模式下的质量校准。 离子源条件如下:离子传输毛细管温度为350 ℃;辅气加热温度为350 ℃;鞘气流速为35 AUs;辅气流速为10 AUs;喷雾电压为 3.50 kV,S-透镜RF 水平 20.0。 MS 采用正离子全扫描模式,并选取特定质荷比(m/z)的离子作为目标物进行二级子离子扫描。代谢产物的精确分子量通过软件Thermo MetWorks 1.3 SP4.200 版本计算得出。 全扫描数据采集参数设置如下:分辨率为70 000;自动增益控制(AGC)1e;最大注入时间(IT)100ms;扫描范围m/z70~1050。目标离子的二级参数设置如下:分辨率为17 500;目标物AGC 为1e;最大IT 为50 ms;分离窗m/z 0.6;正态碰撞能量为20%、40%、60%。
1.3 方法
1.3.1 溶液配制
将AB-CHMINACA溶于甲醇制备成浓度约为5 mmol·L的溶液,吸取2 μL该溶液与初始孵育反应体系混合(由20 μL 0.1 mol·L磷酸钾缓冲液、156 μL超纯水和2 μL NADPH再生系统溶液B组成),充分涡旋混合后加入10μL HLMs(pHLM;蛋白质量浓度:20 mg·mL),涡旋混匀并将其置于37 ℃环境中预孵育3 min,再加入10 μL NADPH再生系统溶液A,涡旋混匀后将其置于37 ℃环境中孵育1 h。 1 h后,加入200μL乙腈终止反应,涡旋后,以14 000 r·min离心10 min。 吸取100 μL上清液并将其转移入玻璃进样瓶中,置于4 ℃环境下待分析。 利用TF软件Xcalibur Qual Browser 4.0.27.10版本进行系统控制和数据采集。
将空白溶液和未加母药的孵育反应系统溶液作为对照同样进行分析。同样进行合成大麻素ABCHMINACA 在未加入微粒体的孵育体系中的稳定性研究(37 ℃,摇床1 h)以确证代谢产物由微粒体的引入而生成。
1.3.2 样本前处理
将一例AB-CHMINACA 滥用者的尿液于-80 ℃条件下取出并解冻,吸取200 μL 该尿液并加入600μL 乙腈稀释涡旋后,以 14 000 r·min离心 10 min。吸取100 μL 上清液并将其转移入玻璃进样瓶中,置于4℃环境下待分析。利用TF 软件Xcalibur Qual Browser 4.0.27.10 版本进行系统控制和数据采集。
2 结果
AB-CHMINACA 体外代谢实验共发现AB-CHMINACA 的 10 种体外代谢 产物 ,AB-CHMINACA 的保留时间为6.85 min,10 种代谢产物的保留时间在1.46~8.34 min 之间,检测误差均在 2.0 ppm 以内(图 1~2,表 2),分别为甲酰胺水解代谢产物 1 种(M1)、酰胺水解代谢产物 1 种(M2)、N-脱烷基代谢产物1种(M3)、甲基丙基侧链羟化代谢产物5 种(M4~M8)、环己基甲基羟化代谢产物 1 种(M9)、N-脱烷基合并甲酰胺水解代谢产物1 种(M10)。 从羟化代谢发生的位点、数目及峰面积上来看,羟化代谢反应优先发生在甲基丙基侧链,其次是环己基甲基部分,羟化的目的是使分子极性增大,更有利于体内通过代谢后排出体外。 图 2 为母药 ABCHMINACA 及其所有代谢产物的提取离子峰色谱图。 图3 阐释了所有代谢产物的特征碎片离子及碎裂途径。 根据提取离子色谱峰的峰面积可知,体外代谢的主要代谢产物为甲酰胺水解代谢产物、甲基丙基侧链羟化代谢产物、N-脱烷基代谢产物和酰胺水解代谢产物。 经提取尿液样本中这些代谢产物的提取离子色谱图发现,甲酰胺水解代谢产物M1、甲基丙基侧链羟化代谢产物M4 和N-脱烷基合并甲酰胺水解代谢产物M10 在AB-CHMINACA 滥用者的尿液样本中也均有发现。 表2 总结了人肝微粒体体外代谢孵育实验1h 后所有代谢产物的代谢反应类型、保留时间、母离子的理论质荷比[M+H](m/z)、实测质荷比[M+H](m/z)、质量误差、化学分子式、离子碎片和峰面积。 代谢产物被标记为“M”,代谢途径如图3 所示。

图1 AB-CHMINACA 的体外代谢产物提取离子流色谱图
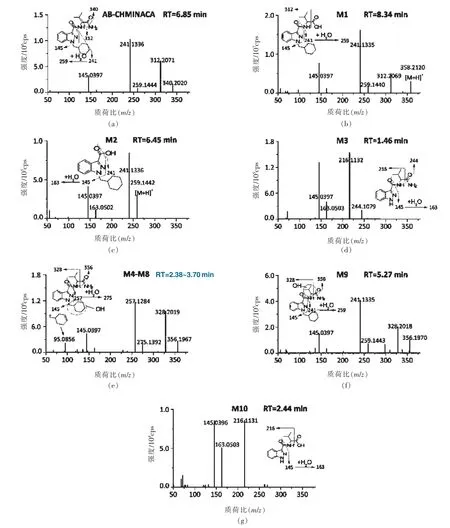
图2 AB-CHMINACA(A)和其代谢产物(B-G)的质谱图、推测结构和断裂模式

图3 AB-CHMINACA 在人肝微粒体中的代谢途径
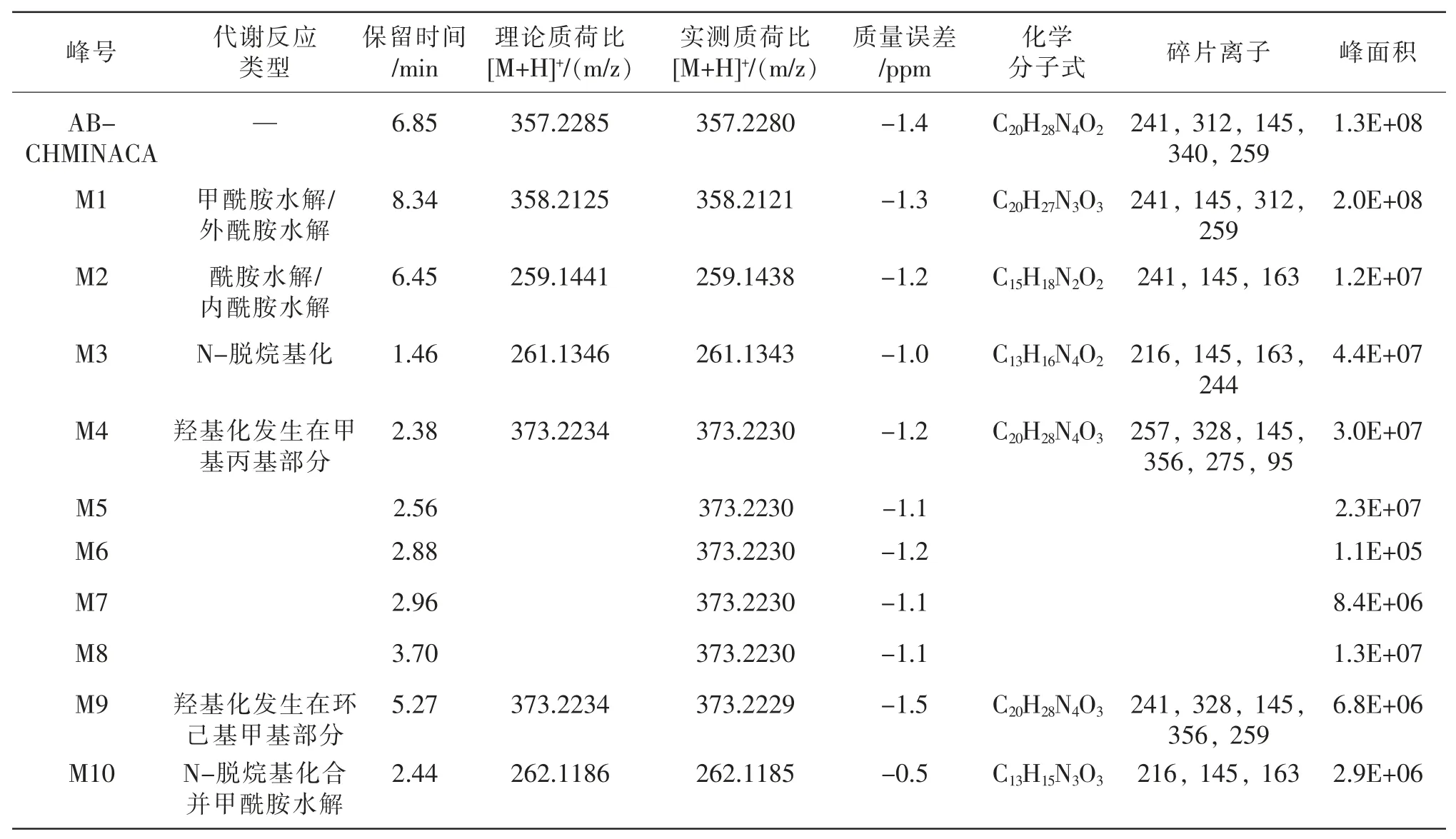
表2 AB-CHMINACA 在人肝微粒体孵育1h 后的推测代谢产物
3 讨论
AB-CHMINACA 的体内代谢研究结果显示,原药仅出现在固体组织中,在血液和尿液样本中均未被发现。 WURITA 等报道了 8 种 AB-CHMINACA代谢产物,仅有2 种非葡醛酸结合代谢产物出现在尿液样本中,分别为4-羟基环己基甲基代谢产物和甲酰胺水解代谢产物。本研究并未在尿液中发现4-羟基环己基甲基代谢产物,仅发现了甲酰胺水解代谢产物(表 3)。 ERRATICO 等的体外代谢研究发现,在肝微粒体体外代谢模型中,共检测发现了7 种单羟化代谢产物、6 种双羟化代谢产物、1 种N-脱烷基代谢产物和2 种酰胺水解代谢产物。 但在本实验的研究中并未发现双羟化代谢产物,单羟化代谢产物也仅发现了5 种,其他代谢产物的数量与种类均与该报道文献一致。 结合前期相关实验研究发现,AB-CHMINACA 滥用者的尿液样本中代谢产物的种类存在显著差异,数量从2 种至13 种不等,说明AB-CHMINACA 的代谢可能存在个体与种族间差异。从体外代谢产物的提取离子色谱图峰面积得知,AB-CHMINACA 以甲酰胺水解代谢产物、甲基丙基侧链羟化代谢产物、N-脱烷基代谢产物和酰胺水解代谢产物为主。综上,推荐AB-CHMINACA 的甲酰胺水解代谢产物(2-(1-(环己基甲基)-1H-吲唑-3-甲酰胺)-3-甲基丁酸)和甲基丙基侧链羟化代谢产物(2-(1-(环己基甲基)-1H-吲唑-3-甲酰胺)-4-羟基-3-甲基丁酸)可作为AB-CHMINACA 滥用常规尿液样本分析的生物标志物。

表3 人体体外AB-CHMINACA 代谢产物和滥用者尿液样本中代谢产物的对比
本研究建立了在肝微粒体体外代谢模型基质中与体内尿液样本中合成大麻素类新精神活性物质AB-CHMINACA 代谢产物的LC-HRMS 分析检测方法。 该方法简便快捷,为临床和法庭科学案例中滥用此新精神活性物质的检测提供了理论依据和技术支持。

