基于网络药理学探讨《温疫论》中药防治新型冠状病毒肺炎分子机制
李小阳,杨 乐,李 兵
(中国中医科学院 中医药信息研究所,北京,100700)
《温疫论》[1]是中国第一部系统研究急性传染病的医学著作。作者吴又可在《温疫论》中创立了“戾气”病因学说,强调瘟疫与伤寒完全不同,书中云:“夫瘟疫之为病,非风、非寒、非暑、非湿,乃天地间别有一种异气所感”,并称之为杂气、戾气、疠气或疫气。《温疫论》提出瘟疫的治疗法则、辨证方药对后世医学影响深远,为现代研究传染病病因病机、理法方药奠定了基础[2-4]。
中医药积极参与新型冠状病毒肺炎(COVID-19)诊疗[5],取得了良好的效果。各省市、地区针对区域和人群特点,发布了不同方案。据统计,各地防疫处方中,《温疫论》中达原饮等方剂应用最广[6]。另外,《温疫论》中频用白虎汤治疗疫邪热在气分,此次也用于各地抗疫。仝小林院士团队以寒湿疫的角度,效法《温疫论》的思路,以达原饮中的厚朴、槟榔、草果开通膜原,祛除秽浊湿,进而制定了“武汉抗疫方”[7-8]。在国家《新型冠状病毒感染的肺炎诊疗方案》中,更是多次提倡、认可了中医药在辅助治疗和预防治疗中的作用,并针对不同证型分期治疗推出了不同复方。针对湿热蕴肺证,推荐处方以达原饮为基础,加柴胡、赤芍、连翘、青蒿、苍术、大青叶等,发挥燥湿清热、疏利疫邪出表的作用;针对寒湿阻肺证,推荐处方为达原饮与平胃散加减方,具有顺气宽中、健脾化湿、和解表里的功效;针对疫毒闭肺证,以《温疫论》方达原饮、桃仁承气汤加上麻杏石甘汤、宣白承气汤等,可清肺平喘、泄热开闭;针对气营两燔证,处方以《温疫论》中两首犀角地黄汤合白虎汤为基础方,加入玄参、连翘、丹皮、黄连等,可清气凉营、熄风开窍。
随着疫情防控逐渐常态化,目前仍未发现治疗COVID-19的特效药。本研究拟通过网络药理学[9]探讨《温疫论》复方的作用机制,为抗新冠肺炎药物开发和应用提供参考。
1 材料与方法
1.1 数据规范及预处理
手工录入《温疫论》中33首处方,按照《中华人民共和国药典》(2015版)[10]将中药名称进行统一,例如:将“白芍药”统一为“白芍”,“枣仁”统一为“酸枣仁”,“真藿香”统一为“广藿香”,“白茯苓”统一为“茯苓”,“广陈皮”统一为“陈皮”,“生地”统一为“地黄”,“花粉”统一为“天花粉”,“草果仁”统一为“草果”,“山栀仁”统一为“栀子”,“天门冬”统一为“天冬”,“麦门冬”统一为“麦冬”,“丹皮”统一为“牡丹皮”,“瓜蒌实”统一为“瓜蒌”,“破故纸”统一为“补骨脂”,“车前”统一为“车前草”。并对所有用药频次、药物四气五味、归经进行统计分析。
1.2 活性成分收集与筛选
在中药系统药理学技术平台TCMSP[11](http://lsp.nwu.edu.cn/tcmsp.php)依据药物吸收、分布、代谢、排泄(Absorption、Distribution、Metabolism、Excretion,ADME)特性,设定口服生物利用度(Oral bioavailability,OB)≥30%,且类药性(Druglikeness,DL)≥0.18,筛选获取活性成分。在中医百科全书数据库ETCM[12](http://www.tcmip.cn/ETCM/index.php)检索,补充活性成分后,构建中药化学成分数据库。因矿物类和动物类药材的特殊性,故本文方法暂未将石膏、龟甲等纳入分析范围。
1.3 候选靶点库的构建
在TCMIP(http://www.tcmip.cn/TCMIP/index.php)的中药靶点预测功能模块,通过化学成分二维结构与美国食品药品管理局(FDA)上市药物相似性比对[12],选择相似性分数≥0.8的靶点作为候选靶点。
1.4 COVID-19靶点收集
2020年3月,David E.Gordon等[13]94位专家在NATURE发表了一篇新冠病毒SARS-CoV-2蛋白与人蛋白相互作用筛选潜在治疗靶点的文章,研究人员在人类细胞中克隆、标记和表达了SARS-CoV-2的29个蛋白中的26个,并通过亲和纯化质谱法(AP-MS)共鉴定出332种高度可信的与病毒蛋白相互作用的人蛋白(PPIs),其中有66种可药物化的靶点。论文经发表后被引用已近600次。本文中使用的COVID-19靶点来源于文章公布的SARS-CoV-2蛋白互作图谱数据中332个与SARS-CoV-2关联的人类靶标数据。
1.5 复方-药物-活性成分-靶点-疾病网络构建
利用Cytoscape 3.7.2[14]网络可视化软件,构建《温疫论》“复方-药物-活性成分-靶点-疾病”网络。
1.6 潜在靶点通路分析
本研究使用Metascape[15](https://metascape.org/gp/index.html)进行靶标的功能富集分析和信号通路分析,并构建网络筛选关键靶标节点。GO富集分析主要涵盖生物学的3个方面:生物过程(BP)、分子功能(MF)及细胞组分(CC)。京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)可对药物作用靶点或差异表达基因进行信号通路分析。
2 结果
2.1 数据规范及预处理
2.1.1 中药频次统计 纳入分析的33例处方中,单味药累计用药195次,共包含单味中药70种。单味药最高使用次数16次,最低使用1次,使用频次前十的中药为:白芍、甘草、当归、大黄、知母、陈皮、地黄、厚朴、柴胡、黄芩。具体情况见表1。

表1 《瘟疫论》中药频次统计
2.1.2 中药属性统计 《温疫论》方剂中所用药物药性主要为温、微寒、寒、平,其中温性药物所占比例最高为30%,其次为微寒、寒、平,分别为22%、21%、17%;所用药物五味主要为甘、辛、苦,其中甘味药所占比例最大为28%,其次为辛、苦所占比例分别为26%、24%;所用药物中归肺经药物所占比例最大为20%,其次为脾、胃、肝、肾、心经,占比分别为15%、14%、13%、11%、11%。见图1。

图1 中药属性统计
2.2 药物活性成分及靶点
经过筛选和删除重复项后,以药物为单位,涉及活性化合物来源及预测靶点个数见表2。

表2 药物活性成分及靶点数
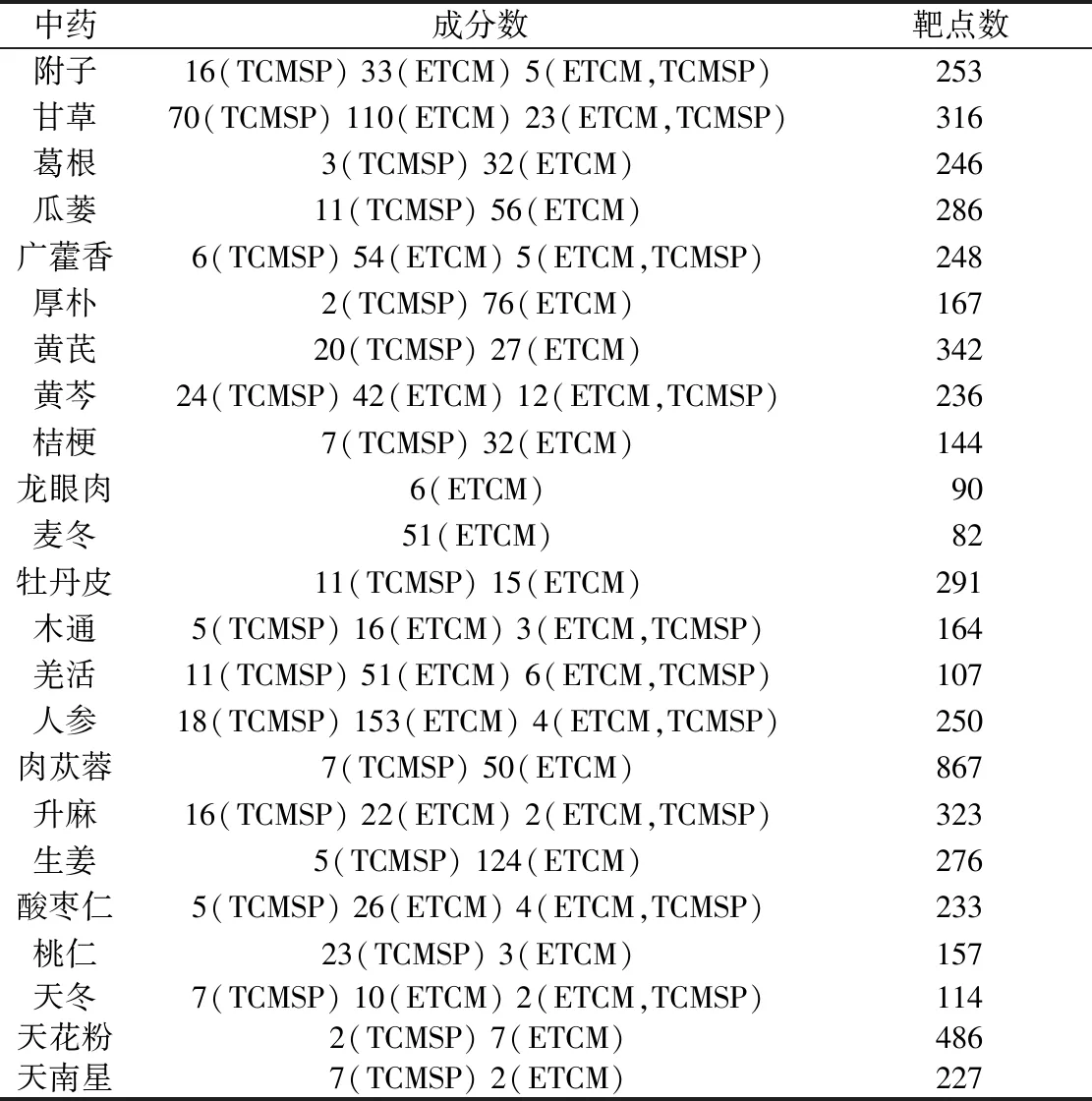
续表2

续表2
2.3 “复方-药物-活性成分-靶点-疾病”网络构建
由于涉及的活性化合物及靶点数较多,将网络中不含药物靶标的化合物及其他靶点剔除,简化后的网络包含480个节点,1 578条边(图2)。其中方剂节点33个,以圆形代替;药物节点70个,以三角形代替;化合物节点342个,以菱形代替;病毒靶点节点34个,以方形代替;边表示节点之间的相互作用关系(见图5)。由图中可以看出,中药存在同一化合物作用于多个靶点和多个化合物作用于同一靶点的现象,体现了中药多成分多靶点共同作用的内涵。将各复方中中药、活性成分及其作用靶点信息作为节点(node)直接导入,以边(edge)作为中药、成分和靶点的相互关系,每个节点的重要性则通过拓扑参数度数进行评估。节点度值为与节点相连边的数量,度值越大,表明该节点在网络中越重要(degree),一般认为节点度值大于该类节点度值中位数2倍的节点为网络中的关键节点。根据网络拓扑学性质度值排序后,符合上述要求的关键药物节点12个及其度值分别为:黄芩(52)、甘草(50)、大黄(37)、白芍(34)、瓜蒌(29)、紫苏子(29)、柴胡(28)、槟榔(25)、茵陈(24)、大枣(23)、当归(20)、茯苓(20);关键化合物节点45个,前15名及其度值分别为豆甾醇(21)、三磷酸腺苷(20)、棕榈酸(19)、谷甾醇(18)、十八酸(15)、槲皮素(15)、亚油酸(13)、黄芩苷(13)、腺苷(12)、胡萝卜甾醇(12)、肉豆蔻酸(11)、10,13-二十碳二烯酸(11)、鸟苷(10)、二十四烷酸(10)。

图2 “复方-药物-活性成分-靶点-疾病”网络
2.4 “靶点-功能-通路”网络分析
由于靶点数较少,将minioverlap值设置为1,导出Metacape分析结果至Cytoscape 3.7.2软件,构建“靶点-功能-通路”关联网络。Metascape中GO功能富集分析得到GO条目625个(P<0.01),其中生物过程(BP)条目476个,细胞组成(CC)条目54个,分子功能(MF)条目95个,分别占76%、9%、15%,KEGG通路富集筛选得到56条信号通路(P<0.01),见图3。根据拓扑学参数,筛选网络中同时满足BC、CC、degree值大于均值的10个关键靶点,为RHOA、HMOX1、PRKACA、ACSL3、SCARB1、ARF6、PPT1、HDAC2、RAB7A、POR。

图3 “靶点-功能-通路”关联网络
Metascape的Mcode聚类结果分别筛选出GO功能富集分析中三个方面及KEGG中排名靠前的功能和通路,结果见图4。

注:A:细胞组成;B:分子功能;C:生物过程;D:KEGG。图4 GO与KEGG分析
3 讨论
分析《温疫论》复方中药物的性味归经发现,复方重点作用于肺经、脾经,辛味、苦味和甘味药比例最大,药物温性、平性和寒性各有分布,该结果与《新型冠状病毒感染的肺炎诊疗方案》推荐复方的用药规律一致[16]。根据统计结果显示,《温疫论》中高频用药包括白芍、甘草、当归、大黄、知母、陈皮、地黄、厚朴、柴胡、黄芩。其中黄芩、甘草、大黄、白芍、柴胡、当归为“复方-药物-活性成分-靶点-疾病”网络中筛选的关键药物节点;豆甾醇、三磷酸腺苷、棕榈酸、谷甾醇、槲皮素、亚油酸、黄芩苷、腺苷、胡萝卜甾醇、肉豆蔻酸、10,13-二十碳二烯酸、鸟苷为关键化合物节点。
黄芩为COVID-19中医药治疗用药组方中最常用的药物[17],典型应用如清肺排毒汤、达原饮、小柴胡汤等方剂及中成药。研究表明,黄芩苷和黄芩素是非共价、非多肽性的SARS-CoV-2 3CLpro抑制剂,它们可以有效抑制新冠病毒中一种重要的蛋白酶3CLpro的复制[18]。根据李婧等[19]的研究,柴胡、甘草、金银花等中药也含有较多潜在抗SARS-CoV-2活性成分。马婧等[20]采用DS中CDOKER对TCMD数据库中成分进行分子对接虚拟筛选,基于PLP靶点筛选得到的中药为白芍、当归、瓜蒌等,宗阳[21]和龚宇晟等[22]分子对接结果显示豆甾醇、槲皮素、谷甾醇等化合物与COVID-19推荐用药的亲和力相似。
通过“靶点-功能-通路”网络,筛选出10个关键靶点为RHOA、HMOX1、PRKACA、ACSL3、SCARB1、ARF6、PPT1、HDAC2、RAB7A、POR。血红素加氧酶(HMOX1)是一种可催化血红素降解过程中的关键酶,具有细胞保护作用,研究证明[23]过量的游离血红素可诱导细胞凋亡。HMOX1在肺中高度表达[24-25],并且已被证明对小鼠中有介导白细胞介素10(IL-10)的抗炎作用,还牵涉包括心肌梗死、糖尿病、慢性阻塞性肺疾病(COPD)等多种病理状态[26-27]。它的上调已被证明具有抵抗HIV、DENV、HCV和IAV感染产生的氧化应激的保护作用[28]。由于SARS-CoV-2感染会严重影响呼吸道的侵袭性炎症反应,因此在病毒感染期间进一步探索HMOX1功能将有助于阐明病毒的发病机理和可能的治疗方法[29];RHOA是小型GTPases Rho家族的成员,激活对于肺损伤至关重要,也是TNF信号传导途径和MAPK信号传导途径中最重要的蛋白之一。He B[30]的研究证明抑制RHOA是治疗急性肺损伤有效的方法;Pinto BGG等[31-32]应用系统生物学方法证实包括HDAC2等与组蛋白修饰相关的基因是人肺ACE2上调的潜在靶点;Ghosh S[33]研究发现RAB7A基因的缺失可以通过改变内质体的运输,将ACE2受体隔离在细胞内,从而减少病毒进入;Ackerman EE[34]利用SARS-CoV-2-宿主蛋白相互作用网络识别在感染后驱动细胞整体行为中具有独特作用的蛋白质,认为SCARB1等预测出的8种蛋白质有可能成为病毒特异性药物靶点,并应被优先用于药物再利用。
基于冠状病毒的复制过程,目前针对ACE2抑制剂、核苷类似物、膜融合抑制剂、蛋白酶抑制剂(HIV蛋白酶、TMPRSS2丝氨酸蛋白酶、3Clpro蛋白酶)等不同靶点成为研发筛选抗SARS-CoV-2潜在治疗药物的主要策略[35]。
《温疫论》复方通过调控Ras蛋白活性、GTPase活性、GDP结合和GTP结合通路,影响ACE2在细胞中的表达。Lukassen S等[36]研究了ACE2和TMPRSS2的表达水平及其在肺组织中跨细胞类型的分布。在节段性支气管分支中,ACE2主要在瞬时分泌细胞中表达,这些细胞显示出丰富的与RHO GTP酶功能和病毒过程相关的途径。RHO-GTPase激活CIT和病毒调节途径,即与膜重塑或免疫系统相关的过程,在瞬时分泌细胞中强烈富集。Ras蛋白也是一种gtpase,作为信号通路的分子开关调节细胞增殖、存活、生长、迁移、分化或细胞骨架动力学。Ras蛋白通过在不活跃的GDP结合态和活跃的GTP结合态之间循环传递来自细胞外生长因子的信号。
核苷酸是多种生命活动所必须的有机小分子,除嘌呤核苷酸合成和分解代谢过程中的部分酶参与病毒感染的发生发展外,还可以通过对代谢酶的竞争性抑制作用干扰或抑制嘌呤核苷酸的合成[37]。目前的研究中有大量重点放在核苷酸抑制剂上,如Sofosbuvir,Ribavirin,Remidisvir,IDX-184等,可以竞争病毒RNA依赖性RNA聚合酶(RdRp)活性位点,渗透到病毒新合成的RNA链中,从而中断了病毒基因组的合成[38]。此外,《温疫论》复方还参与了aminoacyl-tRNA、protein disulfide oxidoreductase、S-adenosylmethionine-dependent methyltransferase等多种连接酶、转移酶活性以及辅酶的合成等功能富集,并在嘌呤核苷酸合成与代谢功能、癌症通路显著富集,示意了复方通过影响核苷酸代谢、酶活性调节的抗COVID-19作用。
凝血功能(Blood Coagulation、Response to Wounding、Wound Healing)是GO分析生物过程中的重要组成,涉及GGCX、HDAC2、PLAT、PRKACA、PRKAR2B几种基因调控。几项研究报告了住院COVID-19患者的心血管并发症和静脉血栓形成事件的发生率增加。研究发现与病毒蛋白NSP7、NSP13、E、M、N、ORF9C和ORF8直接相互作用的10种宿主蛋白参与了凝血途径,并利用这些蛋白作为CoVex的分析起点确定了可以由GGCX编码的维生素K依赖的γ-谷氨酰羧化酶和由PLAT编码的组织纤溶酶原激活剂作为潜在的药物靶点[39]。基于RNA病毒可以通过与依赖于Toll样受体7(TLR7)的机制激活内体NADPH氧化酶的理论,研究推测与COVID-19相关的高血栓并发症的发生率可能反映了血管内皮细胞的病毒感染,血管内皮细胞表达使SARS-CoV-2能够侵袭细胞的ACE2蛋白。SARS-CoV-2整合入内皮细胞后,各种促炎刺激可以通过诱导组织因子(TF)的腔内内皮表达来促进血栓形成,该因子与循环凝血因子VII相互作用以触发外源性凝血。这些刺激引起TF表达的信号传导机制需要激活NADPH氧化酶,而不是驱动TF基因诱导转录的NF-кB转录因子的激活。将单链RNA病毒吸收到细胞内体后,它们会通过RNA响应的Toll样受体7刺激内体形成和NADPH氧化酶复合物的激活。因此建议内皮细胞SARS-CoV-2感染引起TF的表达,其取决于内体NADPH氧化酶的活化。抑制内体NADPH活性的药物可能具有减轻与COVID-19相关的血栓形成风险升高的实际潜力[40]。
在关于COVID-19重症患者血清的蛋白质组学和代谢组学变化研究中,由于干扰素会在病毒感染期间改变尿素循环活性,由此导致了多种代谢产物的失调,COVID-19患者血清中的氨基酸及其衍生物与健康对照相比显著降低。Cellular amino acid metabolic process(Ammonium ion metabolic process)是其中一重要生物过程。代谢组学分析表明,SARS-CoV-2感染对血清氨基酸水平有重大影响。参与SARS-CoV-2感染的另一个重要途径是氨酰基tRNA生物合成。该途径在响应危险信号中起重要作用,并调节针对病毒感染的免疫力[41]。TCA循环导致富马酸和琥珀酸的显著调节结果,与短链脂肪酸上调有关的丁酸酯代谢也参与其中。
此外,Fatty acid metabolism、Fatty acid degradation是KEGG中另外的重要通路,此前已有研究表明添加花生四烯酸可抑制HCoV-229E和MERS-CoV复制[42-43]。高水平的脂肪酸可能是宿主抵抗病毒的防御机制,但同时可能引起炎症。最近的研究发现COVID-19患者的血清显示出酰基肉碱和游离脂肪酸的水平发生了显著变化,脂质代谢重编程在病毒复制中起着重要作用。研究结果显示COVID-19患者甘油磷脂(PC,PE和PI)的下调和溶血磷脂(LPC和LPE)、花生四烯酸和油酸的上调[44]。GO分析显示,protein-lipid complex subunit organization、plasma lipoprotein particle organization、regulation of plasma lipoprotein particle levels高度富集,且cellular component显示定位集中在membrane raft、membrane region、membrane microdomain。研究验证了血浆脂蛋白异常是SARS-CoV-2感染的多器官病理学特征。由于鞘脂与甘油磷脂是膜细胞的重要组成部分,并调节如生长调节和炎症反应等过程,减少的磷脂会削弱感染并限制病毒的进入[45]。因此,磷脂代谢可能是针对COVID-19病毒感染的治疗干预的潜在目标。
综上所述,本研究结合构建“复方-药物-化合物-靶点-疾病”网络,分析筛选《温疫论》中复方防治COVID-19的关键药物和关键成分,通过豆甾醇、三磷酸腺苷、槲皮素、黄芩苷等活性成分,作用于34个人类靶标,并通过多途径发挥作用,通过若干重要信号通路调控内分泌系统、免疫系统、信号转导翻译等生物学进程,为进一步研究《温疫论》中复方应用及中药防治COVID-19提供参考。

