一种新型土壤改良剂的制备及性能研究*
黄 强
(1.厦门大学嘉庚学院环境科学与工程学院,福建 漳州 363105;2.河口生态安全与环境健康福建省高校重点实验室,福建 漳州 363105)
近年来,由于农作过程中长期不合理使用化肥,造成了土壤板结、土壤肥力下降、土壤结构破坏等问题[1],导致土壤水肥流失严重,降低土地生产力,极大地阻碍了生态环境与农林牧业生产的良性循环[2-5]。土壤改良剂可以有效改善土壤肥力,但存在用量大、成本高、作用周期短、施用方法效果低等问题[6]。我国是甘蔗生产大国,每年都有大量的废弃蔗渣产生[7],蔗渣含有丰富的纤维素、半纤维素、木质素,并且含有少量蛋白、淀粉和可溶性糖[8],其中纤维素是合成高吸水性树脂的三大原料之一,其耐盐性和抗生物降解能力较好,天然纤维素的高度结晶结构使大部分羟基处于氢键缔结状态,限制了其吸水能力,但通过接枝、交联等化学方法可破坏这种结构来增强其吸水能力和吸水后的凝胶强度[9]。因此,将蔗渣应用于土壤改良剂的开发中,不但能够大大提高土壤改良剂的吸水和保水性能,使其改善土壤环境,还能更有效地利用蔗渣,达到变废为宝的目的[10]。高效菌群能够快速分解有机物[11],通过驯化后的高效菌群可以有效利用肥料中的营养元素并且结合吸水树脂的作用缓解土壤板结,达到改善土壤的作用[12]。现有研究中,多数学者旨在通过土壤改良剂提高土壤的保水能力或者保肥能力,但制备的土壤改良剂大多性能较单一,适用范围小[13-15],为此本研究尝试以废弃的蔗渣和驯化的高效菌粉为材料制备一种适用范围广、作用周期长,符合实际需求的廉价新型土壤改良剂,并对其性能进行研究。
1 材料与方法
1.1 实验材料
实验材料:蔗渣,取自漳州当地农村菜市场;高效菌株,从漳州某污水处理厂浓缩池底泥经深度分离筛选后获得;2种当前市售的土壤保水剂,分别记为保水剂A、保水剂B。
驯化培养基:尿素 2 g,腐殖酸 5 g,磷酸二氢钾 1 g,氯化钠 5 g,琼脂 20 g,去离子水 1 000 mL,pH调至7.4~7.6。
富集培养基:蛋白胨 10 g,牛肉膏 5 g,腐殖酸 1 g,氯化钠 5 g,去离子水 1 000 mL,pH调至7.4~7.6。
实验仪器:IRAffinity-1型傅立叶红外光谱仪(日本岛津);EVO18型电子扫描显微镜(SEM,德国Zeiss Sigma);ICE3300型原子吸收光谱仪(美国赛默飞世尔);GS945W型高压灭菌锅(美国Zealway);ALPHA1-2 LD plus型冷冻干燥仪(德国Christ)。
1.2 实验方法
1.2.1 土壤改良剂的制备
(1) 纤维微晶的制备。蔗渣经水洗、干燥后粉碎过100目筛得到蔗渣粉,称取20 g蔗渣粉加入100 mL磷酸(5 mol/L)和硝酸(5 mol/L)混合溶液中,80 ℃的水浴条件下糊化消解2~4 h,弃去上清液,把底部的糊状纤维放置在300目筛网上,用去离子水多次冲洗至中性取出,再加入200 mL 5 mol/L的氢氧化钾溶液,在60 ℃水浴加热脱脂1~3 h,弃去上清液后再将底部糊状纤维放置在300目筛网上,用去离子水冲洗至中性,干燥后即为蔗渣纤维微晶,装袋后备用。
(2) 丙烯酸钾溶液的制备。将100 g丙烯酸加入到三口烧瓶中,在不断搅拌和冰浴条件下缓慢滴加93 mL质量分数为50%的氢氧化钾溶液,制备成中和度为60 %的丙烯酸钾溶液。
(3) 高效菌种的筛选与保存。将污水处理厂浓缩池底泥自然风干,取10 g放入盛90 mL无菌水并带有玻璃珠的三角烧瓶中,振摇约20 min使底泥与水充分混合,底泥中的微生物细胞充分分散。用1 mL无菌吸管从中吸取1 mL悬浊液加入盛有9 mL无菌水的试管中充分混匀制成稀释度为10-1的混合溶液,以此类推制成稀释度为10-2、10-3、10-4、10-5的混合溶液,用无菌移液管移取0.1 mL稀释度为10-3、10-4、10-5的混合溶液加在驯化培养基上,然后用无菌玻璃涂棒进行均匀涂布后,放置在37 ℃的恒温箱中培养一定时间,待长出菌落后,再次纯化和驯化,经过3次纯化和驯化后即得到高效土壤分解菌株,通过富集培养基将土壤分解菌株进行扩增,通过离心、洗脱和冷冻干燥技术制成菌粉。菌粉使用前添加至pH为7.4的磷酸缓冲液中,制成菌悬液。
(4) 土壤改良剂制备。取0.1 g蔗渣纤维微晶与60 mL丙烯酸钾溶液,加入0.015 g过硫酸铵为引发剂,0.009 g N,N-亚甲基双丙烯酰胺为交联剂,在60 ℃水浴下搅拌,待溶液成黏稠状降低反应温度至40 ℃,缓慢加入1 mL菌液继续搅拌1 h,取出后静置陈化2 h形成凝胶,用无水乙醇冲洗数次后,放于真空干燥箱中40 ℃下干燥8 h,粉碎后制得土壤改良剂。
1.2.2 土壤改良剂的表征
采用傅立叶红外光谱仪对制得的土壤改良剂表面官能团进行扫描分析;采用SEM对土壤改良剂的表观形貌进行观测。
1.2.3 吸水性能的测定
为考察土壤改良剂与蔗渣吸水性能的差异性,称取土壤改良剂和未处理的蔗渣各0.10 g置于干燥的300目尼龙纱布袋中,分别浸没到1 000 mL去离子水或氯化钠溶液(质量分数0.1%)中,定时取样测定吸水后土壤改良剂和蔗渣质量,按照式(1)计算吸水倍率。
(1)
式中:Qt为样品在吸水t时刻的吸水倍率;Gt为样品在吸水t时刻后的总质量,g;m为样品初始质量,g。
将在去离子水中充分吸水饱和的土壤改良剂和保水剂放置于40 ℃真空干燥箱中干燥8 h,干燥后重复进行吸水实验,考察土壤改良剂在7次重复使用中的吸水倍率变化。
1.2.4 释水性能的测定
将在去离子水中充分吸水饱和的土壤改良剂和保水剂取出,常温下放置于干燥培养皿中22 d,每隔12 h称重1次,计算吸水倍率变化。
1.2.5 土壤改良剂动态保肥能力的测定
为考察土壤改良剂在动态作用下的保肥能力,设计过滤吸收测试实验,为了减少土壤中的养分对于渗滤液的影响,以石英砂来替代真实土壤进行实验。
称取500 g经水洗干燥后的石英砂放置于底部套有300目尼龙纱网的塑料圆管中,分别加入土壤改良剂0、0.02、0.05、0.10、0.15、0.20、0.30、0.40、0.50 g,将200 mL营养液(TN、TP、总钾(TK)质量浓度均为20 mg/L)缓慢滴加到石英砂中,收集全部滤液,测定滤液体积及滤液中TN、TP、TK浓度,以不添加土壤改良剂的石英砂为空白组,计算土壤改良剂在不同添加量下对各元素的净吸收量。
1.2.6 土壤改良剂对金属离子的吸收能力测定
土壤中含有大量金属离子,若没有植物吸收,容易渗透污染地下水体[16],倘若土壤改良剂可以有效存储土壤中的金属离子供植物吸收,能起到缓解地下水污染以及促进植物生长的作用[17]。为考察土壤改良剂吸收金属的能力,分别配置含有Fe、Cu、Zn、Ni、Pd、Cr的金属离子溶液,各金属离子质量浓度均为10 mg/L,将0.2 g土壤改良剂加入各金属离子溶液中,吸胀12 h后用300目的尼龙网进行过滤,采用原子吸收分光光度法测定滤液中各金属离子的浓度,根据式(2)计算土壤改良剂对各种金属离子的吸附率。
P=(c0V0-c1V1)/c0V0×100%
(2)
式中:P为金属离子吸收率,%;c0为溶液中金属离子初始质量浓度,mg/L;V0为溶液初始体积,L;c1为吸胀后溶液中金属离子质量浓度,mg/L;V1为吸胀后滤液体积,L。
1.2.7 土壤改良剂的土壤降解实验
参照文献[18]中的方法将土壤改良剂制成降解膜片,把降解膜片垂直埋入土壤中降解100 d,并保持土壤疏松及瓶内外空气循环流通,每隔20 d取样测定降解膜片中土壤改良剂质量变化,计算降解率。
2 结果分析与讨论
2.1 土壤改良剂的表征结果
2.1.1 红外光谱分析
制得的土壤改良剂红外光谱见图1。由图1可见,土壤改良剂在3 044 cm-1处出现O—H伸缩振动吸收峰,在1 732 cm-1附近出现酰胺基C=O伸缩振动吸收峰,在1 540 cm-1处出现NH2的伸缩振动吸收峰,在1 455 cm-1处出现C—O的伸缩振动吸收峰,此外,在1 055、1 195 cm-1分别出现磺酸基的对称伸缩振动和不对称伸缩振动吸收峰,而在989、847、661、528 cm-1处均出现了不同的取代峰,初步表明各单体已经在交联剂的作用下形成了交联网状大分子,是具有众多亲水基团的共聚体。
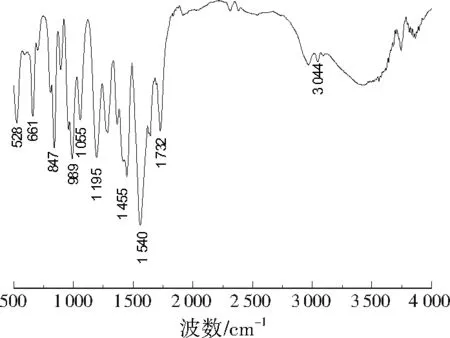
图1 土壤改良剂的红外光谱
2.1.2 土壤改良剂的微观形貌
图2为制得的土壤改良剂在SEM中放大30 000倍的扫描结果,可以看出纤维微晶呈白色条状分布在土壤改良剂中,纤维微晶外有共聚体紧密包裹,纹理清晰,表明制得的土壤改良剂并非物理性填充,而是单体间发生聚合发应,生成了新的共聚体。
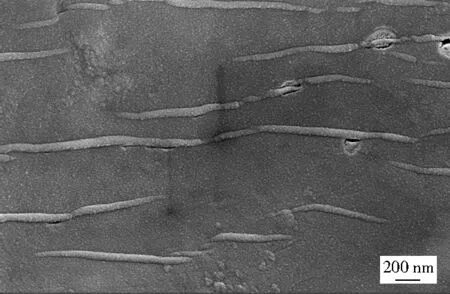
图2 土壤改良剂SEM图
2.2 土壤改良剂保水性能分析
2.2.1 与蔗渣的吸水性能对比
土壤改良剂与蔗渣在去离子水和氯化钠溶液中的吸水性能见图3。由图3可见,土壤改良剂在去离子水和氯化钠溶液中的吸水倍率均明显高于蔗渣。在去离子水中,土壤改良剂在前40 min的吸水倍率增速较快,吸水40 min后吸水倍率增速放缓,但仍然呈缓慢上升趋势,而在氯化钠溶液中,土壤改良剂的吸水倍率则一直呈现较稳定的增速。吸水100 min后,土壤改良剂在去离子水和氯化钠溶液中的吸水倍率分别达395.55、104.35。蔗渣在两种溶液中的吸水倍率增速较平缓,较快达到吸水饱和,吸水100 min后,蔗渣在去离子水与氯化钠溶液中吸水倍率分别为266.33、50.55。通过以上分析可知,土壤改良剂吸水持续时间和吸水性能较蔗渣有明显提升,具有潜在的应用价值。
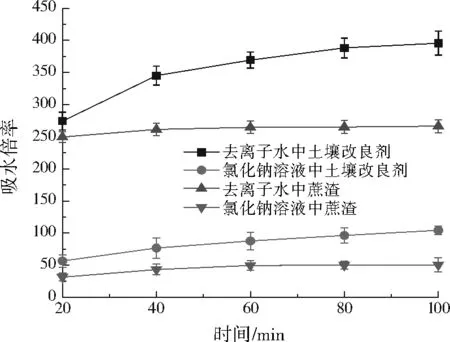
图3 土壤改良剂与蔗渣吸水倍率变化
2.2.2 与保水剂的吸水性能对比
将土壤改良剂与两种市售保水剂分别在去离子水与氯化钠溶液中充分吸水饱和,3种材料吸水倍率对比见表1。可以看出,本研究制备的土壤改良剂在去离子水与氯化钠溶液中的吸水倍率分别为462.07、115.47,明显优于2种市售保水剂,其在去离子水和氯化钠溶液中吸水倍率分别为保水剂A的1.53、1.88倍,为保水剂B的1.59、1.99倍。刘颖等[19]通过γ射线引发合成新型农林保水剂,其在纯水和氯化钠溶液中的吸水倍率分别为437、61,与本研究制备的土壤改良剂相比,该保水剂在去离水中的吸水性能相当,但在氯化钠溶液中的保水效果相对逊色,主要是由于传统的高分子聚合物通过交联反应生成分子量更大的聚合物,虽然吸水能力有所提升,但相应的反应点位减少,而纤维微晶的多糖单体较传统高分子聚合物增加了反应点位,提高了对离子的吸附量,这与黄占斌等[20]的研究结论相符。

表1 土壤改良剂与保水剂吸水倍率比较
2.2.3 土壤改良剂重复吸水性能
将土壤改良剂与2种保水剂进行重复吸水实验,3种材料在重复使用7次后吸水倍率变化见表2。在重复吸水实验中,土壤改良剂在重复使用5次后的吸水倍率仍然达290.14,接近保水剂A和保水剂B初始的吸水倍率水平,而保水剂A和保水剂B经过多次重复吸水后,吸水性能骤降,特别是保水剂A,5次重复吸水后吸水倍率降至100以下,保水剂B在6次重复吸水后吸水倍率也降至100以下,而土壤改良剂在重复吸水7次后吸水倍率仍然保持在170左右,表明本研究制备的土壤改良剂可再生性强,具有较强的推广应用价值。
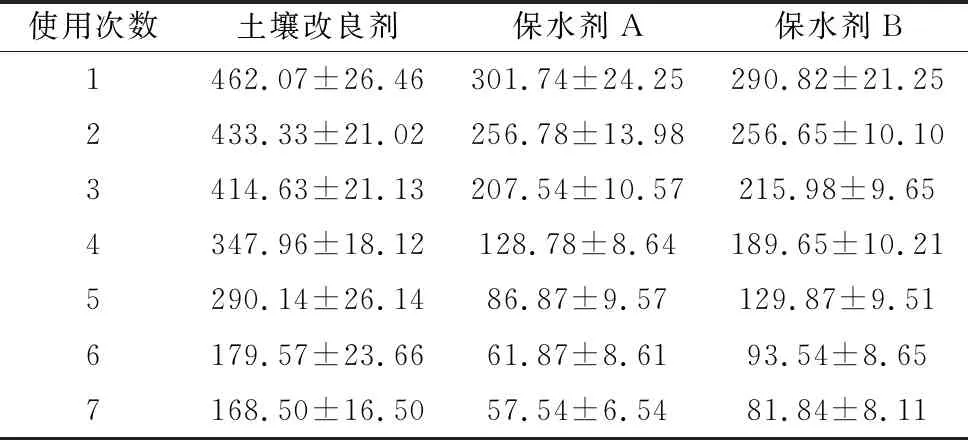
表2 土壤改良剂与保水剂重复吸水倍率比较
2.2.4 释水性能分析
图4为土壤改良剂和2种保水剂在释水过程中的吸水倍率变化。由图4可见,土壤改良剂在前48 h的吸水倍率急剧减少,即释水速度最大,而后其释水速度有所减缓,实验进行528 h后,土壤改良剂吸水倍率仍在100左右。保水剂A和保水剂B的释水趋势较为一致,吸水倍率在前240 h均保持较平稳的下降趋势,释水速度较为稳定,240 h后释水速度放缓,吸水倍率慢慢趋于平稳,528 h后两种保水剂的吸水倍率都降至25左右,约为土壤改良剂的1/4,表明本研究制备的土壤改良剂在充分吸胀后,通过物理化学生物作用对水分子结合力更强,即“锁水”能力较传统保水剂强,能够在较长时间内供应植物水分,特别在干旱地区,这种长期的保水性能更具有现实意义。
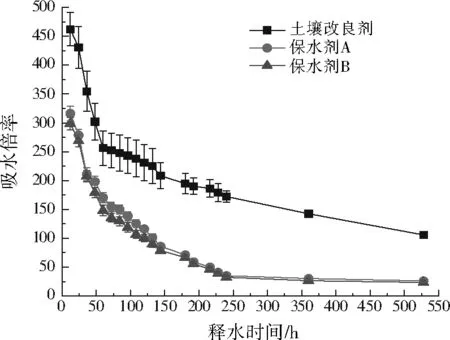
图4 土壤改良剂与保水剂在释水过程中吸水倍率变化
2.3 土壤改良剂的动态保肥性能
土壤改良剂在动态保肥能力测定中对TN、TP、TK的净吸收量见表3。可以看出,土壤改良剂在不同投加量下对于TN和TK的净吸收量均为正值,且随着投加量的增加,TN、TK净吸收量也不断增加,表明其对N、K元素具有较强的吸附能力。然而对于TP,土壤改良剂的投加量为0.02~0.15 g时,TP净吸收量为负值,当投加量在0.20 g时TP净吸收量为正值,并且随着土壤改良剂投加量的增加,TP净吸收量逐渐增加,这主要是由于当土壤改良剂投加量较小时,环境体系中的离子发生竞争性吸附,分子量较小且带正电荷的胶体先被吸附,并且土壤改良剂负载的高效菌自身含有P元素,在动态添加营养液时有部分的P元素被释放出来,导致TP净吸收量较空白组低,当投加量增加后,土壤改良剂锁水固肥能力大幅提升,因此对TP的净吸收量也随之提高。土壤改良剂对TK净吸收量最大,这主要是因为K+在溶液中的电离能力强,极易与土壤改良剂中的亲水基团反应,从而被固定。刘海林等[21]通过土壤培养和土柱淋溶试验,研究了添加聚丙烯酸钠的保水缓释肥料在土壤中的保水性能和养分缓释效果,结果表明当保水缓释肥料投加量为6%(质量分数)时保水性能和养分缓释效果最佳,而本研究的土壤改良剂在投加量为0.50 g(折合质量分数0.1%)就有十分显著的保肥效果,远低于文献[21]中保水缓释肥料的投加量,可见该土壤改良剂投用具有一定经济性。
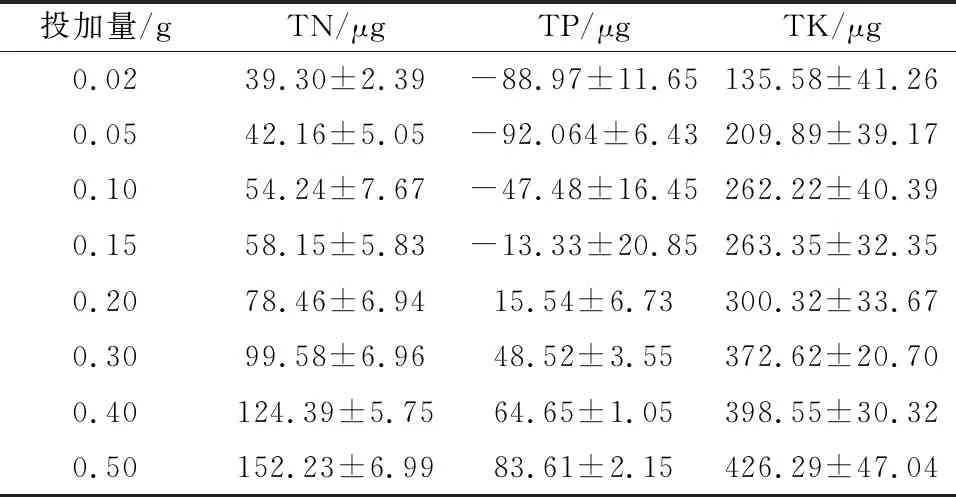
表3 不同投加量下土壤改良剂对于TN、TP、TK的净吸收量
2.4 土壤改良剂对金属离子的吸收能力
在金属离子吸附实验中,本研究制得的土壤改良剂对6种金属离子吸收能力为Cr>Fe>Ni>Cu>Pb>Zn,其中对于Cr的吸收率为55%,而对于Fe、Ni、Cu的吸收率分别为46%、40%、28%,对Pb的吸收率为25%,对Zn的吸收率最低,仅为9%。可以看出,土壤改良剂能够将金属离子固定住,使其不易流失,在植物需要的时候及时供给“储存”的微量元素和必需元素,具有一定的应用价值。张志成等[22]研究了金属离子的加入对交联化羧甲基纤维素(CCMC)保水剂的影响,发现随着金属离子价态增大,CCMC对离子吸附量增加。PING等[23]研究了不同高分子聚合物保水剂在吸水和吸附阳离子后的红外光谱,结果表明保水剂亲水性强弱不仅与基团种类有关,也与亲水基团和阳离子结合形成的离子对电离度有关;HOSNY等[24]结合傅立叶红外光谱与磁电子光谱发现Ni2 +、Cu2 +与羧甲基纤维素钠(CMC)中羧基都是以单原子螯合方式结合,同时连接CMC上的一个羟基。由上述学者研究成果可知,金属离子价态、离子对电离度等都对土壤改良剂吸附金属离子产生影响,本研究的金属离子中Cr价态最高,其次为Fe,因此土壤改良剂对Cr吸附量最大,Fe吸附量次之,过渡金属电离度排序为Ni>Cu>Zn,土壤改良剂对这3重金属离子的吸附率与电离度排序一致,其对Pb的吸附率介于Cu和Zn之间,这可能是Pb作为主族金属元素与其他过渡金属存在不同的吸附机理,具体有待于后续深入研究探讨。
2.5 土壤改良剂的土壤降解情况
土壤改良剂、保水剂A和保水剂B的土壤降解情况见图5。可以看出,随着降解时间的增加,土壤改良剂与保水剂的降解率均呈上升趋势,在降解前60天,降解率表现为保水剂A>保水剂B>土壤改良剂,在第60天时,保水剂A、保水剂B和土壤改良剂的降解率分别为21.84%、18.68%、15.54%,此后土壤改良剂的降解率迅速增大,逐步超过了保水剂B和保水剂A,在降解第100天时,土壤改良剂的降解率达到57.58%,而保水剂A和保水剂B的降解率增长较慢,分别为31.89%、26.87%,表明土壤改良剂与保水剂A和保水剂B相比具备良好的生物降解性能,这主要是由于土壤改良剂含有蔗渣纤维微晶,而保水剂A和保水剂B主要以树脂为主,前期蔗渣的降解主要由土壤中的细菌和真菌分泌各类纤维素酶对其进行侵蚀,使得表面积增加,而后通过复杂的生物化学作用达到降解目的,被降解后,土壤改良剂中的其他物质继续被生物酶所作用,发生分子链断裂而解聚成低聚体,进而降解成二氧化碳和水,酶促反应加速了整个反应过程。而保水剂A和保水剂B中树脂所含的生物质较低甚至没有,因此各种细菌和真菌无需依靠分泌生物酶,可直接利用现有碳源,导致前期降解速率较土壤改良剂快,但由于树脂属于高分子聚合物,微生物利用效率不高,所以后期降解率增速缓慢。朱文渊等[18]以淀粉、海藻酸钠、羽毛蛋白以及沸石等为原料,对丙烯酸-丙烯酸胺类保水剂进行改性,并对改性后保水剂的生物降解性能进行分析。结果表明,单纯的丙烯酸-丙烯酸胺类保水剂生物降解性能较差,通过淀粉、羽毛蛋白等改性后,生物降解性能均有提高,主要由于添加的生物质(淀粉、羽毛蛋白等)促进了酶促反应,从而加速了降解进程,而本研究制得的土壤改良剂同样以生物质(蔗渣)为载体,结合了驯化后的活性菌粉,使得其具有更强的生物降解能力,与传统的市售保水剂相比,土壤改良剂的降解速率更高,完全降解周期更短,这为该土壤改良剂在土壤贫瘠地区的应用与推广提供了条件。
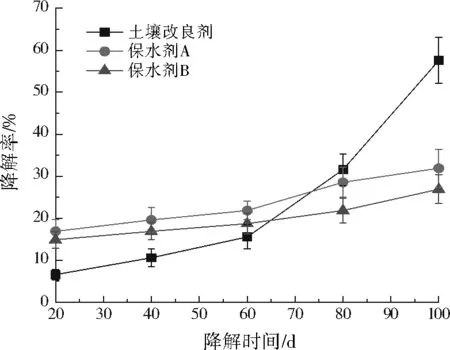
图5 土壤改良剂与保水剂的土壤降解性能
2.6 成本分析
使用成本是土壤改良剂经济性、可行性评价的关键因素,根据土壤改良剂制备条件,生产1 t土壤改良剂的成本分析见表4。经计算,生产1 t土壤改良剂所需成本为2 076.5元,相较于市售保水剂A和保水剂B的价格(分别为6 500、8 000元/t)具有明显的成本优势,并且规模化生产可进一步降低土壤改良剂成本,基本达到低成本的预期效果,具有较可行的市场应用价值。
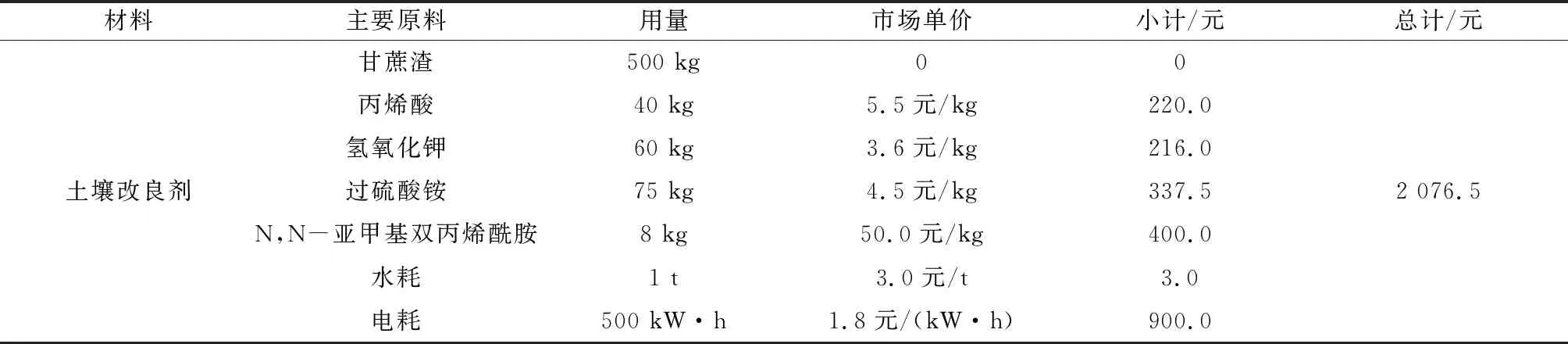
表4 土壤改良剂成本分析
3 结 论
以废弃蔗渣为原料提取纤维微晶,与筛选的高效菌株结合制备新型多功能土壤改良剂,该土壤改良剂内各单体在交联剂的作用下形成交联网状大分子,具有众多亲水基团,蔗渣纤维微晶呈白色条状分布,被共聚体所包裹。土壤改良剂具有吸水量大,重复吸水性强等特点,重复吸水性能和释水过程中的保水能力较传统树脂类保水剂有明显优势,且对于营养元素的吸收较佳,保肥效果良好。土壤改良剂对金属离子具有一定吸收能力,具体表现为Cr>Fe>Ni>Cu>Pb>Zn,可在植物需要时及时供给“储存”的微量元素和必需元素;土壤改良剂生物降解性能良好,降解周期较传统树脂保水剂短;土壤改良剂成本测算为2 076.5元/t,具有现实的推广意义。

