胶原/氧化羟丙基甲基纤维素复合膜的制备与表征
张淑瑜,陈春秀,李国英
(四川大学皮革化学与工程教育部重点实验室,制革清洁技术国家工程研究中心,四川成都 610065)
胶原具有良好的生物相容性、可生物降解性、良好的加工成型性和成膜性,胶原膜可广泛应用于可食性肠衣[1]、猪肉保鲜[2]、油炸食品包装[3]等领域。然而,作为食品包装材料,纯胶原膜的机械强度和热稳定性较差,限制了其应用范围[4]。目前,胶原膜理化性能的提高主要通过物理改性、化学改性和共混改性来实现。物理改性通过在基体中加入填料或助剂来改善制品性能,效果不明显;化学改性通过接枝、嵌段等方法改变聚合物大分子的主链、支链或侧基,作用明显但可能会破坏胶原的三股螺旋结构;共混改性是将两种或两种以上聚合物经混合制备宏观均匀材料的方法,因其操作简单,效果明显且不影响胶原本身生物学性质而备受研究者关注[5,6]。
天然高分子因具有良好的生物相容性及可降解性,研究者们常常将其与胶原共混以获得性能更优的胶原基材料。目前,与胶原共混的天然高分子主要有天然蛋白质和纤维素及其衍生物,包括海藻酸钠[7]、羧甲基纤维素(CMC)[8]、羟丙基甲基纤维素(HPMC)[9]等。HPMC是一种非离子型纤维素衍生物,具有较好的成膜性、耐酶解性以及亲水性,被应用于医药、食品和化妆品等领域[10]。Ding等人[11]采用质量比1:1制备胶原/HPMC共混膜,结果表明共混膜的热稳定性相对于纯胶原膜有所提高,且膜表面更加均匀致密。然而,由于胶原与 HPMC之间仅存在氢键和缠结作用,相互作用较弱,所得复合材料部分性能仍有不足。相关研究表明,醛基能够与胶原的氨基形成席夫碱共价交联键,从而进一步提高胶原的稳定性[12,13]。
纤维素能被高碘酸钠氧化将C2-C3上的羟基转变为醛基,但同时氧化过程导致纤维素的降解,醛基含量和降解程度都与氧化程度成正比[14]。醛基含量的增多有助于纤维素与胶原之间交联键的形成,增强体系之间的相互作用,提高胶原的稳定性;同时醛基含量的增多势必导致纤维素的降解,影响纤维素的理化性能,例如成膜性能下降[15],进而影响其与胶原共混成膜性能。HPMC具有上述纤维素的结构特点,其单体C2-C3上含有羟基,故可用高碘酸钠氧化HPMC获得醛基,与胶原的氨基形成席夫碱共价交联,提高胶原的稳定性。但是,HPMC氧化程度的不同会导致分子链不同程度的降解,从而影响氧化羟丙基甲基纤维素(DHPMC)与胶原共混成膜性能。因此,本文探究不同氧化度DHPMC对复合膜结构和性能的影响。将HPMC进行高碘酸钠氧化,制备不同氧化度的DHPMC,分别将其与胶原以质量比1:1.25共混制膜,测定成膜的机械性能、热稳定性、耐酶降解及亲水性等性能,并表征不同氧化度DHPMC与胶原成膜的前后性能变化,以期得到性能更优良的胶原基复合膜材料。
1 材料与方法
1.1 试剂与仪器
牛皮胶原,实验室自提;HPMC(甲氧基含量27.0%~30.0%,羟丙基含量为4.0%~7.5%),赫克力士有限公司;I型胶原酶(分析纯),美国Sigma-Aldrich公司;冰醋酸、醋酸钠、高碘酸钠,成都科隆化学品有限公司;羟脯氨酸测定试剂盒,南京建成生物工程研究所。
透度/雾度仪,WGT-S;傅里叶变换红外光谱仪,Nicolet iS10;差示扫描量热仪,DSC 200PC;热重分析仪,TG 209-F1;电子万能试验机,UTM2102;扫描电镜,JSM-7500F;接触角测量仪,DSA25。
1.2 测定方法
1.2.1 不同氧化度DHPMC的制备
通过控制 NaIO4用量,分别为 n(NaIO4):n(HPMC)=0.08:1和 0.9:1,制备不同氧化度的DHPMC,根据氧化程度的高低,记为DHPMC(高),DHPMC(低)。制备过程如下:将HPMC溶于去离子水,室温搅拌溶解。然后将其与NaIO4溶液混合搅拌,用1.0 mol/L的H2SO4溶液调节pH值至2.0,于25 ℃下避光反应6 h。待反应完成后,进行遮光透析,除尽未反应的 NaIO4。最后将产物进行冷冻干燥,于干燥器中保存。
1.2.2 DHPMC氧化度的测定
采用盐酸羟胺法[16]测定 DHPMC的氧化度。将DHPMC和盐酸羟胺分别溶于去离子水中,调节 pH至4.5。将两者混合在40 ℃下反应4 h。将反应完成的溶液用0.1 mol/L的NaOH进行滴定直到pH为4.5,将消耗的NaOH的体积记为V1。同时,用同样的方法测得HPMC的醛基含量,将消耗的NaOH的体积记为V0。氧化度的计算公式如下:
式中:
CNaOH——滴定用NaOH浓度,为0.1 mol/L;
m——用于反应的DHPMC干重,g;
162——DHPMC每个重复单元的相对分子质量,g/mol。
1.2.3 复合膜的制备
将胶原海绵溶于 0.5 mol/L醋酸/醋酸钠缓冲液(pH=4.00)中,制备6.25 mg/mL的胶原溶液。同时,用相同方法配置20 mg/mL HPMC、DHPMC(低)和DHPMC(高)。然后将5 mL HPMC、DHPMC(低)和DHPMC(高)分别与20 mL胶原溶液进行共混,m(胶原):m(纤维素)为1.25:1。反应12 h后,透析,离心脱泡,倒入硅胶模具,于室温下干燥成膜,将膜揭下后置于饱和溴化钠溶液的干燥器(RH 59.14%±0.44%,温度20 ℃)中待用。此外,制备等固体质量(225 mg)的纯胶原膜作为对照。为简便起见,将纯胶原膜和复合膜分别命名为 COL、COL/HPMC、COL/DHPMC(低)、COL/DHPMC(高)。
1.2.4 透光率测定
采用透度/雾度测试仪测定薄膜样品的透光率。测量前先将仪器开机预热30 min,然后选取表面洁净、无折痕的膜样品,将其放置于夹具中,置于通光孔处并按下测试按钮。测试3次,取其平均值作为膜样品的透光率。
1.2.5 含水量测试
将称量瓶进行恒重,直至干燥前后质量差不超过2 mg,质量记为M0。然后放入剪碎后的胶原膜,质量记为M1。于105 ℃加热干燥4 h后取出,盖好盖子,于干燥器中冷却至室温后称重,反复操作直至干燥前后的质量差小于2 mg,记录质量为M2。每个样品设置3个平行组,取平均值记作胶原膜的最终含水量。
1.2.6 傅里叶变换红外光谱(FT-IR)测试
将改性处理的胶原膜置于样品架上进行红外扫描,光谱测试范围为650~4000 cm-1,分辨率为4 cm-1,每个样品重复扫描32次。
1.2.7 机械性能测试
将膜剪成分析区域为25 mm×5 mm矩形,用厚度仪测定膜厚度,取测试膜的上、中、下三个位置的厚度,取其平均值。将试样固定于拉力机的夹具中,设置夹具间的间距为25 mm,拉伸速率为5 mm/min,记录其抗张强度和断裂伸长率值,每个样品设置5组平行,取其平均值。
1.2.8 热重(TG)分析测试
称取样品约8.0 mg,置于Al2O3坩埚中。在氮气保护下,从40 ℃加热到800 ℃,升温速率为20 ℃/min。
1.2.9 差示扫描量热仪(DSC)测试
称取约4.0 mg的膜样品,剪碎后密封于铝制坩埚中,以同样密封的空坩埚作为对照。根据牛皮胶原热变性温度的相关研究[17,18],选取40~100 ℃温度范围,在氮气保护下,以5 ℃/min的升温速率进行测试。每个样品至少设置三个平行组。
1.2.10 酶解率测试
取适量的 I型胶原酶溶解于 pH值为 7.4的 50 mmol/L Tris-HCl缓冲液中,该缓冲液中含有 0.36 mmol/L氯化钙,最终得到酶活力为5 U/mL的I型胶原酶酶解液。将其置于37 ℃水浴锅中预先进行活化。将膜样品浸于酶解液中,在37 ℃下酶解4 h,按照羟脯氨酸试剂盒说明书检测酶解液中羟脯氨酸含量ρ(mg/mL)。羟脯氨酸是胶原蛋白的特征成分,其在皮胶原中含量约为14%[19]。因此可根据酶解液中羟脯氨酸的含量计算被酶解的胶原蛋白质量。每个样品测试三次,取其平均值。
式中:
V——酶解液总体积,mL;
M——膜样品中胶原蛋白的总质量,mg。
1.2.11 接触角测试
通过计算去离子水滴在膜表面的接触角来判断膜样品的亲水性。接触角测试如下:将4 μL的水滴滴于样品表面,根据切向法计算膜样品与液滴之间的夹角大小,选取膜上6个不同位置重复上述操作,取其平均值。
1.2.12 扫描电镜(SEM)断面结构测试
采用 SEM 观察膜的横截面。将断裂面的样品固定在导电胶上后进行喷金观察,测试时的加速电压为10 kV。
1.2.13 试验数据的统计分析
文中数据采用SPSS 17.0软件进行显著性分析,p<0.05代表有显著性差异。数据采用平均值±标准偏差表示,使用Microsoft Excel 2013进行分析。
2 结果与讨论
2.1 膜的外观
图1为纯胶原膜及改性胶原膜的光学照片。样品膜的透光率值列于表1。经过氧化所得的DHPMC(低)和DHPMC(高)的氧化度分别为17.78%和45.12%。可以发现,COL、COL/HPMC、COL/DHPMC(低)和COL/DHPMC(高)的透光率均在90%左右,相差不大,均具有较好的透明度。此外,相对于 COL,COL/HPMC、COL/DHPMC(低)和 COL/DHPMC(高)的膜表面更加平整。该结果表明,经过DHPMC改性后的胶原溶液的粘稠度能满足制膜过程中对溶液流平性的要求。
2.2 含水量分析
胶原膜的含水量会直接影响其机械性能及热稳定性。图2为纯胶原膜及各复合膜的含水量。由图可知,膜样品的含水量均在18%左右,由此推测,不同氧化度的DHPMC对胶原膜的含水量没有明显的影响,可判断其含水量与空气湿度相关。因此可以得出,在此条件下测定纯胶原膜与改性胶原膜的机械性能与热稳定性能时,可以对含水量的影响忽略不计。

表1 膜样品的透光率Table 1 The film transmittance of COL, COL/HPMC, COL/DHPMC (low) and COL/DHPMC (high)
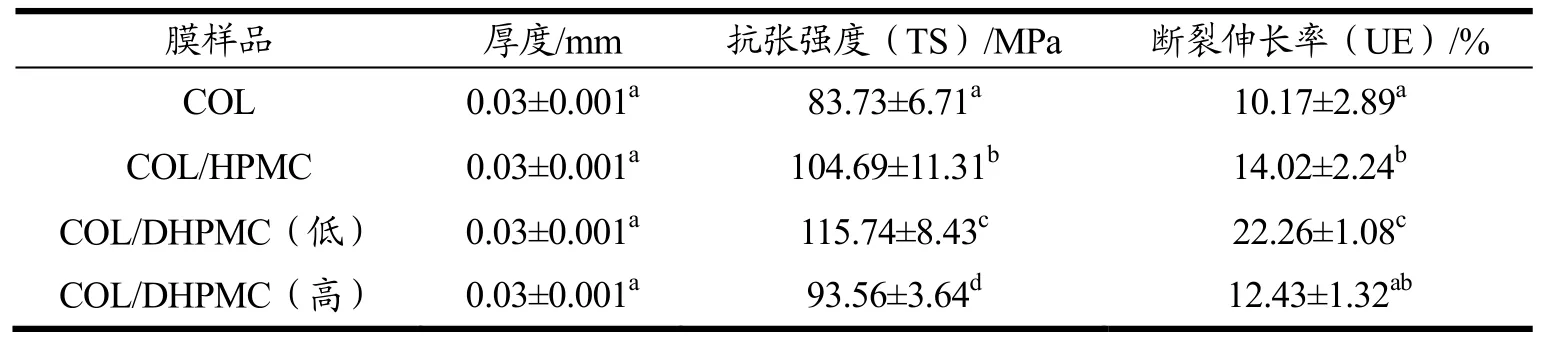
表2 膜样品的厚度以及抗张强度和断裂伸长率Table 2 Parameters of mechanical property of films
2.3 红外吸收光谱分析
图3为COL、COL/HPMC、COL/DHPMC(低)和COL/DHPMC(高)的红外吸收光谱图。由图可知,经过不同氧化度DHPMC共混的胶原复合膜均具有纯胶原膜的特征吸收峰[20],但是发生了不同程度的偏移。其中,酰胺 A带从 COL的 3292 cm-1向COL/DHPMC(高)的3318 cm-1高波数偏移,发生了蓝移,这主要是由于引入的 HPMC中含有羟基,DHPMC中含有羟基和醛基,可以与胶原的氨基之间形成氢键和共价交联,这与程庆甦等[12]的研究结果一致。此外,还可以通过计算酰胺Ⅲ带和1450 cm-1处的吸光度的比值来判断胶原的三股螺旋结构是否完整[21],即AⅢ/A1450。纯胶原的AⅢ/A1450的比值接近与1,而三股螺旋不完整的明胶的 AⅢ/A1450的比值为 0.5。经过计算获得,改性胶原膜样品 COL/HPMC,COL/DHPMC(低)和COL/DHPMC(高)的AⅢ/A1450比值分别为0.96,0.92和0.87,与纯胶原膜的吸光度比值 0.95接近,均接近于 1,表明不同氧化程度的DHPMC的加入没有破坏胶原的三股螺旋结构。
2.4 膜的机械性能分析
将纯胶原膜和复合膜测试的相关参数列于表 2。改性胶原膜的抗张强度和断裂伸长率均高于纯胶原膜,表明共价键的引入有利于增强胶原膜的机械强度[22,23]。同时,应用 DHPMC(低)改性获得的胶原膜的机械性能最好,抗张强度和断裂伸长率分别为115.74 MPa和22.26%,明显优于DHPMC(高)改性的胶原膜(p<0.05),可能是当DHPMC(低)与胶原共混时,由于DHPMC(低)氧化程度低,将部分羟基转变为醛基的同时又使得纤维素具备较好的成膜性和机械强度,延伸性强[24]。因此,DHPMC(低)与胶原具有良好的相容性的同时又形成了分子间交联键和氢键,所以COL/DHPMC(低)机械性能显著提升。而DHPMC(高)与胶原共混时,氧化纤维素自身的成膜性能下降,成膜机械强度较弱,虽然含有较多的醛基能与胶原分子之间形成交联,共混形成的COL/DHPMC(高)机械性能优于 COL,但不如COL/DHPMC(低)和COL/HPMC。
2.5 热稳定性分析
图4是热稳定性分析曲线。图4a、b、c分别为纯胶原膜和复合膜的TG、DTG曲线和DSC曲线。由图4a、b可知,COL,COL/HPMC,COL/DHPMC(低)和 COL/DHPMC(高)的热失重包括两个阶段,第一阶段是样品中胶原分子间和分子内氢键的断裂和自由水的蒸发过程,主要发生在40~150 ℃之间。第二阶段是胶原肽链的热分解过程,肽链发生断裂并逐渐发生降解,同时伴随着结合水还有一些小分子产物挥发,在此阶段质量损失最大且失重速率最快,主要发生在200~800 ℃之间。将COL、COL/HPMC、COL/DHPMC(低)和COL/DHPMC(高)的残留质量,第二阶段的起始分解温度(T0)和最大分解速率时温度(Tm)列于表4。由表可知,经过改性的胶原膜的残留质量均高于纯胶原膜的残留质量,且COL/DHPMC(低)的残留质量最高,为 28.32%。同时,COL/DHPMC(低)的 T0和 Tm分别为 179.58 ℃和338.14 ℃,表明其热稳定性最好。相比于COL,COL/HPMC的热稳定性提高主要是由于HPMC与胶原分子间形成氢键;对于 COL/DHPMC(低)和COL/DHPMC(高),由于DHPMC与胶原之间形成了共价交联,交联键的引入阻碍了胶原肽链的分解和质量损失,故热稳定性提高。此外,可能是由于DHPMC(高)的氧化程度远高于DHPMC(低),因此造成纤维素分子链断裂,形成较小的分子,主要分散在胶原基体中起到一部分填充作用,其交联键主要是在胶原分子内形成;而DHPMC(低)具有较大的分子,能够在胶原分子之间形成桥键作用,进一步促进了与胶原分子间氢键和交联键的形成[25,26]。因此,经过 DHPMC(低)改性的胶原膜的热稳定性优于DHPMC(高)复合的胶原膜。
同时,利用 DSC来测定胶原膜的热变性温度(Td)。胶原的热变性温度是指胶原受热导致三股螺旋结构解旋时的温度,常用于表征胶原材料的热稳定性[27]。胶原膜的DSC曲线如图4c所示。在检测温度范围内出现了一个吸热峰,该峰的峰值所对应的温度即为胶原膜的热变性温度(Td)。COL/DHPMC(低)的Td为 76.24 ℃,高于COL(68.45 ℃),COL/HPMC(69.67 ℃)和COL/DHPMC(高)(71.13 ℃),再次验证了改性胶原膜的热稳定性能够明显提高,且DHPMC(低)与胶原形成的复合膜的热稳定性优于HPMC和DHPMC(高)与胶原形成的复合膜。这与前面TG和DTG分析结果一致。

表3 纯胶原和改性胶原膜的残留质量、起始分解温度(T0)和最大分解速率时温度(Tm)Table 3 The residue weight, T0 and Tm for pure collagen and modified collagen films
2.6 酶解率分析
图5为膜样品的酶解率。未改性的胶原膜酶解率高达 90.41%,经过改性之后酶解率均有降低,COL/HPMC、COL/DHPMC(低)、COL/DHPMC(高)的酶解率分别为 49.88%、62.40%、72.55%。说明共混改性后的胶原膜的耐酶降解能力有所提高,但仍可被酶解。由于DHPMC能够与胶原分子之间形成共价交联,使得复合体系的分子间缠绕更加紧密,阻碍了I型胶原酶与胶原上的位点相互作用[28],故COL/DHPMC(低)和COL/DHPMC(高)的酶解率相比于COL降低。而COL/HPMC的酶解率最低,可能是由于HPMC成膜性好,分子链长,可以很好地包裹胶原分子,使酶难以进攻胶原的作用位点。
2.7 膜的亲水性
亲水性也是评价膜材料性能的一项重要指标。接触角越小,膜材料的亲水性越强;相反,接触角越大,膜材料的疏水性越强[29]。图6为纯胶原膜和复合膜的亲水状态。COL、COL/HPMC、COL/DHPMC(低)、COL/DHPMC(高)的接触角分别为 115.10 °、94.83 °、95.56 °、70.44 °。经改性之后复合膜的接触角均有减小,亲水性明显增强(p<0.05)。Ding等[11]采用质量比 1:1制备胶原/HPMC共混膜,由于HPMC含有大量羟基,故复合膜亲水性相比纯胶原膜增强,本文研究结果与其一致。另外,虽然胶原与DHPMC(低)之间形成交联键,消耗胶原中亲水基团氨基,但是由于DHPMC(低)氧化程度低,本身具有亲水基羟基,故最终表现为亲水性增强。当采用DHPMC(高)与胶原共混时,其氧化度较高,而氧化的同时伴随分子链的断裂,使得亲水基团更多地暴露,且因其能够较好地分散于胶原基体中,故接触角进一步减小[30]。
2.8 膜的截面观察(SEM)
图7为膜样品横截面的SEM图。由图7a可以看出纯胶原膜样品的断面结构为层状结构,而复合膜层状结构相对减弱,变得更加均匀致密,也进一步说明了胶原与HPMC和不同氧化度的DHPMC均具有较好的相容性。DHPMC(低)与胶原之间形成了氢键和交联键,加强了大分子间的连接,从而增强了膜样品的相容性,进而使胶原膜样品变得更加致密;DHPMC(高)均匀地分散于胶原基体中,形成交联键的同时还能起到一部分填充作用;HPMC具有较好的成膜性能,能够与胶原之间形成氢键,具有较好的流平性,从而使膜变得更加均匀致密,这与 Ding等[11]研究结果一致。其团队发现,纯HPMC膜的结构均匀,断面平滑,具有良好的成膜性能。将HPMC与胶原共混制膜,复合膜的表面粗糙度相比于纯胶原膜明显下降。本文进一步说明氧化后的DHPMC与胶原同样具有良好的相容性,与其共混可以使胶原膜的结构更加均匀致密。
3 结论
本文通过测定HPMC和不同氧化度DHPMC共混胶原膜的各项性能指标,得出DHPMC氧化度对复合膜理化性能的影响。结果表明,复合膜具有完整的三股螺旋结构,其机械性能、耐热分解能力、耐酶降解能力以及亲水性能均有所提升。氧化度低的DHPMC(低)能够将部分羟基转变为醛基的同时又具备较好的成膜性和机械强度,延伸性强,与胶原共混时具有良好的相容性,这为胶原基复合膜在食品包装方面的广泛应用提供可能。

