血液样本56 ℃ 30 min加热灭活对精神类药物浓度监测的影响
孙佳琪, 金伟峰, 李 萍, 陈姝子, 林 萍, 李 丹, 陈 庆, 王梦霞, 朱雨昕
(上海市精神卫生中心,上海 200030)
新型冠状病毒肺炎(corona virus disease 2019,COVID-19)是由新型冠状病毒引起的呼吸系统传染病,目前已成为全球性的重大公共卫生事件。《新型冠状病毒肺炎诊疗方案(第八版)》[1]中指出,新型冠状病毒在相对封闭的环境中,暴露于高浓度气溶胶的情况下存在经气溶胶传播的可能。本实验室为药物浓度监测实验室,所用仪器均为质谱仪,空间相对密闭,在此进行血液样本的离心脱盖步骤,极易产生气溶胶,有导致检验工作人员感染的风险。《新型冠状病毒肺炎诊疗方案(第八版)》[1]还指出,新型冠状病毒对热敏感,56 ℃ 30 min可有效灭活。但少有文献报道加热灭活是否会对精神类药物浓度监测产生影响。为此,本研究拟探讨血液样本经56 ℃ 30 min加热灭活后对6种精神类药物(奥氮平、喹硫平、利培酮、锂盐、丙戊酸、氯氮平)浓度监测的影响。
1 材料和方法
1.1 研究对象
选取2021年3—10月上海市精神卫生中心住院患者360例,其中男190例、女170例,年龄(45.23±20.11)岁,服用奥氮平、喹硫平、利培酮、锂盐、丙戊酸、氯氮平的患者各60例。收集360例患者已完成药物浓度检测的剩余血液样本(含促凝剂)。样本要求无明显的脂血、溶血,且尽量覆盖线性范围。
1.2 方法
将当天收集的符合要求的剩余血液样本,加盖置于GNP-9050隔水恒温培养箱(上海精宏实验设备有限公司)内56 ℃干热灭活30 min,然后离心分离血清。采用Waters I-Class/Xevo TQD液相质谱联用仪(美国沃特世公司)检测奥氮平、喹硫平、利培酮与9-羟利培酮(利培酮在体内的主要代谢产物)之和、氯氮平和N-去甲氯氮平的浓度。标准品购自美国Sigma公司,流动相A为0.1%甲酸-2 mmol/L甲酸铵-水溶液、流动相B为100%甲醇或100%乙腈,试剂均购自上海安谱科技股份有限公司。质控品购自上海市临床检验中心。采用K-Lite 8 series电解质分析仪(梅州康立高科技有限公司)及配套试剂(离子选择法)检测血锂浓度。采用AU5800全自动生化分析仪(美国贝克曼库尔特公司)及日本积水公司试剂(胶乳凝集比浊法)检测丙戊酸浓度。
1.3 统计学方法
采用SPSS 23.0软件进行统计分析。采用Kolmogorov-Smirnov检验评估数据的正态性。呈非正态分布的计量资料以中位数(M)[四分位数(P25~P75)]表示,组间比较采用Wilcoxon秩和检验。采用Medcalc 20.0软件绘制Bland-Altman一致性图,如95%的检测结果落在一致性区间(limit of agreement,LOA)的95%可信区间(confidence interval,CI)内,且LOA不超过临床最大允许总误差(allowable total error,TEa),则认为2种方法有较高的一致性。临床TEa可接受范围[2]:血锂的TEa为±20%,其他药物选用《上海市医疗机构临床实验室质量管理规范》[2]中其他治疗药物的TEa(±25%)。以P<0.05为差异有统计学意义。
2 结果
2.1 样本加热灭活前后各项药物检测结果比较
样本加热灭活前后奥氮平、喹硫平、利培酮与9-羟利培酮之和、丙戊酸、氯氮平和N-去甲氯氮平的检测结果差异均无统计学意义(P>0.05),血锂加热灭活后的检测结果显著高于加热灭活前(P<0.05)。见表1。
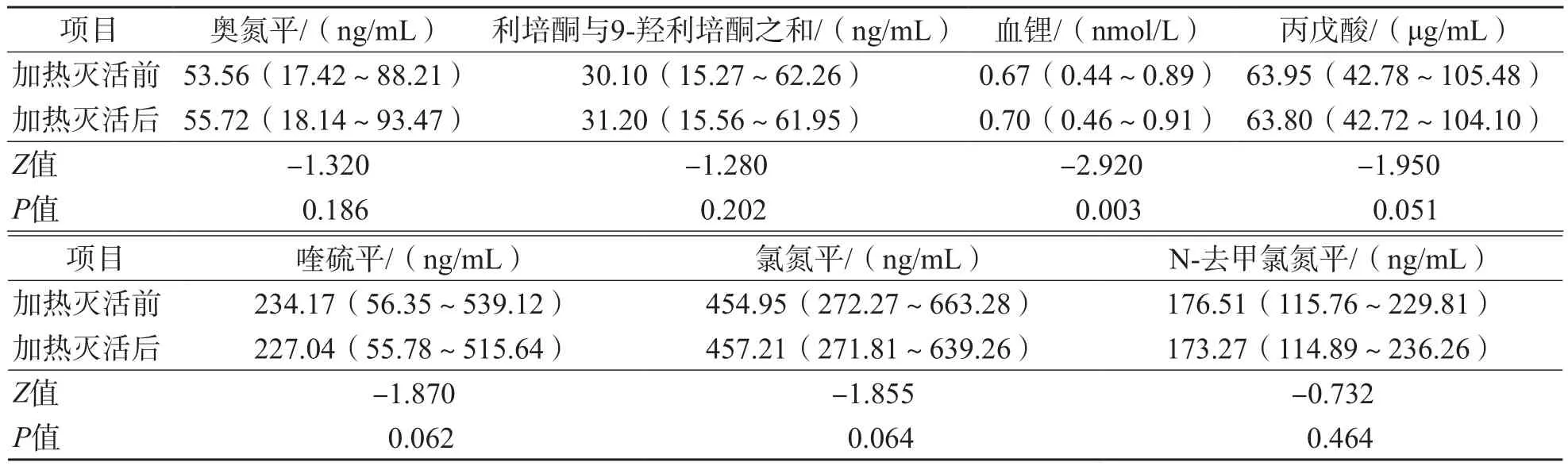
表1 加热灭活前后各项药物浓度检测结果比较
2.2 加热灭活前后各项药物检测结果的一致性评价
奥氮平、喹硫平、利培酮与9-羟利培酮之和、丙戊酸、氯氮平和N-去甲氯氮平分别有100%(60/60)、98.33%(59/60)、95.00%(57/60)、100%(60/60)、96.67%(58/60)、96.67%(58/60)的检测结果位于LOA的95%CI内,且LOA在最大TEa内。加热灭活前后各项药物检测结果一致性较好。见图1。
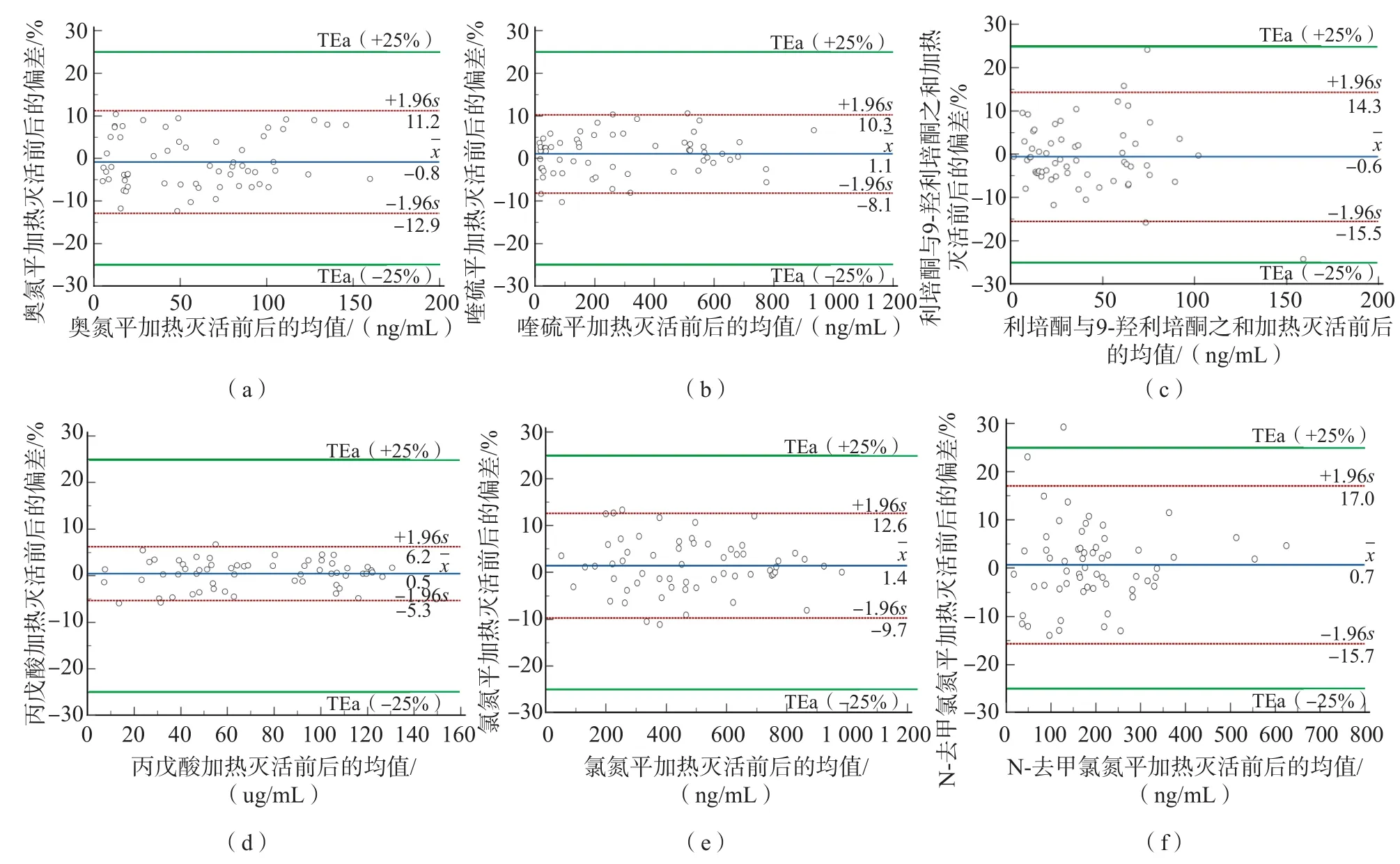
图1 加热灭活前后各项药物检测结果的Bland-Altman一致性分析
血锂项目有96.67%(58/60)的检测结果位于LOA的95%CI内,但LOA下限超过了最大TEa。加热灭活前后血锂检测结果的一致性较差。见图2。
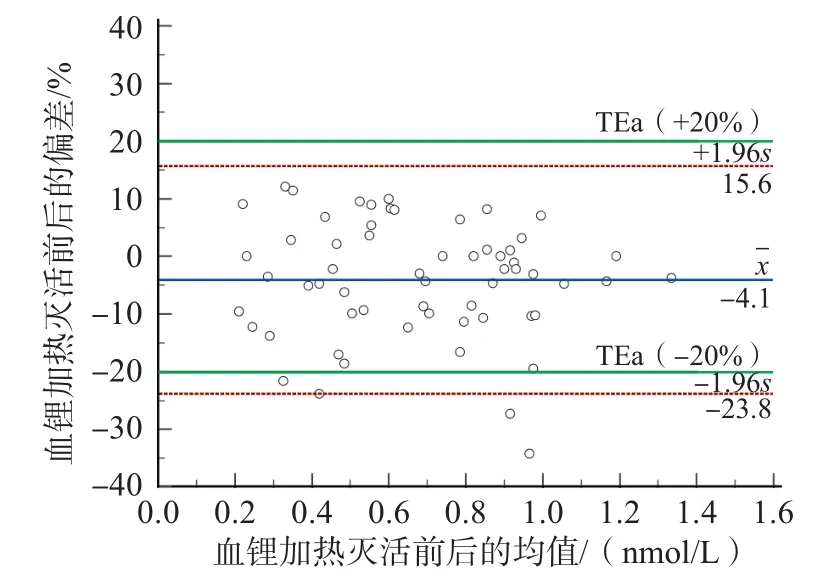
图2 加热灭活前后血锂检测结果的Bland-Altman一致性分析
2.3 血锂项目的校准
补充收集检测血锂的样本42例,对合计102例样本的检测结果进行线性回归分析,回归方程为:Y=0.003+1.026X(r2=0.953)。选取血锂低值、中值、高值各10例,将检测结果代入回归方程进行校准。结果显示,血锂低值、中值、高值样本的校准值与加热灭活前的检测结果差异均无统计学意义(Z=-0.195,P=0.845),见表1。Bland-Altman一致性分析结果显示,有96.67%(29/30)的结果位于LOA的95%CI内,且LOA在最大TEa范围内,校准值与加热灭活前结果的一致性较好。
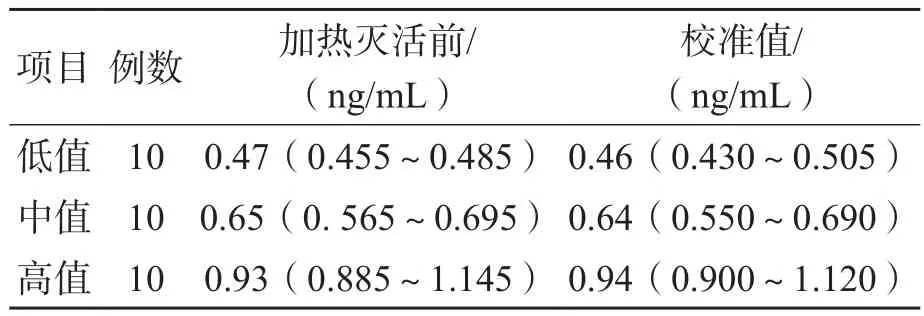
表2 血锂校准值与加热灭活前结果的比较
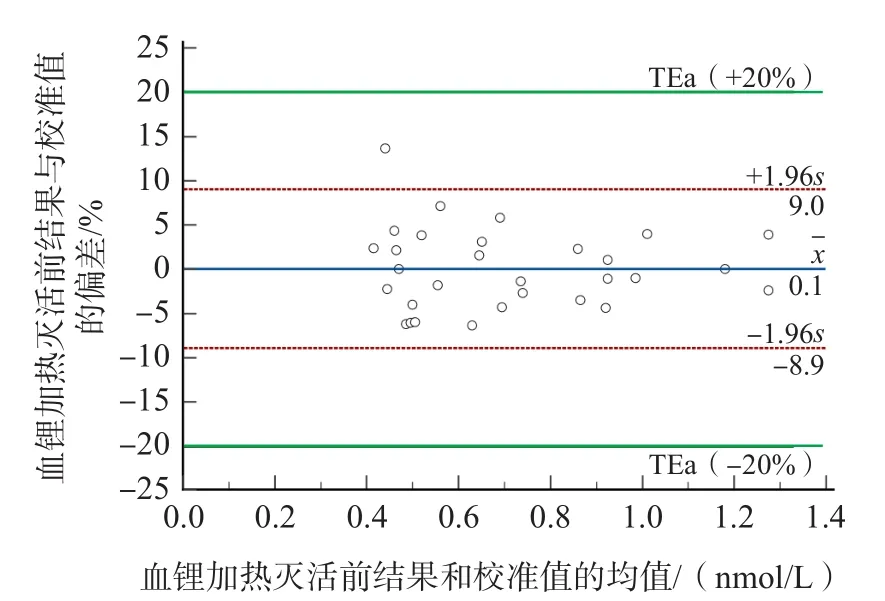
图3 血锂校准值与加热灭活前结果的Bland-Altman一致性分析
3 讨论
虽然通过积极的防控和新型冠状病毒疫苗的使用,COVID-19疫情已基本得到控制。但由于COVID-19外源性输入病例的持续存在和新型冠状病毒突变株的影响[3],该病毒仍具有传播和扩散的风险。
有研究结果显示,当感染了新型冠状病毒后,患者可能会合并神经精神类疾病[4-5]。精神类疾病的主要治疗方式是使用相关药物改善患者的症状,但精神类药物的副作用较大,且个体差异明显,极易产生中毒情况[6-7],因此需要对治疗药物浓度进行监测,以了解患者体内药物的稳态浓度,及时调整药物用量,防止中毒情况的出现。
目前,临床实验室一般采用液相色谱法或质谱法检测精神类药物浓度,但这些方法的样本前处理都需要进行手工操作,在加样、移液、混匀、离心过程中容易产生气溶胶[8],因此有必要在样本处理前进行干预,以保护实验室工作人员,防止实验室污染。根据《新型冠状病毒肺炎诊疗方案(第八版)》[1]的推荐,本实验室在进行样本前处理前对所有样本进行56 ℃30 min灭活。目前,我国有较多探讨加热灭活对生化项目检测结果的影响的研究,但少有其对精神类药物浓度监测结果的影响的报道。本研究结果显示,奥氮平、喹硫平、利培酮与9-羟利培酮之和、丙戊酸、氯氮平和N-去甲氯氮平加热灭活前后差异均无统计学意义(P>0.05),结果一致性较好;血锂加热灭活后的检测结果显著高于加热灭活前(P<0.05),加热灭活前后一致性较差。血锂加热灭活前后检测结果出现差异的原因可能与锂盐在体内的代谢有关:锂盐进入人体后通过钠泵转运,将钠离子从细胞内运出,而锂离子会进入细胞内[9],加热灭活处理会导致样本出现溶血,使细胞内的锂被释放至细胞外,导致血锂的检测结果升高。本研究结果还显示,偏高的血锂结果可通过回归方程进行校准,校准后的结果仍具有临床价值。
综上所述,56 ℃ 30 min加热灭活处理对奥氮平、喹硫平、利培酮、丙戊酸、氯氮平的药物浓度监测无影响,但会影响锂盐的监测,其结果通过回归方程校准后仍有临床价值。

