胎儿圆锥动脉干畸形与染色体异常及临床结局的关系
傅丹 张素华 沈德娟 居云 吴丽娟
圆锥动脉干畸形(conotruncal defects,CTD)是指胚胎期间圆椎动脉干发育异常的复杂性先天性心脏畸形,由圆锥动脉干段发育受到干扰或发育停滞所致,包括法洛四联症、肺动脉闭锁、大动脉转位、右心室双出口、永存动脉干等,约占先天性心脏病的20%~30%,占青紫型先天性心脏病的70%,病情较为严重,胎儿出生后预后较差[1-2]。因此,对CTD胎儿进行正确的产前诊断和预后评估极为重要。先天性心脏病的病因尚不完全明确,大致可分为遗传因素、环境因素及药物因素等,目前认为遗传因素在其中的作用更大[3]。研究发现,染色体异常可以导致发育迟缓、智力障碍、自闭症、精神疾病及多系统先天性畸形,可能与CTD的发生相关联[4-5]。本研究探讨136例CTD胎儿的产前诊断结果和临床结局,并分析CTD与染色体异常的关系,现报道如下。
1 对象和方法
1.1 对象 选取2012年1月至2021年12月在苏北人民医院经产前胎儿畸形筛查确诊胎儿CTD并进行胎儿染色体检查的136例孕妇(均为单胎妊娠)为研究对象,孕妇年龄20~40(28.31±4.53)岁,均于孕中期经胎儿超声心动图检查确诊CTD。根据CTD超声诊断标准及亚型分类标准,136例CTD胎儿中法洛四联症58例、肺动脉闭锁11例、完全性大动脉转位39例、右心室双出口25例、永存动脉干2例、主动脉弓离断1例;根据CTD是否合并心内或心外畸形,136例CTD胎儿可分为单纯组(72例)、合并其他心内畸形组(43例)、合并心外畸形组(4例)、同时合并心内、心外畸形组(14例)、仅合并超声软指标异常组(3例)等5组,后4组统称非单纯型CTD。
1.2 纳入与排除标准 纳入标准:符合《中国出生缺陷防治报告》[6]中CTD胎儿诊断标准;单胎妊娠者;在苏北人民医院进行超声心动图检查及遗传学检查者(包括羊水穿刺产前诊断或引产后胎儿组织检测)。排除标准:先天性心脏畸形诊断不明确;非上述6种类型CTD;双胎妊娠者;孕妇患有妊娠期糖尿病或心脏病等。
1.3 方法
1.3.1 超声心动图检查 采用超声心动图对可疑胎儿畸形者进行检查。使用彩色多普勒超声仪,探头频率为3.5~5.0 MHz,孕妇取仰卧位,先对胎儿进行常规检查,评估胎儿发育情况,筛查有无心外畸形;确定胎方位后,依次获取胎儿上腹部横切面、四腔心切面、左心室流出道切面、右心室流出道切面、三血管气管切面等5个标准切面,以及三血管切面、主动脉弓长轴切面、动脉导管弓长轴切面、腔静脉长轴切面、心底大动脉短轴切面、双心室短轴切面等6个切面,运用心脏节段分析法观察心房与心室、心室与大动脉的连接关系,检查室间隔、心室壁及心包有无异常;同时利用彩色多普勒超声仪监测胎儿心脏血流动力学变化情况。
1.3.2 染色体G显带核型分析 按照实验室标准操作流程,对羊水或脐血样本进行染色体核型分析。具体步骤:使用超声诊断仪,选择穿刺点和穿刺角度,对妊娠18~24周的孕妇行羊膜腔穿刺,取羊水20.0 ml;1 800 r/min离心10 min后去上清液,取约2 ml细胞轻轻吹打混匀后正常培养8~10 d;细胞收获后先加秋水仙素处理,再使用1%枸橼酸三钠液低渗后收集细胞。对妊娠24周后的孕妇行脐血管穿刺,取脐血1.5~2.0 ml,分离收集细胞并正常培养70 h,随后加秋水仙素继续培养2 h;收获细胞,离心,弃上清液,加入氯化钾溶液低渗处理。所有细胞样本均用新鲜配置的甲醇-冰醋酸固定液(体积比为3∶1)固定,离心后制成细胞悬液,滴片,并于56℃烤箱烤片过夜;过夜后用浓度0.02%胰蛋白酶消化,Giemsa染色,流水冲洗晾干,即可进行染色体核型分析。
1.3.3 染色体低深度全基因组高通量测序分析 按照DNA提取的标准操作流程对羊水细胞、脐血淋巴细胞或胎儿组织进行基因组DNA提取及纯化。使用短串联重复序列标记对组织DNA与母血DNA进行检测,对样本母源污染情况进行判断。采用酶切方式将50 ng基因组DNA切割成300 bp大小的DNA片段,通过末端修复,加接头,PCR富集后磁珠纯化,制备DNA文库。DNA文库使用Nextseq 500平台(美国Illumina公司)进行大规模平行测序,采用FASTQ数据质控,检测分析非整倍体及全基因组范围拷贝数变异(copy number variant,CNV)。采用ChAS2.0软件进行数据判断,将样本DNA序列与已知人类参考基因组序列进行比对,检索DECIPHER、OMIM、Clinvar、DGV等数据库,获取基因组范围以及缺失或重复的功能和关联表型的注释,参考美国医学遗传学会指南,对CNV≥100 kb的片段进行客观全面的评价,分为致病性、可疑致病、意义不明、可能良性及良性。采用荧光定量PCR对致病性、可疑致病及意义不明的CNV进行验证,并对意义不明的CNV胎儿父母外周血样本进行低深度全基因组高通量测序分析,判断胎儿CNV是遗传自父母还是新发。
1.3.4 病例随访 通过电话跟踪随访孕妇至预产期后6个月,了解孕妇临床结局和活产新生儿情况。
1.4 统计学处理 采用SPSS 24.0统计软件,计数资料以频数和构成比表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 染色体异常情况分析 136例CTD胎儿中检出染色体异常27例,检出率为19.85%,其中染色体数目异常13例,致病性CNV 14例。13例染色体数目异常中,13-三体综合征、18-三体综合征、21-三体综合征各4例,45 X 1例。14例致病性CNV中,22q11.2微缺失综合征10例,17p11.2微缺失综合征2例,8p21.3微重复综合征1例,2p24.3微重复综合征1例。对14例致病性CNV胎儿的父母进行检测以判断染色体异常来源,发现新发变异10例,3例为父源传递,1例为母源传递。图1(见插页)为完全性大动脉转位的典型图像,该病例的产前诊断结果提示为22q11.2微缺失综合征。图2为22q11.2微缺失综合征胎儿及其父母的CNV检测结果,其中胎儿检测到22q11.2上的微缺失片段,而父、母结果均正常。
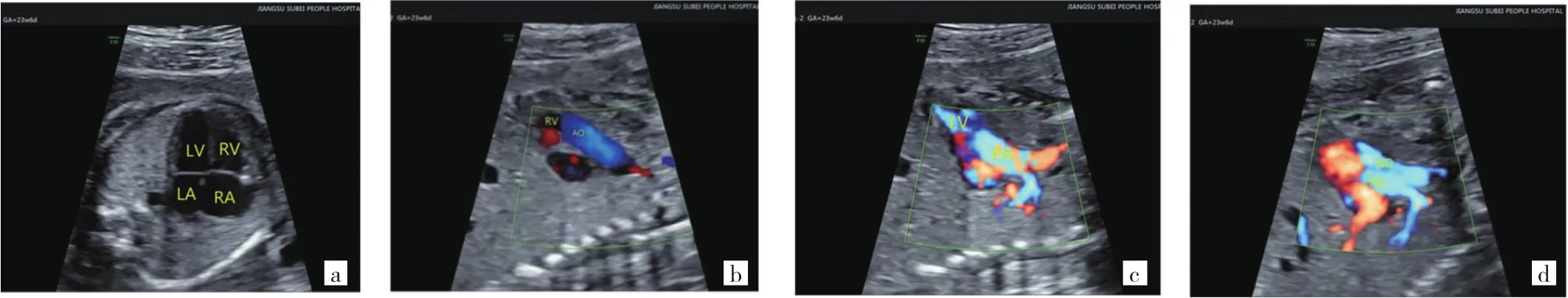
图1 完全性大动脉转位的典型图像(a:四腔心切面,房室连接正常;b:主动脉发自右心室;c:肺动脉发自左心室;d:主动脉、肺动脉起始段交叉关系消失,呈平行排列)
2.2 不同类型CTD胎儿染色体异常情况比较 27例染色体异常中,永存动脉干胎儿的染色体异常检出率最高,完全性大动脉转位胎儿的染色体异常检出率最低,主动脉弓离断胎儿中未检出染色体异常,除永存动脉干和主动脉弓离断因病例数较少未纳入分析外,其他各类型CTD染色体异常检出率比较,差异无统计学意义(P>0.05),见表1。
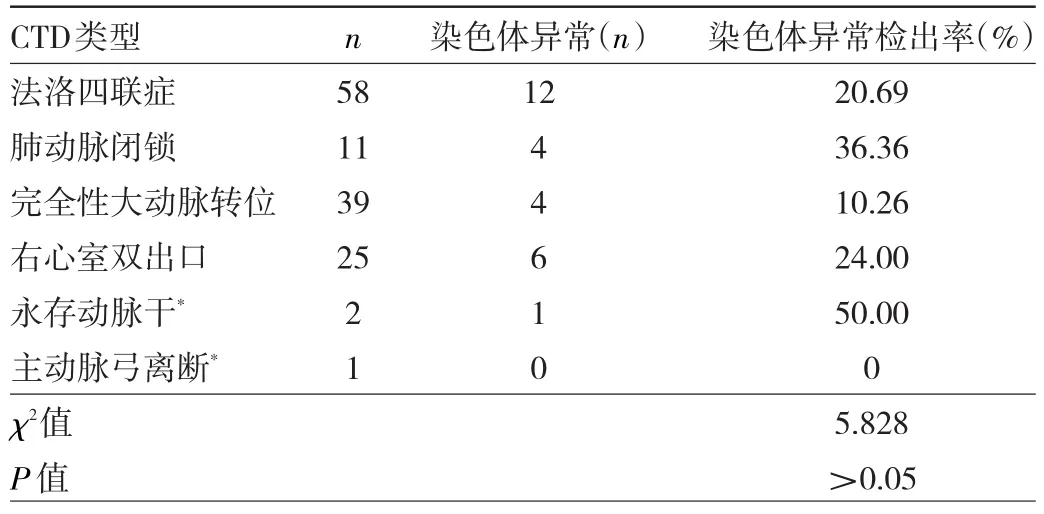
表1 不同类型CTD胎儿染色体异常情况比较
2.3 不同合并心脏畸形分组CTD胎儿染色体异常情况比较 27例染色体异常中,合并心外畸形、同时合并心内、心外畸形胎儿的染色体异常检出率较高,单纯组胎儿的染色体异常检出率最低,合并心外畸形组和仅合并超声软指标异常组因病例数较少未纳入分析,其他各分组CTD胎儿染色体异常检出率比较,差异有统计学意义(P<0.05),见表2。
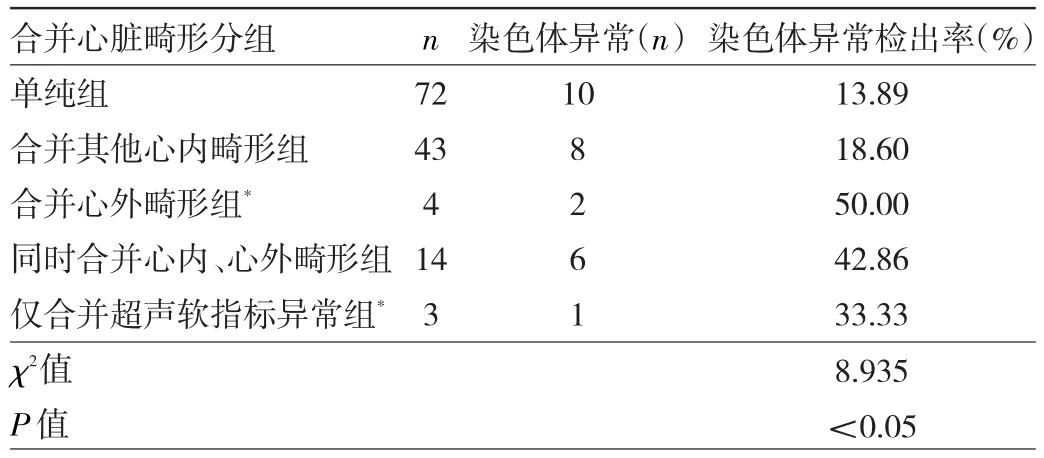
表2 不同合并心脏畸形分组CTD胎儿染色体异常情况比较
2.4 随访结果 136例CTD胎儿中成功随访到130例,随访成功率为95.59%。130例CTD胎儿中有82例引产,引产率为63.08%,所有27例染色体异常均为引产胎儿,占比为32.93%;48例胎儿顺利出生,其中有4例临床结局与产前诊断不一致,见表3。
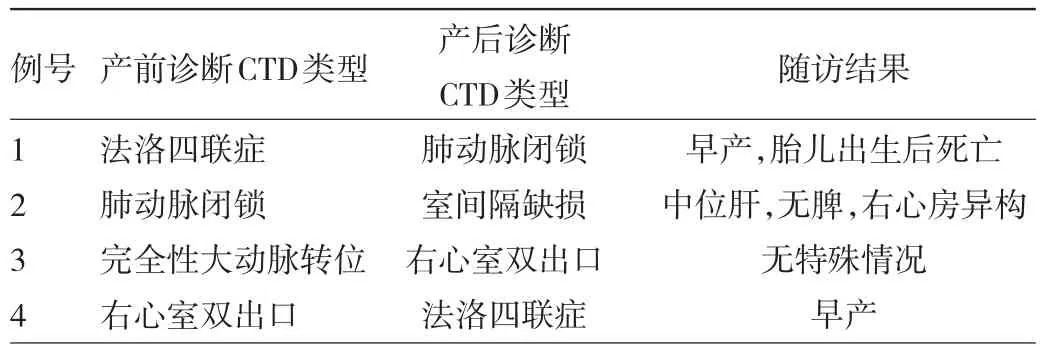
表3 临床结局与产前诊断不一致CTD胎儿随访结果
3 讨论
先天性心脏病是最常见的一类缺陷性疾病。CTD在先天性心脏病中的比例较高,胎儿病情较重,预后较差,容易在婴幼儿期死亡[7]。目前,临床主要运用超声心动图检查于产前对CTD进行诊断,准确率可达90%以上[8]。近年来研究表明,染色体异常与胎儿发生CTD的联系十分密切,产前诊断的CTD中,染色体异常率高达20%[9]。
先天性心脏病的病因多种多样,通常由遗传因素和环境因素共同作用所致,目前遗传因素的影响研究日益受到重视,CTD的遗传学研究也取得了诸多研究成果[10]。先天性心脏病的相关基因十分复杂,这些相关基因在蛋白质表达的时间和空间调控过程中发挥重要作用,当圆锥动脉干发育的相关基因及其产物异常时,心室流出道和大动脉也会出现发育异常[11-12]。染色体畸变可能导致相应基因出现变化,影响相应蛋白质合成,从而影响胎儿心脏形成和发育,最终导致CTD的发生[13]。无论染色体数目异常还是结构异常均可导致胎儿发生CTD,因而对CTD胎儿进行染色体检查尤为重要。本研究运用染色体G显带核型分析和染色体低深度全基因组高通量测序,结果显示,136例CTD胎儿中检出27例染色体异常,检出率为19.85%,其中染色体数目异常13例,致病性CNV 14例,说明CTD与染色体异常之间具有一定联系。
本研究发现,永存动脉干胎儿的染色体异常检出率较高,这可能是因为本研究纳入该类型病例数较少,检测结果不具有代表性;肺动脉闭锁、右心室双出口、法洛四联症染色体异常检出率也较高,而完全性大动脉转位染色体异常检出率最低,与郝晓艳等[14]发现法洛四联症、肺动脉闭锁染色体异常检出率较高的结果相似,提示不同类型CTD可能有共同的遗传学基础,但不同类型CTD合并染色体异常的概率不同。
本研究结果还显示,合并心外畸形、同时合并心内、心外畸形胎儿的染色体异常检出率较高,而单纯组胎儿的染色体异常检出率最低。Lin等[15]发现合并心外畸形胎儿的染色体异常率为58.33%,同时合并心内、心外畸形胎儿的染色体异常率为35.00%,与本研究结果相似,可见由于不同染色体承载的基因不同,导致心脏畸形的复杂程度及合并心外畸形的概率也不同。
本研究中随访结果显示,136例CTD胎儿中有48例胎儿顺利出生,其中4例产前诊断与临床结局不一致,主要表现为CTD类型不一致,出现该现象的原因可能与圆锥动脉干畸形的起源和超声诊断技术有关。
圆锥动脉干的胚胎发育过程十分复杂,任何时间和部位都可能发生不同程度的异常。CTD各类型之间互相关联、互相过渡,其在解剖学和血流动力学上既有相似性,又有各自独一无二的特征,因而部分患者难以得到明确的诊断结果[16]。尽管CTD患者真实的胚胎发育过程不完全清楚,但可以肯定的是圆锥间隔发育完整、分隔均匀、螺旋式生长及瓣下圆锥结构与心室对接良好等发育部分是整体且同时进行的,其与心血管系统内的血流动力学也存在紧密的联系[17]。圆锥间隔发育不良可导致肺间隔缺损,并发半月瓣发育异常,并可能导致共同动脉干;而圆锥间隔发育完整但分隔不均则可导致法洛四联症;螺旋式生长异常会导致大动脉转位、右心室双出口等;若瓣下圆锥结构与心室对接不良则导致法洛四联症、共同动脉干等[18]。
超声心动图检查可准确评估胎儿的心脏结构和功能。病理解剖学将心脏分为心房、心室、大动脉3个节段以及心房-心室、心室-大动脉2个连接,使用超声心动图分别观察心房、房室瓣、心室、动脉圆锥及大动脉,可有效明确CTD类型[19-20]。但由于肺动脉内径过于狭小,超声心动图检查可能无法明确显示其与右心室及主动脉之间的关系,也会导致误诊。
综上所述,CTD胎儿的染色体异常率较高,同时发生心内、心外畸形的CTD胎儿更易伴有染色体异常。产前检查若发现胎儿患有CTD或超声心动图检查提示CTD胎儿合并多器官异常时,应行介入性产前诊断排除染色体异常。由于本研究纳入样本量较少,无法全面反映部分CTD类型的染色体异常情况,因此后期需扩大样本量以获取更具说服力的研究结果,从而更好地指导临床工作。

