肺部超声、机械功与重症肺炎肺水肿及ARDS关系分析
吴 军,吴怀标
安徽省皖南康复医院/芜湖市第五人民医院急诊与重症医学科,安徽 芜湖 241000
重症肺炎(severe pneumonia,SP)是呼吸科常见危重症之一,主要特征为肺部感染、肺泡与毛细血管损伤、肺水肿、通气/血流比例紊乱等,可迅速进展为急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)与多器官功能不全综合征,病死率高达46%[1,2]。因此,早期预测ARDS发生意义重大。近年来,超声凭借可床旁、无创、检查时间短等特点逐渐应用于重症医学领域,且国内外研究均已证实[3-5],通过肺部超声检测肺部超声评分(lung ultrasound,LUS)对成人肺炎具有良好诊断价值,可观测肺部炎症反应情况,评估患者病情与预后。机械功(mechanical power,MP)涵盖了潮气量、气道峰压、气道阻力、呼吸频率等多种力学因素,有助于评估肺通气状态,判断肺组织损伤程度和通气状态[6]。但目前关于LUS、MP与重症肺炎肺水肿及ARDS关系的报道较少,是否有助于评估肺水肿及预测ARDS的发生尚不明确。基于此,本研究通过监测SP患者机械通气早期MP、LUS评分,探讨二者与肺水肿的关系及对ARDS的预测效能,以期为临床预测ARDS发生、早期预防干预提供参考。
1 资料与方法
1.1 一般资料
选取2018年2月至2020年8月我院收治的95例SP患者,根据是否发生ARDS分为ARDS组(n=38)、无ARDS组(n=57)。其中ARDS组严重程度:轻度[200 mmHg<氧合指数(PaO2/FiO2)≤300 mmHg]10例,中度(100 mmHg
1.2 方法
患者均给予纠正电解质紊乱、呼吸支持、营养支持等对症治疗,并根据病原学和药敏试验选取敏感型抗菌药物。
LUS评估:采用索诺声超声诊断仪进行检查,应用相控阵凸面探头,分别检测两侧前胸壁、侧胸壁及后胸壁上、下部共12个肺区,详细监测治疗前、治疗24 h后、治疗48 h后LUS评分:(1)正常通气区(N):肺滑动征伴A线或单独B线<2个,计0分;(2)中度肺通气减少区(B1线):伴多发、典型B线,计1分;(3)重度肺通气减少区(B2线):多发融合B线,计2分;(4)肺实变区(C):组织影像伴典型支气管充气征,计3分[8]。对每个区域最严重表现进行评分,LUS评分总分范围为0~36分。上述操作均由2名具备丰富超声检查经验的放射科医师评估。
MP:对患者实施深镇静,使其Richmond躁动-镇静评分达到-4~-3分,以规避自主呼吸、人机不同步对检测结果的影响,应用压力-容积曲线获得患者治疗前、治疗24 h后、治疗48 h后MP数据。
1.3 统计学方法
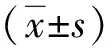
2 结果
2.1 两组LUS评分、MP比较
两组患者比较,ARDS组治疗24 h、48 h后LUS评分、MP高于无ARDS组(P<0.05)。见表1。
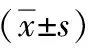
表1 两组LUS评分、MP比较
2.2 不同LUS评分、MP水平者肺水肿发生率比较
以治疗48 h后LUS评分、MP均值(分别为14.03分、16.70 J/min)为分界将患者分为高水平组、低水平组,比较不同LUS评分、MP水平者肺水肿发生率。结果显示,LUS评分、MP高水平者肺水肿发生率高于低水平者(P<0.05)。见表2。

表2 不同LUS评分、MP水平者肺水肿发生率比较n(%)
2.3 LUS评分、MP与ARDS严重程度关系
采用Spearman进行相关性分析,严重程度赋值:1=轻度,2=中度,3=重度。结果显示,治疗24 h后LUS评分、MP与ARDS严重程度呈正相关;治疗48 h后LUS评分、MP与ARDS严重程度呈正相关。见图1和图2。

图1 治疗24 h(a)、48 h(b)后LUS评分与ARDS严重程度关系

图2 治疗24 h(a)、48 h(b)后MP与ARDS严重程度关系
2.4 多因素分析
以ARDS发生情况为因变量(0=无,1=有),以治疗24 h、48 h后LUS评分、MP为自变量(1=低水平,2=高水平),采用多因素Logistic回归方程分析,结果显示,治疗24 h、48 h后LUS评分、MP均与ARDS发病相关(P<0.05)。见表3。
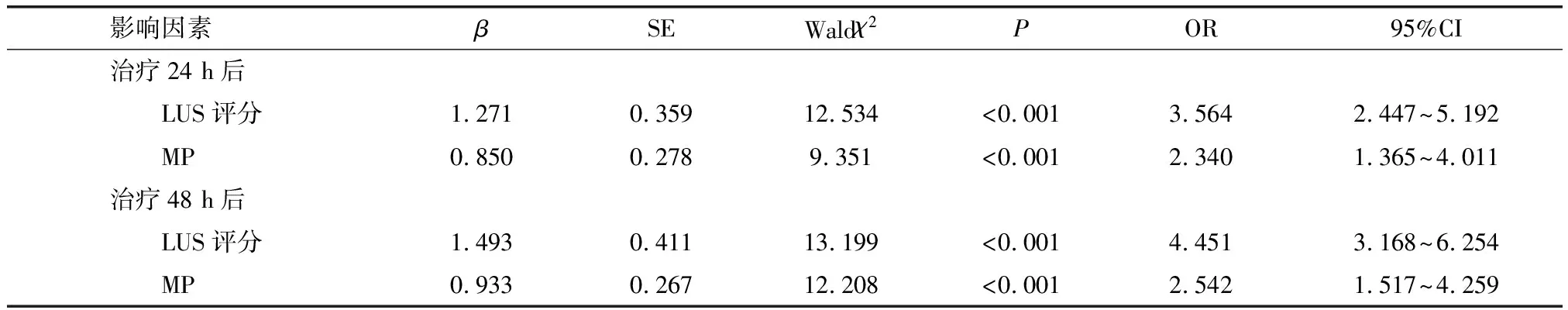
表3 ARDS的多因素Logistic回归方程分析
2.5 LUS评分、MP预测ARDS的ROC
以治疗24 h后、治疗48 h后ARDS组LUS评分、MP为阳性样本,以对应时间点无ARDS组为阴性样本,绘制各指标预测ARDS的ROC曲线,并应用SPSS的联合应用ROC理论模式,构建LUS评分、MP联合的预测模型,结果见图3。治疗24 h、48 h后,LUS评分联合MP预测ARDS的曲线下面积(AUC)分别为0.874、0.915(P<0.05),均高于单独预测的AUC。

图3 LUS评分、MP预测ARDS的ROC曲线
3 讨论
重症监护室中重症肺炎患者30天病死率可高达27.0%~47.0%,而并发肺水肿、ARDS是患者不良预后的危险因素[9]。因此,早期评估肺水肿与ARDS的发生是必要的。
肺是一个气液共存的组织,正常肺组织可完全反射超声波,产生A线或少量B线等伪像;肺组织损伤则会改变肺内气体与液体比例,引起不同程度肺组织失气化现象,其中,中度肺组织失气化呈现多条距离清晰的B线,重度则产生密集融合的B线,肺实变则表现为类似肝样组织结构及支气管充气征[10,11]。本研究通过对比研究显示,LUS评分升高与SP患者肺水肿发生风险有关,分析其原因发现,肺水肿可诱导毛细血管扩张充血,促使肺泡腔内大量水肿液聚集,造成肺泡内气体与液体比例下降,B线密集,从而导致LUS评分升高。连细华等[12]研究显示,肺部超声B线征可反映肺水肿病理学严重程度,半定量判断肺水肿,本研究观点与之相似。此外,谢永鹏等[13]报道,LUS评分可有效评估ARDS患者肺脏组织肺泡塌陷、肺不张甚至肺实变情况。本研究发现,治疗24 h、48 h后发生ARDS者LUS评分较未发生ARDS者更高,提示LUS评分升高与ARDS发生有关,且LUS评分越高,ARDS病情程度越严重。究其机制,可能与ARDS肺累及范围广、肺毛细血管通透性增加、血管外肺水增多等因素有关,提示LUS评分在预测ARDS发生、评估ARDS严重程度方面具有一定临床价值,有助于指导临床实施对症处理[14]。进一步分析发现,治疗24 h、48 h后LUS评分升高是ARDS发生的危险因素,再次佐证了LUS评分对ARDS发生的预测价值。
MP是单位时间内潮气容积改变生成的动态能量总和,可有效评估肺组织炎症反应与肺泡应力水平,相关研究表明,其是判断机械通气时肺组织承受呼吸力学状态的综合指标[15-17]。本研究显示,发生ARDS的SP者治疗24 h、48 h后MP高于未发生ARDS者,提示MP与ARDS发生有关。发生ARDS患者经机械通气治疗后,肺部通气面积、肺水肿状态及肺组织顺应性改善效果不甚理想,死腔容积未显著减少,进而影响机体通气过程中呼吸机做功量,导致MP无明显变化[18]。由此推测,持续高MP可能预示SP患者ARDS发生。本研究还发现,治疗24 h、48 h后MP与ARDS严重程度存在正相关关系,这可能是由于随ARDS病情进展,肺泡大量塌陷,肺顺应性不断下降,肺水肿状态未得到改善甚至恶化,肺通气面积持续减少,导致机械通气需更大呼吸机做功,即需要更大MP。然而受ARDS病情较为复杂、严重程度等因素影响,治疗48 h后单一MP预测ARDS效果不甚理想,特异度仅为59.65%,故本研究绘制联合ROC曲线,结果显示,治疗48 h后LUS评分与MP联合预测ARDS的AUC最大,提示LUS评分与MP联合对ARDS预测效能最佳,有助于指导临床实施保护性通气、限制性液体治疗等抢救措施,减少病死风险。
综上所述,LUS评分、MP与SP患者肺水肿、ARDS发生有关,联合上述指标可为临床预测ARDS提供客观参考。但本研究中纳入病例数较少,尚需进行大规模、多中心的临床研究,进一步验证所得研究结果。

