微型流化床中焦油热裂解和水蒸气重整的反应特性及动力学对比
武鹏,王芳,曾玺,战洪仁,岳君容,王婷婷,许光文
(1 沈阳化工大学机械与动力工程学院,辽宁沈阳 110142; 2 北京工商大学生态环境学院,北京 100048;3 中国科学院过程工程研究所多相复杂系统国家重点实验室,北京 100190)
引 言
气化技术是含碳燃料清洁、高效热转化的主要途径,能将固体燃料转化为高品位的可燃气或合成气,广泛用于燃气生产、IGCC 发电和化学品合成等[1-4]。生物质气化常采用固定床和流化床技术,其较低的操作温度(600~900℃)不可避免地生成大量焦油。作为液体副产物和重要环境污染物,焦油在低温下(<300℃)易凝结,堵塞管路,腐蚀设备,生成含酚废水,既降低气化效率,影响设备运行,还导致催化剂中毒,给气体净化带来很大挑战,影响气化技术的终端应用[5-9];且生成焦油的热值占燃料的5%~15%,不加以利用将降低气体产物的品质和产量。因此,针对生物质气化,很有必要深入研究焦油的转化与脱除方法。
根据脱除单元在气化工艺中的位置,现有焦油脱除技术可分为气化炉外非原位脱除和气化炉内原位脱除。非原位脱除技术包括:物理法、微生物降解法、催化法、热裂解法等[8,10-13]。原位脱除技术主要通过操作条件优化(温度、压力、气氛、气体停留时间等)、反应器结构创新和新型催化剂开发等措施将焦油在炉内转化为气体产物。与非原位脱除技术相比,原位脱除技术能有效提高气化效率、改善气体产物品质、降低气体净化单元的投资[14]。
工业运行的生物质气化炉内往往是一个高温、有氧、含水蒸气的反应气氛,高温热裂解、部分氧化和水蒸气重整均会对炉内的焦油转化和脱除产生促进效果。研究表明,焦油热裂解主要是利用高温的热冲击作用使焦油中侧链和小分子组分降解为气体产物,而大分子组分通常会缩聚成重质组分,甚至积炭,其有效温度通常在1000℃以上。焦油的水蒸气重整是在一定温度(700~1000℃)和水蒸气解离形成的·H 和·OH 自由基作用下,使焦油受热脱氢,裂解成小分子烃类、苯酚、含氧杂环等成分,并最终形成H2、CH4、CO、CO2等气体产物。焦油热裂解和水蒸气重整过程的反应路径如图1[15-16]所示,其涉及到的主要化学反应见表1[17-19]。与热裂解相比,焦油水蒸气重整过程涉及更多的反应,焦油脱除的效果更明显,且能有效降低反应温度。

表1 焦油水蒸气重整过程中涉及到的化学反应Table 1 Reactions involved in the tar steam reforming process
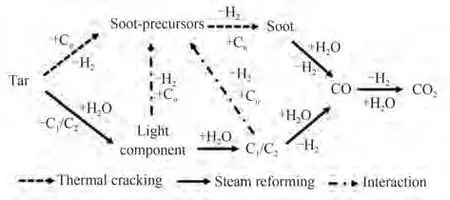
图1 焦油水蒸气重整反应路径Fig.1 Simplified reaction diagram of tar steam reforming
目前,文献研究已充分证实水蒸气对焦油良好的重整效果[20]。例如,Garcia等[21]发现在水蒸气存在时,H2和CH4的产率是热裂解的五倍。Li等[22]和Zhu等[23]的研究表明水蒸气可以提高焦油模型化合物的转化率,但存在最佳的水蒸气分压。Warsita 等[24]采用微波辐射加热方法在水油比为0.3 时获得萘和甲苯的去除率分别达到96.3%和95.8%。此外,研究也发现,焦油水蒸气重整过程与温度、水蒸气分压、气体停留时间和催化剂等因素紧密相关[20]。例如,在焦油水蒸气重整过程中加入石灰石、橄榄石、铁矿石、碱土金属氧化物等催化剂[25-29],可以进一步加快反应进行,提高合成气产率。分析发现,大部分研究集中在脱除焦油的可行性验证和焦油去除效率的提高方面,很少进行焦油水蒸气重整的气体产物生成特性和对应反应动力学的研究。众所周知,焦油水蒸气重整是一个复杂的反应系统,而常见的基于样品质量改变的热重分析方法只能反映焦油总体质量的宏观变化趋势,无法反映产物生成信息和据此进行反应机理推测,势必影响对焦油转化过程的深入认识和气化工艺的设计创新。
基于此,本研究利用新型的微型流化床反应分析仪(micro fluidized bed reaction analyzer,MFBRA)研究生物质焦油水蒸气重整过程的反应特性,重点考察温度和水蒸气分压对主要气体组分(H2、CH4、CO、CO2)的生成、针对气体产物的总碳转化及焦油转化的影响,分析反应行为,计算反应动力学,并与焦油热裂解对比。本研究既深化了对焦油水蒸气重整反应的认识,也为气化炉内焦油脱除技术和工艺的创新提供依据。
1 实 验
1.1 实验原料
实验用焦油样品由松木颗粒在10℃/min的升温速率下加热到800℃并停留30 min 热解制成,热解反应器的结构和操作见团队前期研究[30-31]。收集到的焦油经除尘、脱水后低温冷藏。焦油元素分析中C、H、O、N 和S 的含量(%(质量),daf)分别为50.08%、8.01%、41.24%、0.35%和0.32%。
1.2 实验装置与操作
实验用微型流化床反应分析仪主要由供气系统、MFB 反应器、微型电加热系统、焦油进样系统、气体净化与分析系统、控制与数据采集系统等组成,如图2(a)所示。实验用气体包括载气(高纯Ar,99.9995%)和水蒸气,载气用于流化石英砂颗粒和携带水蒸气,其流速由质量流量计精确控制。水蒸气由蒸汽发生器生成(300℃),流量由高精度恒流泵(P230Ⅱ)控制,其分压通过载气进行调节。MFB 反应器为石英材质,内径为20 mm,由4 个石英烧结板将其自下而上分为:(1)载气通入区;(2)水蒸气通入和气体预热区;(3)焦油加入区;(4)石英砂流化和焦油反应区;(5)气体逃逸区,反应器的结构和尺寸如图2(b)所示。微型电加热炉最高温度为1200℃,利用热电偶进行温度检测。焦油通过微型注射器加样,样品体积控制在(10±0.2)μl范围内,注射器有手动和自动两种操作模式。焦油样品注入到加样区后,在载气携带下经分布板均匀分散后进入反应区。焦油在流化床内石英砂颗粒作用下发生热裂解(Ar 气氛)及重整反应(含水蒸气气氛)。焦油裂解生成的气体组分快速通过逃逸区,经冷却处理后进入气体检测单元。实验温度、压力和气体流量通过控制软件进行实时检测。与TGA 相比,该分析仪通过MFB 反应器强化热、质传递,有效限制反应器内气体扩散;能在任意温度下进行瞬时进样;实现气体产物快速在线检测。目前,该分析仪已在能源、化工、材料、冶金等领域的反应分析方面得到较好应用。

图2 实验装置原理图(a)和微型流化床反应器结构图(b)Fig.2 Schematic diagram of experimental device(a)and structure of micro-fluidized bed reactor(b)
焦油热裂解和水蒸气重整实验前,在MFB 反应器中装填高度约2 cm 的石英砂颗粒(粒径:150~180 μm),将反应器安置在微型加热炉中,依次连接供气、进样、分析装置,并对装置进行气密性检查;启动微型加热系统,采用30℃/min 的升温速率将反应器加热到指定温度(750、850、950℃);通入氩气,调节气体流量,确保石英砂颗粒正常流化;打开蒸汽发生器,在载气作用下将水蒸气通入反应器中,调节蒸汽和载气流量,形成稳定的水蒸气分压(steam partial pressure,SP:10%~30%)。考虑到温度对气体膨胀的影响,实验过程中,不同温度下的操作气速保持一致,焦油在反应区的停留时间维持在0.3 s 左右;将装有一定量焦油的微型注射器安置在进样系统上;待温度、颗粒流化状态和在线过程质谱(MS,Ametek Dycorsystem 2000)稳定后,手动将焦油快速注入加样区(<0.3 s),利用过程质谱在线监测气体组分变化。当MS 检测信号与基线一致时,停止实验;反应过程中生成的全部气体由气袋收集,其组分由微型气相色谱(GC,Agilent Micro 3000A)定量。为确保实验结果的准确性,每次实验后均更换石英砂,并用氧气焙烧反应器。
1.3 数据处理及分析方法
基于MS 检测的各气体组分信号强度随反应时间的演变和GC 检测到的气体组分平均浓度对实验数据进行综合处理,求算气体组分的生成质量(m)、各气体组分的生成率(X)和反应速率(R),进而开展动力学解析。
1.3.1 气体质量、转化率和反应速率的计算方法
图3 展示了850℃、10%水蒸气分压下焦油重整过程中MS 检测气体产物的释放曲线,气态产物包括H2、CH4、CO、CO2、C2H6和C3H6等,其中C2H6和C3H6含量很少,可以忽略。现以CH4为例说明MS检测信号的处理方法。
依据公式(3)可获得2004—2016陕西体育与旅游产业融合度,并根据融合度划分标准对两大产业融合发展程度做出评判(表2)。

图3 焦油水蒸气重整反应的数据处理方法Fig.3 Data treating approch of tar reforming in steam
图中t0为反应起始时间,即焦油瞬间注入到反应器中的时间;te为终止时间,即反应结束后MS 信号值重新回到基线的时间。S0-i定义为从t0到反应过程中任意时刻(ti)区间内的MS 信号强度曲线与基线之间的面积积分;S0-e定义为从t0到te区间内MS信号强度曲线与基线之间的面积积分,计算见式(1)和式(2)。
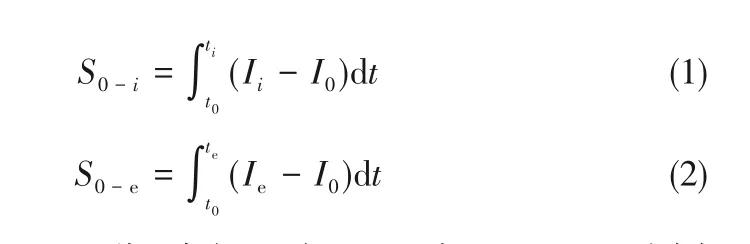
式中,I0、Ii和Ie分别为反应过程中t0、ti和te时刻的MS信号强度。
实验过程中通入Ar 的总流量可通过Ar 体积流量(F)和通入时间进行计算;生成气体的总体积(Ve)及各气体组分的体积可基于GC 检测的气体组分浓度(C)进行确定,反应过程中生成CH4的总体积(Ve-CH4)及任意时刻生成CH4体积(Vi-CH4)的计算公式见式(3)~式(5)。

反应过程中,从t0到ti和从t0到te过程中生成CH4的质量(mi-CH4、me-CH4)分别由式(6)和式(7)进行计算。气体产物中的总碳质量mi-C和me-C及总质量mi-T和me-T分别通过式(8)~式(11)进行计算。
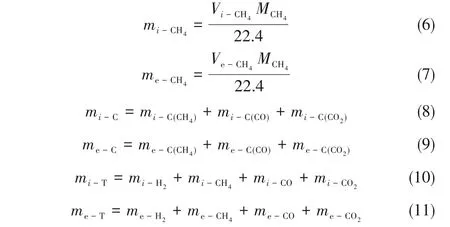
式中,MCH4为CH4的摩尔质量。
反应过程中ti时刻生成CH4的转化率(Xi-CH4)定义为t0~ti时间内生成CH4的质量与加入的焦油样品质量之比,Xi-CH4和Xe-CH4的计算公式见式(12)和式(13);ti时刻的气体产物中总碳转化率(Xi-C)定义为t0~ti时间内生成的CH4、CO和CO2中碳的质量(mi-C)与加入的焦油样品质量之比;Xi-T、Xe-T分别定义为t0~ti、t0~te时间内生成气体的总质量(mi-T和me-T)与加入的焦油样品质量之比;Xi-C、Xe-C、Xi-T和Xe-T的计算公式见式(14)~式(17)。
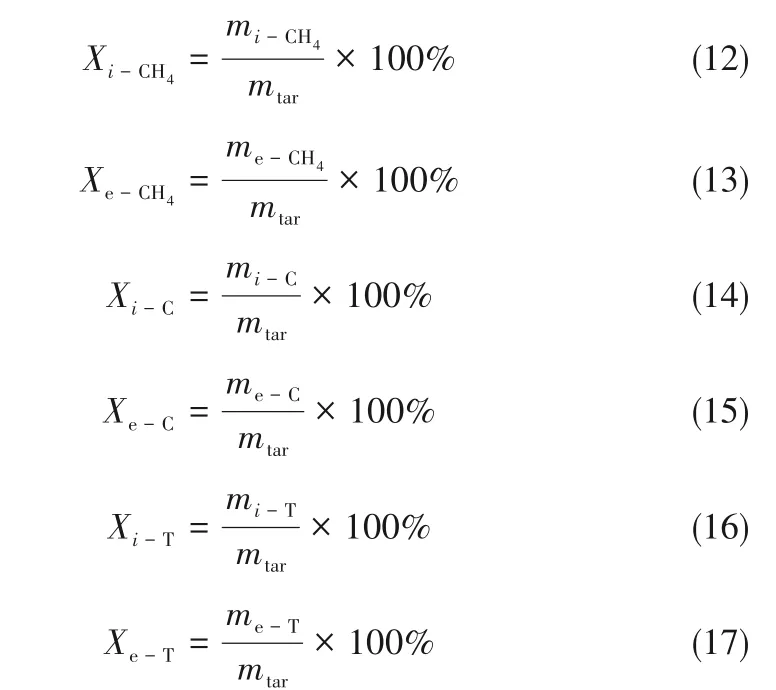
反应速率(R)定义为单位时间内转化率的变化量,ti时刻CH4、气体产物中总碳和焦油的反应速率(Ri-CH4,Ri-C,Ri-T)见式(18)~式(20)。

2 实验结果与讨论
2.1 焦油热裂解和水蒸气重整反应特性对比
图4 对比了不同温度下(T,750、850、950℃)焦油热裂解(Ar)和水蒸气重整(SP,10%、20%和30%)过程中H2产率的变化趋势。实验发现,热裂解过程中(纯Ar 气氛),750℃时,H2生成率低;>750℃时,随温度升高,反应时间逐渐缩短,且相同时间下的转化率增加,说明温度对H2生成的促进作用。热裂解过程中,H2主要来自焦油中大分子烃类分解、烃类环化和芳香环缩合等反应,升高温度有助于反应进行[17-18]。

图4 焦油热裂解(a)和水蒸气重整[(b)~(d)]过程中H2产率变化Fig.4 Variation of H2 yield in tar thermal cracking(a)and steam reforming[(b)—(d)]
焦油重整过程中,引入水蒸气后,在相同SP 下(10%、20%、30%),随温度增加,反应时间逐渐延长,且H2转化率快速增大,尤其是>850℃时。例如,在SP 为10%时,随温度升高,反应完成时间依次为6.6、8.8 和11.9 s;对应H2产率分别为0.002、0.005 和0.012,增加了5 倍左右,与文献[21]相符合。该过程中,H2主要来自:(1)水蒸气分解生成的·H 和·OH 自由基促进焦油大分子组分的裂解;(2)焦油裂解生成的积炭与水蒸气发生反应(R6);(3)焦油重整气态产物CO与水蒸气发生变换反应(R4)。
图5 对比了不同温度下(T,750、850、950℃)焦油热裂解(Ar)和水蒸气重整(SP,10%、20%和30%)过程中CO 产率的变化趋势。热裂解过程中,随温度升高,反应完成时间依次减小,而CO 产率明显提高,分别为0.18、0.34和0.37,这与H2生成趋势近似。在750~850℃内,增加温度对焦油热裂解的促进作用明显;而在850~950℃内,该促进作用变弱。在此过程中,CO 主要来自焦油中含氧官能团裂解,如羰基(C====O)、苯酚、含氧杂环[32-33]等。温度越高,热裂解越充分。焦油水蒸气重整过程中,等温下CO 生成的反应时间延长,且最终产率明显提高。例如,与Ar 气氛相比,当SP 为10%时,750、850 和950℃下反应时间分别从4.7、3.9、3.1 s延长到16.7、21.1、24.8 s;转化率也分别从0.18、0.34和0.37增加到0.27、0.41、0.50;此外,在850~950℃内,CO 最终产率仍显著增加,说明水蒸气良好的促进作用。

图5 焦油热裂解(a)和水蒸气重整[(b)~(d)]过程中CO产率变化Fig.5 Variation of CO yield in tar thermal cracking(a)and steam reforming[(b)—(d)]
实验也发现,在SP 为10%和20%的水蒸气气氛中,850℃和950℃时,初始反应段中CO 的产率非常接近,且高于750℃。而当SP 为30%时,750℃和850℃下初始反应过程中CO 的产率接近,且低于950℃。高温下,水分子分解剧烈,产生大量的·H和·OH 自由基,促进焦油中含氧官能团裂解及C2/C3等产物与·OH 自由基反应,最终生成CO[34]。实验结束后发现,反应器内壁上的积炭明显消失,这也证实了积炭与水蒸气气化反应的发生(R6)。对比水蒸气分压的影响发现,随SP 增加,750、850 和950℃下反应结束时XSP-30%/XSP-10%的比值分别为1.11、1.07 和1.12,说明水蒸气分压虽然改变了CO 的生成行为,但是对最终产率的影响较小。
图6 展示了不同温度下(T,750、850、950℃)焦油热裂解(Ar)和水蒸气重整(SP,10%、20%和30%)过程中CO2产率的变化趋势。在热裂解过程中,其变化趋势与H2、CO 近似。引入水蒸气后,不仅延长了焦油重整的反应时间,还改变了CO2产率的变化趋势。在等SP 下,随温度增加,CO2产率呈现先增加后减小的趋势,在850℃时达到最大值。例如,在SP为20%时,750、850 和950℃下CO2最终产率分别为0.15、0.27、0.15。焦油热裂解过程中,CO2主要来自焦油组分中羧基(—COOH)分解[33,35];焦油水蒸气重整过程中,CO2不仅是反应产物,也是焦油干重整反应(R3)和碳还原反应(R7)的反应物,导致其产率下降。
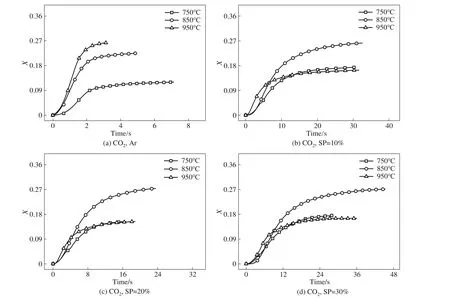
图6 焦油热裂解(a)和水蒸气重整(b)~(d)过程中CO2产率变化Fig.6 Variation of CO2 yield in tar thermal cracking(a)and steam reforming[(b)—(d)]
图7 展示了不同温度下(T,750、850、950℃)焦油热裂解(Ar)和水蒸气重整(SP,10%、20%和30%)过程中CH4产率随时间的变化趋势。在焦油热裂解过程中,其整体变化趋势与H2、CO和CO2近似,且在750~850℃内增加明显。此时,CH4主要来自芳香烃、脂肪烃的脂肪侧链断裂及芳甲基脱甲基作用[33,35]。焦油水蒸气重整过程不仅延长了反应时间,也大幅提高了CH4产率,尤其是在950℃时。相同SP 下,随温度增加,反应结束时CH4产率明显提高,以SP=10%为例,850℃和950℃时的CH4产率分别是750℃时的2.21 倍和2.92 倍,说明温度对CH4产率有重要影响。对比等温条件下SP 的影响发现,随SP 增加,CH4产率逐渐增加。例如,750、850和950℃时,SP 为10%、20%、30% 时CH4最大产率依次为0.062、0.066、0.073,0.136、0.148、0.153 和0.179、0.185、0.193。此外,在SP 为10%和20%时,850℃和950℃时初始反应段的CH4产率接近(反应时间小于5 s),远高于750℃时,与CO 生成率趋势近似;而在SP为30%时,在整个反应阶段内,相同时间下的产率依次为950℃>850℃>750℃。

图7 焦油热裂解(a)和水蒸气重整(b)~(d)过程中CH4产率变化Fig.7 Variation of CH4 yield in tar thermal cracking(a)and steam reforming[(b)—(d)]
图8 对比了不同温度下(T,750、850、950℃)焦油热裂解(Ar)和水蒸气重整(SP,10%、20%和30%)过程中气体产物中总碳转化率随时间的变化趋势,其整体变化趋势与H2、CH4、CO 近似,以焦油热裂解为例,温度升高促使反应进行,气体产物中的总碳转化率从750℃的34.3%提升到950℃的76.4%,说明温度对气体产物中碳转化起决定性作用。在焦油水蒸气重整过程中,气体产物中的总碳转化率在750~850℃内快速增加,而在850~950℃内增幅变缓。在950℃、SP为30%条件下,气体产物中的总碳转化率可达到92.34%。水蒸气气氛下,焦油中轻质组分裂解完全,重质组分缩聚成积炭与水蒸气进一步反应,转化成更多的CO、CO2和CH4。
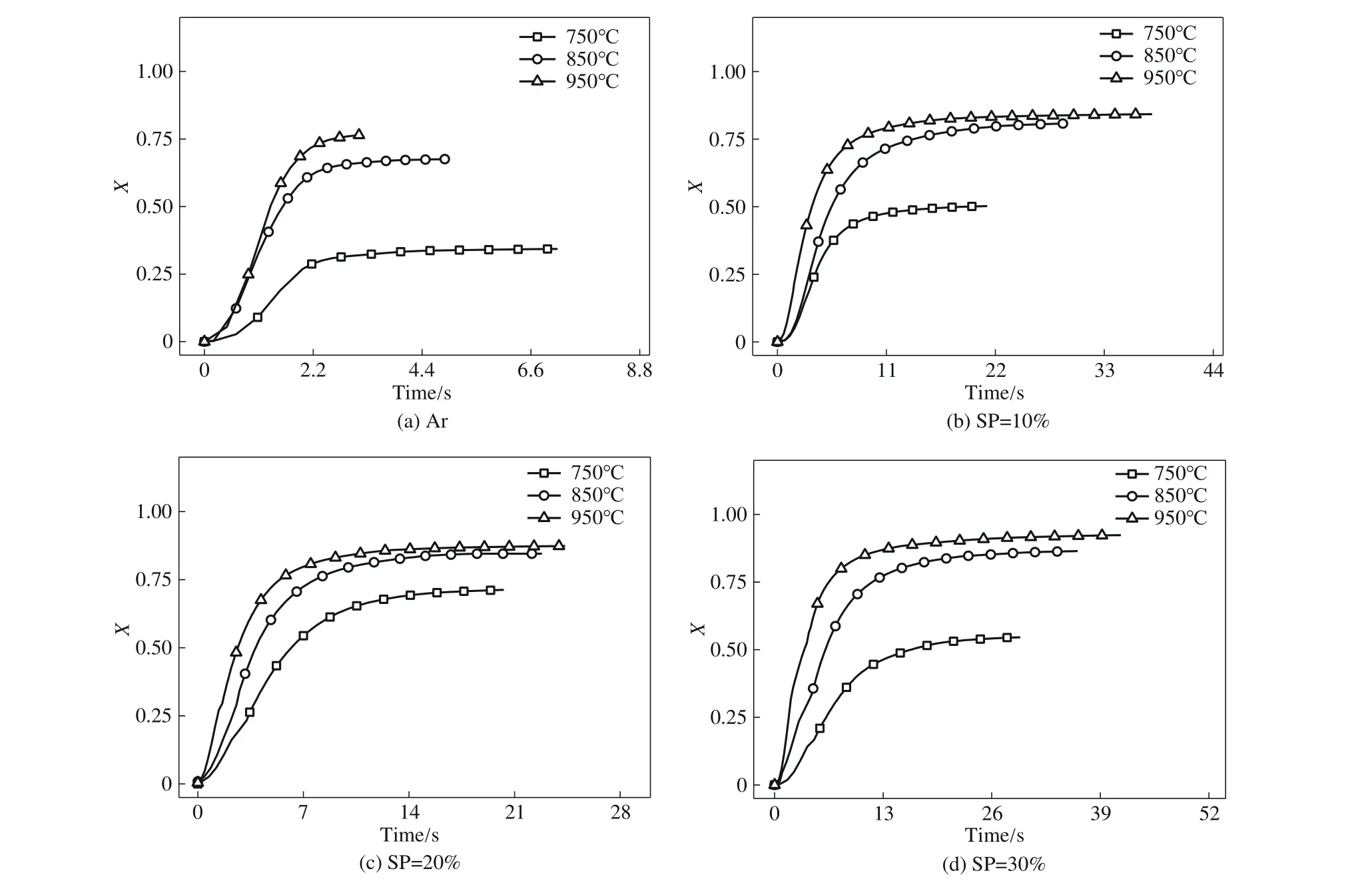
图8 焦油热裂解(a)和水蒸气重整[(b)~(d)]过程中气体产物中的总碳转化率变化Fig.8 Variation of carbon conversion in the gaseous products during tar thermal cracking (a)and steam reforming[(b)—(d)]
2.2 焦油热裂解和水蒸气重整反应速率对比
图9对比了实验温度范围内焦油热裂解和水蒸气重整(SP=10%)过程中气体组分和气体产物中总碳的反应速率与产率/转化率的关系。整体上,各速率曲线均呈先增加后减小的抛物线状变化趋势,在初始反应阶段即能达到最大反应速率。对于焦油热裂解和水蒸气重整,相同产率/转化率下,H2、CO、CH4生成速率和气体产物中总碳转化的反应速率均随温度提高而快速增加,说明温度的促进作用。分析也发现,水蒸气气氛中CO2的生成趋势有所不同,其在850℃时达到最大值,在950℃时反而较低,这主要是由于高温下CO2不仅参与焦油干重整反应(R3),还与焦油裂解产生的积炭发生反应(R7);且高温下,上述反应过程均被促进,导致CO2生成速率降低。与热裂解对比,焦油水蒸气重整过程中,虽然气体的产率和气体产物中总碳转化率增加,但是气体的生成速率和气体产物中总碳转化的反应速率反而降低,最大反应速率对应的产率/转化率也随之增加。这主要是由于焦油水蒸气反应过程不仅有官能团、支链的裂解[36],还有含碳组分及中间产物与水蒸气的反应,导致反应时间明显较热裂解长。

图9 不同条件下气体产率及气体产物中碳转化率与反应速率之间的关系Fig.9 Relationship of reaction rate vs.gas generation yield and carbon conversion at different conditions
图10以950℃为例对比了焦油重整过程中水蒸气分压对气体生成速率和气体产物中总碳转化速率的影响。随SP 增加,H2产率增加,而最大反应速率逐渐下降,曲线变宽,速率稳定段扩大。高SP下,焦油组分与·H 和·OH 自由基的接触机会增多,焦油裂解中间产物参与反应[37],H2生成路径变化。在SP=10%和20%时,CO 的初始生成过程中反应速率的变化接近,随转化率增加,高分压下CO 生成速率稍微偏高;当SP=30%时,CO 生成速率显著增大,说明CO 的生成路径发生改变,这与CO2参与反应有关。对CO2,随SP 增加,其生成速率逐渐下降,说明在此温度下,CO2参与反应加剧,使得反应速率降低。CH4和气体产物中总碳的反应速率变化趋势相似,转化率与最大反应速率均随SP 的增加而增大。

图10 不同水蒸气分压下气体产率/气体产物中碳转化率与反应速率曲线的变化Fig.10 Variation of reaction rate vs.gas yield or carbon conversion at different SP
2.3 反应动力学分析
对于焦油热裂解和水蒸气重整反应,本研究采用均相模型对实验温度范围内所得的数据进行线性拟合。以10%水蒸气分压为例,各温度下气体产率函数/气体产物中碳转化率函数[-ln(1-X)]与反应时间(t)的关系如图11 所示,在考察的转化率范围内,-ln(1-X)与t呈现出良好的线性关系,其拟合度大于0.99,说明均相模型能很好地描述上述反应和转化过程。由拟合曲线的斜率即可求取对应的反应速率常数kV。
在图11 的基础上,利用式(23),对lnkV与反应温度的倒数(1/T)作图,并进行线性拟合,结果见图12。根据不同实验温度范围内拟合曲线的斜率和截距即可求出反应的活化能(Ea)和指前因子(A)。
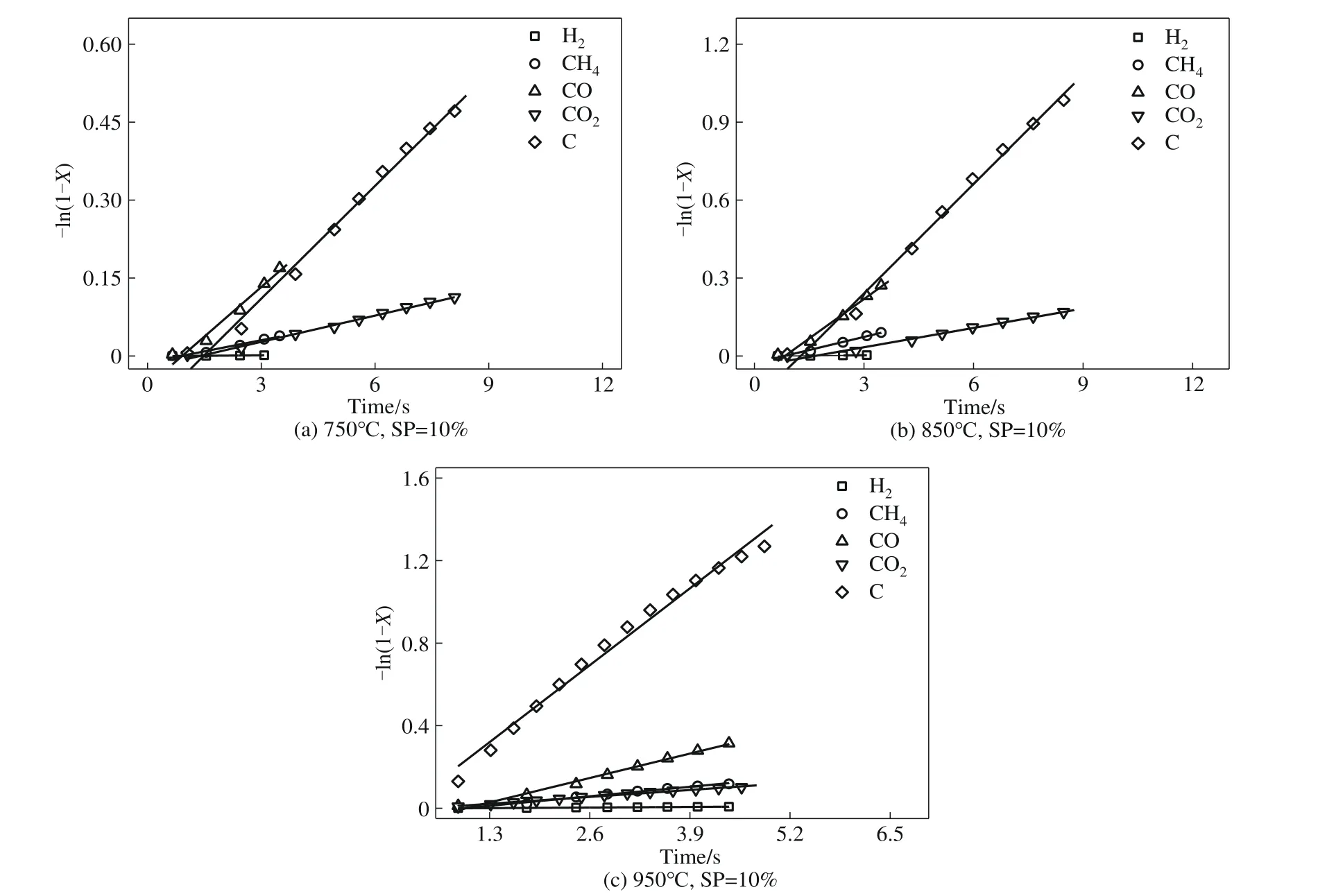
图11 不同温度下各气体和气体产物中总碳转化的均相模型数据拟合Fig.11 Fitting of homogeneous model data of gas generation and total carbon conversion in gaseous products at different temperatures

图12 不同水蒸气分压下速率常数与温度倒数的线性拟合Fig.12 Linear fitting of rate constant vs.1/T at different SP
表2 列出了主要气体产物(H2、CH4、CO、CO2)的生成、气体产物中总碳转化及焦油转化的反应动力学数据。对于焦油热裂解过程,H2、CO、CO2、CH4、气体产物中总碳及焦油转化的活化能分别为117.05、45.28、62.24、62.55、69.64和71.14 kJ/mol。反应活化能的不同说明了焦油组分在高温热裂解过程中生成气体或转化的难易程度。H2活化能最大说明其最难生成,官能团的裂解需要克服更高的能垒。对于水蒸气重整过程,在不同分压下(10%、20%、30%),H2、CO、CO2、CH4、气体产物中总碳及焦油转化的活化能分别在86.40~94.49、39.67~44.87、56.33~59.91、62.90~67.51、60.55~62.51 和62.81~63.55 kJ/mol范围内变化。分压不同,各活化能数据稍有差距,但是变化不大,对应的平均值为90.10、42.01、58.56、64.92、61.44和63.26 kJ/mol。与热裂解相比,水蒸气重整过程中H2、CO、CO2的生成和气体产物中总碳及焦油转化的活化能数据明显偏小,尤其是H2,说明通入水蒸气后,H2的生成途径改变,焦油组分与·H和·OH自由基接触增多,焦油裂解中间产物也参与反应,使得H2的平均活化能降低。此外,CH4在焦油热裂解和水蒸气重整反应过程中的活化能接近,后者略有增加,说明水蒸气存在对CH4生成的微弱抑制作用。
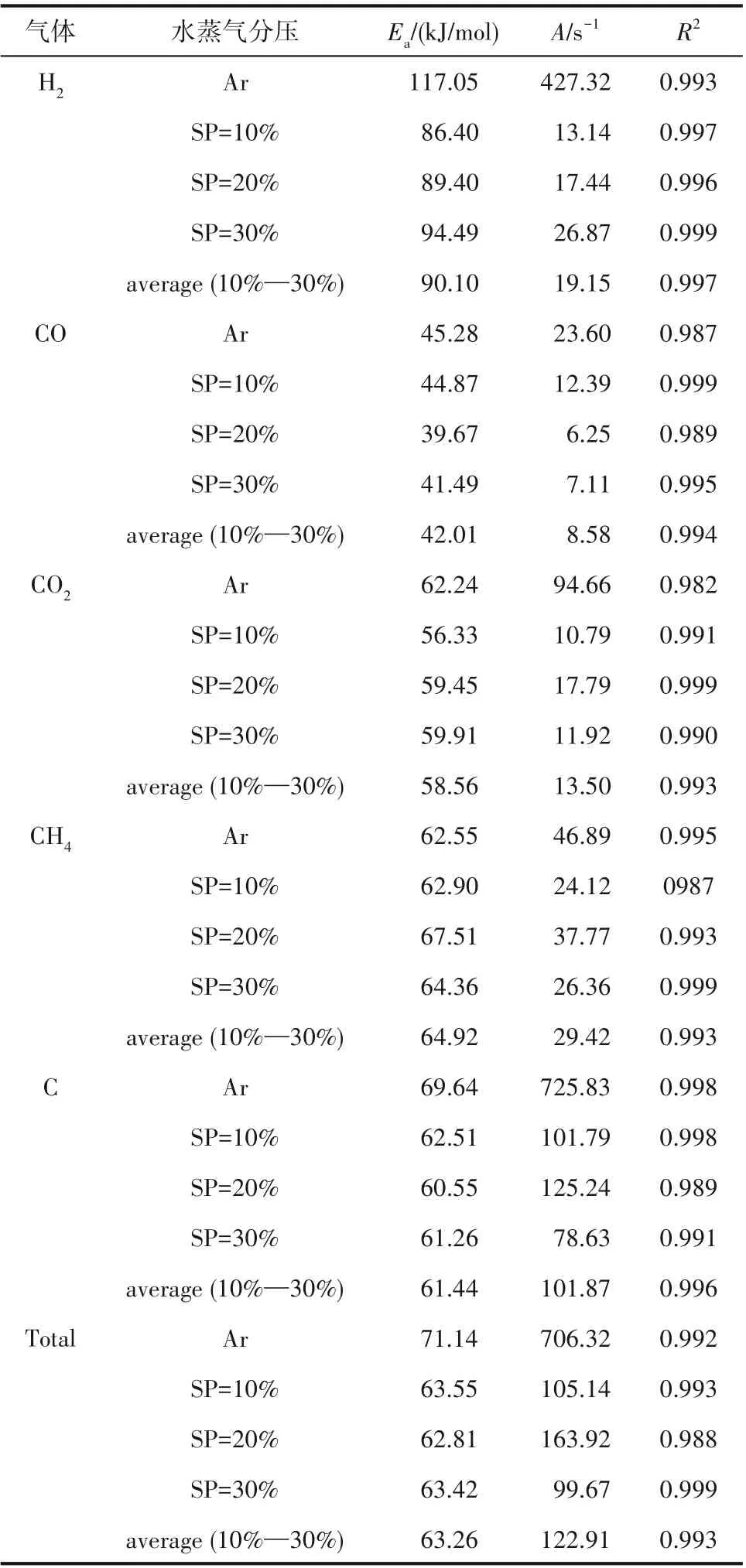
表2 焦油热裂解和水蒸气重整的反应动力学数据Table 2 Reaction kinetics data of tar thermal cracking and steam reforming
表3统计了文献中生物质焦油热裂解的动力学数据,涉及到的反应器包括流化床、热重反应分析仪、固定床反应分析仪等。文献中,热裂解过程中生物质焦油反应活化能在70.5~79.6 kJ/mol 范围内变化,与本研究数据近似,说明了MFBRA 求取动力学数据的可靠性。此外,Hu 等[38]采用MFBRA 进行热裂解实验,得到CH4的活化能为63.19 kJ/mol;Boroson 等[42]利用固定床进行焦油热裂解计算的H2生成活化能为129 kJ/mol,与本研究所求取的活化能数据相接近,也说明了本研究求取动力学数据的合理性。

表3 焦油热裂解活化能与文献数据对比Table 3 Comparison of Ea between tar thermal cracking in this study and literatures
3 结 论
本实验采用微型流化床反应分析仪考察了在750~950℃温度范围下焦油水蒸气重整的等温反应特性,求取了反应动力学,并与焦油热裂解进行对比,结论如下。
(1)焦油热裂解过程中,随温度升高,反应时间逐渐缩短,H2、CH4、CO、CO2的产率逐渐增大。与热裂解对比,在焦油水蒸气重整过程中,当分压一定时,随温度升高,反应时间增长,H2、CH4和CO 的产率和气体产物中的总碳转化率显著提高,CO2产率呈现先增加后减小的趋势,在850℃时有最大值。等温下,随水蒸气分压的增加,CO、CO2和CH4的最终产率变化不大,而H2产率和气体产物中总碳转化率增加明显。在950℃、SP=30%时,气体产物中的总碳转化率达到92.34%。
(2) 对于焦油热裂解和水蒸气重整,等产率/转化率下的H2、CO、CH4生成反应速率和气体产物中总碳转化反应速率均随温度增加而快速升高,且在初始阶段具有速率最大值。随水蒸气分压增加,CO、CH4和气体产物中总碳转化的反应速率增加,曲线变宽,速率稳定段扩大;H2反应速率逐渐下降,速率稳定段扩大;CO2反应速率在850℃时有最大值。
(3) 利用均相模型计算得到焦油水蒸气重整过程中H2、CO、CO2和CH4的平均生成活化能分别.是90.10、42.01、58.56、64.92 kJ/mol,气体产物中总碳转化及焦油转化的平均活化能分别为61.44、63.26 kJ/mol。与热裂解对比,焦油水蒸气重整过程中的气体生成活化能、气体产物中总碳转化活化能、焦油转化活化能均明显偏小。焦油重整过程中,水蒸气不仅降低反应活化能,还明显改善气体组分和提高气体产率。

