内镜下射频消融术治疗胃黏膜病变的短期疗效观察
朱春娴,陈宏扬,庞雨馨,孙蕾民
内镜下射频消融术(ERFA)指在消化内镜直视下将射频消融电极贴敷于消化道扁平黏膜病变处,通过高频射频波产生热量导致细胞凝固坏死从而消除病变的一种内镜微创治疗技术。近年来,ERFA的治疗范围从巴雷特食管(BE)合并上皮内瘤变拓展至平坦型消化道早期癌及其癌前病变、重度萎缩性胃炎、消化道毛细血管扩张症等表浅病变[1-2]。胃黏膜萎缩和肠化属于癌前状态,胃上皮内瘤变(GIN)也属于癌前病变,二者均有胃癌发生风险[3]。ERFA 应用于胃黏膜低级别上皮内瘤变(LGIN),短期临床疗效显著,并发症少,但尚未经充分临床验证。本研究回顾性分析行ERFA 治疗的慢性萎缩性胃炎(CAG)伴重度肠化及胃黏膜LGIN 患者的临床资料,探讨其对患者短期疗效的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2017 年9 月至2021 年3 月于浙江大学医学院附属邵逸夫医院行ERFA 的患者。纳入标准:(1)胃镜+活检病理诊断为CAG 伴重度肠化和(或)胃黏膜LGIN;(2)根除幽门螺旋杆菌(Hp)或者Hp阴性;(3)至少有术后3 个月时的随访胃镜及组织活检结果。共纳入41 例,其中男27 例,女14例;年龄(58.4±10.6)岁。本研究经浙江大学医学院附属邵逸夫医院伦理委员会同意并批准实施(伦理批号:科研20210330-38)。
1.2 方法 胃镜采用Olympus(日本)GIF-Q260J、GIF-HQ290 及附属设备和射频消融设备包括BARRXTM 射频消融发生器(Covidien llc,美国)和局灶性消融导管[13 mm×20 mm(BARRXTM 90),10 mm×15 mm(BARRXTM 60)]。常规上消化道内镜检查术前准备,发现病变部位后使用放大内镜(ME)+窄带成像技术(NBI)观察病变,确定病变大小、范围。消融能量设置为12 J 或15 J。视电极贴合程度治疗处可注射或不注射抬高病灶黏膜,将电极置于病变处进行消融,消融后病灶表面凝固坏死、颜色变白。一次消融完成后再进行下一次消融前,清除或不清除表面已凝固坏死组织。病灶每处灼烧2~5 次。
1.3 观察指标 记录术后3 个月胃镜复查病理缓解率,根据《胃炎的分类和分级:悉尼系统修正版》:(1)缓解:CAG伴重度肠化病灶处腺体萎缩至少改善一个级别并且肠化程度有下降或消失,LGIN病灶处上皮内瘤变消失;(2)未缓解:CAG 伴重度肠化病灶处腺体萎缩或肠化未改善甚至加重,LGIN病灶上皮内瘤变未改善甚至进展。次要结果为术后3个月胃镜复查影像缓解率:(1)缓解:病灶处内镜下异常改变缩小或消失;(2)未缓解:病灶处内镜下异常改变较前无明显变化或有新发异常改变。
1.4 统计方法 采用SPSS 25.0 统计软件进行统计分析,计量资料以均数±标准差表示,采用t 检验;计数资料采用检验或Fisher 确切概率法。P<0.05 为差异有统计学意义。
2 结果
2.1 术前病理诊断病灶的随访结果 41例中LGIN 病灶27 处,CAG 伴重度肠化84 处。27 处术前病理诊断存在LGIN 的病灶,18 处经过射频治疗随访病理结果未回报任何异型增生,9 处术前术后病理均显示LGIN。84 处术前病理诊断CAG伴重度肠化的病灶中,62 处经过射频治疗获得病理缓解,其中37 处转为中度肠化,20 处转为轻度肠化,5 处肠化消失。见表1。
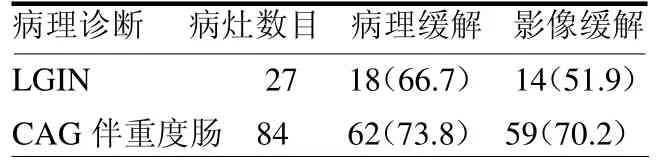
表1 术前病理诊断病灶的随访结果 处(%)
2.2 胃黏膜LGIN病理缓解的影响因素胃黏膜LGIN 病灶射频治疗后病理是否缓解与治疗后是否影像缓解相关(P=0.004),而与病灶部位、形态、是否合并肠化及不同射频方案参数无关(均P>0.05)。见表2~3。

表2 不同特征的胃黏膜LGIN 的病理缓解结果
2.3 CAG 伴重度肠化病理缓解的影响因素 CAG伴重度肠化病灶射频治疗后病理是否缓解与治疗后是否影像缓解、射频能量大小相关(均P<0.05),而与病灶部位、形态、是否合并肠化及射频电极、消融次数、术中是否铲除、术前是否注射抬高无关(均P>0.05)。见表4~5。
3 讨论
胃癌是全球发病率第4,死亡率第5的癌症,肠型胃腺癌是主要的胃癌亚型,其进展从正常黏膜到慢性胃炎、多灶性萎缩性胃炎、肠上皮化,直至最终的上皮内瘤变和腺癌。在胃癌筛查流程实际应用中,通过胃镜检查和病理活组织检查证实的CAG 和上皮内瘤变等病变状态的比例高达30%[4]。据报道,CAG 伴肠化患者的胃癌年发生率为0.25%。一项Meta分析显示1985—2016 年的21 项肠化患者胃癌风险调查研究结果表明肠化患者发生胃癌的风险更高(OR=3.58)[5]。上皮内瘤变是一种肿瘤性、非浸润性改变,是目前肯定的癌前病变。有文献报道高级别上皮内瘤变(HGIN)大部分情况下实际已同时存在癌变[6],因此对LGIN 患者进行积极的随访和科学的监测成为防治胃癌的有效途径。ERFA 能否长期改善甚至逆转胃黏膜的肠化及上皮内瘤变,目前仅有病例报道[7]。

表3 不同射频方案的胃黏膜LGIN 的病理缓解结果 例
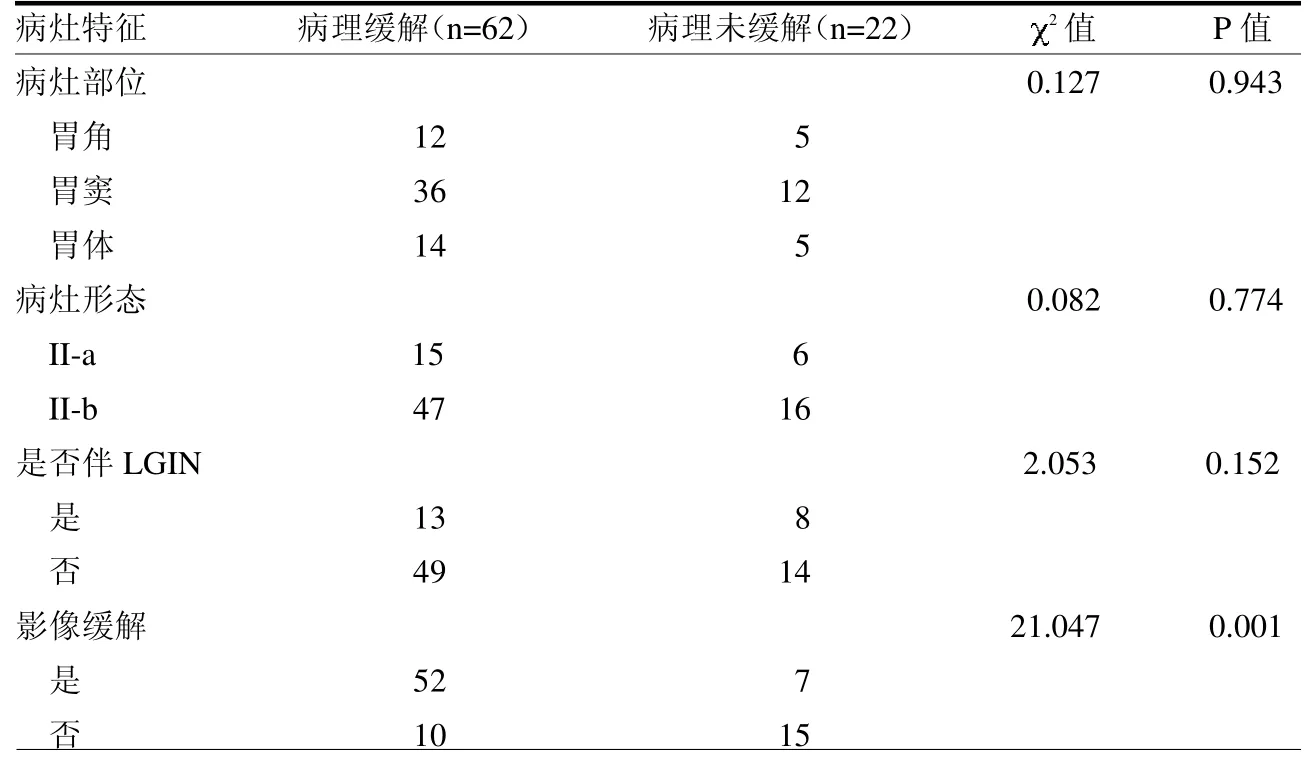
表4 不同特征的CAG 伴重度肠化病灶的病理缓解结果 例
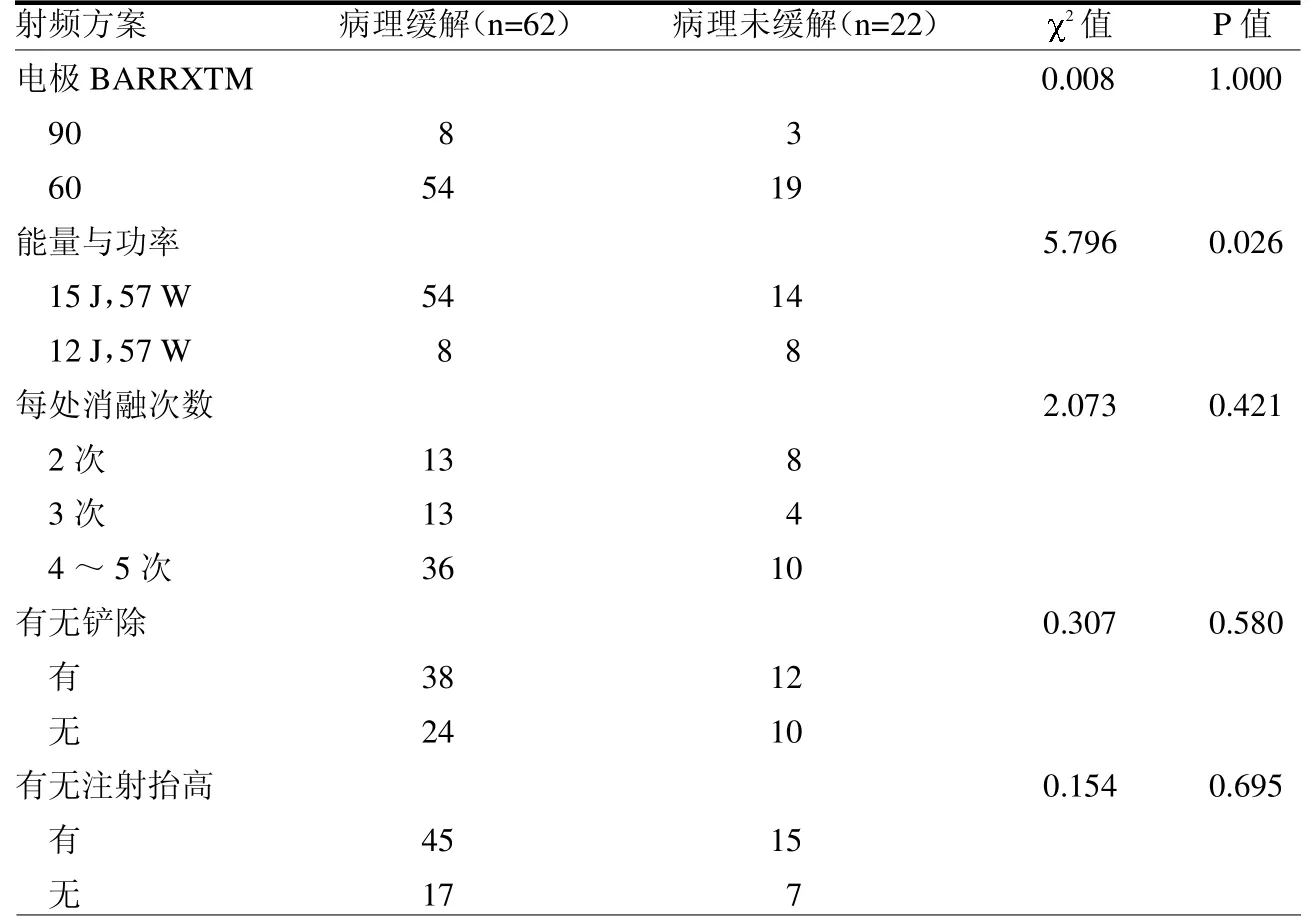
表5 不同射频方案的CAG 伴重度肠化病灶的病理缓解结果 例
本研究LGIN 和CAG 伴重度肠化的病理缓解率分别为66.7%和73.8%,尽管随访时间短,但笔者认为ERFA 用于LGIN 及CAG 伴重度肠化具有积极意义,在保证安全性的条件下寻求疗效最佳的射频方案值得进一步探索。疗效分析结果显示不同射频能量(12 J 和15 J)对CAG 伴重度肠化病灶的病理缓解有统计学意义(<0.05)。由于本研究纳入病例时间跨度大,既往胃黏膜病灶延续了巴雷特食管的射频治疗参数,目前公认的胃黏膜病灶射频治疗能量为15 J,本研究结果也证实了对于胃黏膜病灶,15 J 比12 J 的短期病理缓解率更高。理论上认为下一次消融前应铲除上一次消融导致的凝结坏死物,因其可能影响热传导从而降低疗效,而消融前行黏膜下注射抬高有利于电极与黏膜贴合更紧密从而增加疗效,但本研究结果显示有无铲除凝结坏死物和有无消融前黏膜下注射抬高对胃黏膜射频治疗后的病理缓解差异无统计学意义(>0.05)。这可能说明铲除凝结物和黏膜下注射抬高均不是影响射频消融疗效的绝对因素。
本研究有以下几个局限性:首先,作为单中心研究,不能完全排除选择与信息偏见,不同内镜医师技术水平也存在差异;其次,尽管有部分患者在治疗前采取了定标活检,未采取定标活检的病例在射频治疗前后获取病理标本时存在病灶部位的误差;再次,目前行ERFA 治疗人数少,随访时间短,很多疗效相关因素分析只能得出阴性结果,需进一步拓展并随访患者。

