一个基于偶氮六酸的稀土金属-有机框架
韩宗甦,于晓泳,闵 辉,师 唯,程 鹏
(南开大学化学学院,天津 300071)
金属-有机框架(MOFs)是由金属离子节点和有机配体通过配位键连接形成的微孔配位聚合物,由于其结构的多样性和性能的可调性引起了学者们的广泛关注[1~3].过渡金属离子和稀土金属离子均可用作节点来构筑MOFs.与过渡金属离子相比,稀土离子具有更高的配位数和多变的配位模式,可以形成在过渡金属MOFs中难以形成的结构,极大地推动了配位化学的发展.在性质方面,稀土金属-有机框架(Ln-MOFs)基于稀土离子独特的电子结构而具有发光特性,当作为“天线”的有机配体和稀土离子配位后,在紫外光下有机配体被激发,稀土离子从有机配体接收能量从而产生特征的发射光谱[4,5].
基于主-客体相互作用对能量传递过程的调控,Ln-MOFs已在各种离子、有机小分子、气体分子、爆炸物和生物功能分子等物种的化学传感研究方面引起了各国学者的关注[6~14].针对这些客体的检测通常是通过色谱法或者电化学法进行的,需要使用额外的溶剂和大型设备,检测程序繁琐且分析时间长,不利于实时快速检测.荧光传感技术具有响应快、成本低及操作方便等优点.国内外一些课题组围绕Ln-MOF传感材料已经取得了系列的研究进展并从不同的角度对其进行了总结.例如,Chen等[6]对MOF发光机理、相关性质研究和应用方面的研究工作进行了系统归纳;Li等[7]总结了过渡/稀土发光MOFs用于常见化学品和爆炸物检测方面的研究进展;Yan等[8]总结了构造多发光中心稀土MOFs并应用于温度、酸碱度、阴阳离子、分子、空气污染物及食物等的检测方面的研究工作;Zhou等[9]系统总结了MOFs用于荧光传感的最新进展,尤其是针对离子、有机分子、气体和温度的传感性质及其应用方面的研究进展;Su等[10]对白光MOFs的发光机理和应用进行了详细总结;本课题组[11]和Yin等[12]都对多发光中心MOF的设计和传感应用进行了深入的研究.
芳香多羧酸类配体不但具有多变的配位模式,其芳香基团也是良好的能量传递“天线”,在发光Ln-MOF的构筑及其传感应用中具有重要的研究价值.常用的芳香多羧酸类配体,如对苯二甲酸(IRMOF系列[15]等)、均苯三酸(HKUST-1[16]和MIL-100[17]等)、1,2,4,5-苯四甲酸[UiO-66-(COOH)2[18]等]和苯六甲酸[UiO-66-(COOH)4[18]等]等,已经被广泛应用于MOF的研究中.但当羧基数量增加时,单苯环的羧酸配体由于其分子内氢键增加和空间位阻等因素会导致对配位反应的调控相对困难,引入多芳基多羧酸类配体是解决这个问题的一个有效途径.本课题组[19]曾选择1,2,3-三羧基-(1′,2′,3′-三羧基偶氮苯)-苯(简称为偶氮六酸,H6TTAB)与铜(II)离子构筑了一例MOF,并研究了其对二氧化碳的选择性吸附性质.
本文使用H6TTAB作为桥连配体,合成了一例由H6TTAB配体与铕(III)离子构筑的Ln-MOF,[Eu2(H2TTAB)1.5(H2O)3]·3H2O(Eu-TTAB),并详细研究了其荧光性质.
1 实验部分
1.1 试剂与仪器
锌粉,天津市光复科技发展有限公司;盐酸(质量分数38%),永清县永飞化学试剂有限公司;5-硝基-1,2,3-苯三酸,济南恒化科技有限公司;氢氧化钠,阿拉丁试剂有限公司;无水乙醇,天津市康科德科技有限公司.所用试剂均为分析纯;蒸馏水,南大友嘉水站.
英国珀金埃尔默公司Perkin-Elemer 240型元素分析仪;英国牛津公司Oxford Supernova型单晶X射线衍射仪(SXRD),MoKα射线;日本理学公司Rigaku Smartlab SE型粉末X射线衍射仪(PXRD),CuKα射线;瑞士梅特勒-托利多公司Mettler Toledo TGA 2型热重分析仪(TGA),测试温度40~800℃,氮气氛围;瑞士布鲁克公司Bruker AV400型核磁共振波谱仪(NMR);美国赛默飞公司Thermofisher Scientific Nicolet iS50 FTIR型红外光谱仪(IR);英国爱丁堡公司Edinburgh FS5型荧光光谱仪(氙灯光源).
1.2 配体与MOF的合成
参考文献[19]方法制备H6TTAB,合成路线如Scheme 1所示.
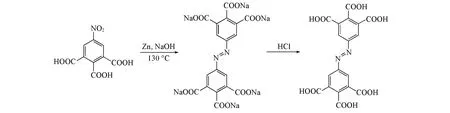
Scheme 1 Synthesis of H 6TTAB
将锌粉在新配制的3 mol/L盐酸中浸泡2 min,以去除表面氧化物,抽滤后用乙醇洗涤,晾干.
将2.53 g 5-硝基-1,2,3-苯三酸、1.5 g处理后的锌粉和2 g氢氧化钠置于250 mL圆底烧瓶中,加入50 mL乙醇和20 mL水,加热回流24 h,得到粗产物;过滤后将粗产物溶于100 mL 1 mol/L氢氧化钠溶液中,抽滤,滤液用3 mol/L盐酸调节pH值为3,得到大量橘色粉末,抽滤,晾干.1H NMR(400 MHz,D2O),δ:8.40.根据元素分析和热重分析结果,产物中有水和氯化钠同时析出,化学式为H6TTAB·3NaCl·5H2O.元素分析计算值(%,实测值):C 30.38(30.67),N 3.94(4.03),H 2.83(3.06).基于5-硝基-1,2,3-苯三酸计算的产率为70%.
将45 mg H6TTAB·3NaCl·5H2O和136 mg六水合硝酸铕溶于5 mL水和50µL浓盐酸的混合物中,在容积为23 mL的反应釜中于160℃反应48 h,经24 h降温到室温,得到大量Eu-TTAB橘黄色块状晶体.基于配体计算产率为75%.
1.3 晶体数据分析
选择一颗合适尺寸的单晶,采用石墨单色器单色化的MoKα(λ=0.071073 nm)射线作为入射光源,在X射线单晶衍射仪上收集衍射数据.所有非氢原子坐标利用SHELXS程序通过直接法解析,并利用SHELX程序对其坐标及各向异性参数进行精修[20].所有氢原子的位置通过理论加氢得到,并在结构精修中加入固定的各向同性热参数.Eu-TTAB的晶体学数据列于表1,CCDC号为2020713.PXRD图谱显示该MOF具有好的相纯度和结晶性[图1(A)].根据单晶衍射数据、元素分析和热重分析[TGA,图1(B)]结果,确定其分子式为[Eu2(H2TTAB)1.5(H2O)3]·3H2O.元素分析计算值(%,实测值),
C 30.16(30.14),N 3.91(3.85),H 1.97(2.64).
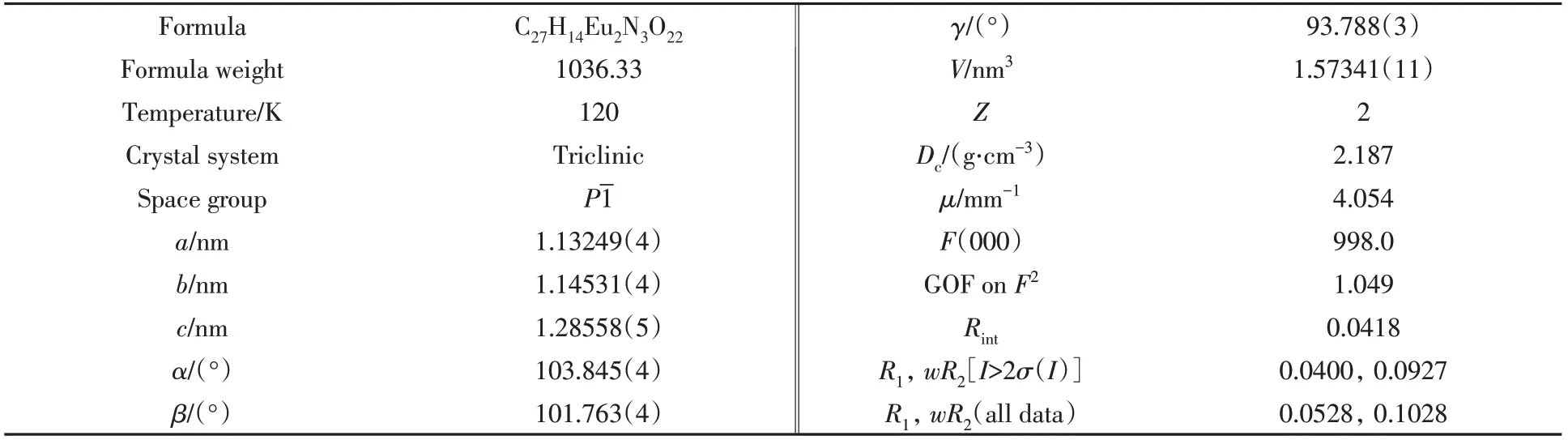
Table 1 Crystal data and structure refinement for Eu-TTAB

Fig.1 PXRD pattern(A)and TGA curve(B)of Eu⁃TTAB
2 结果与讨论
2.1 晶体结构分析
SXRD分析表明,Eu-TTAB结晶在三斜晶系的P-1空间群.图2给出Eu(III)离子的配位环境和Eu-TTAB的拓扑结构.其最小不对称结构单元由2个Eu、1.5个配体和3个配位水组成.2个Eu都分别与9个氧原子配位.与Eu1配位的9个氧原子中有8个分别来自于5个配体,其中有3个配体提供2个氧原子,有2个配体提供1个氧原子,另外1个氧原子来自于配位水分子;与Eu2配位的9个氧原子中有7个分别来自于4个配体,其中有3个配体提供2个氧原子,有1个配体提供1个氧原子,另外2个氧原子来自于配位水分子.每4个Eu之间由配体羧基的氧原子连接,形成Eu1-Eu2-Eu2-Eu1的线性四核配位单元,这些配位单元之间通过配体连接,形成三维框架结构.根据SXRD分析、元素分析及TGA结果确定Eu-TTAB的分子式,其最小结构单元中含有3个游离的水分子.如果去除水分子,根据SXRD数据分析,Eu-TTAB具有尺寸为0.4 nm×0.6 nm的一维孔道.
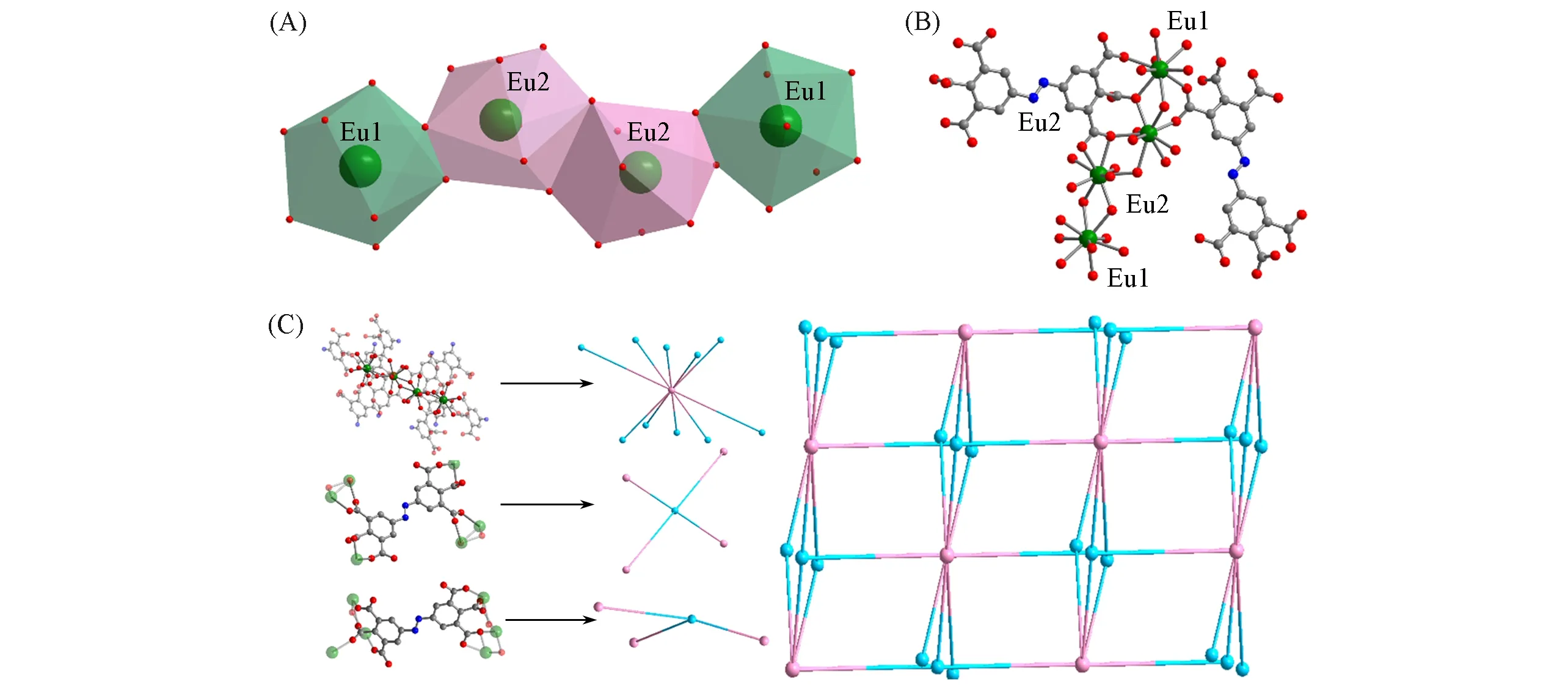
Fig.2 Coordination environment of Eu(A),Eu1⁃Eu2⁃Eu2⁃Eu1 linear coordination unit(B)and topology of Eu⁃TTAB(C)
进一步的结构分析表明,Eu1和Eu2,Eu2和Eu2之间由分别由2个配体的羧基μ3-O桥联.每个线性四核铕配位单元周围有10个配体,其中4个配体周围有4个线性四核铕配位单元,6个配体周围有3个线性四核铕配位单元.将连接3个线性四核铕配位单元的配体、连接4个线性四核铕配位单元的配体和线性四核铕配位单元分别视为3连接、4连接和10连接的节点,Eu-TTAB的结构可以被简化为一个三节点的(3,4,10)网络,Schläfli符号为{414·620·811}{43}2{45·6}.文献中报道了两例具有三节点(3,4,10)网络的MOF结构,但其拓扑分别为{414·624·87}{43}2{45·6}[21]和{418·624·83}{43}2{44·62}[22].
2.2 稳定性
将Eu-TTAB放入烘箱中,在特定温度下加热20 min后取出,对其进行PXRD测试.于200℃处理后,Eu-TTAB的PXRD图谱仍与室温图谱相吻合[图3(A)],表明其具有较好的热稳定性.对Eu-TTAB进行了变温原位红外测试,结果表明在200℃时其红外特征峰仍基本保持[图3(B)],进一步说明Eu-TTAB具有较好的热稳定性.

Fig.3 PXRD patterns(A)and in situ IR spectra(B)of Eu⁃TTAB under different temperatures
将Eu-TTAB在常用有机溶剂中浸泡5 h后对其进行PXRD测试(图4),结果表明Eu-TTAB具有很好的溶剂稳定性.Eu-TTAB表现出良好的热稳定性和溶剂稳定性,这是由于该MOF的结构中配体与配体之间存在π-π相互作用和氢键,稳定了框架结构.

Fig.4 PXRD patterns of Eu⁃TTAB treated by different solvents
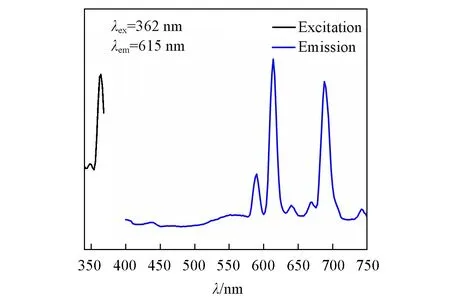
Fig.5 Fluorescence spectra of Eu⁃TTAB
2.3 荧光性质
在紫外光激发下测试了Eu-TTAB的固体发射图,其最强峰出现在615 nm处.再以615 nm为发射波长测试Eu-TTAB的固体激发图谱,发现最强吸收出现在362 nm处(图5).在Eu-TTAB的发射光谱中,由Eu3+离子f-f跃迁产生的4个特征发射峰分别出现在590,615,641和690 nm处,对应于5D0→7FJ(J=1~4)的跃迁[23~25].
我们还尝试通过稀土掺杂调控发光颜色,制备了同构的EuTb-TTAB.PXRD图谱显示Tb(III)离子的引入不会对其结构造成影响[图6(A)].当反应原料中硝酸铕和硝酸铽的投料摩尔比为1∶1时,615 nm处的发射峰强度和545 nm处的发射峰强度大致相同,产物显示淡黄色.将EuTb-TTAB在硝酸银溶液中浸泡过后,其荧光发射强度会明显增强[图6(B)].当将50 mg EuTb-TTAB在10 mmol/L的硝酸银水溶液中浸泡2 d后,Tb离子在545 nm处的发光强度增强到原来的2倍,Eu离子在615 nm处的发光强度增强到原来的4.5倍.这种发光增强效应是由Ag+增强了从配体到稀土离子的能量转移引起的[26].
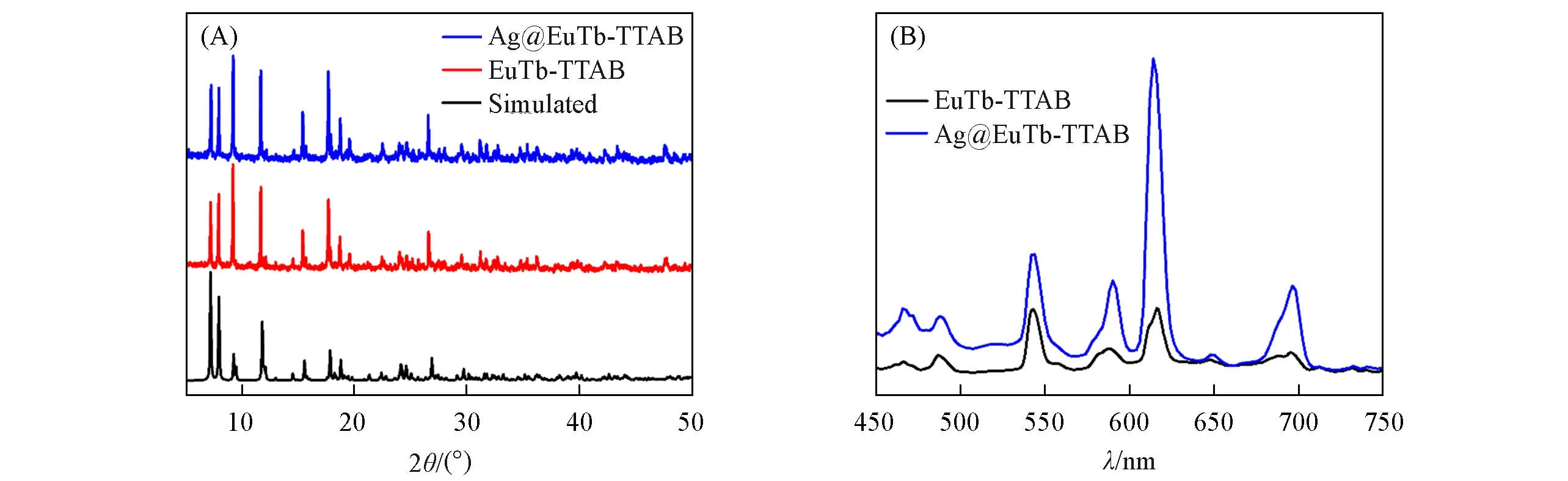
Fig.6 PXRD patterns(A)and fluorescence emission spectra(B)of EuTb⁃TTAB and Ag@EuTb⁃TTAB
3 结 论
基于偶氮六酸H6TTAB构筑了一例稀土金属-有机框架.该稀土金属-有机框架具有好的热稳定性、溶剂稳定性和发光性能.光致发光研究表明,铽离子和银离子的引入可以有效调控该稀土金属-有机框架的发光性能.

