黄芪/淫羊藿多糖微针制备及免疫效果分析
张学柏 兰州理工大学生命科学与工程学院,兰州 730050
微针作为一种新型的经皮免疫技术,具有高效、无痛、安全的特点,能打破角质层对药物的阻滞作用,提高递送效率,可用于疫苗递送[1-2]。微针可分为固体微针、涂布微针、中空微针和可溶性微针。其中可溶性微针的制备材料具有生物相容性的优点,当可溶性微针刺入皮肤后针体可以溶解在组织中也不会给皮肤增加负担。可溶性微针也存在力学性能较差等问题[3]。目前,可溶性微针的制备方法有两种,一种方法是将基质溶化与所需药物一起倒入模具中,将模具置于真空条件下,在一定温度下持续一定时间,干燥后即可得到载药的可降解微针,另一种方法是将药物和基质加入溶剂中,蒸发除去部分溶剂后,浇入模具中,高速离心,使药物和基质充分填满模具的空间,采用适当的干燥条件干燥使其慢慢固化,脱模即成[4]。
研究采用真空法制备聚乙烯吡咯烷酮(PVP)/黄芪多糖微针和聚乙烯吡咯烷酮(PVP)/淫羊藿多糖微针,通过对其成型性、机械强度和免疫效果进行分析,以期制备出以中药多糖为主要材料的微针。
1 试验与方法
1.1 试剂与仪器
黄芪/淫羊藿,甘肃兰州黄河中药材市场;聚乙烯吡咯烷酮(分析纯),合肥巴斯夫生物科技有限公司;蔗糖(分析纯),沈阳市新化试剂厂;吉林五星宠安士佳4联疫苗,飘扬猫咪宠物医院;Vero细胞,赛默飞世尔科技有限公司;所有其他化学品均为分析级,无需进一步纯化。SD大鼠,雄性,180 g-220 g,SPF级,购自兰州大学实验动物中心
恒温水浴锅(B-220型),上海亚荣生化仪器厂;磁力搅拌器(ZF-7),江苏省金坛市医疗仪器厂;光学显微镜(XSP-3CB),上海光学仪器一厂;体式显微镜(Stemi305),北京普瑞赛司仪器有限公司;真空干燥箱(DZF-6020),上海一恒科学仪器有限公司;拉力机(SMT-5000),扬州市赛思检测设备有限公司;冷冻干燥机(FD-1A-50),北京博医康实验仪器有限公司;酶标分析仪(DNM9206A),北京普朗新技术有限公司。
1.2 黄芪多糖/淫羊藿多糖的提取
分别称取处理的黄芪根茎和淫羊藿茎叶置于烧杯中,在烧杯中加入80%乙醇(料液比1:10),80 ℃条件下,水浴加热脱脂三次,每次3h。用四层医用纱布将醇提液过滤掉,留下药渣,将脱脂后的药渣放入恒温干燥箱中干燥。干燥好的药渣继续加入圆底烧杯中,并添加蒸馏水(料液比为1:10),在80℃下水浴提取三次,每次3h[5]。三次的提取液合并在4000 r/min转速下离心10 min,除去底部沉淀后,将上清液继续合并在一起,用旋转蒸发仪进行浓缩至一定体积,将浓缩液放置室温,用Sevage法除蛋白,蛋白除完全后,将浓缩液置于透析袋中进行透析,时间为3d,每24h更换一次去离子水,透析结束后将提前冷冻好的溶液放入冷冻干燥箱中冷冻干燥48h,最终得到初步纯化的淫羊藿和黄芪多糖。
1.3 黄芪/淫羊藿多糖微针的制备及形态观察
分别配置2%的黄芪/淫羊藿多糖溶液,25% PVP溶液,分别以黄芪/淫羊藿多糖溶液与PVP溶液体积比为1:1制备成混合溶液,并在混合溶液中添加0.15 g蔗糖。使用真空法,在室温干燥的条件下制备黄芪/淫羊藿多糖微针,然后将黄芪多糖制备的可溶性微针命名为HQ-1,淫羊藿多糖制备的命名为YYH-1,使用光学显微镜和体视显微镜观察微针的形态。
1.4 黄芪/淫羊藿多糖微针的机械强度测定
使用拉力机测定微针的机械强度,分别将HQ-1,YYH-1针尖朝上放在下压头上,设置移动速度为1 mm/min,测定不同比例下黄芪多糖微针的最大断裂力度,选出具有最大机械强度的黄芪多糖微针,拉力机的力与位移会被记录在电脑上,每个样品测试三次。
1.5 黄芪/淫羊藿多糖微针的免疫效果试验
1.5.1 负载犬四联疫苗的两种多糖微针的制备本次购买的疫苗是犬疫苗,需将狗的药用量换算成大鼠的药用量。因此,采用动物的体表面积计算法Meeh-Rubner氏公式进行换算[6]:
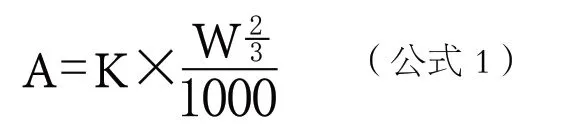
A:体表面积[m2];K:常数,K狗为11.2,K大鼠为9.1;W:体重[g]
称取适量犬四联疫苗粉末分别溶于提前制备好的两种多糖混合液中混匀。用真空法制备微针,由于犬四联疫苗的最适温度为2–8℃,因此用真空法制备好微针后将微针放入4℃硅胶盒中干燥,干燥结束后取出,即得负载犬四联疫苗的黄芪/淫羊藿多糖微针,记为QHQ-1和QYH-1,制备三组。
1.5.2 两种多糖微针的免疫效果试验
试验采用SD雄性大鼠作为免疫效果评价的动物模型。首先,对SD大鼠腹腔注射10%的水合氯醛溶液(0.3 mL/100 g)进行术前麻醉、固定,并用苦味酸进行标记。麻醉扎针时应有落空感,回抽时无尿液或血液[7]。给大鼠背部剃毛并用75%酒精消毒,将制备好的HQ-1、YYH-1、QHQ-1、QYH-1分别用大拇指按压1min,并用无菌纱布及弹性绷带包扎,处理结束后将老鼠放入笼中观察[8]。
将犬四联疫苗干粉溶于PBS溶液中,搅拌均匀,对大鼠皮下注射。其中阳性对照组为皮下注,阴性对照组为HQ-1,空白对照组为不做任何处理的健康大鼠。初次免疫时间10d后对大鼠进行眼眶取血,分离血清,存入-20℃冰箱中。继续重复初次免疫的操作步骤,进行二次免疫,20d后对大鼠进行眼眶取血,分离血清,存入-20℃冰箱中。
犬四联疫苗中包含犬瘟、细小、犬副流感、犬腺病毒四种,本实验选用犬四联疫苗中的犬副流感作为检测对象来检测大鼠体内的免疫效果。
1.6 细胞毒性检测
分别配置淫羊藿多糖溶液,黄芪多糖溶液,PVP溶液,蔗糖溶液(每种溶液设置低,中,高三个浓度),分别记为Y-1、Y-2、Y-3、H-1、H-2、H-3、Z-1、Z-2、Z-3、P-1、P-2、P-3。
非洲绿猴肾细胞(Vero细胞)的复苏:Vero细胞活化后,加入DMEM培养基,置于37℃二氧化碳培养箱中培养[9]。本实验采用MTT法检测细胞毒性[10]。
2 结果与讨论
2.1 微针的形态观察
通过在显微镜下观察制备的两种多糖微针,可以看到微针成四棱锥型,其中每个微针的针长为550 µm,针体底部尺寸为250×250 µm,相邻每两个针的针尖距离为600 µm,每个微针阵列的针体数目是225个,微针背衬部面积为9.5×9.5mm。并且微针的形态完整均一,微针的背衬部具有适当的厚度和柔软性。
2.2 机械强度分析
通过拉力机来测定微针的机械强度见图1。由力与位移的受力图可知,制备的微针具有一定的抗压性能,随着位移的增加,所受的力也呈现上升趋势,当微针完全破碎时,曲线会出现一个拐点,该点的力即为微针所能承受的最大压力,随后曲线呈直线上升。其中HQ-1的最大受力为768 N, YYH-1能承受的最大压力为676 N,这表明所制备的微针具有一定的机械强度,可以用于微针疫苗。
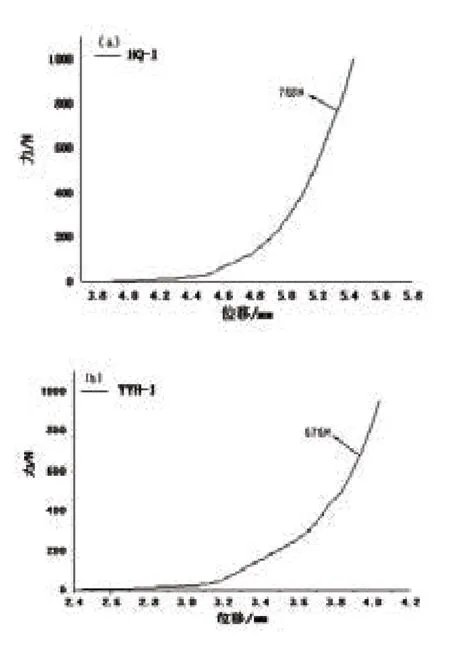
图1 黄芪多糖微针图(a)和淫羊藿多糖微针图(b)的机械强度图
2.3 免疫效果评价与分析
通过酶联免疫间接法对微针进行免疫效果的定性检测,分别是QYH-1组,QHQ-1组,皮下注射组,HQ-1组,健康大鼠组,试剂盒中的阳性对照和阴性对照。结果显示HQ-1组与健康大鼠组两次免疫后测得血清的OD值几乎没有变化,均小于0.343,PIV-Ab呈阴性。QYH-1组,QHQ-1组和皮下注射组初次免疫后各有一组血清的OD值大于0.343,PIV-Ab呈阳性,且QYH-1组和QHQ-1组测得血清的OD值略高于皮下注射组血清的OD值。二次免疫后QYH-1组和QHQ-1组的血清OD值均大于0.343,PIV–Ab呈阳性,并且OD值明显高于皮下注射组。这表明QYH-1和QHQ-1使大鼠产生了免疫应答,并且免疫效果高于皮下注射。黄芪多糖,淫羊藿多糖具有免疫增强作用,可能起到了佐剂的功效,这为黄芪多糖和淫羊藿多糖作为佐剂应用在微针疫苗中提供了可能性。
2.4 细胞毒性结果分析
培养72 h后,H-1,H-2,H-3,Y-1,Y-2,Y-3,Z-1,Z-2,Z-3,P-1,P-2,P-3对应的细胞存活率分别为100.84±12.94%,69.94±15.87%,76.58±11.20%,65.9±15.14%,54.66 ±8.77%,217.12 ±38.15%,141.72±16.99%,126.7±20.92%,84.4 8 ±20.95%,290.5±42.87%,243.28±39.17%,1 47.32±21.86%,其中H-2,Y-1,Y-2的细胞存活率在50%~75%的范围内。根据细胞毒性的评级划分2级,结合细胞形态进行评价后,判为合格,其余的微针材料溶液根据细胞毒性的评级划分0级或1级,判为合格。根据黄芪多糖,淫羊藿多糖,PVP,蔗糖溶液的低、中、高浓度的细胞毒性测量结果显示,此次制备的黄芪多糖微针和淫羊藿多糖微针的水溶性材料无细胞毒性。
结语
淫羊藿多糖微针,其具有适当的机械强度和生物相容性,可以在大鼠体内产生免疫应答。目前,市场上没有黄芪多糖和淫羊藿多糖作为佐剂用于微针疫苗,研究对中药多糖作为辅料兼佐剂用于微针疫苗及对微针疫苗的开发具有启发意义。

