把握电性规则 厘清有机化学反应原理
安徽 董 顺 广东 邱 萍


卤代烃、羧酸衍生物及醛酮的性质是高考的热点,而涉及的反应往往是陌生的,教材中没有介绍的,但是高考中遇到的反应的原理与教材介绍的反应原理是类似的,都可以借助电性规则来学习和理解。
一、从电性角度认识卤代烃的取代反应
卤代烃是烃分子里的氢原子被卤素原子取代后生成的化合物。通式可表示为R—X(其中R—表示烃基),官能团为—X(卤素原子),也称为碳卤键,如CH3CH2Br的官能团为C—Br(碳溴键),命名时以烃为母体,卤素原子作为取代基,选定官能团在内的碳链为主链。例如:
2-甲基-4-溴戊烷
3-甲基-2-氯戊烷
2-乙基-1-氯丁烷
4-溴-2-戊烯
教材中介绍,卤代烃在碱的水溶液中发生取代反应生成醇,比如:
从电性规则视角对上述反应进行分析,由于溴原子吸引电子能力比碳原子强,因此,碳溴键是碳原子带部分正电荷,溴原子带部分负电荷(Cδ+—Brδ-)的极性共价键,这种共价键在极性试剂的作用下容易发生共价键的异裂,带负电荷的溴原子被带负电的羟基取代,生成乙醇。
卤代烃的化学反应主要发生在碳卤键(Cδ+—Xδ-)上,带部分负电荷的卤素原子容易被带负电的其他原子或基团取代,生成各种类型的化合物。可简单表示如下:



【例1】(2018·全国卷Ⅰ·36)化合物W可用作高分子膨胀剂,一种合成路线如下:

回答下列问题:
(1)A的化学名称为________。
(2)②的反应类型是________。
(3)反应④所需试剂、条件分别为________。
(4)G的分子式为________。
(5)W中含氧官能团的名称是________。
(6)写出与E互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,峰面积比为1∶1)________。
【答案】(1)氯乙酸
(2)取代反应
(3)乙醇/浓硫酸、加热
(4)C12H18O3
(5)羟基、醚键


【分析】氯乙酸与碳酸钠反应生成氯乙酸钠,氯乙酸钠与NaCN发生取代反应生成C,C酸性条件下水解生成2个羧基,得到D(丙二酸)。D与乙醇发生酯化反应生成E(丙二酸二乙酯),E在强碱性条件下与卤代烃发生取代反应生成F,在催化剂作用下F与氢气发生反应将酯基转化为醇羟基,2分子G发生反应成环。
【说明】本试题中涉及两个陌生信息,一是B向D的转化,利用卤代烃与NaCN发生亲核取代反应,得到比卤代烃多一个碳原子的腈,然后酸性水解氰基(—CN)转化为羧基,该方法是制备羧酸的重要方法;二是E向F的转化,利用丙二酸二乙酯结构中中间的—CH2—为两个酯基的 α位,氢原子有一定的活性,在强碱(乙醇钠)作用下转化为碳负离子[⊖CH(COOC2H5)2],再与卤代烃发生亲核取代反应,实现α-烃基化。
二、从电性角度认识羧酸衍生物的取代反应
教材中介绍了酯的重要性质——水解反应,乙酸乙酯的酸性水解和碱性水解可分别表示为


该反应是分加成-消除两步进行的亲核取代反应,其过程可表示为

(1)水解反应
酰卤、酸酐、酯、酰胺和腈均可以在酸性或碱性条件下水解生成羧酸。
(2)醇解反应
酰卤、酸酐、酯和酰胺与醇反应生成酯,称为羧酸衍生物的醇解。
(3)氨(胺)解反应
酰卤、酸酐和酯与氨(胺)反应生成相应的酰胺,称为羧酸衍生物的氨(胺)解。
【例2】(2021·山东省选择性考试·19)信息
【说明】本题信息为酯的胺解,酯结构中带部分负电荷的烃氧基(R′O—)被带部分负电荷的R″NH—代替,如果考生掌握有机反应的电性规则,该信息非常容易理解,做题时就不会发慌。
三、从电性角度认识醛酮的加成反应
教材中介绍了醛的氧化反应和醛酮与H2的加成反应(还原反应),但高考中对醛铜性质的考查多为加成反应。
如醛酮与H—Y型试剂反应的通式可表示为
以乙醛为例,常见的反应如下:
α-羟基丙腈
α-羟基乙胺
乙醛半缩甲醇
【典例分析】近两年高考中常见的醛酮的加成反应信息分析。
【例3】(2021·全国乙卷·36)信息
【分析】
【说明】本题信息可理解为极性不饱和键碳氧双键首先与极性键氮氢键按照电性规则发生加成反应,形成α-羟基胺,然后两个羟基脱水形成稳定的五元环状结构。
【例4】(2021·河北省普通高中学业水平选择性考试·18)信息

【分析】
【说明】本题信息可理解为极性不饱和键碳氧双键首先与羧基α位的极性键碳氢键按照电性规则发生加成反应,形成β-羟基酸,然后再发生羟基的分子内脱水形成α,β-不饱和羧酸。
【例5】(2020·全国卷Ⅱ·36)信息
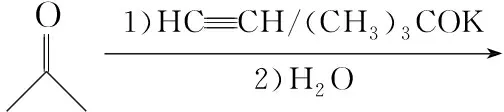
【分析】

【例6】(2020·全国卷Ⅲ·36)信息
【分析】
【说明】本题信息可理解为苯甲醛中的极性不饱和键碳氧双键与乙醛的α位的极性键碳氢键按照电性规则发生加成反应,形成β-羟基醛。
【例7】(2020·浙江七月选考·31)信息
【分析】
【说明】本题信息可理解为极性不饱和键碳氧双键首先与亚氨基中的极性键碳氢键按照电性规则发生加成反应,形成羟基,然后羟基再与亚氨基中的氮氢键脱水得到目标产物。
四、教学建议
电子效应包括诱导效应、共轭效应和超共轭效应,根据电子效应能解释亲电加成反应、亲核加成反应和亲电取代反应等的定位效应。比如丙烯与HBr发生加成反应可能生成1-溴丙烷和2-溴丙烷,由于甲基的供电子诱导效应使得与甲基直接相连的碳原子带有部分正电荷,根据电性规则加成产物以2-溴丙烷为主。再比如芳香烃发生取代有些是以邻对位产物为主,有些是以间位产物为主,都可以根据电子效应来解释。学生理解并熟练掌握电子效应及其应用,可以说是拿到了开启有机化学学习之门的钥匙,很多有机难题可以迎刃而解,对有机化学重点、难点内容会有更清晰的认识和理解。
但是,教师在中学阶段没必要对电子效应进行详细介绍,只需从键的极性角度理解,不宜拓展太多,即学生只需清楚有机反应电性遵循“异性相吸”的原则,这样就能够判断常见的取代反应和加成反应的产物。


