陌生物质化学式推断题的试题类型及解题模型
浙江 俞真蓉
浙江选考中出现的无机推断题,考查陌生物质的化学式推断,已与高考其他省份的试题有较大差异,试题多以小流程形式呈现。该题型常以物质的组成及反应产物的探究为背景,浓缩了元素及其化合物的知识,具有鲜明的化学学科特点,此类试题涉及的试题情境广,具有可考查内容多且容易控制卷面难度的题型特点,成了选考试题中一种十分重要的题型。
分析和解决此类试题需要学生将所学的化学学科知识与题给流程信息相融合,对学生综合应用化学知识的能力要求高,试题区分度较大。本文试从解题基础、推理模型、试题类型三个维度深度梳理陌生物质化学式推断题,提高学生对此类试题的分析与解决能力,培养学生化学学科思维的有序性、逻辑性、严密性和科学性,提升学生运用化学知识解决实际问题的能力,体现了化学学科核心素养“证据推理与模型认知”的价值。
1.解题基础
陌生物质化学式推断题是将基本概念、基本理论、元素单质及其重要化合物的知识与化学实验及简单计算有机结合的综合题型,该题解题时遵循浏览、整体扫描、把握信息(如“常见”“过量”等关键字眼)三个步骤,依物质的特性或特征转化来确定“突破口”,结合实验数据定量分析,进而完成全部未知物的推断。
1.1 必备知识
必备知识是学习者在面对与化学学科相关的生活实践或学习探索问题情境时,能够高质量地认识问题、分析问题和解决问题必备的知识。
1.1.1 具有一定特征的物质
(1)固体类
(淡)黄(棕)色固体:Na2O2、S、FeCl3;
黑色固体:MnO2、C、CuO、FeO、Fe3O4;
紫(黑)色固体:KMnO4、I2;
红色固体:Cu;
绿色固体:Cu2(OH)2CO3。
(2)气体类
有色气体:NO2(红棕色)、F2(浅黄绿色)、Cl2(黄绿色);
无色有刺激性气味气体:SO2、NH3、HX(X为卤族元素);
无色无味气体:H2、N2、O2、CO2、CO、CH4、NO。

(4)Br2在水中显黄(橙)色,在有机溶剂中显橙(红)色;I2在水中显黄(褐)色,在有机溶剂中显紫(红)色。
(5)沉淀类
白色沉淀:H2SiO3、AgCl、BaSO4、BaSO3、Mg(OH)2、Fe(OH)2、Al(OH)3、BaCO3、CaCO3、CaSO3、MgCO3等;
(淡)黄色沉淀:AgBr、AgI、S;
红褐色沉淀:Fe(OH)3;
蓝色沉淀:Cu(OH)2;
红色沉淀:Cu2O。
1.1.2 具有特殊状态的物质
(1)常温下呈液态的特殊物质:Br2(非金属单质)、Hg(金属单质)、H2O、H2O2等。
(2)易升华的物质:I2。
1.1.3 具有特殊现象的反应
(1)燃烧:H2与Cl2反应有苍白色火焰;C2H2(C6H6)与O2反应有明亮火焰并伴有大量黑烟;Al与O2、Mg与O2反应有耀眼白光,有白色固体生成。
(2)淀粉遇碘变蓝,蛋白质遇浓硝酸变黄。
(3)使湿润红色石蕊试纸变蓝的气体是NH3,使品红溶液褪色的气体是Cl2、SO2等。
(4)在空气中由无色变为红棕色气体的是NO。
(5)Fe3+遇OH-生成红褐色沉淀,遇苯酚显紫色,遇SCN-显血红色。
(6)Fe2+遇OH-生成白色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色;Fe2+遇SCN-无明显现象,在通入Cl2后溶液显血红色。
(8)既能与酸反应又能与碱反应并产生气体的物质:Al、弱酸的铵盐(碳酸铵、硫化铵等)、弱酸的酸式铵盐(碳酸氢铵、硫氢化铵等)。
(9)焰色试验:很多金属或它们的化合物在灼烧时都会使火焰呈现出特征颜色,一些金属的焰色如表1所示。
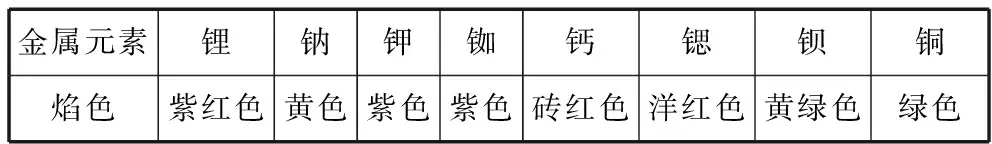
表1
(10)燃烧能生成烟:Na在氯气中燃烧生成白烟,Fe在氯气中燃烧生成红棕色烟,Cu在氯气中燃烧生成棕黄色烟。
1.1.4 需要特殊反应条件的反应
(1)“催化剂”:无机化学反应需要的催化剂不同,但是根据“催化剂”这一条件,可把氯酸钾分解、双氧水分解、工业合成氨、SO2催化氧化、氨催化氧化联系起来,形成知识链。
(2)“通电”或“电解”:可以锁定在电解水、氯化钠、氯化镁、氯化铜、硫酸铜、硝酸盐等溶液、熔融氯化钠和氧化铝的范围内。
(3)“高温”:常见的有碳酸钙分解、SiO2和C的置换反应、制造普通玻璃的反应、铝热反应等。
1.1.5 具有特殊用途的物质
(1)制造光导纤维的原料是SiO2;
(2)制造太阳能电池板的材料是Si;
(3)MgO、Al2O3可用作耐高温材料;
(4)能用作红色油漆的颜料中含有Fe2O3;
(5)可作制冷剂的物质是液氨或液氮;
(6)能作供氧剂的物质是Na2O2;
(7)用于治疗胃酸过多的物质可能是NaHCO3或Al(OH)3;
(8)治疗缺铁性贫血药物的物质是FeSO4;
(9)高效安全灭菌消毒剂是ClO2;
(10)用于自来水消毒或生成漂白粉的气体是Cl2。
1.1.6 具有特殊摩尔质量的物质
(1)氧化物:Na2O2—78 MgO—40 CaO—56
Al2O3—102 SiO2—60 FeO—72 Fe2O3—160
Fe3O4—232 CuO—80 Cu2O—144 SO2—64
SO3—80 CO—28 CO2—44
(2)氢化物:H2S—34 HCl—36.5
(3)氢氧化物:Mg(OH)2—58 Al(OH)3—78
Cu(OH)2—98 H2SiO3—78
(4)盐:Na2CO3—106 NaHCO3—84 CuSO4—160
CuSO4·5H2O—250 CaCO3—100 BaCO3—197
BaSO4—233 AgCl—143.5
1.2 关键能力
关键能力是指学习者初步运用化学视角和化学原理去观察和解决生活、生产和社会现象中某些化学问题的能力。《普通高中化学课程标准(2017年版2020年修订)》指出,学科核心素养是学科育人价值的集中体现,是学生通过学科学习而逐步形成的正确价值观、必备品格和关键能力。《2018年普通高等学校招生全国统一考试(总纲)》同样明确“必备知识、关键能力、学科素养、核心价值”四层考查内容。
浙江选考对于化学学科的考查,注重在与化学学科相关的生活实践或学习探索的问题情境中,从化学语言及应用能力、化学方法及分析能力、化学实验及研究能力、化学原理及推理能力和化学计量和计算能力等五个方面考查考生的学科核心素养。
在掌握解题必备知识的基础上,本题型的考查重点是化学方法及分析能力,解题问题的关键是采用定性和定量相结合的方式,通过守恒思想以及快速和准确的计算来确定陌生物质中所含元素的物质的量,以此求得各种元素的物质的量之比,具体如下:(1)质量守恒;(2)元素守恒;(3)得失电子守恒(氧化还原反应);(4)电荷守恒(电解质溶液)。
2.推理模型
试题的命制涉及立意、情境和设问三个要素。立意是试题所要考査的目标,情境是实现立意的材料和介质,设问是考査的呈现形式。“陌生物质化学式推断题”的情境与化学基本概念、基本理论、元素单质及其重要化合物知识以及化学实验及简单计算有机结合起来,对学生的学科能力也提出了更高的要求。试题设问方式多为陌生物质化学式的判断以及信息型化学方程式的书写,思维要求高、能力要求高,试题难度大,笔者基于教学实践,总结了如图1推理模型:

图1
定性分析环节:推断题思维过程的起点是该流程中显现的最显著的特征,依据题给条件、现象推断出流程中的相关物质,根据守恒思想,即可确定陌生物质所含的元素种类。
定量计算环节:推断题思维过程的展开,在确定了陌生物质所含的元素种类的基础上,根据守恒思想(质量守恒、元素守恒、得失电子守恒和电荷守恒等),计算得出相关元素的物质的量和各原子的个数比,从而确定陌生物质的化学式。
3.试题类型
3.1 热分解反应类型
【例1】为探究固体化合物X(仅含四种元素)的组成和性质,某同学设计并完成如图2实验。

图2
请回答:X的化学式是________。
【答案】3CuO·H2O·2CO2或Cu3(OH)2(CO3)2或Cu(OH)2·2CuCO3

第二步进行定量计算环节,确定陌生物质的化学式:
根据质量守恒定律,可以求出CO2的物质的量为0.02 mol,黑色化合物CuO的物质的量为0.03 mol,H2O的物质的量为0.01 mol,
质量守恒:3.46 g=2.40 g+0.18 g+0.88 g

元素守恒: 0.03 mol 0.01 mol 0.02 mol
物质的量之比: 3 ∶ 1 ∶ 2
则X的化学式为
(1)氧化物的形式:3CuO·H2O·2CO2
(2)盐的形式:Cu3(OH)2(CO3)2或Cu(OH)2·2CuCO3。
3.2 与氧气反应类型
【例2】已知化合物X、A均为红色固体,X含有四种元素,气体单质H密度为1.25 g·L-1(标准状况下)。流程中每一步反应试剂均过量且完全反应。
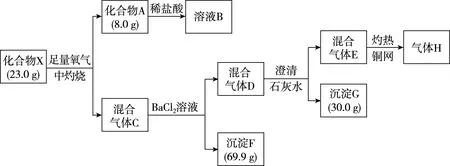
图3
请回答:固体X与足量氧气反应的化学方程式:____________________。
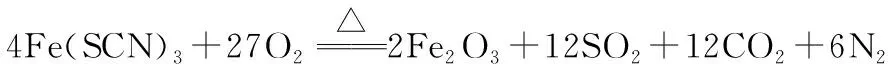

第二步进行定量计算环节,确定陌生物质的化学式:8.0 g Fe2O3的物质的量为0.05 mol;30.0 g的CaCO3的物质的量为0.3 mol,依据定量关系:CO2~CaCO3,CO2的物质的量为0.3 mol;69.9 g的BaSO4的物质的量为0.3 mol,依据定量关系:SO2~BaSO4,SO2的物质的量为0.3 mol。
根据质量守恒定律,可列下列等式:
质量守恒:23.0 g=5.6 g+9.6 g+3.6 g+4.2 g Fe S C N
元素守恒: 0.1 mol 0.3 mol 0.3 mol
0.3 mol
物质的量之比: 1 ∶ 3 ∶ 3 ∶ 3

3.3 与氢气反应类型
【例3】(2019·浙江4月选考·27节选)固体化合物X由三种元素组成。某学习小组进行了如图4实验:

图4
请回答:X的化学式是________。
【答案】NaCuO2
【分析】依据推理模型,第一步进行定性分析环节,推断出陌生物质的组成元素:从题给的流程推断可知,固体化合物X在干燥的H2中反应生成能使白色CuSO4变蓝色的气体,可推测为水蒸气,说明X中含有氧元素;固体混合物Y加水溶解得到1.28 g紫红色固体单质,该单质为Cu;得到的碱性溶液的焰色反应呈黄色,说明该碱性溶液中存在Na+;又因固体化合物X由三种元素组成,则三种元素分别为O、Cu、Na。
第二步进行定量计算环节,确定陌生物质的化学式:1.28 g紫红色固体单质Cu的物质的量为0.02 mol;该碱性溶液为NaOH溶液,与HCl恰好中和时消耗0.020 0 mol HCl,说明NaOH的物质的量为0.020 0 mol,固体X中含有钠元素的质量为0.46 g,
根据质量守恒定律,可列出下列等式:
质量守恒:2.38 g=0.46 g+1.28 g+0.64 g
Na Cu O
元素守恒: 0.02 mol 0.02 mol 0.04 mol
物质的量之比: 1 ∶ 1 ∶ 2
则X的化学式为NaCuO2
3.4 与酸反应类型
【例4】(2020·浙江7月选考·28节选)化合物X由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝的气体Y,Y为纯净物;取3.01 g X,用含HCl 0.060 0 mol的盐酸完全溶解得溶液A,将溶液A分成A1和A2两等份,完成如图5实验(白色沉淀C可溶于NaOH溶液):

图5
请回答:X的化学式是________。
【答案】AlCl3NH3
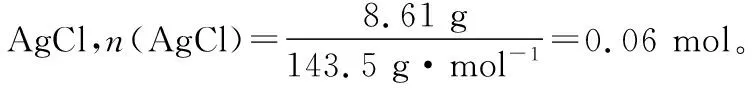
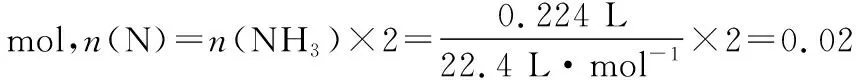
质量守恒:3.01 g=0.54 g+2.13 g+0.28 g+0.06 g
Al Cl N H
元素守恒: 0.02 mol 0.06 mol 0.02 mol
0.06 mol
物质的量之比: 1 ∶ 3 ∶ 1 ∶ 3
故X的化学式为AlCl3NH3。
3.5 与碱反应类型
【例5】(2021·浙江6月选考·28节选)固体化合物X由三种元素组成,某学习小组开展如图6探究实验。

图6
其中,白色沉淀B能溶于NaOH溶液。
请回答:化合物X的化学式是________。
【答案】CuAl2Cl8
【分析】依据推理模型,第一步进行定性分析环节,推断出陌生物质的组成元素:从题给流程推断可知,白色沉淀B能溶于NaOH溶液,则B是Al(OH)3,可推测C为Al2O3;根据蓝色溶液D,确定存在Cu2+;根据白色沉淀E,可确定存在Cl-;所以组成X的元素有Al、Cu和Cl。
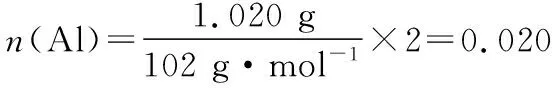
质量守恒:4.020 g = 0.540 g+2.840 g+0.640 g
Al Cl Cu
元素守恒: 0.02 mol 0.08 mol
0.01 mol
物质的量之比: 2 ∶ 8 ∶ 1
故X的化学式为CuAl2Cl8。
3.6 解题模式
由上述例题的分析可知,陌生物质化学式推断题的解题模式有两种,分别适用于不同类型的试题。
(1)试题类型属于热分解反应,宜采用解题模式1:

(2)试题类型属于氧化还原反应和复分解反应,宜采用解题模式2:

4.教学反思
陌生物质化学式推断题型复杂,思维容量大。因此,在“陌生物质化学式推断题”的教学中,合理分类试题类型、应用相匹配的解题模式,有利于提高学生解决此类试题的能力,培养学生化学思维的有序性、逻辑性、严密性和科学性。


