缬草中1个新的单环氧木脂素
张东东,樊 浩,孙 玉,张化为,姜 祎,李玉泽,王 薇,宋小妹*
缬草中1个新的单环氧木脂素
张东东1, 2,樊 浩1,孙 玉1,张化为1,姜 祎1,李玉泽1, 2,王 薇1,宋小妹1*
1. 陕西中医药大学药学院,陕西 咸阳 712046 2. 陕西省中药基础与新药研究重点实验室,陕西 咸阳 712046
研究缬草的化学成分及其细胞毒活性。采用硅胶柱色谱、葡聚糖凝胶柱色谱以及半制备HPLC等方法进行分离纯化,根据理化性质、MS、NMR和ECD数据鉴定化合物的结构,采用MTT法测定化合物的细胞毒活性。从缬草中分离得到15个化合物,分别鉴定为缬草木脂素A(1)、(7,8,8′)-tetrahydro- 7-(4-hydroxy-3-methoxyphenyl)-8′-[(4′-hydroxy-3′-methoxyphenyl)methyl]-8-(hydroxylmethyl)-8,8′-furandiol(2)、schisanpropinin(3)、(+)-异落叶松脂素(4)、ecdysanol B(5)、(−)-2-(3′-甲氧基-4′-羟基-苯基)-3,4-二羟基-4-(3″-甲氧基-4″-羟基-苄基)-3-四氢呋喃甲醇(6)、jatamanin A(7)、jatamanin K(8)、jatamanin R(9)、longiflorone(10)、阿魏酸(11)、咖啡酸(12)、对香豆酸(13)、咖啡酸甲酯(14)、对羟基肉桂酸甲酯(15),化合物10对人结肠癌HCT116细胞具有细胞毒活性,半数抑制浓度(median inhibition concentration,IC50)值为(70.9±6.4)μmol/L。化合物1为新化合物,化合物2、3、5~10首次从缬草中分离得到,化合物10具有一定的细胞毒活性。
缬草;单环氧木脂素;缬草木脂素A;longiflorone;细胞毒活性
缬草L.为败酱科(Valerianaceae)缬草属Linn. 植物缬草的干燥根及根茎[1]。其性寒,味辛、苦,归心、肝经,具有镇静安神、解痉止痛之功效。临床主要用于治疗心神不安、心悸失眠、焦虑等症[2]。缬草属是败酱科多年生草本植物,包括约250种、28个变种[3]。缬草广泛分布于温带地区,在陕西省主要分布于长安、宁陕、蓝田、黄龙等地区。
缬草中主要含有木脂素、环烯醚萜、倍半萜类等化学成分[4]。近年来研究发现,缬草生物活性多集中于对神经系统的作用,其中包括有镇静作用、解痉镇痛作用、抗抑郁作用、抗焦虑与抗癫痫作用等[5]。本课题组在前期研究基础上[6-7]对缬草的化学成分进行了进一步的系统分离和鉴定,从中共得到了15个化合物,分别为缬草木脂素A(valeofficinlignan A,1)、(7,8,8′)-tetrahydro-7- (4- hydroxy-3-methoxyphenyl)-8′-[(4′-hydroxy-3′-methoxy- phenyl) methyl]-8-(hydroxyl-methyl)-8,8′-furandiol(2)、schisanpropinin(3)、(+)-异落叶松脂素 [(+)-isolariciresinol,4]、ecdysanol B(5)、(−)-2-(3′-甲氧基-4′-羟基-苯基)-3,4-二羟基-4-(3″-甲氧基-4″-羟基-苄基)-3-四氢呋喃甲醇 [(‒)-3,4-dihydroxy- 2-(4-hydroxy-3-methoxyphenyl)-4-(4-hydroxy-3-methoxybenzyl)-3-tetrahydrofuran-methanol,6]、jatamanin A(7)、jatamanin K(8)、jatamanin R(9)、longiflorone(10)、阿魏酸(ferulic acid,11)、咖啡酸(caffeic acid,12)、对香豆酸(coumaric acid,13)、咖啡酸甲酯(methylcaffeate,14)、对羟基肉桂酸甲酯(methyl--hydroxycinnamate,15)。其中,化合物1为新化合物,命名为缬草木脂素A,化合物2、3、5~10为首次从该植物中分离得到,细胞毒活性测试结果显示化合物10具有抑制作用。
1 仪器与材料
AVANCE 型核磁共振波谱仪(德国 Burker 公司);YMC-Pack Pro C18半制备色谱柱(250 mm×10 mm,5 μm);LC-6AD 型半制备液相色谱仪(日本岛津公司);Sephadex LH-20(GE Healthcare Bio-Sciences AB公司);DLSB series型低温冷凝循环泵(郑州长城科工贸公司);柱色谱硅胶(100~200、200~300目,青岛海洋化工厂);薄层硅胶板(烟台江友硅胶发展有限公司);其他试剂均为分析纯;水为超纯水。
缬草于2018年7月采自陕西省眉县境内,经陕西中医药大学药学院王薇教授鉴定为败酱科缬草属植物缬草L.的干燥根。
2 提取与分离
缬草药材10.0 kg,粉碎后用10倍量80%乙醇回流提取3次,每次1.5 h。合并提取液,减压浓缩至浸膏,分散于水中,分别用石油醚和水饱和正丁醇萃取3次,得石油醚部位14.0 g、正丁醇部位289.0 g。
取正丁醇部位采用硅胶柱色谱分离,以二氯甲烷-甲醇(80∶1、60∶1、40∶1、20∶1、10∶1、5∶1)系统洗脱,得到8个组分Fr. 1~8。Fr. 3(23.2 g)柱硅胶柱色谱分离,石油醚-醋酸乙酯(40∶1、30∶1、20∶1、10∶1、5∶1)梯度洗脱,得到5个组分Fr. 3.1~3.5。Fr. 3.1(2.1 g)采用葡聚糖凝胶LH-20柱色谱分离(二氯甲烷-甲醇1∶1),合并相同流分,再经SP-HPLC纯化(甲醇-水55∶45,2 mL/min),得化合物11(27.4 mg,R=19.2 min)、12(28.0 mg,R=13.4 min)、13(15.5 mg,R=35.6 min)、14(19.6 mg,R=47.2 min)。Fr. 3.2(1.7 g)经SP-HPLC纯化(甲醇-水44∶56,2 mL/min),得化合物1(25.2 mg,R=28.4 min)、2(21.1 mg,R=31.3 min)、15(26.0 mg,R=42.1 min)。Fr. 3.3(2.9 g)经SP-HPLC纯化(甲醇-水30∶70,2 mL/min),得化合物7(19.4 mg,R=14.4 min)、8(25.0 mg,R=25.6 min)、9(32.2 mg,R=36.2 min)、10(23.3 mg,R=38.6 min)。Fr. 3.4(3.5 g)采用葡聚糖凝胶LH-20柱色谱分离(二氯甲烷-甲醇1∶1),合并相同流分,再经SP-HPLC纯化(甲醇-水45∶55,2 mL/min),得化合物3(19.7 mg,R=24.4 min)、4(25.8 mg,R=28.7 min)。Fr. 3.5(3.7 g)采用葡聚糖凝胶LH-20柱色谱(二氯甲烷-甲醇1∶1)反复纯化得化合物5(22.6 mg)和6(19.0 mg)。
3 结构鉴定
表1 化合物1的1H-NMR (400 MHz, CDCl3)和13C-NMR (100 MHz, CDCl3)数据
Table 1 1H-NMR (400 MHz, CDCl3) and 13C-NMR (100 MHz, CDCl3) data of compound 1
碳位δCδH碳位δCδH 1127.9—5′114.46.87 (1H, overlap) 2112.76.78 (1H, d, J= 1.7 Hz)6′119.96.88 (1H, overlap) 3146.8—7′84.54.69 (1H, d, J= 7.1 Hz) 4144.8—8′56.52.58 (1H, ddd, J= 7.1, 6.6, 5.8 Hz) 5114.66.88 (1H, overlapped)9′62.34.18 (1H, dd, J= 11.6, 6.6 Hz)4.37 (1H, dd, J= 11.6, 5.8 Hz) 6122.76.74 (1H, dd, J= 1.7, 8.0 Hz)1′′173.0— 739.42.85 (1H, d, J= 13.7 Hz)2.97 (1H, d, J= 13.7 Hz)2′′43.52.17 (2H, d, J= 6.9 Hz) 881.5—3′′25.82.07 (1H, m) 977.83.70 (1H, d, J= 9.5 Hz), 3.90 (1H, m)4′′22.60.94 (3H, d, J= 6.6 Hz) 1′133.5—5′′22.60.96 (3H, d, J= 6.6 Hz) 2′108.97.02 (1H, d, J= 1.7 Hz)3-OCH356.53.88 (3H, s) 3′146.9—3′-OCH356.53.88 (3H, s) 4′145.7—
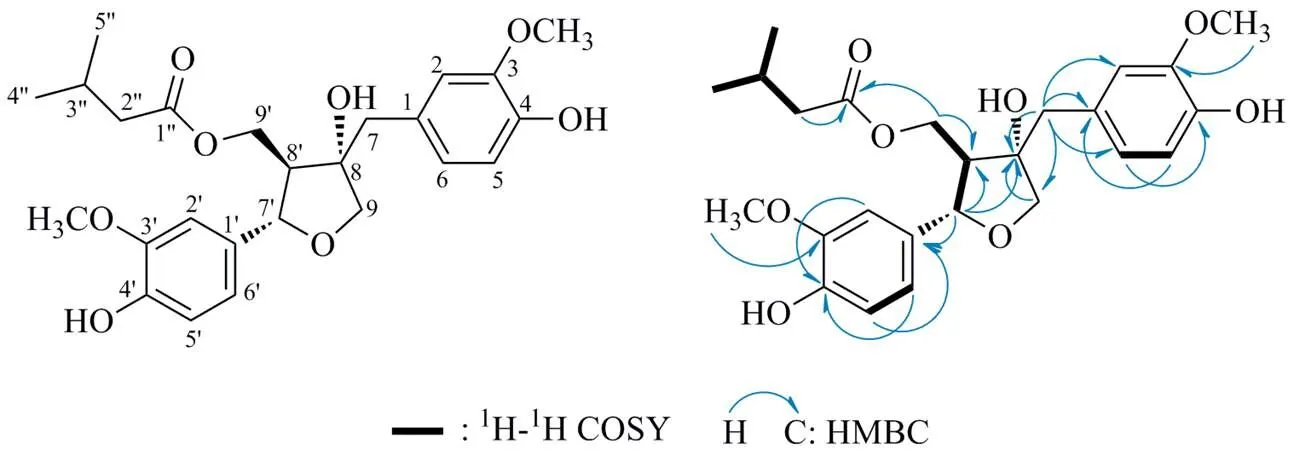
图1 化合物1的化学结构及主要的1H-1H COSY和HMBC相关信号
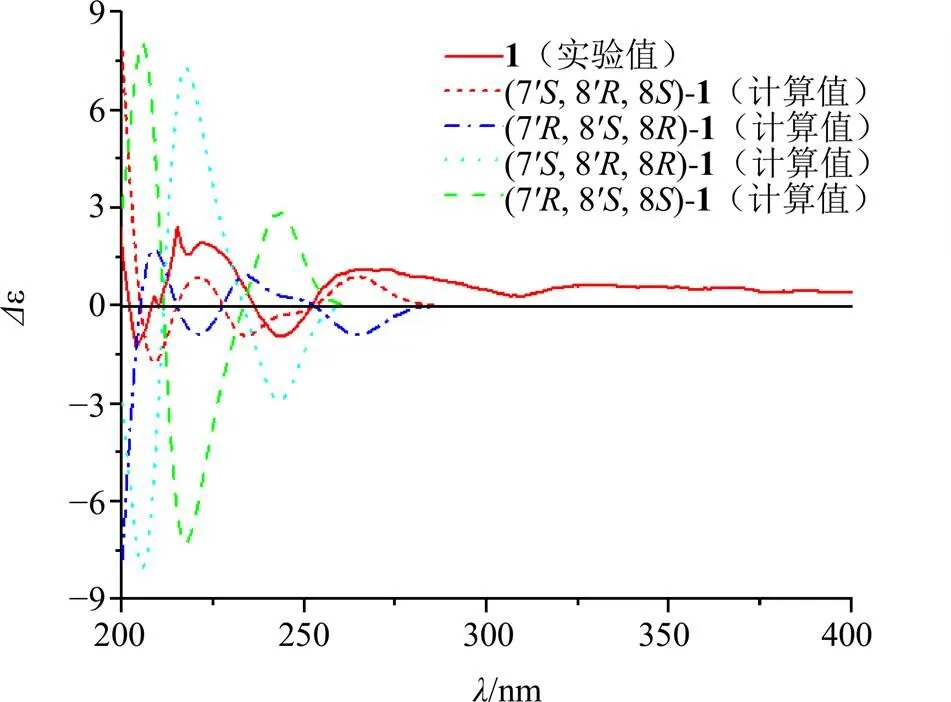
图2 化合物1的实验和计算ECD谱图
化合物7:无色针状结晶(甲醇),ESI-MS/:199 [M+H]+。1H-NMR (400 MHz, CD3OD): 4.33 (1H, d,= 11.5 Hz, H-3a), 4.98 (1H, d,= 10.8 Hz, H-3b), 3.23 (1H, m, H-5), 1.89 (1H, t,= 10.9 Hz, H-6α), 2.06 (1H, t,= 11.5 Hz, H-6β), 3.65 (1H, brs, H-7), 2.88 (1H, d,= 10.8 Hz, H-9), 1.36 (3H, s, H-10), 4.94 (1H, s, H-11a), 5.01 (1H, s, H-11b);13C-NMR (100 MHz, CD3OD): 175.2 (C-1), 71.3 (C-3), 144.1 (C-4), 41.2 (C-5), 40.7 (C-6), 81.4 (C-7), 86.4 (C-8), 53.6 (C-9), 22.3 (C-10), 113.8 (C-11)。以上数据与文献报道进行对比[8],鉴定化合物7为jatamanin A。
化合物11:白色粉末(甲醇),ESI-MS/:195 [M+H]+。1H-NMR (400 MHz, CDCl3): 6.30 (1H, d,= 15.9 Hz, H-2), 7.59 (1H, d,= 15.9 Hz, H-3), 7.17 (1H, d,= 2.0 Hz, H-5), 6.80 (1H, d,= 8.2 Hz, H-8), 7.05 (1H, dd,= 8.2, 2.0 Hz, H-9), 3.88 (3H, s, -OCH3);13C-NMR (100 MHz, CDCl3): 171.0 (C-1), 115.9 (C-2), 146.9 (C-3), 127.8 (C-4), 111.7 (C-5), 150.5 (C-6), 149.4 (C-7), 116.4 (C-8), 124.0 (C-9), 56.4 (-OCH3)。以上数据与文献报道进行对比[17],鉴定化合物11为阿魏酸。
化合物12:白色针状结晶(甲醇),ESI-MS/181 [M+H]+。1H-NMR (400 MHz, CDCl3): 7.02 (1H, d,= 2.0 Hz, H-2), 6.76 (1H, d,= 8.0 Hz, H-5), 6.99 (1H, dd,= 8.0, 2.0 Hz, H-6), 7.43 (1H, d,= 16.0 Hz, H-7), 6.23 (1H, d,= 16.0 Hz, H-8), 3.65 (3H, s, -OCH3);13C-NMR (100 MHz, CDCl3): 125.6 (C-1), 116.5 (C-2), 146.3 (C-3), 149.7 (C-4), 121.7 (C-5), 115.2 (C-6), 145.5 (C-7), 114.3 (C-8), 167.2 (C-9), 51.6 (-OCH3)。以上数据与文献报道进行对比[18],鉴定化合物12为咖啡酸。
化合物13:白色针状结晶(甲醇),ESI-MS/:165.2 [M+H]+。1H-NMR (400 MHz, CDCl3): 7.54 (2H, d,= 8.4 Hz, H-2, 6), 6.86 (2H, d,= 8.4 Hz, H-3, 5), 7.63 (1H, d,= 16.0 Hz, H-7), 6.37 (1H, d,= 16.0 Hz, H-8);13C-NMR (100 MHz, CDCl3): 126.3 (C-1), 130.6 (C-2, 6), 115.8 (C-3, 5), 159.4 (C-4), 145.2 (C-7), 115.3 (C-8), 168.3 (C-9)。以上数据与文献报道进行对比[19],鉴定化合物13为对香豆酸。
化合物14:白色针状结晶(甲醇),ESI-MS/:195.3 [M-H]−。1H-NMR (400 MHz, CD3OD): 7.07 (1H, d,= 1.6 Hz, H-2), 6.77 (1H, d,= 8.0 Hz, H-5), 6.95 (1H, dd,= 8.0, 1.6 Hz, H-6), 7.53 (1H, d,= 15.6 Hz, H-7), 6.22 (1H, d,= 15.6 Hz, H-8), 3.83 (3H, s, -OCH3);13C-NMR (100 MHz, CD3OD): 127.6 (C-1), 111.4 (C-2), 149.2 (C-3), 150.3 (C-4), 115.7 (C-5), 123.8 (C-6), 146.7 (C-7), 116.3 (C-8), 171.2 (C-9), 56.3 (9-OCH3)。以上数据与文献报道进行对比[20],鉴定化合物14为咖啡酸甲酯。
化合物15:白色粉末(甲醇),ESI-MS/:179 [M+H]+。1H-NMR (400 MHz, CD3OD): 7.43 (2H, dd,= 7.8, 1.9 Hz, H-2, 6), 6.72 (2H, dd,= 7.8, 1.9 Hz, H-3, 5), 7.62 (1H, d,= 15.9 Hz, H-7), 6.33 (1H, d,= 15.9 Hz, H-8), 3.74 (3H, s, -OCH3);13C-NMR (100 MHz, CD3OD): 127.2 (C-1), 131.4 (C-2, 6), 162.3 (C-4), 117.2 (C-3, 5), 146.7 (C-7), 114.7 (C-8), 170.2 (C-9), 52.2 (-OCH3)。以上数据与文献报道进行对比[21],鉴定化合物15为对羟基肉桂酸甲酯。
4 细胞毒活性测试
根据本课题组前期研究[22],采用MTT法分别测定了化合物1~15对3种肿瘤细胞(人肺癌A549细胞、人结直肠癌细胞HCT116和SW620)的细胞毒活性。结果显示,仅化合物10对HCT116细胞具有温和的细胞毒活性,半数抑制浓度(median inhibition concentration,IC50)值为(70.9±6.4)μmol/L,其余化合物的IC50值均大于100 μmol/L。
5 讨论
本研究综合运用多种现代色谱分离技术和波谱鉴定手段对缬草的80%乙醇提取物中的化学成分进行了系统研究,从中分离鉴定了15个化合物,其中化合物1为新化合物,化合物2、3、5~10首次从该植物中分离得到,同时细胞毒活性测试结果显示仅化合物10对HCT116细胞具有细胞毒活性,关于以上化合物的其他活性测试有待进一步研究。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国科学院中国植物志编辑委员会. 中国植物志[M]. 北京: 科学出版社, 1980: 31-32.
[2] 樊浩, 严淑婷, 梁小飞, 等. 缬草化学成分及生理活性研究进展 [J]. 辽宁中医药大学学报, 2019, 21(12): 172-175.
[3] 刘娟, 汪洋. 缬草属药用植物的研究进展 [J]. 黑龙江医药科学, 2007, 30(1): 94-95.
[4] 王茹静, 黄青, 雍妍, 等. 缬草属植物的化学成分及生物活性研究概况 [J]. 中国中药杂志, 2016, 41(8): 1405-1414.
[5] 陕西省食品药品监督管理局. 陕西省药材标准起草说明: 2015年版 [M]. 西安: 陕西科学技术出版社, 2017: 353-357.
[6] 樊浩, 李玉泽, 严淑婷, 等. 缬草化学成分的研究 [J]. 中成药, 2020, 42(11): 2930-2934.
[7] Fan H, Li Y Z, Liang X F,. Chemical constituents isolated fromL [J]., 2020, 93: 104143.
[8] Lin S, Chen T, Liu X H,. Iridoids and lignans from[J]., 2010, 73(4): 632-638.
[9] Zhang D, Li J, Ruan D,. Lignans fromroots and their inhibitory effects on nitric oxide production [J]., 2019, 137: 104189.
[10] Zhang D D, Ruan D Q, Li J Y,. Four undescribed sulfur-containing indole alkaloids with nitric oxide inhibitory activities fromL. roots [J]., 2020, 174: 112337.
[11] Huang Y Y, Qiu X, Xie Y G,. New acetylenic compounds and lignans from(Franch.) Shih [J]., 2019, 31: 125-130.
[12] Liu M, Hu Z X, Luo Y Q,. Two new compounds fromvar.[J]., 2017, 7(3): 257-262.
[13] Jutiviboonsuk A, Zhang H J, Tan G T,. Bioactive constituents from roots of[J]., 2005, 66(23): 2745-2751.
[14] Dong D D, Li H, Jiang K,. Diverse lignans with anti-inflammatory activity from[J]., 2019, 134: 96-100.
[15] 陆颖, 段书涛, 潘家祜, 等. 中药大蓟化学成分的研究 [J]. 天然产物研究与开发, 2009, 21(4): 563-565.
[16] Quan L Q, Su L H, Qi S G,. Bioactive 3, 8-epoxy iridoids from[J]., 2019, 16(5): e1800474.
[17] Ricardo L L, Bernardi D I, Mantovanelli G C,. Phytochemical investigation and phytotoxic activity of aerial parts of oilseed radish (var.Stokes) [J]., 2018, 78: 52-58.
[18] Lv Q, Lin Y, Tan Z,. Dihydrochalcone-derived polyphenols from tea crab apple () and their inhibitory effects on α-glucosidase[J]., 2019, 10(5): 2881-2887.
[19] 黄正, 霍会霞, 任易, 等. 大花益母草的化学成分研究[J]. 中草药, 2017, 48(09): 1724-1729
[20] 刘晓, 叶江海, 李继新, 等. 道真产淡黄香茶菜化学成分研究 [J]. 中草药, 2021, 52(11): 3187-3192.
[21] 刘年珍, 赵碧清, 钱群刚, 等. 玄参化学成分的研究 [J]. 中成药, 2019, 41(3): 576-579.
[22] Sun Y, Ding C, Wang F R,. Pregnane alkaloids with BRD4 inhibitory and cytotoxic activities from[J]., 2021, 45: 63-67.
A new monoepoxylignan from
ZHANG Dong-dong1, 2, FAN Hao1, SUN Yu1, ZHANG Hua-wei1, JIANG Yi1, LI Yu-ze1, 2, WANG Wei1, SONG Xiao-mei1
1. School of Pharmacy, Shaanxi University of Chinese Medicine, Xianyang 712046, China 2. Shaanxi Key Laboratory of Traditional Chinese Medicine Foundation and New Drug Research, Xianyang 712046, China
To study the chemical constituents fromand their cytotoxic activities.The compounds were separated by silica gel column chromatography, Sephadex LH-20 gel column chromatography and semi-preparative HPLC. The structures were identified by their physicochemical properties, MS, 1D and 2D NMR spectra and ECD data analysis. The cytotoxic activities were tested by MTT assay.Fifteen compounds were isolated from., which were identified as: valeofficinlignan A (1), (7,8,8′)-tetrahydro-7-(4-hydroxy-3-methoxyphenyl)-8′-[(4′-hydroxy-3′-methoxyphenyl)methyl]-8- (hydroxylmethyl)-8,8′-furandiol (2), schisanpropinin (3), (+)-isolariciresinol (4), ecdysanol B (5), (‒)-3,4-dihydroxy-2- (4-hydroxy-3-methoxyphenyl)-4-(4-hydroxy-3-methoxybenzyl)-3-tetrahydrofuranmethanol (6), jatamanin A (7), jatamanin K (8), jatamanin R (9), longiflorone (10), ferulic acid (11), caffeic acid (12),-coumaric acid (13), methylcaffeate (14), and methyl-hydroxycinnamate (15). Compound 10 showed cytotoxic activity against HCT116 cell line with IC50value of (70.9 ± 6.4) μmol/L.Compound 1 is a new monoepoxylignan, namely valeofficinlignan A, and compounds 2, 3, 5―10 are isolated fromfor the first time, compound 10 exhibits cytotoxic activities.
L.; monoepoxylignan; valeofficinlignan A; longiflorone; cytotoxic activities
R284.1
A
0253 - 2670(2022)01 - 0025 - 06
10.7501/j.issn.0253-2670.2022.01.005
2021-08-27
陕西省科技厅自然科学基础研究计划项目(2021JQ-744);陕西中医药大学创新团队项目(2019-YL12)
张东东,男,博士,讲师,主要从事中药药效物质基础研究。E-mail: zhangnatprod@163.com
宋小妹,女,博士,教授。Tel: (029)38185165 E-mail: songxiaom@126.com
[责任编辑 王文倩]

