Ru/固体碱协同催化生物质糠醇水热氢解的研究
翁育靖 ,孟士航 ,朱万胜 ,张明威 ,孙 琦,2 ,张玉龙,2
(1.河南理工大学 化学化工学院,河南 焦作 454003;2.河南省煤炭绿色转化重点实验室,河南 焦作 454003)
生物质资源主要是光合作用产物聚合而成的超分子碳水化合物(主要元素:C、H、O),跟煤炭、石油等化石资源(主要元素:C、H)相比最大的特点是含氧量高[1-3]。在传统化石资源储量下降以及环境污染日趋严峻的背景下,探索开发生物质化工中含氧类燃料和高附加值化学品的技术路线不仅很好地利用了生物质原料的结构特征,也具有深远的科学意义和应用前景。其中,5-羟甲基糠醛和糠醛是重要的呋喃类生物质平台化合物,分别源于纤维素和半纤维素的糖类衍生物,广泛应用于树脂合成、润滑油精制、香料生产等行业,也是唯一无法从化石原料中提取的化工品。中国既是糠醛产品生产大国又是出口大国,目前,中国有300 余套糠醛生产装置,生产规模一般为1000-3000 t/a,但下游产品仅糠醇和呋喃树脂较为成熟,因此,开发高附加值衍生物对于生物质呋喃产业链的发展具有重要的战略意义。
四氢糠醇,又名四氢呋喃甲醇,无色透明液体,有吸湿性,能与水、乙醇、乙醚、丙酮、氯仿等混溶,不溶于石蜡烃。用于制备丁二酸、戊二醇、四氢呋喃、吡喃等,或者作为涂料、树脂、油脂、醋酸纤维素、乙基纤维素等的溶剂,在印染工业中用作润滑剂和分散剂,在制药工业中用于药品的脱臭、脱色剂,也是增塑剂、除草剂、杀虫剂等有机合成的基础原料。另外,1,2-戊二醇是直链的二醇,它兼具极性和非极性,这种特殊的性质使得其被广泛用来制造聚酯纤维、表面活性剂、抗菌剂等产品(图1)[1,2]。丙环唑是一种性能优越的杀菌剂,用途十分广泛,1,2-戊二醇是制备丙环唑的关键中间体,全世界约80%的1,2-戊二醇用于生产丙环唑[3,4]。目前,1,2-戊二醇的工业生产方法主要有正戊醇法、正戊酸法、正戊烯氧化法[5,6],但其过度依赖化石资源,且工艺路线复杂、能耗高、收率低、环境污染严重。尽管从生物质糠醛(糠醇)制备下游衍生物已经取得了部分工业化成果,但通过选择性加氢制备四氢糠醇和1,2-戊二醇的研究目前很少有系统的工作。同时,中国是农业大国,国内有很多化工企业生产糠醛,产能巨大,其中由玉米芯、甘蔗渣和小麦秸秆等农林废弃物为原料经水解精制生产糠醛和糠醛加氢制糠醇均已实现大规模生产[7-9]。因此,研究如何从糠醇氢解制备高附加值化学品,尤其是1,2-戊二醇,对中国生物质呋喃化合物的产业发展有重要意义。

图1 生物质转化为高价值化学品[10]Figure 1 Conversion of biomass to value-added chemicals[10]
根据相关文献[11-15],从生物质糠醇开环可以得到 1,5-戊二醇[16-20]和 1,2-戊二醇[2,21]以及 1,4-戊二醇[15],糠醛反应过度加氢可以产生四氢糠醇,但四氢糠醇很难再进行氢解开环[2,22,23]。催化生物质糠醇开环制备1,5-戊二醇和1,2-戊二醇的催化剂主要有 Pd[24]基、Pt[25-28]基、Ru[2,29]基和 Cu基[29,30]催化剂。Tong等[25]报道了糠醇通过Pt/CeO2(碱性金属氧化物)催化剂催化制备1,2-戊二醇的生产过程,并且详述了不同氧化铈晶型结构对于催化反应的性能影响,研究发现,纳米立方晶型的氧化铈作为载体能够显著提高产物中1,2-戊二醇的收率和选择性。另外,Mizugaki等[26]报道了用Pt/HT(碱性水滑石)催化剂催化糠醛制1,2-戊二醇,以2-丙醇作溶剂,在423 K、3 MPa H2压力下反应4 h后,产物中1,2-戊二醇的选择性为73%。Gao等[29]采用柠檬酸盐一步络合法制备出具有钙钛矿结构的Cu-LaCoO3催化剂,并且在413 K和6 MPa H2下糠醇的转化率达到100%,1,5-戊二醇的选择性达到40.3%,1,2-戊二醇的选择性达到15.2%。但总的来讲,糠醇氢解制备1,2-戊二醇的技术目前仍然处于研究的起步阶段,仍缺乏高浓度糠醇定向氢解制备二元醇的有效催化体系和反应网络控制的规律性认识。
相比Pt金属而言,Ru的价格较为低廉,且具有较好的水相加氢活性以及耐水耐酸碱性能[2,26,28,30,31]。Zhang等[2]研究了以 MnOx为载体制备Ru/MnOx、Pt/MnOx、Pd/MnOx、Rh/MnOx等催化剂,通过实验发现Ru/MnOx催化剂对1,2-戊二醇具有较高的选择性,在 120 ℃,3 MPa(氢压)Ru/MnOx的反应条件下反应4 h后,糠醇水溶液转化率为99.6%,1,2-戊二醇的选择性达到24.4%。研究团队前期一直从事Ru基催化剂的水热加氢反应研究,研究发现,Ru催化剂表面存在氢的强吸附现象,而这种氢效应则非常有利于生物质水相加氢反应。另外,1,2-戊二醇则来源于呋喃环仲碳的C-O键的氢解开环,这个常发生于碱催化下亲核试剂进攻位阻较小的碳原子发生SN2取代使环氧化合物开环。因此,本研究针对生物质糠醇氢解开环制备1,2-戊二醇的反应特点,提出了Ru/固体碱双功能催化剂的研究方案,重点研究催化剂的制备工艺和活化条件对催化剂微结构和反应性能的影响,并以优化的催化剂为基础,探索和优化反应条件,实现了生物质糠醇到1,2-戊二醇类产物的绿色转化。
1 实验部分
1.1 试剂与仪器
二氧化锰(MnO2)和氧化镁(MgO),分析纯,天津科密欧化学试剂有限公司;二氧化铈(CeO2)、纳米二氧化钛(TiO2)、纳米二氧化锆(ZrO2)、无水乙醇(C2H5OH)、埃洛石、异丙醇(C3H8O)和乙二醇(C2H6O2),分析纯,阿拉丁;镁铝水滑石(MgAl-LDH),分析纯,合肥巴斯夫生物科技有限公司;氯化钌 [RuCl3·3H2O],分析纯,九鼎化学;糠醛(C5H4O2)、糠醇(C5H6O2),分析纯,麦克林;甲醇(CH4O),分析纯,购于烟台市双双化工有限公司。
K-PSA-50ML型机械搅拌反应釜,江苏省滨海县正信仪器厂;KMTF-1200-I-60-450型实验室助力级管式炉,安徽科幂机械有限公司;OTF-1200X型管式炉,合肥科晶材料技术有限公司;SHZ-D(III)型循环水式真空泵,巩义市予华仪器有限公司;FA2104型电子天平,上海亚津电子科技有限公司;KQ5200DE型超声波清洗器,昆山市超声仪器有限公司;DZF-6030A型真空干燥箱,上海一恒科学仪器有限公司;TG16-WS型台式高速离心机,湘仪实验室仪器开发有限公司;Autosorb iQ Station:1型N2吸附仪,美国康塔仪器;Scion456-G型气相色谱;X射线衍射仪,SmartLab,Rigaku;X射线光电子能谱仪;
1.2 催化剂的制备
本实验采用浸渍法[2]制备催化剂,载体为金属氧化物(MnO2、TiO2、MgO、CeO2和 ZrO2)和矿石(MgAl-LDH、埃洛石),活性组分为Ru。以Ru/MnO2的制备为例,其他催化剂制备方法与此相同。操作方法为称取指定用量的RuCl3·3H2O(37% Ru)放入坩埚中,加入适量蒸馏水使Ru盐溶解,后加入称好的MnO2粉末,用玻璃棒搅拌至浆状,放入超声波清洗器中超声0.5 h,后放入80 ℃干燥箱中老化24 h。将干燥好的样品放入管式炉中煅烧,煅烧温度设为500 ℃,煅烧3 h,N2环境。最后在管式炉中进行还原,还原温度设为300 ℃,还原3 h,气流为Ar和H2的混合气(Ar/H2= 8∶2,100 mL/min)。
1.3 催化剂测试
糠醇加氢开环的反应在一个50 mL机械搅拌釜中进行,以其中一组反应为例,将0.1 g催化剂、0.5 g糠醇、10 mL水加入反应釜中,将反应釜密封,后通入H2扫气10 min,扫气结束后加压至1.5 MPa,检查气密性,气密性检查完后,通入冷凝水,设置升温程序和转速进行反应,当温度稳定后开始计时,反应4 h。反应结束后,用离心机分离催化剂残渣和液体产物,液体产物用10 mL玻璃瓶收集,催化剂残渣放入干燥箱中,干燥24 h后收集。最终产物用气相色谱检测(Scion456-G),通过内标法定量分析,用N,N-二甲基酰胺作为内标物。转化率和选择性的计算方法如下:

2 结果与讨论
2.1 实验结果
首先,以Ru为加氢金属,筛选了一批碱性金属氧化物作为载体制备金属/碱双功能催化剂,Ru/CeO2、 Ru/MgO、 Ru/TiO2、 Ru/MnO2、 Ru/ZrO2、Ru/M (MgAl-LDH,水滑石)、Ru/H (埃洛石,多水高岭土)。结果如图2所示,从图2中可以看出,大部分催化剂在水热条件下都有较高的催化活性和原料转化率,只有Ru/TiO2催化剂反应中转化率较低(为 38%)。另外,以 MgO、MnO2、MgAl-LDH(M)为载体的催化剂,在相同的反应条件下,1,2-戊二醇(1,2-PeD)的选择性相比于其他载体的催化剂较高,同时以上述三种物质为载体的催化剂对四氢糠醇(THFA)的选择性也较高。另外,以ZrO2、CeO2和埃洛石(H)为载体的催化剂,反应中产物出现了副产物环戊酮 (CPO)和环戊醇 (CPL)。一般而言,环戊酮(CPO)和环戊醇(CPL)是糠醇呋喃环加氢重排以后的产物,多为碳正离子机理,发生在酸性催化条件中。综上,以MgO、MnO2、MgAl-LDH为载体的金属/碱催化剂较好,较适合糠醇直接氢解制备1,2-戊二醇(1,2-PeD)催化剂的开发。

图2 不同载体的催化剂反应Figure 2 Reaction results of catalysts with different support(Furfuryl alcohol 0.5 g, catalyst 0.1 g (4% Ru), H2O 10 mL,600 r/min, 1.5 MPa (hydrogen pressure), 4 h, 150 ℃)
随后,以Ru/MnO2和Ru/MgO两组催化剂(Ru的负载量为4%)进行溶剂的筛选。其中,实验使用的溶剂包括水、异丙醇、甲醇、乙醇、乙二醇。其结果表明对于Ru/MnO2催化剂,在甲醇溶剂和乙二醇溶剂中原料的转化率较低,为19%和40%。而在异丙醇和水中原料的转化率较高,分别为94%和100%。在乙醇溶液中原料的转化率为73%。在反应后并没有出现环戊醇(CPL)和环戊酮(CPO)等副产物,只有四氢糠醇(THFA)和1,2-戊二醇(1,2-PeD)。在异丙醇和乙醇中1,2-戊二醇(1,2-PeD)的选择性相对较高,达到22%,在乙二醇中1,2-戊二醇(1,2-PeD)的选择性为11%,在水中1,2-戊二醇(1,2-PeD)的选择性为16%。副产物四氢糠醇(THFA)的选择性按照异丙醇、乙醇、水、甲醇、乙二醇的顺序逐渐减小。综上,Ru/MnO2在异丙醇中的反应效果最好,1,2-戊二醇(1,2-PeD)的选择性最高,四氢糠醇(THFA)选择性最低。由图3(b)可以看出,对于Ru/MgO催化剂,原料在水中和乙二醇中转化率较高,分别为96%和86%,在甲醇、乙醇、异丙醇中转化率较低,低于40%。而1,2-戊二醇(1,2-PeD)的选择性在乙醇溶液中达到最高为17%,其次分别是水、异丙醇、甲醇、乙二醇。而副产物四氢糠醇(THFA)的含量比较高,在这五种溶剂中其选择性为40%左右。和MnO2相同,生成物中没有环戊醇(CPL)和环戊酮(CPO),由此可以看出,在乙醇中的转化率不高,但1,2-戊二醇(1,2-PeD)的选择性较高,效果良好,所以溶剂乙醇的效果较好。

图3 不同溶剂对反应结果的影响Figure 3 Effects of solvents on the reaction
鉴于此,本实验以Ru/MnO2作为优化催化剂,考察原料质量浓度对反应的影响。分别采用0.10、0.05、0.02、0.01 g/mL的原料质量浓度进行测试,保持反应条件一致。图4(a)结果表明,底物质量浓度过低或者过高都不利于反应朝着1,2-戊二醇的方向进行,最佳质量浓度为0.02 g/mL(约2%)。呋喃类化合物是热敏性的生物质原料,目前,高浓度转化技术是其产业化利用的一个技术瓶颈,因为高浓度原料在高温水热下容易导致缩合等副反应发生。另外,底物浓度过低的情况下,四氢糠醇和1,2-戊二醇是两个平行反应的产物,但过低的浓度对1,2-戊二醇的生成反应影响更大。实验中,原料质量浓度为0.02 g/mL时1,2-戊二醇(1,2-PeD)的产率最高达到了32.0%,是目前为止产率最高的一组反应。当原料质量浓度降到0.01 g/mL时,此时生成物中没有1,2-戊二醇(1,2-PeD),只有四氢糠醇(THFA)。综上,适当降低原料浓度对反应有利,但浓度过低对反应不利。同时,本实验室也以Ru/MnO2催化剂考察了不同反应物种类对催化性能的影响,分别用糠醇(FFA)和糠醛(FFL)进行催化性能的测试,如图4(b)所示,当原料为糠醛时,生成物只有糠醇,没有1,2-戊二醇(1,2-PeD)和四氢糠醇(THFA),而且糠醛不能完全转化为糠醇。说明以糠醇为原料催化剂能表现出较好的催化性能。另外,实验以5%糠醇为原料,通过在不同的反应时间取样分析,得到了其产物分布跟反应时间的关联图(图4(c))。从图中可以看出,在该条件下反应在0.5 h时已经接近完全转化并达到反应平衡浓度。随后在1、2 和4 h也分别取样进行分析,结果表明,延长反应时间对1,2-戊二醇的产率影响较小,但四氢糠醇的收率随着反应时间的延长反而逐步降低。然后,做了一个催化剂重复使用的实验,在实验中催化剂没有再生或者更换,每次结束后离心分离然后直接投入下一次的重复实验中。下图(图4(d))是催化剂重复使用的产物分布结果,可以看到催化剂在不经过活化再生的情况下重复使用仍然具有较好的稳定性。

图4 (a)不同糠醇原料质量浓度,(b)不同原料对反应的影响,(c)产物分布和反应时间的关联图,(d)催化剂稳定性测试Figure 4 (a) Effect of raw material concentrations on the reaction (furfuryl alcohol 0.5/0.2/0.1/1 g, 4% Ru/MnO2 0.1 g, H2O 10 mL,600 r/min, 1.5 MPa (hydrogen pressure), 4 h, 150 ℃), (b) Effect of raw material on the reaction (furfuryl alcohol/Furfural 0.5 g, 4%Ru/MnO2 0.1 g, H2O 10 mL, 600 r/min, 1.5 MPa (hydrogen pressure), 4 h, 150 ℃), (c) products distribution at different reaction time(Furfuryl alcohol 0.5 g, 4% Ru/MnO2 0.1 g, H2O 10 mL, 600 r/min, 1.5 MPa (hydrogen pressure), 150 ℃) and (d) catalyst reusability test (furfuryl alcohol 0.5 g, 4% Ru/MnO2 0.1 g, H2O 10 mL, 600 r/min, 1.5 MPa (hydrogen pressure), 4 h, 150 ℃)
最后,以氧化锰为载体,考察Ru负载量对催化性能的影响,其中,Ru负载量为4%、2%。实验结果如图5所示,在相同的反应条件下,对于1,2-戊二醇(1,2-PeD)来说,Ru负载量为2%的催化剂,反应效果比Ru负载量为4%的催化剂稍好,其选择性为19.4%,而在Ru负载量为4%的催化反应中,1,2-戊二醇(1,2-PeD)的选择性为16%。此外,Ru负载量为2%的催化反应结束后出现了副产物环戊酮(CPO)。在原料转化率和四氢糠醇(THFA)选择性方面Ru负载量为4%催化剂比2%催化剂的催化效果好。由此可以看出,Ru负载量为4%、2%的Mn基催化剂的催化效果没有明显的分别,只是钌负载量少的催化反应中可能会出现较多的副产物。对于此反应来说,钌负载量为4%的催化剂催化效果更好,虽然1,2-戊二醇(1,2-PeD)的选择性稍低,但原料的转化率较高,无副产物。另外,作者也考察了催化剂还原温度(200、300 、400 ℃)对反应性能的影响(图5(b)),但仅从目标产物1,2-戊二醇的选择性的角度来看,还原温度对实验的影响比较小,提高还原温度并不能提高1,2-戊二醇的产率,目前,还是300 ℃的情况下反应效果最好。
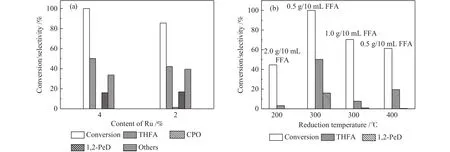
图5 (a)不同Ru负载量催化剂(b)还原温度对反应的影响Figure 5 (a) Effect of Ru loading on the reaction (furfuryl alcohol/furfural 0.5 g, 4% / 2% Ru/MnO2 0.1 g, H2O 10 mL, 600 r/min,1.5 MPa (H2), 4 h, 150 ℃);(b) effect of reduction conditions on product distribution (Ru/MnO2, 10 mL water,600 r/min, 1.5 MPa(H2),4 h, 150 ℃)
2.2 催化剂表征分析
本次实验所用催化剂用XRD(X-ray diffraction)表征,分别选取了Ru/MgO未还原、已还原、反应后残渣的三组样品,以及Ru/MnO2已还原和残渣两组样品进行了XRD测试。将所测样品均匀放入载玻片上,后放入粉末衍射仪(SmartLab,Rigaku)进行测试。扫描电压设定为40 kV,扫描电流设定为 150 mA,扫描 5°-80°,扫描速率为 10(°)/min。Mg基催化剂的XRD分析图如图6(a)所示,反应条件为150 ℃,1.5 MPa(氢压),溶剂为乙醇。在残渣中不仅能分析出载体MgO还能分析出Mg(OH)2,这说明催化剂在催化开环反应的同时,载体表面的MgO吸水变为Mg(OH)2,在图6(a)中并没有发现Ru的特征峰,说明其分散非常均匀且粒径较小[32]。另外,MgO未还原和已还原的Mg基催化剂的XRD的分析中只有MgO。

图6 (a)Mg 基催化剂和(b)Mn 基催化剂的 XRD 谱图Figure 6 XRD patterns of relevant (a) Ru/MgO and (b)Ru/MnO2 catalysts
Mn基催化剂残渣的XRD的分析图如图6(b)所示,在残渣中并未分析出来MnO2而只有Mn(OH)2,说明Mn和Mg的催化剂一样,载体都变成了相应的氢氧化物。而在已还原的催化剂中,MnO2被还原成MnO。另外,和Mg基催化剂一样,在Mn基催化剂中并未检测到Ru,可能是Ru的粒径太小或者Ru在催化剂中分散均匀无法被检测出。而在残渣中只分析出Mn(OH)2,反应后出现了氢氧化物,说明金属氧化物在反应中发生了变化,根据相关文献,可能原因是碱性金属氧化物参与了反应,夺取了水分子质子形成氢氧根,或者直接进攻仲碳原子,从而进一步促进呋喃环不对称开环得到 1,2-戊二醇[19]。
本实验对两组Mn基催化剂进行了N2吸附-脱附测试,两组催化剂分别为Mn基催化剂残渣(溶剂为水)和还原后未参加反应的Mn基催化剂,测试样品质量分别为0.0514 g(残渣)、0.0557 g(还原),测试仪器为美国康塔仪器Autosorb iQ Station:1,在-196 ℃条件下进行测试。如图7所示,其N2吸附-脱附等温线在整个压力范围内有拐点存在,属于Ⅳ类等温线,由此判断所检测的催化剂为大孔材料。相关比表面积和孔体积的结果如表1,其中,发现比表面积较大的为Mn基催化剂残渣,比表面积为41.1 m2/g(而已还原样品只有17.2 m2/g),这一现象说明催化剂在反应过程中,出现了一些变化,使得催化剂的比表面积和微观结构有所变化[28]。
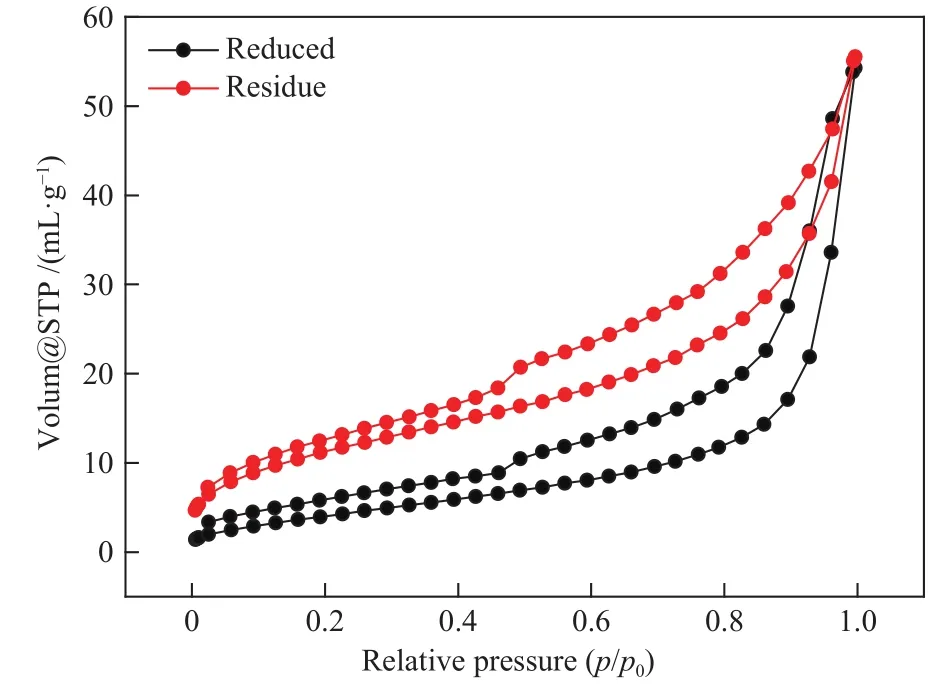
图7 Mn基催化剂N2吸附-脱附曲线Figure 7 N2 adsorption-desorption isotherms of Mn-based catalyst

表1 催化剂的比表面积、孔容、孔径Table 1 Catalyst specific surface area, pore volume, pore size
另外,利用X射线光电子能谱仪(XPS)对Mn基催化剂系列样品的表面元素的化学价态进行了分析,其中,C 1s的248.6 eV作为仪器荷电校正的参考[25]。图8(a)是 O 1s(539-529 eV)的能谱峰,主要反映了催化剂上面不同的含氧基团,根据相关的分峰拟合规则,其中低位结合能(529-530 eV)可能归结于金属氧化物,而中位结合能主要归结于催化剂表面的含氧有机基团(C-O 531 eV, C=O 533 eV),高位结合能(> 534 eV)主要由于催化剂吸附的水分子的影响。O 1s的结果显示催化剂经过反应以后表面C-O的官能团强度有所增加,这可能是氧化锰吸收水以后形成的M-OH(M表示碱性金属Mg和Mn)结构[2]。关于Mn元素的分析,由于Mn的不同价态氧化物在Mn 2p区域的峰差别较小,综合分析了Mn 2p和Mn 3s的结合能能谱。从图中可以看出还原样品的Mn 2p出现了一个明显的卫星峰(647 eV),这说明催化剂中出现了低价态的MnO物种,但MnO的峰在反应后面的残渣中没有找到,这说明还原后这种低配位状态的Mn物种在反应时发生了化学吸附产生了变化。而Mn 3s的结果(Mn的3d轨道有未成对电子,XPS中发生3s和3d耦合形成两个终态)也进一步证明这种价态变化,经过还原和反应以后的样品Mn 3s的双峰间距较未还原的样品有所增加,根据相关文献这说明还原后样品的化学价态有所降低[2]。综上所述,催化剂经过还原以后出现了低价态的氧化锰物种,在反应过程中这些氧化锰物种跟水分子进行配位结合产生M-OH结构。

图8 Mn基催化剂未还原、还原和反应残渣中O(a)和Mn(b)、(c)元素的XPS谱图Figure 8 XPS spectra of Mn based series samples
3 结 论
糠醇作为生物质化工中呋喃平台化合物的一个典型代表,通过它可以开辟众多精细化工产品,本研究针对糠醇选择性氢解制备1,2-戊二醇的水热反应特点,以水热加氢性能优异的Ru基金属/碱双功能催化剂为切入点,通过在载体、催化剂制备条件、反应溶剂和反应工况条件等方面入手,以提高糠醇直接氢解开环制备1,2-戊二醇为导向构建匹配的金属/碱协同催化反应体系。研究发现,催化剂制备工艺对其催化性能具有较大影响、溶剂对催化性能的影响因载体的不同而不同、原料浓度低有利于目标产物生成但浓度过低也降低了反应效率,其中,Ru/MnO2在最佳反应条件下最高可以得到四氢糠醇(53%)和1,2-戊二醇(32%)总收率85%。另外,结合物理吸附-脱附、XRD、XPS等表征手段对反应前后催化剂进行深入分析,发现催化剂经过还原以后出现了低价态的氧化锰物种,在反应过程中这些氧化锰物种跟水分子进行配位结合产生M-OH基团,而这些碱性基团有利于与Ru协同催化糠醇分子的氢解开环。

