人tau转基因小鼠模型及其在tau蛋白病研究中的应用*
郑 铮, 胡 娟, 李夏春
(1三峡大学第一临床医学院神经内科,湖北宜昌443000;2三峡大学第一临床医学院肿瘤科,湖北宜昌443000;3三峡大学医学院机能学系,湖北宜昌443000)
阿尔茨海默病(Alzheimer disease,AD)和额颞叶痴呆(frontotemporal dementia,FLTD)是最主要的痴呆相关疾病,记忆下降是AD 的主要症状,FLTD 还伴有行为个性变化。近年来,随着国外转基因小鼠的引入,越来越多的研究者采用转基因小鼠研究痴呆相关疾病。鉴于不少研究者对各tau 转基因小鼠的特点缺乏了解,选择tau 转基因动物模型不恰当,其实验结果和结论对人类疾病机制的揭示帮助不大,还可能会使研究误入歧途。本文就各常用人tau转基因动物模型的特点及其适用性进行综述,以期对 tau 蛋白病(tauopathies)研究者在选择人tau 转基因动物时有所帮助。
1 人tau基因和tau蛋白病
人微管相关蛋白tau(microtubule-associated protein tau,MAPT)基因位于17 号染色体,包含16 个外显子,其中外显子1、4、5、7、9、11、12 和13 是结构性外显子,外显子 2 和 3 可编码 tau 的 N 突起端序列,外显子 10 表达与否生成 4Rtau 或 3Rtau,外显子 2、3 和10 选择性剪切可表达6 种tau 蛋白亚型,分别为0N3R、1N3R、2N3R、0N4R、1N4R 和 2N4R。正常成人脑内3Rtau 和4Rtau 水平相近,而0N3Rtau 只存于人脑和鼠脑发育期。由异常过度磷酸化tau 蛋白组成的神经原纤维缠结(neurofibrillary tangles,NFT)是AD、进展性核上性麻痹(progressive supranuclear palsy,PSP)、皮质基底节变性(corticobasal degeneration,CBD)、Pick 病(Pick disease,PiD)、进展性亚皮层胶质增生(progressive subcortical gliosis,PSG)、17号染色体连锁额颞叶痴呆和帕金森综合征(frontotemporal dementia and parkinsonism linked to chromosome 17,FTDP-17)等的主要病理特征,故这些疾病又称为tau 蛋白病。每一种tau 蛋白病都有独特的神经病理学特点和进展速率及区域细胞参与。AD 和额颞叶痴呆(frontotemporal dementia,FTD)的NFT 由6 种 tau 亚型组成,PSP 和 CBD 的神经元和胶质细胞内的tau 包涵体主要由4Rtau 组成,而PiD 的神经元内球形tau 包涵体则由3Rtau 组成。为研究tau 蛋白病的发病机制,研究者已建立了许多转入人MAPT基因的动物模型,本文选择运用较多或新建模型进行介绍。
2 转入野生型人MAPT基因的小鼠模型
2.1 转野生型人 3Rtau 小鼠 Ishihara 等[1]用小鼠PrP 启动子连接0N3Rtau 的cDNA 建立了转野生型人3Rtau小鼠,其1月龄脊髓神经元出现球状tau蛋白包涵体,6~9 月龄包涵体数量升高,12 月龄下降,伴进行性胶质细胞增生和轴突退变,髓鞘轴突内有10~20 nm的直丝聚集,12月龄有快速轴浆运输减慢和进行性运动障碍;大脑皮层6 月龄出现含过度磷酸化tau、神经细丝和微管蛋白的tau 蛋白包涵体,其形态比脊髓的小。用鼠Tα1-微管蛋白启动子构建的转野生型人Tα-3Rtau 小鼠和3Rtau-KO(鼠tau 基因敲除)小鼠,1 月龄脑干和脊髓胶质细胞过表达3 种3Rtau亚型且12 月龄出现tau 蛋白斑块;6 月龄前无tau 蛋白斑块时少突胶质细胞有显著丢失;24 月龄少突胶质细胞出现CBD 的卷曲小体样异常tau 蛋白丝及髓鞘变薄;6~24 月龄运动障碍和嗅球功能障碍逐月加重[2-3]。前一种3Rtau 小鼠可模拟肌萎缩侧索硬化/帕金森综合征-痴呆复合征(amyotrophic lateral sclerosis/parkinsonism-dementia complex,ALS/PDC)和PSP病变的脊髓神经元病变及运动障碍,也可模拟部分AD和PiD的皮层神经元tau蛋白包涵体的特点。Tα-3R 小鼠神经胶质细胞tau 蛋白病变显著且明显退变,可用于模拟PSP、PiD、CBD、PSG 和FTDP-17 的胶质细胞tau蛋白病。
2.2 转野生型人4Rtau 小鼠 用小鼠Thy1 启动子表达人2N4Rtau 的小鼠和tau-KO/KI 小鼠,分别于早期和晚期出现运动障碍,但均无NFT 样包涵体形成[4]。用人 tau 启动子构建的转人 2N4Rtau 小鼠和用MoPrP 载体构建的转人1N4Rtau 小鼠都无NFT 和tau蛋白直丝,亦无胶质细胞激活[5-6]。这些4Rtau 小鼠无经典tau 蛋白病变(NFT 形成),未能成为tau 蛋白病模型,促使科学家怀疑鼠tau 蛋白可能干扰tau 蛋白病形成并开始敲除鼠tau 基因而构建新的人tau 转基因小鼠。Andorfer 等[7]用人 PAC 启动子表达人 tau基因的8C 小鼠与鼠tau 敲除小鼠杂交的F1 代小鼠,再与KO 小鼠回交获得了纯合子人tau 转基因小鼠。这种小鼠表达6 种人tau 亚型,3Rtau 显著高于4Rtau,3 月龄新皮层和海马首现磷酸化tau 蛋白积聚,9 月龄人AD 病变严重区域均有配对螺旋纤维(paired helical filament,PHF)样 tau 蛋白积聚,13 月龄tau 蛋白积聚神经元出现形状不规则伴突起扭曲的退变,8~18月龄皮层变薄脑室扩大逐月加重,电镜下神经元内有人AD 脑内PHF 样tau 蛋白丝积聚;小鼠4~12 月龄无感觉、运动和焦虑水平改变,逐渐出现突触功能障碍,12 月龄新目标识别和空间记忆均受损[7-8]。这种小鼠的发病过程和tau 蛋白病理变化近似AD,伴行为学变化且无运动障碍,是研究野生型人tau 蛋白在AD 发病机制中作用的较好模型,美国杰克逊实验室出售品系名为STOCK 0005491。2.1和2.2的比较见表1。
3 转人MAPT基因单突变小鼠
3.1 转人P301L-tau 小鼠 P301L 突变是最常见的人FTDP-17 突变,其病理特征为前脑有NFT 和神经元丢失。用PrP 启动子表达人P301L-0N4Rtau 建立的 JNPL3 小鼠,4.5~6.5 月龄皮层、海马和脊髓出现过度磷酸化tau 蛋白、NFT 和Pick 样小体,神经元进行性轴突退变和丢失,周围神经和骨骼肌有神经性萎缩;电镜下胞浆内见tau 蛋白直丝和波浪状丝;12月龄以上小鼠运动受损,有短期和长期恐惧记忆受损伴海马GABA 神经元丢失[9-11]。由四环素反应元件和CaMKII 启动子诱导神经元特异性表达P301L-0N4Rtau的rTg4510转基因小鼠,4和5.5月龄皮层海马出现NFT 样包涵体,10 月龄神经元丢失和反应性星形胶质细胞增生伴前脑萎缩;2.5月龄空间参考记忆维持障碍,9.5 月龄皮质脊髓背束萎缩致运动受损[12];2.5月龄时终止人tau表达,小鼠记忆功能恢复但不溶性 tau 蛋白和 NFT 仍进展[13];雌性小鼠 tau 蛋白病变和空间学习记忆障碍更重[14]。然而,2019 年rTg4510 小鼠的母本 CaMKIIα-tTA 转基因小鼠和MAPT-P301L转基因小鼠的插入位点定位时发现,前者基因插入12 号染色体影响了5 个小鼠基因表达,后者插入14 号染色体的成纤维生长因子14(fibroblast growth factor 14,Fgf14)基因导致其表达破坏,提示破坏Fgf14可能有助于rTg4510小鼠的神经退变表型[15]。用神经元特异性鼠Thy1.2 启动子表达P301L-2N4Rtau的pR5转基因小鼠,3月龄出现海马、杏仁核、脊髓和皮层早期磷酸化tau 蛋白积聚,杏仁核和皮层神经元凋亡伴星形胶质细胞激活,海马神经元很少凋亡;6 月龄NFT 从杏仁核扩至海马CA1区;8月龄可见比AD脑内的直丝更细更短的tau蛋白丝及恐惧记忆障碍和空间记忆障碍[16-18]。这3 种P301L 小鼠均有典型tau 蛋白病变、脑萎缩及行为学受损,是研究tau 蛋白病机制及防治措施效果使用最多的模型。

表1 转野生型人3Rtau小鼠与转野生型人4Rtau小鼠的比较Table 1. The comparison of wild-type tau transgenic mice
3.2 转人tau-P301S 突变小鼠模型 P301S-tau 引起FTD 和CBD,且和tau 蛋白病变的广泛分布和疾病早发相关。用鼠Thy1.2 启动子表达P301S-0N4Rtau 的TAU58 小鼠,全脑神经元tau 蛋白积聚和NFT 增多,伴轴突肿胀,4 月龄空间学习和记忆巩固提取受损,运动障碍早发且进行性加重[19-20]。用小鼠PrP 启动子表达P301S-1N4Rtau的PS19小鼠,3月龄神经元不溶性tau 蛋白积聚伴突触受损和功能障碍,6 月龄前脑NFT 积聚,电镜下tau 蛋白丝积聚在胞浆和突触,内质网和线粒体肿胀数量减少,3~8月龄海马小胶质细胞炎症反应明显、神经元丢失和脑萎缩,抑制小胶质细胞炎症反应减轻tau病变和突触损伤,9~10月龄出现目标识别记忆障碍[6,21]。该 PS19 小鼠现由美国杰克逊实验室出售(008169),可用于tau 蛋白病机制及治疗措施的有效性评价研究,也可与目标基因小鼠交配构建目标基因×PS19 双转基因小鼠以探讨目标基因在tau蛋白病中的作用。Shi等[22]用PS19小鼠和ApoE敲入小鼠交配建立了P301S/E2、P301S/E3 和P301S/E4 转基因小鼠,发现 P301S/E4 小鼠 3 月龄磷酸化tau 蛋白水平比前两者更高,9 月龄比前两者脑萎缩更严重,提示ApoE4加速神经退变过程。
3.3 转人MAPT基因外显子12、13 突变的小鼠 人MAPT基因外显子 12 的 V337M 突变在 FTD 的 Seattle家系被发现,患者额顶叶皮层、颞叶和杏仁核有NFT,临床表现为性格改变、偏执及反社会行为和注意记忆下降。用PDGFβ 启动子表达V337M-2N4Rtau 的转基因小鼠,4~15 月龄人 tau 蛋白表达恒定且水平低于内源性鼠tau蛋白;11月龄时小鼠海马含PHF-tau 神经元呈小而凸的AD 样退变,无凋亡特征,并有海马神经元活性下降和恐惧记忆障碍,无空间记忆障碍;电镜下神经元内电子致密物增多,膜皱褶,核糖体浓缩,高尔基体肿胀,有脂质体和NFT 样tau 蛋白丝[23]。此小鼠显示AD 样神经病变和行为学特征,可用作AD 临床前期模型检测抗神经退变药物的治疗效果。人MAPT基因外显子13 的R406W 突变可致6 种tau 蛋白亚型聚集形成NFT 并出现AD 和FTDP-17 的临床特征。用CaMKII 启动子表达人R406W-2N4Rtau的转基因小鼠,19月龄时海马、杏仁核、新皮层和嗅球出现磷酸化不溶性tau 蛋白沉积及NFT 样tau 蛋白丝,无感觉运动反射和运动协调能力下降,有场景和线索恐惧记忆障碍[24]。此小鼠也可用于有R406W 突变的FTDP-17 和AD 早期机制的研究。用 mThy1.2 启动子表达 K369I-1N4Rtau 的 K3 系小鼠,1~2 月龄皮层、海马和基底节神经元有像Pick小体的tau蛋白包涵体却无退变,12月龄后多巴胺神经元丢失;4 月龄无tau 蛋白病变前出现帕金森综合征样运动障碍和肌萎缩,伴纹状体突触淀粉样前体蛋白(amyloid precursor protein,APP)和酪氨酸羟化酶囊泡及线粒体转运障碍,新目标识别工作记忆障碍[25]。该K3 小鼠主要用于有帕金森综合征表现的FTD 和记忆障碍造模,也用于tau 蛋白积聚早期轴突转运障碍机制的研究。
3.4 转人MAPT基因外显子10 突变的小鼠 人MAPT基因外显子10 的N279 突变可改变外显子10的拼接,在几个无关家系中表现出帕金森综合征、痴呆、运动功能障碍及个性改变,病理表现为广泛的神经元和胶质细胞tau 蛋白积聚。用人tau 启动子表达N279K-2N4Rtau 的 T-279 小鼠,人 tau 蛋白表达低于内源性鼠tau蛋白,13月龄小鼠多个脑区神经元和星形胶质细胞内有弥散性粒状或丝状tau 蛋白积聚,黑质纹状体多巴胺能神经元出现串珠样腊肠样肿胀退变,全脑caspase-3 阳性却无tau 蛋白截短片段增多,23 周龄有运动协调受损和学习记忆减退[5]。该小鼠部分模拟外显子10 剪切失调导致的PSP、CBD 等tau蛋白病,杰克逊实验室市售(035794)。ΔK280 是在FTDP-17 患者发现的突变,体外实验发现其具有促进tau 蛋白聚集的作用。用四环素操纵子-双向CMV启动子-TauRD 的cDNA 建立的人tau 转基因小鼠和CaMKIIα-tTA 转基因小鼠交配获得了促聚集的ΔK280-4Rtau 转基因小鼠,2~3 月龄出现 tau 蛋白聚集体和NFT,5 月龄有胶质增生及神经元和突触丢失;促聚集tau蛋白停止表达1.5月后其可溶性tau蛋白会消失[26];tau 蛋白表达 10 月再停止表达 4 月后其突触丢失及空间学习和被动学习减慢均可恢复,tau蛋白聚集体中度降低且人tau 蛋白消失[27]。此转基因小鼠tau 蛋白表达可调节,是探讨tau 蛋白聚集可逆损伤机制较好的动物模型。
3.5 转人MAPT基因 A152T 突变小鼠 A152T 突变是人MAPT基因外显子7 编码的tau 蛋白的N 突起端突变,是PSP、AD、帕金森病和CBD患者的风险因素,可引起非经典tau蛋白病的临床病理特征。用tTA结合TRE 启动A152T-1N4Rtau 表达建立的转基因小鼠,4~10 月龄体重低,皮层和海马总人tau 蛋白水平升高伴星形胶质细胞增生,其早期磷酸化可溶性tau蛋白和星形胶质细胞增生均可逆,突触传递强度增强和癫痫样放电增多,20~23月龄海马齿状回和CA3区神经元丢失但无NFT,10~19月龄建巢能力和空间学习记忆进行性下降,但焦虑、社交能力及运动能力无改变[28]。杰克逊实验室市售(007004)。转人tau基因单突变小鼠的比较见表2。
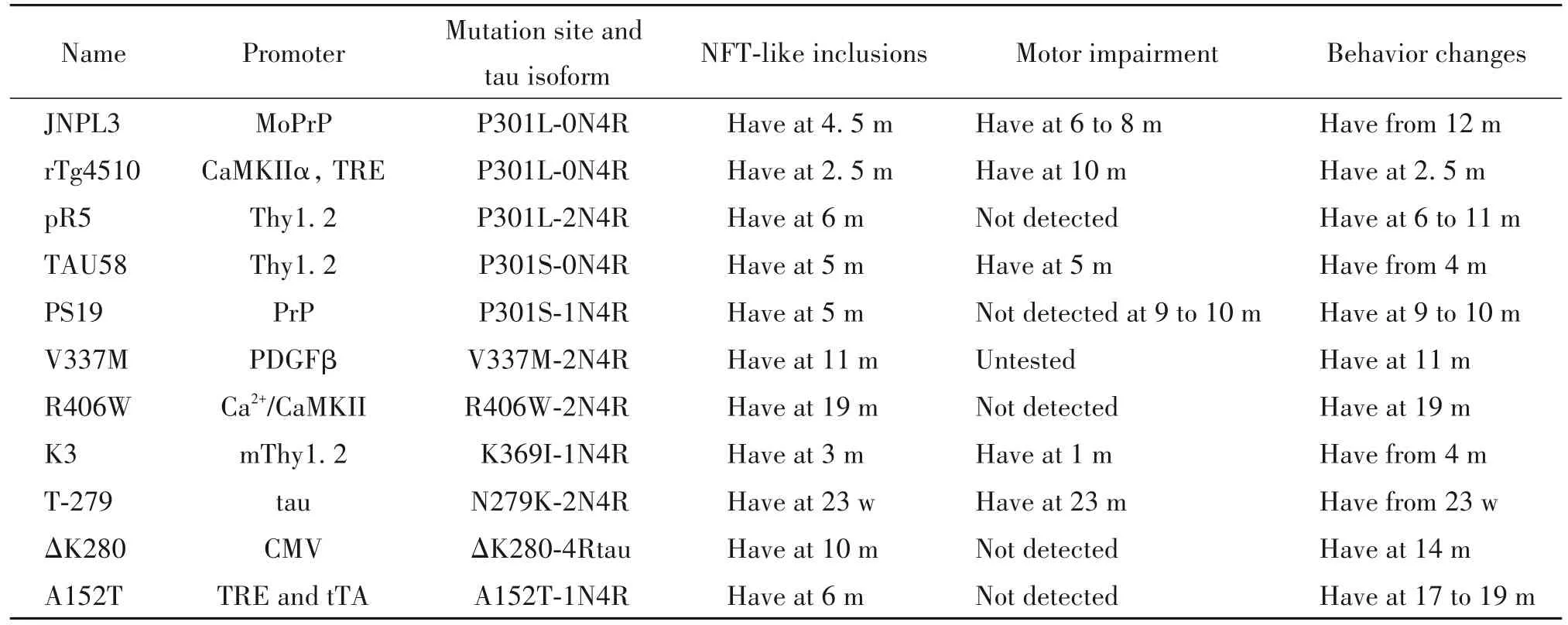
表2 转人MAPT基因单突变小鼠的比较Table 2. The comparison of mice with single-site mutation of MAPT gene
4 转人MAPT基因多位点突变基因小鼠
4.1 转人多位点突变4Rtau 小鼠 用Thy1.2 启动子表达人G272V-P301S-tau46 的THY-Tau22 小鼠3月龄即表现出海马突触传递障碍和焦虑行为增加,10 月龄有空间记忆障碍无任何运动障碍,12 月龄出现AD 样NFT 样包涵体和轻度星形胶质增生伴神经元退变或丢失[29]。THY-Tau22 小鼠模拟了 tau 蛋白病的主要特征,被用于研究各种措施对tau 蛋白病的干预效果和tau蛋白病的形成机制。用改良Thy-1启动子表达G272V-P301S-1N4Rtau 建立的Tg30小鼠,1月龄无NFT前即有轴突球形变,3月龄NFT广泛分布在皮层、海马、脑干和脊髓,海马的NFT 含tau 蛋白直丝或PHF 样丝和神经细丝,6~8 月龄出现运动障碍,进行性肌萎缩,坐骨神经轴突退变,12月龄脑重和海马体积显著下降但无细胞丢失[30]。Tg30小鼠适合有运动障碍的FTD造模。
4.2 转人多位点突变3Rtau 小鼠 用mThy-1 启动子表达L266V-G272V-3Rtau(家族性PiD 的突变)的转基因小鼠,3Rtau 蛋白表达高的13系小鼠6~8月龄新皮层和海马磷酸化3Rtau蛋白进行性升高,出现高活动性和运动平衡障碍及空间记忆维持障碍;8~10月龄有Pick小体样包涵体,12~14月龄新皮层和海马神经元突触前末端和树突3Rtau 蛋白广泛积聚伴萎缩和胶质细胞增生;电镜下齿状回神经元线粒体受损,轴突萎缩,突触电子致密物积聚,树突板层小体和直丝积聚[31]。此3Rtau小鼠模拟了突变tau蛋白积聚导致的新皮层和边缘系统的神经病变和行为学障碍,有Pick 小体样包涵体,可作为PiD 的动物模型,也可用于研究3Rtau 和线粒体损伤的关系。4.1 和4.2的比较见表3。

表3 转人多位点突变4Rtau小鼠与转人多位点突变3Rtau小鼠的比较Table 3. The comparison of Tau22,Tg30 and 3Rtau mice
5 转人MAPT基因+其它基因的小鼠
5.1 转人MAPT基因+APP基因的小鼠 tauP301L×APPswe 小鼠由JNPL3 小鼠和表达人突变APP(L670A,M671L)的Tg2576 小鼠交配建立,其内、外源性tau 蛋白表达与JNPL3 小鼠无差异,3 月龄脊髓和脑桥即出现NFT,雌性的NFT 密度和缠结前tau 蛋白水平高于JNPL3 小鼠,8.5 月龄出现广泛老年斑,9.5~11月龄皮层内不溶性tau 蛋白比JNPL3小鼠高,但运动障碍发作年龄同JNPL3 小鼠,Aβ40 和Aβ42水平及老年斑与Tg2576 小鼠相似[32]。该小鼠早期出现脊髓NFT和运动障碍不同于AD 发病过程,故不是AD 研究的理想模型。21 月龄B6/P301L 雌性小鼠中脑、海马内嗅皮层有NFT 样tau 蛋白病变,雄性28月龄该区也无NFT 样tau 蛋白病变;由B6/P301L 小鼠和APP23(APP-KM670/671NL)小鼠杂交而得的APP23×B6/P301L 雄性小鼠,28月龄时内嗅皮层和海马的Aβ 沉积区可见NFT 样tau 蛋白病变显著增多,但tau 蛋白病变对老年斑沉积无影响,此模型提示Aβ 病 变可 通过 多 种途 径诱 导 NFT 病变[33]。 将MAPT KI 小鼠(用人MAPT基因取代小鼠MAPT基因)与APPNL-G-F小鼠杂交建立的APPNL-G-F/MAPTdKI 小鼠,其6 和24 月龄时磷酸化tau 蛋白水平比同龄MAPT KI 小鼠高且有更多营养不良性神经突,其Aβ斑的周围比APPNL-G-F 小鼠有更多磷酸化tau 蛋白聚集体但无NFT形成;但Aβ并不影响3R/4Rtau的表达比例及神经退变过程,同时tau 蛋白的人源化也不加重 Aβ 沉积和神经炎症及空间记忆[34]。野生型hAPP/hMAPT 双转基因小鼠与2 种单转基因小鼠相比,δ-分泌酶升高,伴 APP 的 N373 片段和 tau-N368截短体增多,AT8 阳性,小胶质细胞激活,神经元丢失,caspase-3增加,12月龄空间学习和恐惧记忆障碍及皮层NFT 和Aβ 聚集的丝状结构比2 种单转基因小鼠更严重,拥有部分单转基因小鼠不具备的AD 病理特征,可作为AD 疾病模型研究其发病机制[35]。hAPP-K670N/761NL/V717I 小鼠和人3Rtau-L266V/G272V 小鼠[32]交配建立的APP×3Rtau 小鼠,3~4月龄运动和记忆损伤较3Rtau 小鼠更严重,新皮层、海马齿状回及CA1区的3Rtau蛋白积聚和tau蛋白磷酸化水平高于APP 或3Rtau 小鼠,神经元丢失也更严重;5~9 月龄 Aβ 水平高于 3Rtau 小鼠,3~4 月龄活性GSK3(p-Y216)较 3Rtau 小鼠低,P35 水平高于 2 种单转基因小鼠[36]。APP×3Rtau 小鼠的神经病变和行为表现极像PiD 和AD,是其较好的动物模型。转人MAPT基因+APP基因小鼠的比较见表4。
5.2 转APP+PS1+MAPT基因的小鼠 Oddo 等[37]将APPSwecDNA 和 tauP301LcDNA 注入 PS1M146V小鼠的单个卵细胞构建了APPSwe/PS1M146V/tauP301L三转基因小鼠(3×Tg-AD 小鼠),该小鼠海马和皮层表达的APP 和tau蛋白水平最高,6月龄出现明显老年斑,12月龄出现NFT,构象改变的过度磷酸化tau 蛋白先沉积于海马CA1 区锥体神经元再进展到皮层区,在老年斑和NFT 出现前突触出现功能障碍和长时程增强(longterm potentiation,LTP)受损,提示突触功能障碍与老年斑或NFT 无明显关系。该3×Tg-AD 小鼠用于研究Aβ 和tau 蛋白对突触功能的影响机制及评价抗AD治疗的效果。
5.3 5×FAD/tau 小 鼠 和 6×Tg-AD 小 鼠 5×FAD/PS19 小鼠由 5×FAD 小鼠与 PS19 小鼠交配建立,其 9月龄皮层和海马的磷酸化tau 蛋白病变、磷酸化GSK3(Tyr216/279)及磷酸化 JNK(Thr183/Tyr185)比PS19 小鼠更多,Aβ 斑块与5×FAD 小鼠相似,磷酸化tau 蛋白与Aβ 分布不同,内侧内嗅皮层磷酸化tau蛋白分布较多处Aβ 斑分布很少,且CA1 区Schaffer侧枝传导减慢,神经元萎缩比非转基因小鼠更严重,空间学习记忆能力比单转基因及非转基因小鼠都差[38]。5×FAD/Tg30 小鼠由 5×FAD(转人突变 APPKM670/671NL-I716V-V717I 和人突变PS1-M146L/L286V)小鼠与Tg30小鼠交配而成,其有比Tg30小鼠更严重的运动障碍和更快的NFT 沉积,不溶性tau 蛋白的磷酸化水平更高,tau 蛋白的错误折叠和截短等类似 AD 的 PHF 病变更多;与 5×FAD 小鼠相比,淀粉样变性更低,有显著神经元萎缩[39]。6×Tg-AD 小鼠由5×FAD 小鼠与JNPL3 小鼠交配获得,与其它基因型小鼠相比,该小鼠2 月龄皮层和海马有更多Aβ 斑块并有空间参考记忆和工作记忆降低,6月龄皮层比JNPL3 小鼠有更多PHF 沉积伴皮层和海马神经元丢失及突触蛋白表达降低[40]。APP/PS1/MAPT转基因小鼠既有NFT 病变和老年斑,也有神经退变,均可用于AD的机制和预防研究,其比较见表5。

表4 转人MAPT基因+APP基因小鼠的比较Table 4. The comparison of APP/MAPT transgenic mice
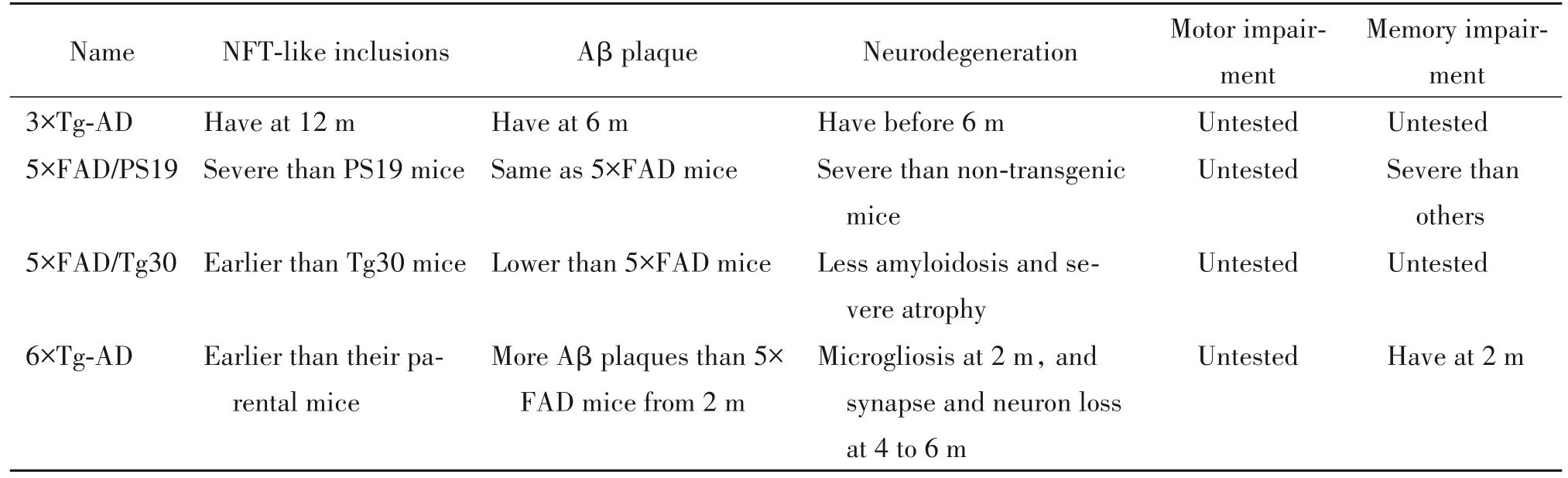
表5 APP/PS1/MAPT转基因小鼠的比较Table 5. The comparison of APP/PS1/MAPT transgenic mice
6 小结与展望
20 多年来,通过优化启动子或使用多启动子或人启动子建立了转单突变人MAPT基因、调节性转突变人MAPT基因、转人MAPT基因+鼠tau基因敲除等多种人MAPT转基因小鼠模型,这些小鼠模型越来越接近模拟人体tau蛋白病或AD 的发病过程和主要病理变化,但总体来说还没有建成最理想的人MAPT转基因小鼠模型。同时,这些人MAPT转基因小鼠模型还存在以下问题:(1)少量模型尚有部分重要指标未检测;(2)模型的退行性变形态学和神经功能学指标尚待完善;(3)应增加临床前期生化和形态判断指标以及磁共振等功能学指标以适应早期tau蛋白病的研究需要;(4)各模型的阶段性生化指标和病理指标待完善,以便为研究tau 蛋白病不同阶段的研究者提供参考标准。
总之,未来tau 转基因小鼠模型的开发和应用必将越来越多,其在以AD 为代表的tau 蛋白病研究中的作用越来越必不可少。在人MAPT转基因小鼠模型的检测标准方面还有许多工作可做。

