BI-RADS评分与CEUS检查联合用于乳腺肿块良恶性诊断的价值
陈艳艳
河南省安阳市内黄县人民医院,河南安阳 456350
乳腺肿块是临床女性乳房疾病的常见体征,发生率逐年升高且有年轻化趋势。有乳腺肿块的患者恶性疾病的发病率为30%,若发展为乳腺癌,病死率高达14%,严重威胁女性健康与生命安全。乳腺肿块初期缺乏典型特征,临床应尽早明确诊断,为治疗方案的制订提供参考。乳腺超声影像学报告及数据系统(BI-RADS)是在二维超声基础上从微钙化、实性结节等多方面判断结节性质,提供诊断分级依据,但误诊率仍较高[1]。超声造影(CEUS)能通过显示肿块血管、血流灌注模式、增强均匀性等微循环血流信息判断结节良恶性[2]。本研究选取了于本院就诊的乳腺肿块患者84例,旨在探讨BI-RADS评分联合CEUS检查的应用价值,并分析了CEUS检查误诊的发生原因,现报道如下。
1 资料与方法
1.1一般资料 经本院医学伦理委员会批准,将2019年3月至2020年3月本院乳腺肿块患者84例纳入研究。患者均为女性;年龄29~77岁,平均(47.69±9.24)岁;肿块最大直径0.8~5.6 cm,平均(2.71±0.91)cm;肿块位置:外上象限25例,内上象限21例,外下象限22例,内下象限15例,乳头后方1例。
1.2纳入及排除标准 纳入标准:(1)经常规超声检查发现乳腺肿块;(2)为初诊患者,未接受过任何处理或治疗;(3)对本研究知情同意并签署知情同意书。排除标准:(1)病变同侧乳腺或相邻部位曾接受过外科手术或穿刺检查;(2)乳腺内有植入物;(3)妊娠或哺乳期女性;(4)有囊性病变;(5)有影像学检查禁忌证;(6)合并严重肝肾功能障碍;(7)合并恶性肿瘤;(8)有精神或意识障碍,无法配合检查。
1.3方法
1.3.1BI-RADS分级与良恶性评估 采用彩色多普勒超声诊断仪进行常规超声检查,探头频率设置为4~13 MHz,对发现的肿块进行BI-RADS分级。1级为完全阴性;2级为良性病变且无恶性病变的风险;3级为高度良性病变,无恶性病变特征且恶性病变风险小于3%;4级为可疑恶性,恶性病变的风险为3%~90%(其中4a级为存在1个超声疑似恶性特征,恶性病变的风险为3%~10%,4b级为存在2个超声疑似恶性特征,恶性病变的风险为>10%~50%,4c级为存在3~4个超声疑似恶性特征,恶性病变的风险为>50%~90%);5级为存在5个超声疑似恶性特征,恶性病变的风险为>90%~95%;低于4a级可判断肿块为良性,4b至5级则判断为恶性。
1.3.2CEUS检查 经常规彩色多普勒超声显示乳腺内病灶,采用声诺维造影剂,选择病灶血流丰富的切面,并切换到造影模式。25 mg声诺维造影剂冻干粉+5 mL 0.9%氯化钠溶液,振荡摇匀后配制成混悬液,经肘静脉快速注射2.4 mL造影剂,然后注射5 mL生理盐水。采用超声仪器、工作站等同步储存常规二维图像及造影图像,实时连续观察病灶动态灌注过程,总时间≥3 min。恶性肿块评估标准:(1)与周围组织无明显分界、边缘不规则;(2)周围有扭曲、粗大血管进入;(3)增强后荧光不均匀;(4)内部存在充盈缺损区;(5)增强后病灶面积明显增大;(6)增强幅度高于周围组织;符合其中(1)、(2)条或符合≥3条为恶性。
1.3.3BI-RADS评分联合CEUS检查 两项中其中1项为恶性则判断为恶性。
1.4观察指标 (1)统计病理检查结果。(2)统计BI-RADS评分结果。(3)比较良恶性乳腺肿块患者CEUS检查参数(增强开始时间、达峰时间、峰值强度)。(4)比较BI-RADS评分、CEUS检测及联合检查用于乳腺肿块良恶性诊断的结果。(5)比较BI-RADS评分、CEUS及联合检查用于乳腺肿块良恶性诊断的效能(灵敏度、特异度、准确度)。(6)CEUS检查误诊的原因。
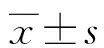
2 结 果
2.1病理检查 84例乳腺肿块患者中,乳腺肿块为恶性38例,以浸润性导管癌为主,占36.90%(31/84);乳腺肿块为良性46例,以纤维腺瘤为主,占42.86%(36/84)。见表1。

表1 病理检查结果[n(%),n=84]
2.2BI-RADS评分 采用BI-RADS评分对乳腺肿块分级,结果见表2。

表2 BI-RADS评分结果[n(%)]
2.3CEUS检查参数 恶性乳腺肿块峰值强度大于良性乳腺肿块(P<0.05),增强开始时间、达峰时间短于良性乳腺肿块(P<0.05)。见表3。

表3 CEUS检查参数
2.4诊断结果 BI-RADS评分诊断乳腺肿块良恶性:真阳性28例,真阴性37例;CEUS检查:真阳性29例,真阴性37例;联合检查:真阳性36例,真阴性36例。见表4。

表4 诊断结果(n=84)
2.5诊断效能 联合检查的灵敏度高于BI-RADS评分及CEUS检查,差异均有统计学意义(P<0.05);3种检查方法的灵敏度、准确度比较,差异均无统计学意义(P>0.05)。见表5。
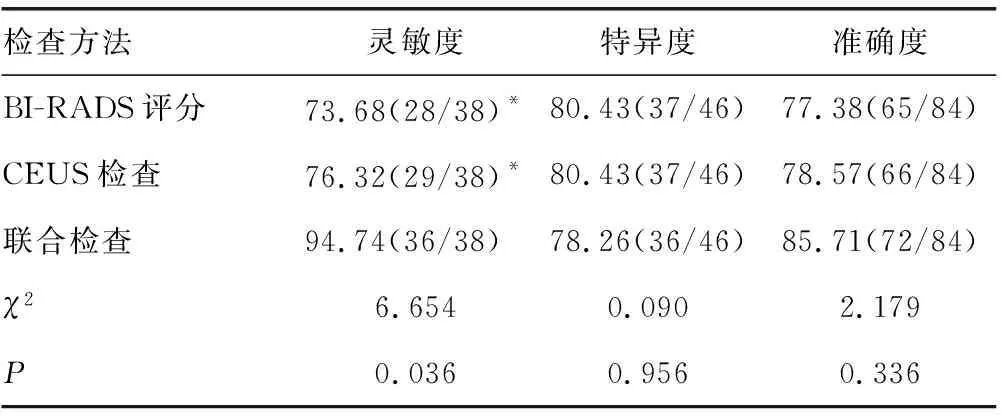
表5 诊断效能[%(n/n)]
2.6CEUS检查误诊的原因 9例误诊患者中3例乳腺肿块良恶性病变相似性极高;2例病灶较小,边界不清晰;2例病灶肿块血供较为丰富;2例呈现局部增生。
3 讨 论
乳腺肿块良恶性鉴别是目前临床重点研究的内容,采取有效手段诊断肿块良恶性具有重要意义。临床可以根据肿块恶性程度给予有针对性的治疗措施,挽救患者生命。
病理活检是临床诊断乳腺肿块良恶性的“金标准”。本研究中,接受病理学检查的84例乳腺肿块患者中,恶性38例,良性46例。由于良性比例占比高于恶性,而穿刺活检会有一定创伤,患者接受度较低;乳腺周围血管、神经均较为丰富,穿刺活检易破坏血供,增加组织损伤风险,临床应用受到一定限制。超声检查是临床常用的乳腺肿块鉴别手段,具有创伤小、结果显示迅速,操作简单、方便的特点。BI-RADS评分、CEUS等超声技术在乳腺肿块良恶性诊断中应用广泛,能提高乳腺恶性肿瘤诊断的灵敏度、特异度[3-4]。BI-RADS分级是根据常规二维超声检查中肿块病变范围、形态、边缘、钙化、回声等进行综合判断,并据此进行分级,保证超声工作的规范化、标准化,有助于临床诊治。但乳腺肿块声像图复杂,不同性质肿块声像图表现存在一定交叉现象,尤其是3级与4级,4a、4b、4c之间极易发生部分重叠,会影响临床良恶性诊断[5]。恶性肿瘤细胞易发生退行性病变甚至坏死,从而发生营养不良性钙化,与乳腺腺病、导管内乳头状瘤等良性病变有一定差异。CEUS检查是近年发展的新型诊断方法,通过分析病灶超声增强模式,可判断病灶大小、扭曲或粗大血管进入病灶、放射状汇聚等特征,并记录整体增强伴充盈缺损、快进快出增强等CEUS特征[6];同时,记录时间-强度曲线,获得CEUS参数。本研究显示,恶性乳腺肿块峰值强度大于良性乳腺肿块,增强开始时间、达峰时间短于良性乳腺肿块(P<0.05),表明CEUS参数对乳腺肿块的良恶性判断具有重要价值。因为正常乳腺组织注射造影剂后会呈现均匀增强,而良性结节增强速度缓慢,恶性结节增强速度极快,且峰值强度较大[7]。本研究分析了CEUS检查误诊的原因,由于乳腺肿块良恶性病变在影像学上具有一定相似性,且有些病灶较小边界不清晰,部分肿块血供丰富或呈现局部增生,单纯CEUS检查仍存在一定漏诊、误诊病例[8]。在上述研究基础上,本研究采用BI-RADS评分联合CEUS检查,结果显示联合检查用于乳腺肿块良恶性诊断的灵敏度为94.74%,高于BI-RADS评分(73.68%)和CEUS检查(76.32%),差异有统计学意义(P<0.05)。两种方法联合应用能提高诊断灵敏度,减少不必要活检操作,指导治疗方案的制订。在对乳腺肿块诊断的过程中,可先用BI-RADS分级初步规范地判断乳腺肿块的恶性风险,然后对性质不确定的肿块采用CEUS检查进一步提高良恶性诊断的效能[9]。联合诊断为良性肿块的患者仍有2例为误诊,可能是由于血液供应或体积较小所致,临床应结合更多检查操作进行综合诊断。
综上所述,BI-RADS评分联合CEUS检查用于乳腺肿块的良恶性诊断灵敏度较高,有助于临床病情的评估,可为治疗方案的制订提供参考依据。

