越鞠丸治疗血脂异常机制的网络药理学预测及分子对接验证
常 燕 林建国 姚魁武
1.中国中医科学院广安门医院心血管科,北京 100053;2.北京中医药大学研究生院,北京 100029
血脂异常,又称高脂血症,是指血清中总胆固醇(total cholesterol,TC)和/或甘油三酯(triglyceride,TG)水平升高,包括低、高密度脂蛋白胆固醇血症在内的各种脂质代谢紊乱。流行病学研究表明,TG 水平升高与动脉粥样硬化和冠心病风险的增加密切相关,积极有效地预防和治疗血脂异常可以明显降低动脉粥样硬化性心血管疾病的发病率和死亡率[1]。目前西药降脂治疗主要以他汀类药物为主,虽能有效降低患者低密度脂蛋白胆固醇(low density lipoprotein-choles terol,LDL-C)水平,但在治疗过程中需监测其安全性,避免药物潜在的不良反应的发生[2]。中医药干预血脂异常具有多靶点、多途径、多层次、副作用小、药物依赖性低等特点,治疗上具有明显优势[3]。
越鞠丸出自朱丹溪的《丹溪心法》,由川芎、栀子、苍术、香附、神曲组成,是治疗郁证之名方,能解因痰、湿、热、血、食所致诸郁。中医将血脂异常归于“痰湿”“痰瘀”“血浊”等范畴,认为痰、瘀、膏、浊均为水谷精微在病理情况下化生的郁滞产物,发病与中焦脾胃密切相关[4]。现代药理研究证实越鞠丸具有降低炎症因子、提高心肌抗氧化能力、调节机体代谢等功能[5],其中川芎有调节脂质代谢和抗动脉粥样硬化的作用[6];栀子具有抑菌抗炎、抗氧化、降糖降脂等药理活性[7];苍术具有调节胃肠的功能,通过抑制组织中前列素E2的生成,从而降低炎症反应,对心血管有保护作用[8];香附可降低血液中的血浆纤维蛋白原及血液黏度,从而纠正血脂紊乱,同时还具有降糖、抗炎、调节胃肠功能等药理作用[9];神曲具有降血脂的功效。临床研究证实,越鞠丸能够显著降低血清TC 水平,提高高密度脂蛋白胆固醇与TC 的比值,在调控血脂方面有明显效果,但其具体作用机制尚不清楚[10]。故在此基础上,本研究通过网络药理学方法预测越鞠丸的活性成分、作用靶点、信号通路,分析其治疗血脂异常的作用机制。
1 资料与方法
1.1 越鞠丸的靶点收集
通过中药系统药理学数据库与分析平台(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP)以口服利用度(oral bioavailability,OB)≥30%、类 药 性(drug likeness,DL)≥0.18 进行条件筛选,检索川芎、苍术、栀子、香附的活性成分及对应靶点,借助Uniprot 数据库转化为相应基因名称;神曲的活性成分根据已发表的文献[11]收集获取,在PubChem 数据库获取活性成分化学结构,通过Swiss Target Prediction 数据库进行靶点预测,最后整合得到越鞠丸活性成分及其作用靶点。
1.2 血脂异常靶点收集
通过GeneCards、DrugBank 和OMIM 数据库,以“hyperlipidemia” “hypercholesterolemia” “hypertriglyceridemia”为关键检索词进行查找,并对检索得到的基因靶点进行处理,将上述3 个疾病数据库的靶点整合,删除重复值后获得最终疾病靶点。
1.3 活性成分-交集靶点网络图的绘制
获取药物活性成分作用靶点和疾病靶点的交集靶点,运用Cytoscape 3.8.2 软件绘制活性成分-交集靶点网络图,利用Network Analyzer 分析功能对网络图进行计算,根据结果筛选出核心活性成分。
1.4 核心蛋白的收集
通过STRING 平台对交集靶点进行蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络的绘制,将PPI 网络信息导入Cytoscape 中,对蛋白网络进行模块化聚类处理,核心蛋白由CytoNCA 计算得出。
1.5 基因本体(GO)与京都基因和基因组数据库(KEGG)富集分析
借助Metascape 平台对交集靶点进行GO 和KEGG 富集分析,设定阈值P <0.01,并以富集的基因数目为筛选标准,选出目标数据,结果采用R 语言和Excel 2019 软件对数据进行可视化。
1.6 分子对接
将“活性成分-交集靶点”网络图中节点度值排名前5 的活性成分与PPI 网络图中节点度值排名前4 的核心蛋白进行分子对接,验证其相互作用强度,活性成分结构通过PubChem 数据库取得,蛋白质结构由PDB 数据库获取。随后利用Autodock Vina 1.1.2软件实现分子对接,并将对接结果通过LigPlot 和Pymol 2.4.0 软件优化制图。
2 结果
2.1 越鞠丸活性成分及其靶点获取
通过TCMSP 平台将筛选条件定为OB≥30%,DL≥0.18,检索川芎、苍术、栀子、香附的活性成分,通过已发表的文献搜索神曲的活性成分,经筛选收集到药物活性成分56 个,其中川芎7 个、苍术9 个、栀子15 个、香附18 个、神曲7 个,其中有6 个为共有活性成分,通过Uniprot 数据库和Swiss Target Prediction数据库对活性成分进行靶点预测,删除重复项,共获取376 个靶点基因。
2.2 血脂异常靶点获取
通过GeneCards、DrugBank、OMIM 数据库,分别收集到潜在靶点1153、58、129 个,合并靶点并删除重复项后,共获得潜在靶点1237 个。对疾病靶点与活性成分靶点取交集,共获得113 个交集靶点。
2.3 活性成分-交集靶点网络图分析
将113 个交集靶点借助Cytoscape 进行网络图绘制,见图1。应用Network Analyzer 进行计算分析,得出159 个节点、611 条边,平均度值为7.69。根据度值筛选出前5 名的活性成分为槲皮素、山柰酚、木樨草素、豆甾醇、汉黄芩素,见表1。推测上述化合物可能是越鞠丸治疗血脂异常的主要活性成分。
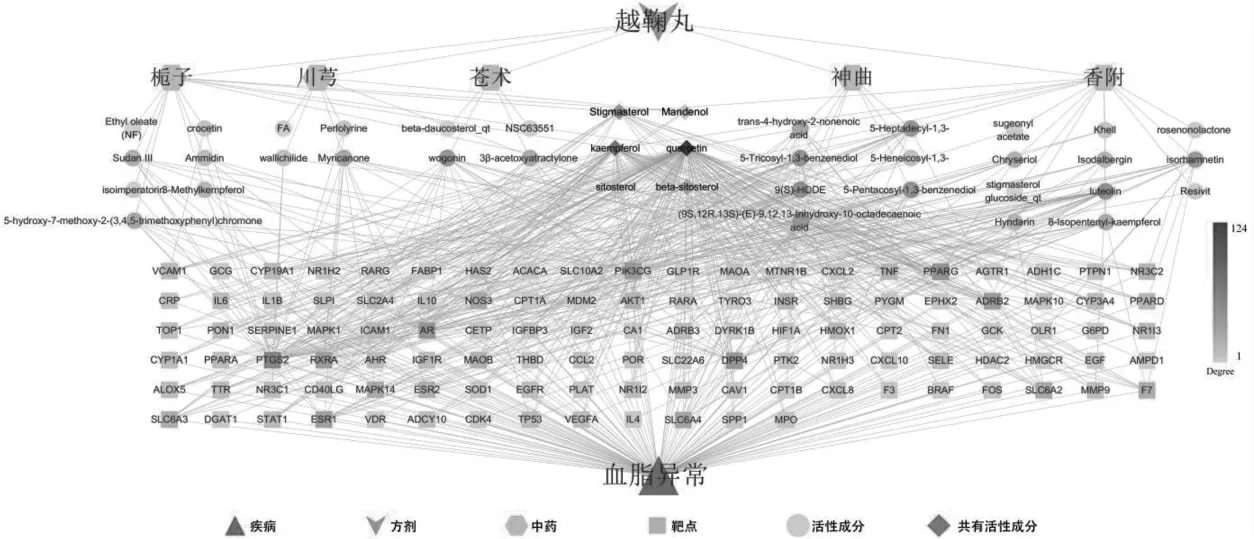
图1 活性成分-交集靶点网络图

表1 度值前5 的活性成分
2.4 PPI 网络分析
将113 个交集靶点导入STRING 数据库,从中获取PPI 网络数据,将其数据导入Cytoscape 中绘制网络图,使用CytoNCA 插件对网络节点进行分析,得到112 个节点、1415 条边,平均度值为25.3,见图2。图中节点大小与颜色深浅代表其度值大小,度值越大,提示该节点蛋白与其他蛋白作用越广泛。其中度值排名较高的有AKT1、IL6、VEGFA、TNF、EGF 等核心靶点。

图2 蛋白质-蛋白质相互作用网络图
2.5 GO 富集分析
借助Metascape 数据库对113 个交集靶点进行基因富集分析,生物过程主要涉及细胞对脂质、激素刺激、脂多糖的应答等过程,分子功能涉及细胞核受体活性、类固醇结合、磷酸酶结合等功能,细胞组分涉及膜筏、膜微域、膜区等成分。根据校正P 值排序,绘制3 个聚类分析前10 的条目。见图3。
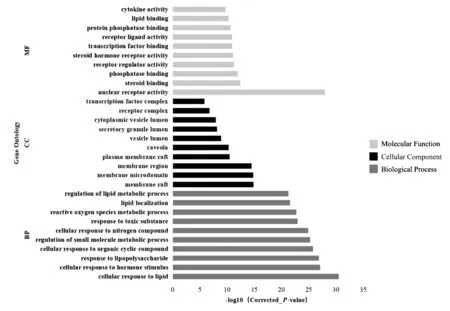
图3 基因本体富集分析图
2.6 KEGG 富集分析
KEGG 通路得到170 个条目,根据校正后P 值进行排序,将前20 条通路绘制成气泡图,见图4。结果显示与血脂异常密切相关的信号通路有AGERAGE、TNF、PPAR、insulin 等。通过整合以上数据,以大于平均度值(7.69)的活性成分为核心成分,以大于平均度值(25.3)的作用靶点为核心靶点,校对P 值前10 的生物过程条目和KEGG 为主要生物过程和信号通路,通过Cytoscape 软件绘制成分-靶点-生物功能-通路网络图,见图5。该图展示了越鞠丸治疗血脂异常的主要作用机制。
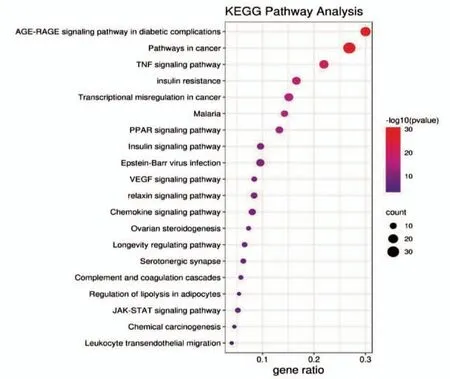
图4 KEGG 富集气泡图

图5 越鞠丸成分-靶点-生物功能-通路网络图
2.7 分子对接
利用Autodock Vina 软件将活性成分-作用靶点网络图中节点度值排名前5 的活性成分和PPI 网络图中4 个关键核心蛋白进行分子对接,利用LigPlot和Pymol 软件对结果进行输出。一般来说配体和受体二者结合越稳定,其结合能就越低。分子对接结果显示,各活性成分与目标受体蛋白对接的结合能均<-6 kJ/mol,说明活性成分能够与配体自发结合,并借助氢键等分子间作用力形成较为稳定的构象,具体结果见表2。分子对接构像见图6,其中豆甾醇与AKT1(-11.5 kJ/mol)结合性最好,对接最稳定。
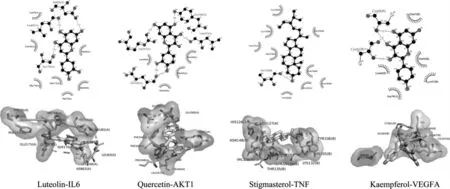
图6 部分蛋白和活性成分分子对接图
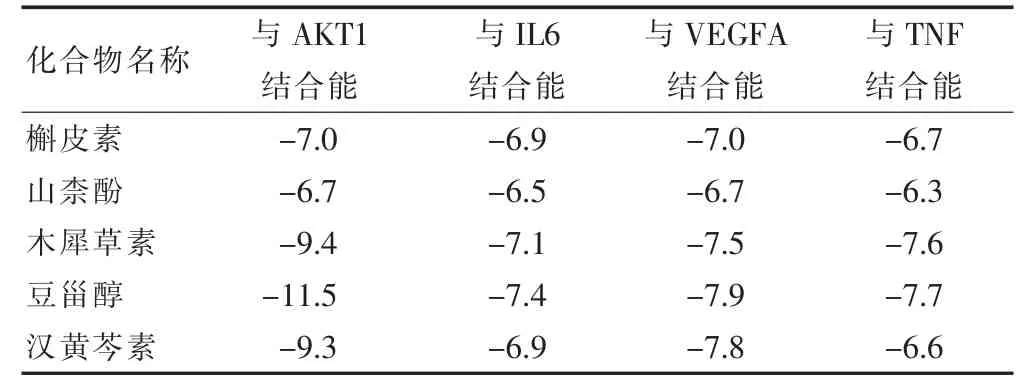
表2 核心活性化合物与核心蛋白结合能(kJ/mol)
3 讨论
近年来,我国人群血脂异常发病率逐渐呈上升趋势,其发生受肥胖、遗传因素、饮食、年龄等各个因素影响。现代研究发现血脂异常发病机制主要与内质网应激、基因多态性、相关炎症因子升高、氧化应激增强、肠道菌群失调相关[12]。临床观察性研究发现,越鞠丸在降低血清炎症因子、抗动脉粥样硬化、降脂固斑等方面疗效显著[13-14]。在小鼠动脉粥样硬化斑块模型中,通过服用越鞠丸后,小鼠肠道菌群多样性增多,其血清中TC 和LDL-C 含量明显降低[15]。
本研究从网络药理学分析得出,越鞠丸治疗血脂异常的药物活性成分主要有槲皮素、山柰酚、木樨草素、豆甾醇、汉黄芩素。相关基础研究发现,槲皮素可通过抑制内皮细胞黏附和内皮细胞NF-κB 信号通路减轻炎症过程,降低动脉粥样硬化大鼠的炎症反应,抑制动脉粥样硬化斑块的发展;血浆槲皮素升高后,血清TC 和LDL-C 水平均有降低[16];木樨草素可以调节转录因子降低NPC1L1 的表达,通过调节NPC1L1蛋白抑制胆固醇的转运活性,从而降低血清中胆固醇含量[17];豆甾醇通过部分阻断胆固醇的吸收来降低LDL-C 的水平,同时防止INS-1 细胞中糖脂毒性诱导的游离胆固醇和活性氧水平的增加,具有抗动脉粥样硬化作用[18]。分子对接提示,上述活性成分与主要核心靶点(AKT1、IL6、VEGFA、TNF)结合力较强,因此推测越鞠丸可能通过上述主要活性成分在降低炎症反应、减少脂质合成、促进脂质转运和分布等方面发挥降脂作用。
通过PPI 网络得到AKT1、IL6、VEGFA、TNF 等核心靶点,主要与细胞代谢、炎症反应、基因表达、信号传导等相关。其中AKT1 具有调节内皮细胞和血管平滑肌细胞(vessel smooth muscle cell,VSMC)的功能,增强VSMC 中AKT1 表达会延缓动脉粥样硬化斑块的进展[19]。VEGFA 作为调节脂肪组织血管生成的关键因素,通过调节脂肪组织VEGFA 的表达,对增强血管生成、减少炎症反应和改善脂肪组织功能有着重要意义[20]。KEGG 富集分析得知,越鞠丸调治血脂异常主要通过AGE-RAGE、PPAR、insulin 等信号通路。AGE-RAGE 通过激活NF-κB 诱导炎症反应,增强氧化应激。有学者认为AGE-RAGE 和NF-κB 两者之间的相互作用与高脂血症诱导的动脉粥样硬化的发病机制有关,实验研究表明血清中sRAGE 水平与HDL 呈正相关,其含量升高可以减弱高脂血症产生的氧化损伤[21-22]。PPAR 是一种转录因子,可调节基因表达以改变组织脂解和血浆脂蛋白代谢,通过激活PPAR 信号通路调节参与脂质代谢的PPARα 靶基因的转录,从而降低肝细胞中TG 和TC 水平[23]。脑内insulin 信号通过刺激肝脏TG 分泌而不引起高甘油三酯血症,来保护肝脏免受异位脂肪堆积,并且可以改善如肥胖和糖尿病等情况下的肝脂肪变性[24]。
综上,本研究利用网络药理学及分子对接技术初步预测越鞠丸中药物主要活性成分与核心蛋白结合,通过调节炎症因子、参与脂质代谢和脂肪组织血管生成等方式,调控AGE-RAGE、PPAR、insulin 等内分泌、炎症信号通路,以降低氧化损伤,促进血脂代谢,改善肝脏功能,纠正机体脂质代谢紊乱。然而,本研究仅从网络药理学和分子对接层面分析越鞠丸治疗血脂异常的作用机制稍显单薄,还需进一步完善和深入实验研究的验证,以期为今后的临床应用和基础研究提供相应的药理依据。

