宫腔镜系统治疗宫腔粘连效果及影响因素分析
尤俊霞 钟细妹 黄 平
深圳市宝安区松岗人民医院(518105)
宫腔粘连是临床常见妇科病[1]。常引起闭经、月经过少、周期性腹痛,部分病情严重者由于子宫内膜受破坏,影响正常的胚胎着床,导致不孕、流产或早产[2]。目前宫腔镜手术为治疗宫腔粘连的金标准,但术中采用电热处理可能导致子宫内膜由于受到热辐射出现损伤,内膜基底层过度破坏,易导致宫腔粘连再次复发,多需反复手术进行解粘连,因而临床亟待探索新的安全有效治疗方案[3]。宫腔镜系统(HEOS)俗称冷刀,冷器械操作具有无需电切,创面小、无电热损伤、修复快等优势[4]。近年来本院采用HEOS治疗宫腔粘连,取得了较好的临床疗效。
1 资料与方法
1.1 入组及排除标准
入组标准:①经宫腔镜确诊;②符合宫腔粘连分类标准[5];③无宫腔镜手术禁忌证;④完整的临床、治疗及随访资料;⑤患者及法定监护人均签署知情同意书。排除标准:①合并自身免疫性疾病或肿瘤;②合并甲状腺疾病或肝肾功能障碍;③由于垂体、卵巢、下丘脑等其他病变引起的闭经;④主动申请退出本研究或失访。
1.2 一般资料
经本院伦理委员会审议并批准,将本院2018年1月-2020年1月收治的106例符合上述标准的宫腔粘连患者作为研究对象,并依照随机信封法分为观察组和对照组各53例。
1.3 方法
所有患者入院后行常规评估,评估是否存在麻醉或手术禁忌证。患者闭经或月经干净后3~7d手术,术前晚患者使用0.4 mg米索前列醇进行阴道上药对宫颈软化扩张,部分患者术前30min静脉注射80 mg间苯三酚对宫颈进行软化扩张。静脉麻醉后取膀胱截石位,行宫腔镜检查确认宫腔内粘连程度,使用扩张棒扩张宫颈管,超声监视下手术。观察组使用HEOS系统治疗,将HEOS置入,膨宫后观察宫腔形态,直视下使用3 mm微型手术剪剪开粘连带,宫底及前后壁粘连使用平头剪,宫腔两侧壁及宫角粘连使用单页尖头剪,侧壁粘连采用犁田式剪开,由于粘连瘢痕处血运差,若可见血管或粉红色肌肉组织则适度考虑为粘连已分开,无需继续深入操作。对照组采用传统宫腔镜方案钝性分离,使用电器械分离致密的纤维性粘连,切割粘连带时采用热能量方案,并采用电切分离粘连,可见血管或粉红色肌肉组织则适度考虑为粘连已分开,无需继续深入操作,由于需要采用电器械操作,故术中对内膜基底层造成小范围的热辐射。两组术后48h内给予抗厌氧菌抗生素和广谱抗生素,术后第二天开始,每天给予4 mg戊酸雌二醇,持续给药3周,术后11天开始每天加服20 mg地屈孕酮。
1.4 观察指标
详细记录患者临床资料,统计术中出血量、手术时间、术中并发症情况;手术前及治疗3个月时采集空腹静脉血,检测血清中孕酮(P)和雌二醇(E2) 水平,同时采用B超测量患者子宫内膜厚度。术后半年随访评估临床疗效:治愈,宫腔已成形,月经恢复正常;有效,宫腔成形较好,但仍伴随轻度异常,月经基本恢复;无效,宫腔未成形,且患者月经未见变化。
1.5 统计学方法
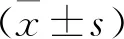
2 结果
2.1 一般临床资料
观察组年龄(30.8±4.5)岁,体质指数(22.4±2.2)kg/m2,轻度粘连16例、中度粘连26例、重度粘连11例;对照组年龄(29.7±6.1)岁,体质指数(22.5±2.5)kg/m2,轻度粘连19例、中度粘连24例、重度粘连10例。两组一般资料无差异(P>0.05)。
2.2 手术情况
两组术中出血量和并发症无差异(P>0.05),手术时间观察组低于对照组(P<0.05)。见表1。

表1 两组手术治疗情况比较
2.3 治疗前后血清P、E2水平及子宫内膜厚度
血清P和E2水平,治疗前两组无差异(P>0.05),治疗后两组均升高且观察组高于对照组(P<0.05)。见表2。治疗后观察组患者子宫内膜厚度(8.87±0.83mm)高于对照组(6.48±0.92mm)(t=10.530,P=0.000)。

表2 两组治疗前后血清性激素水平比较
2.4 临床疗效
治疗后观察组53例中,治愈32例、有效17例,无效4例;对照组53例中,治愈19例,有效25例,无效9例。临床总有效率观察组(49例,92.5%)高于对照组(44例,83.0%)(χ2=4.132,P=0.042)。
2.5 不同临床疗效患者临床指标单因素分析
HEOS治疗后,临床疗效不同患者的病程、宫腔粘连范围、粘连性质、节育器放置及粘连分级存在差异(P<0.05),但人工流产次数、孕次和年龄无差异(P>0.05)。见表3。

表3 HEOS宫腔镜治疗不同临床疗效患者临床指标比[例(%)]
2.6 影响HEOS治疗效果的多因素分析
分析结果表明,宫腔粘连患者病程、宫腔粘连范围、粘连性质、放置宫内节育器及粘连分级均为影响HEOS治疗后临床疗效的独立危险因素(P<0.05)。见表4。

表4 影响HEOS临床疗效的logistics回归分析
3 讨论
宫腔粘连本质为子宫内膜纤维化,可能导致不孕、月经异常、反复流产等[6]。包括宫腔侵入性操作等导致的医源性损伤和宫腔感染等因素均可能导致子宫内膜基底层损伤,诱发子宫粘连[7]。临床对宫腔粘连处理的首选方法为宫腔镜下宫腔粘连切除术[8]。宫腔镜手术对宫腔粘连治疗手术视野清晰,术中无菌操作,术后应用方案辅助治疗预防粘连可有效降低患者术后再次粘连风险[9]。但有研究指出,宫腔镜下宫腔粘连切除术可能对子宫内膜造成新的损伤,进而可能导致宫腔粘连,电切时电切环温度高引起组织损伤,如何降低电切损伤是临床关注热点[10]。
近年来冷刀治疗宫腔粘连已逐渐形成新的趋势。HEOS是集检查、取活检、手术于一体的手术系统,属于非能量器械,不会产生热能,避免电热损伤,并可以特有形式器械完成宫腔角部、底部、侧壁粘连的分离[11]。HEOS冷切割操作灵活多变,可有效处理如重度宫腔粘连[12]。此外,HEOS还配置双极电钩和冷切器械可显著降低子宫穿孔风险。HEOS进行冷切割,降低子宫内膜热损伤,有效保护子宫内膜[13]。减少宫腔粘连再次发病几率,缩短月经恢复时间,恢复生育能力[14]。
本研究结果显示,采用HEOS对宫腔粘连患者治疗可降低手术时间,治疗后有效提高临床疗效,有助于修复子宫内膜,加速月经和宫腔形态恢复正常。性激素是评估和反映卵巢和子宫功能常用血清学指标。本研究结果显示,相较于常规宫腔镜手术治疗方案,采用HEOS对宫腔粘连患者治疗后可更好地改善改善血清P和E2水平,提高子宫内膜厚度。分析认为,可能与HEOS手术治疗中可避免热损伤,降低对邻近器官和组织的累及,利于术后恢复。
一般情况下,宫腔粘连位置、纤维组织深度、范围、病理性质等均与患者临床特征密切相关,且临床特征还可能是影响宫腔粘连患者治疗临床疗效的重要因素。有研究指出,病灶存在时间越长、粘连越严重,患者伴随出现的永久性破坏和组织纤维化越严重,导致子宫内膜修复难度增加[15]。此外,还有研究显示,随着患者疾病进展还可能导致子宫内膜萎缩,对临床预后造成严重不良影响[16]。本研究结果显示,HEOS治疗后,临床疗效不同患者的病程、宫腔粘连范围、粘连性质、节育器放置及粘连分级存明显差异。多因素分析显示,病程长、宫腔粘连范围大、粘连性质致密、放置节育器及粘连分级高均为影响患者HEOS治疗后临床疗效的独立性影响因素。提示临床为有效提高宫腔粘连患者治疗效果,术前应对患者的病程、宫腔粘连范围、粘连性质、节育器放置及粘连分级进行系统评估,提高对宫腔粘连范围、粘连性质和粘连分级的判断准确性,有助于提高临床疗效。
综上所述,采用HEOS治疗宫腔粘连可显著提高临床疗效,且宫腔粘连患者病程、宫腔粘连范围、粘连性质、节育器放置及粘连分级均为影响临床疗效的危险因素,应予以重视。但本研究临床样本数不足,是否具有广泛临床意义还有待后续深入研究。

