HPLC法测定丹参-红花配方颗粒中5种成分的含量
杜少兵,王鹏飞,白吉庆,周慧慧,薛志鹏,高 速,李 菁,王小平,2
(1.陕西中医药大学药学院,陕西 咸阳 712046;2.陕西省中药基础与新药研究重点实验室,陕西 咸阳 712046)
丹参为唇形科植物丹参(Salvia miltiorrhizaBge.)的干燥根及根茎,始载于《神农本草经》,性微寒,味苦,归心、肝经,具有活血调经、祛瘀止痛、凉血消痈,除烦安神的功效[1]。红花为菊科植物红花(Carthamus tinctoriusL.)的干燥管状花,始载于《开宝本草》,味辛微苦、性温,具有活血通经、祛瘀止痛、解毒的功效,用于经闭、痛经、恶露不行、癥瘕痞块、胸痹心痛等症[2]。丹参-红花药对是经典的活血化瘀相须药对,两药配伍使用,一升一降,内外通和,使行气活血之功尤为显著。有文献表明,二药合用祛瘀生新,除邪而不伤正,共奏活血通络、祛瘀生新之功[3-4]。临床上广泛用于冠心病、心绞痛、心肌梗死、心肌缺血等心血管疾病[5-7],且疗效确切[8-10]。
中药配方颗粒是以符合规范的中药饮片为主要原材料,利用现代化技术对有效成分进行提取、分离以及浓缩,之后进行干燥处理、制成供中医临床配方使用的颗粒,具有便于调配、免煎、易服、携带方便、剂量准确等特点[11]。丹参-红花配方颗粒的文献研究较少,缺乏质量控制与评价的方法。基于此,本试验建立HPLC法测定丹参-红花配方颗粒中5种(丹参素、羟基红花黄色素A、迷迭香酸、紫草酸、丹酚酸B)主要活性成分含量,为丹参-红花配方颗粒的多指标质量控制和全面的质量评价提供科学数据。
1 仪器、试剂与试药
1.1 仪器
Dionex Ultimate3000高效液相色谱仪(上海赛默飞世尔仪器有限公司);Discovery DV215CD电子分析天平(瑞士赛多利斯集团);Direct-Q 3UV纯化水机(美国Millipore公司);SFY-20A卤素快速水分测定仪(苏州市莱顿科学仪器有限公司);KQ-300VDE超声清洗机(昆山市超声仪器有限公司);HX-25电子恒温不锈钢水浴锅(上海宜昌仪器纱筛厂)。
1.2 试剂与试药
丹参采自山东省菏泽市鄄城县,红花采自新疆维吾尔自治区塔城市裕民县,经陕西中医药大学白吉庆副教授鉴定均为正品。丹酚酸B对照品(批号:111562-201716,质量分数≥99.8%),羟基红花黄色素A对照品(批号:111637-201810,质量分数≥93.1%)购自中国食品药品检定研究院;丹参素对照品(批号:DST170420-015,质量分数≥98.0%)购自成都德思特生物技术有限公司;紫草酸对照品(批号:19053003,质量分数≥99.8%)购自森岚科技有限公司;迷迭香酸对照品(批号:BZP0004,质量分数≥98.0%)购自江西佰草源生物科技有限公司;乙腈(色谱纯),美国默克公司;其他试剂均为分析纯;水为超纯水(自制)。
2 方法
2.1 丹参-红花配方颗粒样品的制备
取丹参30 g,加320 mL水浸泡60 min,加入红花10 g,温浸120 min,放至室温,过滤,滤渣加8倍量的水温浸提取2次,每次120 min,滤液合并减压浓缩后干燥,得干浸膏粉,粉碎过3号筛,以干浸膏粉-糊精(1:1,m/m)混匀,70%乙醇为润湿剂,湿法制粒,整粒,即得丹参-红花配方颗粒(20190808、20190822、20190830)。
2.2 含量测定
2.2.1 色谱条件
色谱柱:Thermo Hypersil GOLD C18(250 mm×4.6 mm,5μm);流动相:A为乙腈,B为0.2%磷酸水溶液,梯度洗脱(0~15 min,5%A;15~40 min,5%~10%A;40~130 min,10%~20%A;130~150 min,20%~23%A);柱温25℃;检测波长288 nm;流速1 mL/min;进样量为5μL。
2.2.2 对照品溶液的制备
分别精密称取丹参素0.84 mg、羟基红花黄色素A 0.67 mg、迷迭香酸0.58 mg、紫草酸0.36 mg、丹酚酸B 3.15 mg,置同一100 mL容量瓶中,用甲醇定容,摇匀,即得混合对照品溶液。
2.2.3 供试品溶液的制备
取本品颗粒适量,研细,精密称取0.1 g的粉末,置锥形瓶中,精密加入25 mL甲醇,密塞,称定质量,超声处理5 min。取出,放冷,加水补充减失质量,摇匀,0.22μm微孔滤膜过滤,取续滤液即得供试品溶液。
2.2.4 系统适用性试验
分别精密吸取混合对照品溶液和供试品溶液各5μL,按拟定色谱条件测定,记录色谱图。
2.2.5 线性关系考察
分别精密吸取“2.2.2”项下混合对照品溶液1,2,5,8,10μL,按拟定色谱条件,注入液相色谱仪,记录各对照品的峰面积。
2.2.6 精密度试验
精密吸取同一供试品溶液3μL,按拟定色谱条件,连续进样6次,记录各待测成分的峰面积。
2.2.7 稳定性试验
精密吸取同一供试品溶液3μL,按拟定色谱条件,分别于0、1、2、4、8、12、24 h进行测定,记录各待测成分的峰面积。
2.2.8 重复性试验
取同一批号样品6份,按照“2.2.3”项下的方法制备供试品溶液,按拟定色谱条件测定,各待测成分的峰面积,代入工作曲线计算其含量,以各成分含量的RSD值来评价方法的重复性。
2.2.9 加样回收率试验
取已知含量同一批号的丹参-红花配方颗粒0.05 g,平行6份,分别精密加入适量的丹参素、羟基红花黄色素A、迷迭香酸、紫草酸、丹酚酸B对照品,按“2.2.3”项下的方法制备供试品溶液,按拟定色谱条件测定,计算加样回收率。
2.2.10 样品的测定
分别称取丹参-红花颗粒3批适量,按“2.2.3”项下的方法制备供试品溶液,按拟定色谱条件,进样3 μL,记录丹参素、羟基红花黄色素A、迷迭香酸、紫草酸和丹酚酸B的峰面积,计算其含量。
3 结果
3.1 系统适用性试验
结果显示供试品色谱图中,在与对照品色谱图丹参素(峰1)、羟基红花黄色素A(峰2)、迷迭香酸(峰3)、紫草酸(峰4)及丹酚酸B(峰5)相应位置上,均有相同保留时间,各成分的分离度均大于1.5,理论板数按丹酚酸B峰计算应不低于6000,见图1。
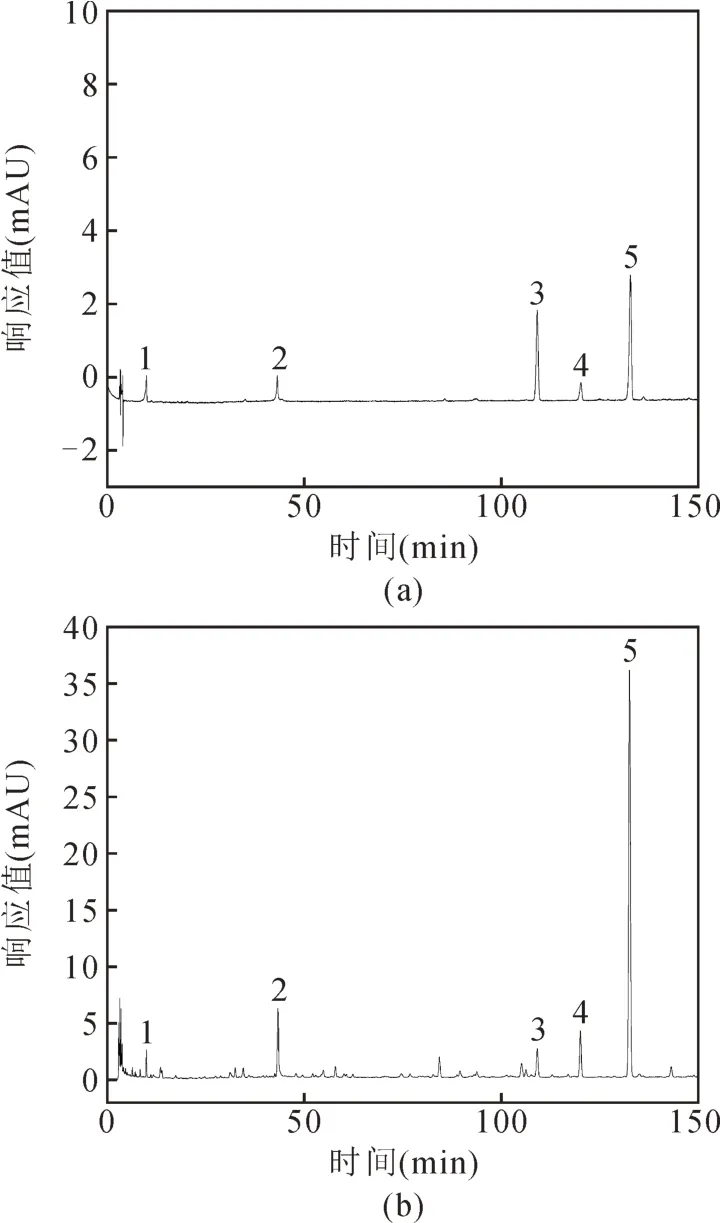
图1 混标溶液和丹参-红花配方颗粒HPLC色谱图Fig.1 HPLCchromatogramsof mixed standard solution and Danshen-Honghua dispensing granule
3.2 线性关系考察
以对照品进样量(ng)为横坐标、峰面积为纵坐标进行线性回归。线性关系结果见表1,结果表明各待测成分在试验浓度范围内线性关系良好。

表1 各成分线性关系Table 1 Linear relationships of various constituents
3.3 精密度试验
丹参素、羟基红花黄色素A、迷迭香酸、紫草酸、丹酚酸B峰面积的RSD(n=6)分别为2.55%、1.55%、2.74%、1.79%、1.77%,表明该仪器的精密度良好。
3.4 稳定性试验
丹参素、羟基红花黄色素A、迷迭香酸、紫草酸、丹酚酸B峰面积的RSD(n=6)分别为2.30%、2.49%、2.13%、2.74%、1.31%,表明供试品溶液中各待测成分24 h内基本稳定。
3.5 重复性试验
丹参素、羟基红花黄色素A、迷迭香酸、紫草酸、丹酚酸B峰面积的RSD(n=6)分别为1.76%、1.50%、2.82%、2.75%、1.33%,表明该方法重复性良好。
3.6 加样回收率试验
由表2可知,该方法的回收率良好,表明试验结果可靠。
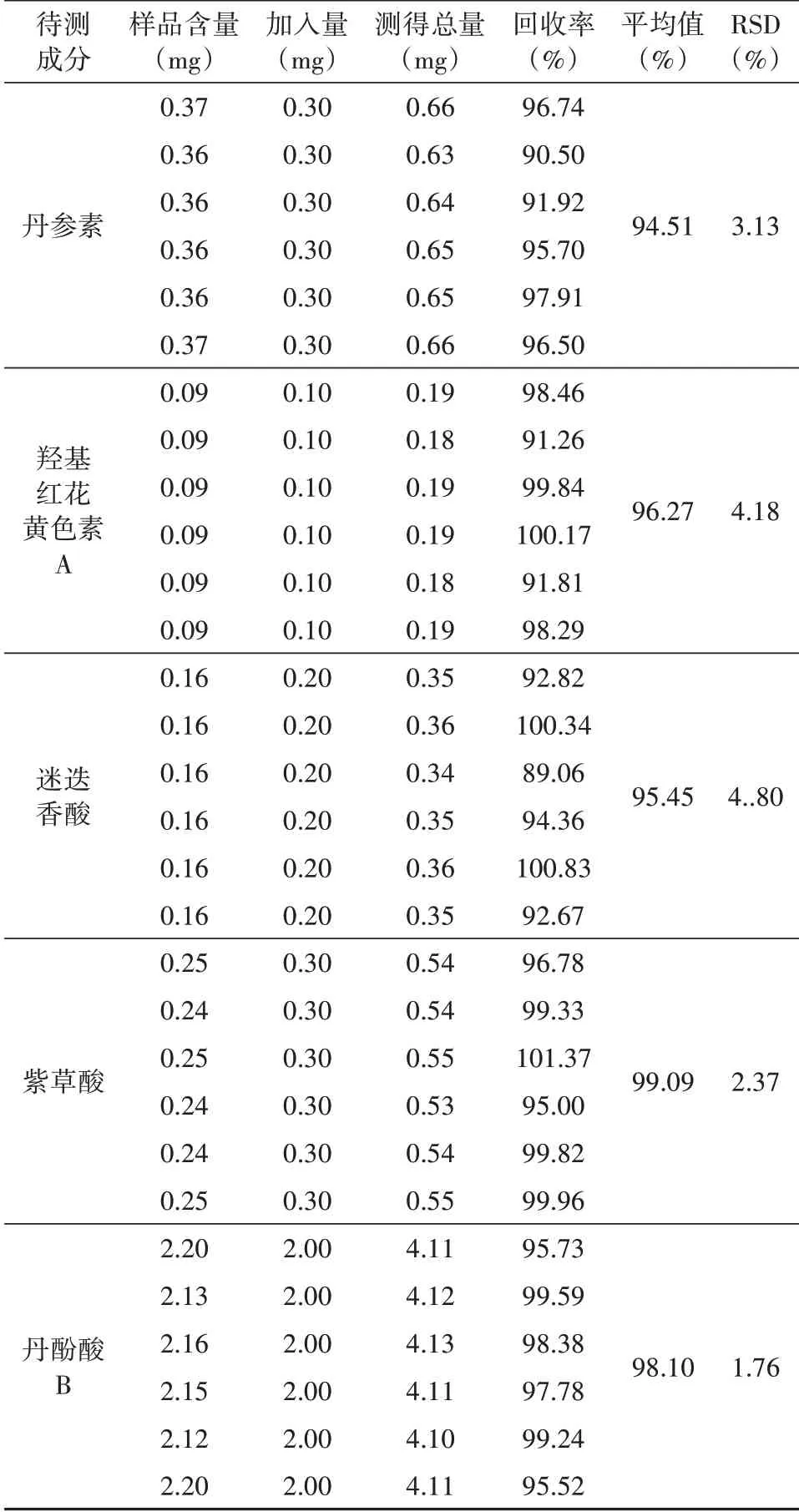
表2 加样回收率试验结果(n=6)Table 2 Results of recovery test
3.7 样品的测定
样品中丹参素、羟基红花黄色素A、迷迭香酸、紫草酸、丹酚酸B含量测定结果见表3。

表3 样品含量测定结果(mg/g)Table 3 Determination of five components in the sample
4 讨论
现代研究表明,丹参的主要活性成分为亲水性成分(丹参素、紫草酸、迷迭香酸、丹酚酸B)和亲脂成分[12]。而红花的主要活性成分是查耳酮类化合物红花黄色素,其中羟基红花黄色素A是活性较高的成分[13],其具有抗氧化、抗血栓、神经保护、抑制炎症因子的产生等药理作用,而且可以改善因脑缺血再灌注引起的脑损伤[14-16]。所以本试验选择这5种活性成分为评价指标,为丹参-红花配方颗粒质量控制与评价提供参考。
本试验采用二极管阵列检测器对其进行全波长扫描,结果表明丹参素、紫草酸、迷迭香酸的最大吸收波长为280 nm,丹酚酸B的最大吸收波长为286 nm,羟基红花黄色素A的最大吸收波长为403 nm,考察了不同波长下各成分的吸收情况,发现各成分在288 nm处均有中强吸收,基线稳定,所得各个色谱峰的峰面积较高,且色谱峰分离度较好,故选用288 nm为检测波长,便于该方法的广泛地应用。本试验考察乙腈-水、乙腈-0.2%磷酸水溶液、甲醇-水、甲醇-0.2%磷酸水溶液等流动相系统,结果显示以乙腈-0.2%磷酸水溶液为流动相,峰形较对称。通过对乙腈-0.2%磷酸水溶液流动相的洗脱方式进行比较,发现等度洗脱无法得到较好的分离度,故最终选用梯度洗脱。
本试验以丹酚酸B、丹参素、紫草酸、迷迭香酸和羟基红花黄色素A为指标,建立了HPLC法测定丹参-红花配方颗粒中这5种成分的含量。该方法简便、高效、准确、重复性好,对丹参-红花配方颗粒进行了一定程度的质量研究,为其后续研究提供技术参考。

