1q21微缺失微重复综合征的产前诊断及遗传学分析
宋婷婷,徐 盈,黎 昱,李 佳,郑 娇,郭芬芬,杨 红
(空军军医大学第一附属医院妇产科,西安 710032;*通讯作者,E-mail:yanghongfck@163.com)
染色体1q21.1微缺失综合征,在线人类孟德尔遗传数据库(Online Mendelian Inheritance in Man, OMIM, 612474)显示其通常由1号染色体长臂2区1带146.5-147.8 Mb(NCBI build 37)区域约1.35 Mb的缺失所致,呈常染色体显性遗传的方式。1q21.1微缺失综合征患者临床表现多样且具有不完全外显率,患者可能无明显或轻度的临床表现,也可能有小头畸形、特殊面容、智力低下、发育迟缓、先心病等临床表现[1]。若该区域发生片段重复则导致1q21.1微重复综合征(OMIM, 612475),患者亦有与缺失相似的临床表现且具有不完全外显率,患者可能有大头畸形、特殊面容、举止异常、自闭症、智力低下等临床表现[2]。1q21.1微缺失/重复综合征为较罕见的染色体异常,文献及数据库对该区域缺失或重复的报道尤其是产前诊断的病例报道相对较少。由于该区域缺失或重复相关的表型多样性、不完全外显和缺乏明显的症状特征使得1q21.1微缺失/重复综合征的产前遗传咨询面临极大的挑战。本文报告2例1q21.1缺失及2例1q21.1重复的病例,分析这些病例的产前临床表现,旨在提高对该病的认识。
1 病例报告
病例1:20岁,孕29周,孕2产0,第一次怀孕32周时B超提示胎儿为无脑儿,引产;此次怀孕为自然怀孕,否认个人史及不良接触史,外院定期产前检查,孕12周外院超声检查显示胎儿颈部透明层(nuchal translucency, NT)2.1 mm,孕中期血清学唐筛综合征筛查低风险。孕27周外院四维B超提示胎儿双侧侧脑室增宽,脊柱裂,于孕28周来我院进行遗传咨询。孕28周本院超声提示:胎儿双侧侧脑室宽约2.1 cm、脊柱裂。夫妻双方遗传咨询及签署知情同意书后,常规消毒超声引导下行羊膜腔穿刺术,同时进行染色体G显带核型分析。G显带核型分析未见异常,染色体微阵列分析结果显示1号染色体1q21.1q21.2区域存在约1.94 Mb的缺失(见表1、图1),进行遗传咨询后最终决定终止妊娠。
病例2:孕妇,26岁,孕28+3周,孕1产0,此次怀孕为自然怀孕,否认不良接触史、个人史及家族病史。本院定期产前检查,孕12+2周本院超声检查显示NT 1.8 mm,孕中期血清学唐筛综合征筛查低风险。孕27周产前超声心动图检查发现胎儿膜周部室间隔缺损,大小约3.3 mm。G显带核型分析未见异常,染色体微阵列分析结果显示1号染色体1q21.1q21.2区域存在约1.78 Mb的缺失,夫妻双方进行遗传咨询后决定继续妊娠,足月顺产一女婴,出生时身长50 cm,体重3 kg,目前电话随访至出生后6个月,家长主诉发育尚可,出生后3个月时复查心脏B超提示室间隔缺损,与孕期超声心动图结果基本一致(见表1、图1)。
病例3:孕妇,41岁,孕20周,孕3产2,曾产2女,一女唇裂畸形,一女无耳廓耳道。此次怀孕为自然怀孕,否认不良接触史,孕12+2周外院超声显示NT 2.1 mm,因不良孕产史孕20周于我院进行遗传咨询,超声检查未见异常。G显带核型分析未见异常,染色体微阵列分析结果显示1号染色体1q21.1q21.2区域存在约1.74 Mb的重复(见表1、图1),夫妻双方进行遗传咨询后决定终止妊娠。
病例4:孕妇,45岁,孕23+5周,孕4产0,主诉年轻时人流2次,胚胎停育1次。此次怀孕为自然怀孕,否认不良接触史,孕11+6周外院超声显示胎儿颈部透明层NT 1.7 mm,因不良孕产史孕23周于我院进行遗传咨询,超声检查未见异常。G显带核型分析未见异常,染色体微阵列分析结果显示1号染色体1q21.1q21.2区域存在约1.84 Mb的重复,夫妻双方进行遗传咨询后决定继续妊娠,足月剖宫产一子,但家长拒绝配合电话随访,产后发育情况未知(见表1、图1)。
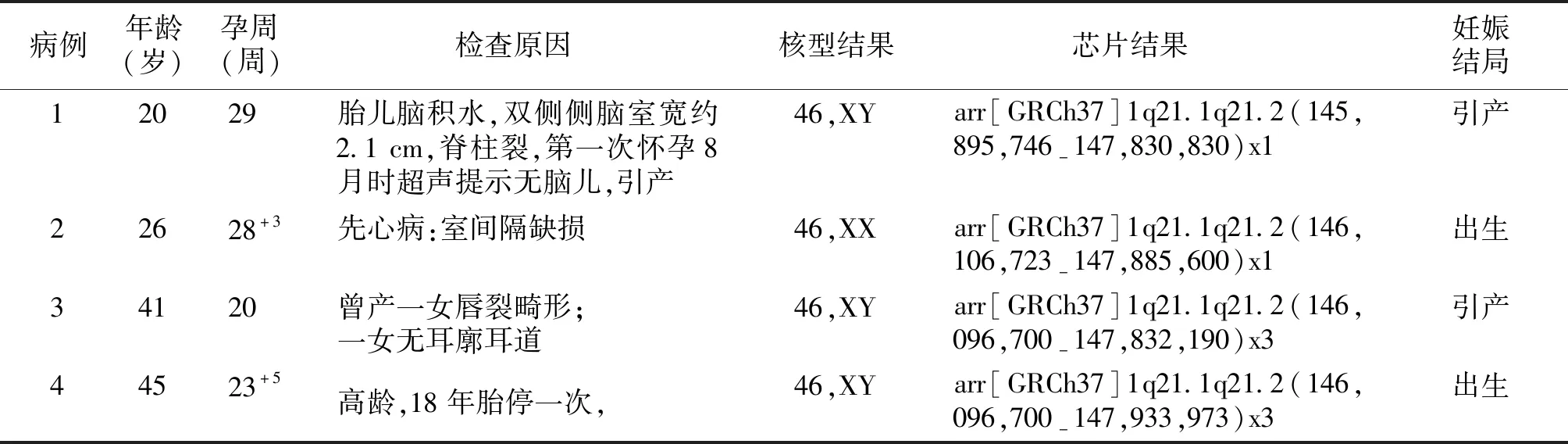
表1 4例产前诊断1q21.1微重复/缺失综合征病例的临床资料
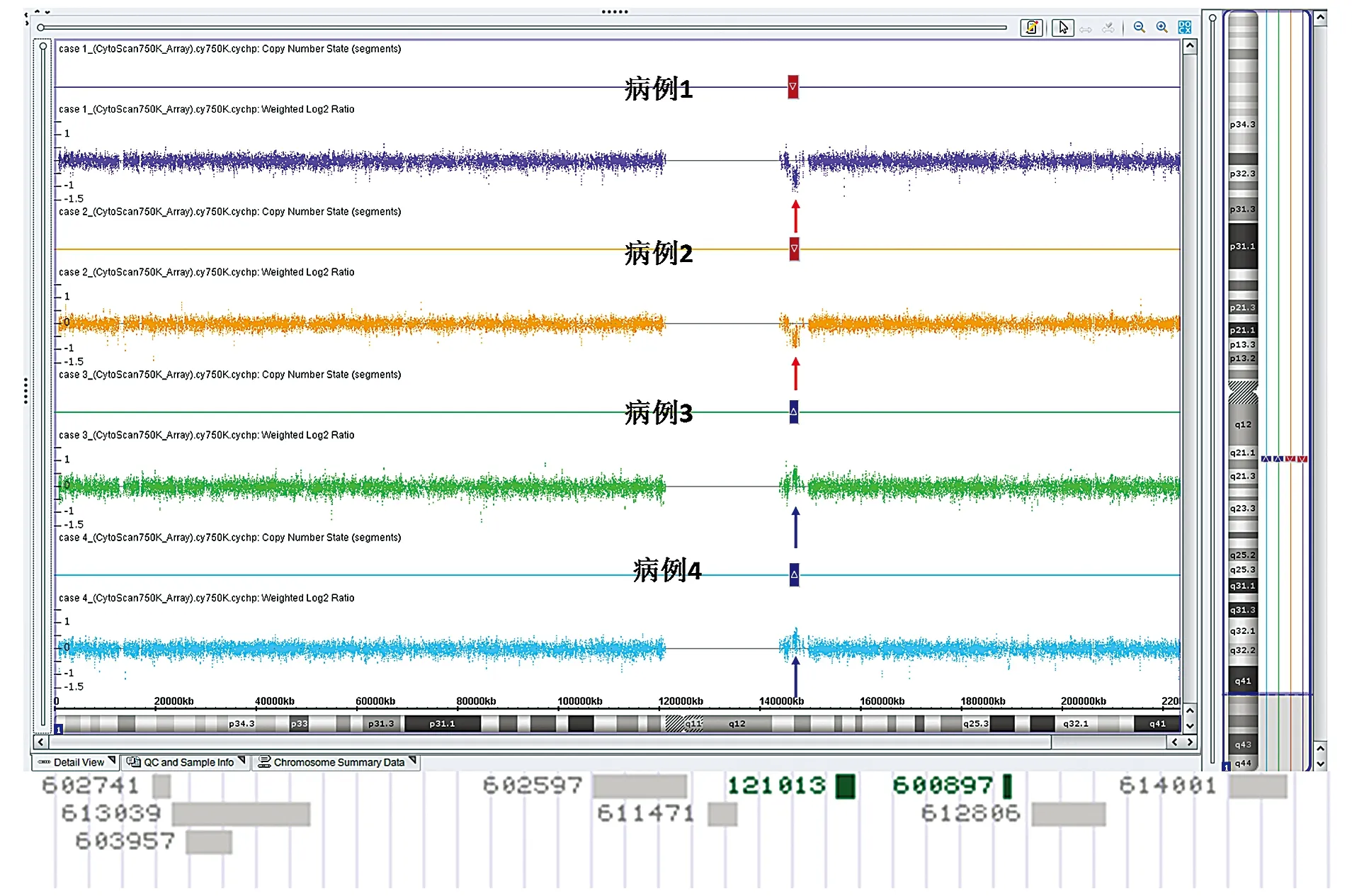
红色箭头指示的为缺失区域,蓝色箭头指示的为重复区域,底部红线框内为1q21.1q21.1区域所涉及的OMIM基因,其中深绿色的为已知的致病基因,灰色的为临床意义不完全明确的基因,数字为基因在OMIM数据库中的编号图1 本文报告的4例病例的染色体微阵列分析结果
2 讨论
1号染色体1q21.1区域富含低拷贝重复序列(low copy repeats, LCRs),这些LCRs容易导致该区域发生非等位同源重组(non-allelic homologous recombination, NAHR),而非等位同源重组是染色体发生缺失或重复的原因之一,因此,该区域易发生染色体片段的缺失或重复。近年来,随着产前筛查技术和分子检测技术的进步,尤其是染色体微阵列分析(chromosome microarray analysis, CMA)技术在产前诊断的广泛运用[3],包括1q21.1微缺失及微重复在内的染色体拷贝数变异的检出率显著增加[4,5]。该区域最小的缺失或重复片段大小约为1.35 Mb(146.5-147.8 Mb,NCBI build 37),涉及PRKAB2、CHD1L、FMO5、BCL9、ACP6、GJA5、GJA8、GPR89B、NBPF11 9个OMIM基因。尽管有文献报道[6]显示1q21.1微缺失/重复综合征临床表现多样且具有不完全外显率,患者可能无明显或轻度的临床表现,也可能有颅面部异常、智力低下、发育迟缓、先心病、举止异常、自闭症、癫痫等临床表现[7,8],但国内外对该区域缺失重复产前诊断的病例报道极少。检索中文知识期刊网、万方数据知识服务平台等中文数据库仅见龚亚飞等[9]报道了1例1q21.1微缺失胎儿合并长骨发育异常,未见该区域重复产前诊断相关的病例报道。尽管符芳等[10]报道了产前诊断胎儿泌尿系统畸形与染色体1q21.1微缺失,但该区域所涉及的基因与本文报道的病例不一致。文献中有1q21.1微缺失综合征胎儿羊水少、肾发育不良、脑膜膨出、房间隔缺损[11]、法洛四联症、多趾畸形、心室强光点、脉络膜囊肿、NT增厚[12]的报道。本文报告2例产前诊断的1q21.1微缺失综合征胎儿,这2例均因产前超声检查异常进行介入性产前诊断,其中1例为脑积水合并脊柱裂,1例为超声心动图检查提示膜周部室间隔缺损,对1q21.1微缺失胎儿的产前临床表现进行了补充。文献中有1q21.1微重复综合征胎儿鼻骨缺失、十二指肠闭锁[13]、室间隔缺损、肺动脉瓣狭窄及永存左上腔静脉的报道[14]。本文报告了2例产前诊断的1q21.1微重复综合征胎儿,但二者均为高龄孕妇且有家族不良病史,其中病例3孕妇曾产2女,一女为唇裂畸形、一女无耳廓耳道,病例4孕妇因不明原因自然流产一次,在此次怀孕中这两个病例产前超声检查均未见异常,可能与孕周小有关,也可能由于外显率不全,一些1q21.1微重复综合征胎儿产前无明显临床表现,但即便产前超声检查未见异常,也不代表胎儿出生后没有智力低下、自闭症、举止异常等1q21.1微重复综合征患者可能的临床表现,这为产前遗传咨询带来巨大挑战。
本文报道的缺失或重复的大小在1.74-1.94 Mb之间,涉及1q21.1微缺失/重复综合征的关键区域,包含PRKAB2、CHD1L、FMO5、BCL9、ACP6、GJA5、GJA8、GPR89B等关键基因。PRKAB2基因编码AMP活化蛋白激酶的一个调节亚基,有文献报道显示其在右室双出口患者中高表达[15]。CHD1L基因编码参与DNA修复的DNA解旋酶蛋白,Brockschmidt等[16]研究发现CHD1L在肾脏发育中起重要作用,可能为先天性肾和泌尿系统异常相关候选基因,而Dou等[17]发现CHD1L能够促进人胚胎干细胞神经元分化,其在神经系统发育中发挥作用,亦有文献报道显示其在法洛四联症、右室双出口及肺动脉狭窄患者中过表达[18]。Harvard等[19]研究表明环境因素与遗传因素共同作用,CHD1L和PRKAB2功能失调的个体在环境较差的条件下表型可能更为严重。GJA5基因编码一种心脏连接蛋白-40,它在细胞黏附和细胞间通讯中起关键作用[18],该基因缺陷与常染色体显性遗传的心房停滞相关(OMIM:108770),但近年来亦有该基因突变与法洛四联症相关的报道[20]。GJA8基因编码Connexin 50,该基因缺陷与常染色体显性遗传1型先天性白内障相关。目前,该区域其他基因对组织器官发育和分化影响的相关报道较少,还需要更多的文献支持,有待进一步探讨。
1q21.1微重复/缺失综合征患者临床表现多样,从无明显的临床表现到严重的临床表现,部分患者拷贝数变异源自无明显临床表型的父母,其临床表型并非单一基因所导致的,而是多个基因及环境的共同相互作用所致。由于该区域缺失或重复相关的表型多样性、不完全外显和缺乏特异性临床表现,且即便家庭成员也可能有相同的微缺失,临床表现也并不完全一致,使得产前CMA检出的1q21.1q21.2微缺失重复的遗传咨询对产科医生和遗传咨询师来说仍然是一个挑战。对于产前诊断出的1q21.1微重复/缺失综合征的胎儿,还应使用其他产前诊断技术综合评估胎儿发育,结合影像检查定期评估胎儿生长发育各项指标,加强随访,充分知情告知。
本研究收集了4例1q21.1微重复/缺失综合征的胎儿的临床资料,发现该区域重复或缺失的患者可能有先天性心脏病、侧脑室增宽等临床表现,也可能无明显临床表现,不同临床表型的阐明为明确该疾病的致病机制、诊断及治疗提供有价值的理论依据。同时强调,对于产前超声检查中发现的异常、高龄及不良孕产史孕妇进行包括染色体微阵列分析在内的产前诊断,排除胎儿染色体异常非常必要。

